先知先覺 輕松規避“阿伏加德羅常數的應用”的命題陷阱
云南 趙旭東
阿伏加德羅常數的應用是高考全國卷中的高頻考點,在《中國高考評價體系》指導下的新高考中仍然將是高頻考點。之所以這樣推測,原因有三:一是它能落實《普通高中化學課程標準(2017年版2020年修訂)》中“宏觀辨識與微觀探析”“證據推理與模型認知”等高中化學學科核心素養;二是它能承載“理解與辨析能力”“分析與推測能力”的考查;三是它能體現微粒觀和變化觀等化學觀念。2020年、2021年高考證實了這個推測,如2020年7月浙江選考化學19題、2020年理綜全國卷Ⅲ9題、2021年理綜全國甲卷8題,都考查了“阿伏加德常數的應用”。講述如何避免“阿伏加德羅常數的應用”的考查陷阱的文獻很多,但是分析怎樣設置陷阱的文章幾乎沒有。本文通過一些典型的例子,領悟陷阱是怎樣設置的,以實現做題時對陷阱先知先覺,從而輕松規避,高效復習。
1.怎樣設置陷阱
1.1 利用遺忘知識設置陷阱
與“記住”相比,遺忘是永恒的。記憶化學知識時,不去聯系生活、生產、實驗而是死記硬背,通過這種方式記住的知識容易遺忘,從而造成做題時犯低級錯誤。出題者利用遺忘知識設置陷阱,促成誤判。舉例如下表1:
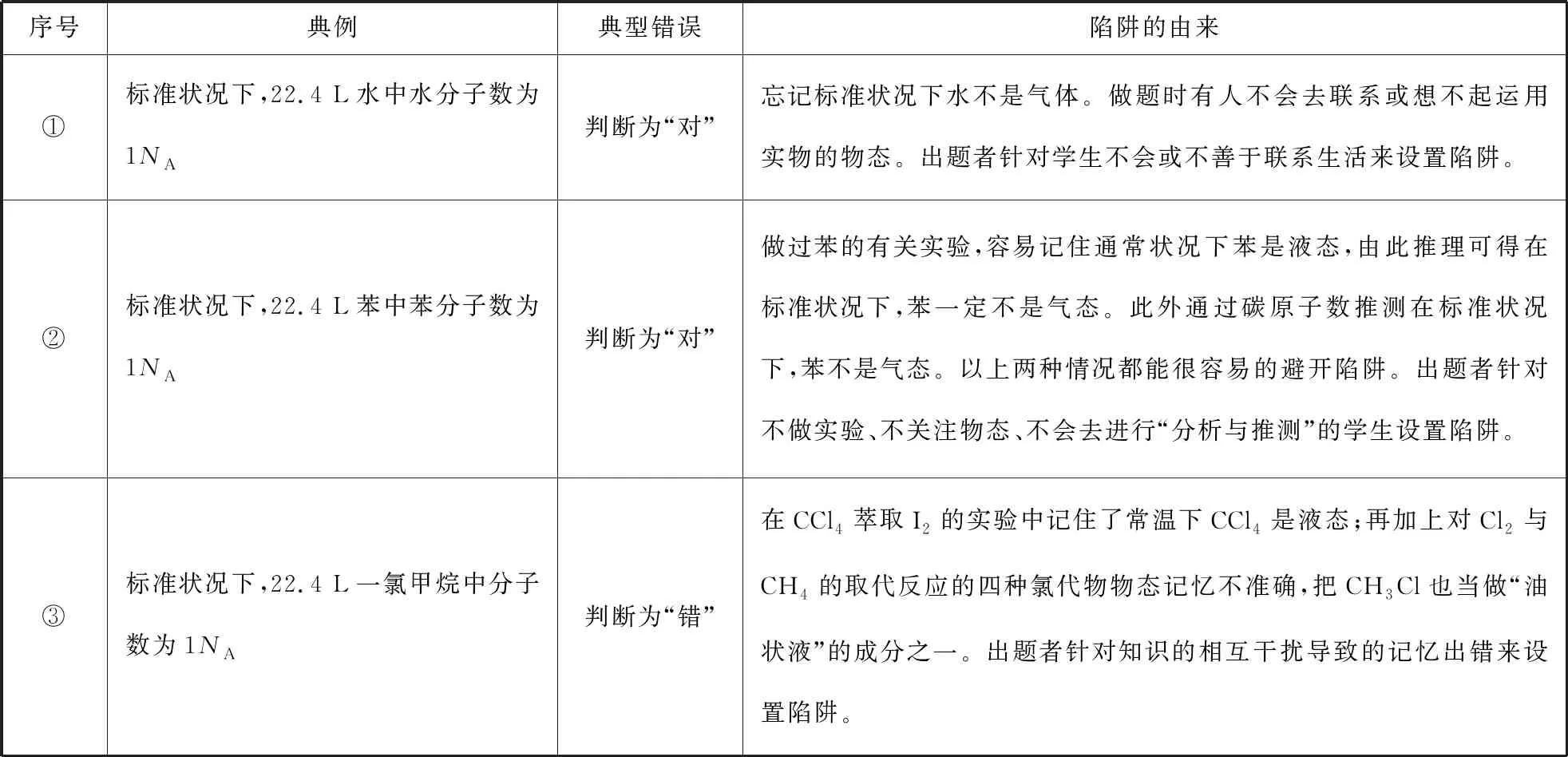
表1
1.2 利用思維定式設置陷阱
思維定式,也稱思維慣性,是由先前活動而造成的一種對當前活動的特殊的心理準備,或活動的傾向性。思維定式有一定的積極作用,在環境不變的情況下,可使人能夠應用已掌握的方法迅速解決問題。思維定式也有消極作用,在情境發生變化時,會讓人用原有的思維方式思考問題而容易做出錯誤判斷。出題者利用思維定式的消極作用,甚至設法強化原有思維方式,使判斷錯誤。舉例如表2:

表2
1.3 利用“偷換概念”設置陷阱
⑥“1 mol Fe在一定條件下與足量Cl2充分反應,Fe得到的電子數目為3NA”。錯誤之處在于,此反應中,Fe不是“得到”電子而是“失去”,而在實際解題時常出現錯誤。這種說法中,一開始反映在頭腦中的是與我們認知一致的信息,在我們的認知中Fe一定是失去電子,出題者將“失去電子”偷偷換成“得到電子”,因而很難發現;有主觀上“Fe失去電子”的先入為主,加上思維的“自我糾錯”功能,將信息向“失去電子”方向“糾正”,于是就更加難以發現了。
1.4 多種方法綜合利用設置陷阱
阿伏加德常數的應用通常是在選擇題中考查,四個選項給命題者設置陷阱提供了一個很大的平臺,所以往往同時運用多種方法設置陷阱。
【例1】設阿伏加德羅常數為NA,下列說法錯誤的是
( )
A.標準狀況下,22.4 L O2中含有分子數為1NA
B.標準狀況下,22.4 L Cl2中含有分子數為1NA
C.常溫常壓下,28 g N2中含有分子數為1NA
D.標準狀況下,22.4 L氦氣中所含原子數為2NA
【答案】D
誤導錯選C的陷阱設置:A、B兩項連續強化“標準狀況下”選項是正確的,同時也就強化了“常溫常壓下”的選項是錯誤的判斷,C項出現“常溫常壓下”,因此很容易錯選C;在此情況下很難再認真往后看,也就發現不了題中所給“28 g”是質量而不是體積,從而失去糾錯的機會。誤導不選D的陷阱設置則是忘記稀有氣體是單原子分子,A、B、C選項中O2、Cl2、N2這幾種常見氣體單質是雙原子分子,推理方法被引向類比推理,從而得到錯誤的結論“稀有氣體分子也是雙原子分子”。
2.怎樣規避陷阱
2.1 規避“標準狀況下,氣體摩爾體積為22.4 L·mol-1”的陷阱
“警覺”:看到選項中有“標準狀況”,一定還要看后面跟的是否是氣體體積;看到“常溫常壓”,一定還要看后面跟的是不是質量。
“記憶”:在保證常規物質的物態沒有記錯的前提下,主要記憶易忘記、易記錯的物質的物態,以減少記憶量。標準狀況下是氣體的物質有CH3Cl、碳數≤4的烴類、HCHO;標準狀況下不是氣態的物質:HF、SO3、NO2、碳數≥5的烴類、氯代烴(除CH3Cl外)、溴代烴、醇、乙醛、羧酸。強調一下,要看準是“HCHO”還是“甲醛溶液”;HF、NO2常溫下是氣體,容易誤認為標準狀況下也是氣體。
2.2 規避“摩爾質量、微粒數”的陷阱
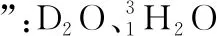
2.3 規避“物質組成”陷阱
“警覺”:出現物質名稱,要警覺物質組成的陷阱。見前【例1】D;是不是給出了化學式,就不會有陷阱呢?不是,有時給出化學式恰恰也是為了設置陷阱。
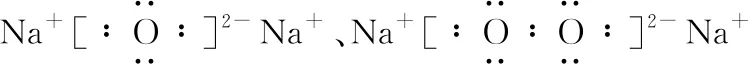
2.4 規避“化學鍵”陷阱
“警覺”:發現涉及化學鍵,要警覺很可能有陷阱。
“記憶”:用化學鍵設置陷阱,主要利用思維定式和沒有理解結構來實現。如,受“1 mol CH4中共價鍵數目為4NA”的影響,錯誤認為1 mol P4中共價鍵數目為4NA;受“1 mol SiO2含共價鍵數目為4NA”的影響,錯誤認為1 mol C(金剛石)含C—C鍵數目為4NA,1 mol C(石墨)含C—C鍵數目為3NA。解決金剛石、石墨中C—C鍵數目,要用均分原理,晶體硅的結構與金剛石類似,石墨烯的結構與石墨相似,需要用均分原理分析,以鞏固均分原理的應用。
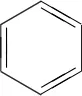
2.5 規避“弱電解質電離”陷阱
“警覺”:見到弱電解質,馬上想到忘記考慮“弱電解質不能全部電離”就會落入陷阱。
2.6 規避“水解”陷阱
“警覺”:心存會水解的離子,見到后馬上想到忘記考慮水解會進陷阱、沒有發現已經考慮水解卻認為還要考慮水解也會落入陷阱,見前④。
2.7 規避“隱含反應”陷阱

“記憶”:易被忽視會反應的物質及反應。除上兩例外,遇到及時補充、完善。
2.8 規避“反應的階段性”陷阱
“警覺”:Cu與濃硫酸共熱、MnO2與濃鹽酸共熱等,隨著反應進行,酸被消耗而變為稀酸,反應停止。
“記憶”:除上兩例外,CO2通入NaOH溶液量不同反應的不同的情況,也要及時補充、完善。
2.9 規避“可逆反應”陷阱


2.10 規避“轉移電子數”陷阱
“警覺”:變價金屬單質與非金屬單質的反應,轉移電子數有陷阱;Na2O2在不同的反應中轉移電子數可能相同也可能不同。這些都可用來設置陷阱。
“記憶”:變價金屬單質與S反應,金屬生成低價,與Cl2反應,生成高價;Na2O2與H2O、CO2等發生歧化反應,-1價的O發生歧化一個升一個降,如有其他還原劑參加,往往變為-2價的O,等等。


