SPF金黃倉鼠籠具及飲水脈動真空滅菌的效果驗證
范方玲趙 田張華瓊
(成都生物制品研究所有限責任公司,成都 610023)
本公司SPF金黃倉鼠飼養在屏障環境中,為乙腦減毒活疫苗的生產提供原代腎細胞。按照實驗動物環境及設施的國家標準(GB14925-2010)規定,屏障設施要嚴格控制人員、物品和環境空氣進出[1]。動物飼養所需要的籠具、墊料、毛巾、抹布和動物飲水需要經過滅菌后傳遞到工作區域[2]。目前脈動真空滅菌器所運用的高壓蒸汽滅菌技術的方法是公認的最可靠的滅菌技術之一[3],廣泛應用于實驗動物屏障設施,主要承擔進入屏障設施內的動物籠具、飼料、墊料、飲水和實驗物品的消毒滅菌工作[4],是保障屏障設施內環境、動物安全及控制傳染性疾病蔓延的重要環節[5]。我司也使用脈動真空滅菌器對進入屏障設施內的動物籠具、墊料、飲水等耐高溫高壓物品進行消毒滅菌工作。脈動真空滅菌器的設備性能和對物品的滅菌效果將直接影響到屏障設施內環境及實驗動物的質量。驗證是更加安全和更加先進的質量保證方法[6]。因SPF金黃倉鼠飼養過程中所使用的需要高壓滅菌的物品種類較多,不可能單一品種物品進行高壓滅菌。故本研究以脈動真空滅菌器的性能驗證為基礎,將多種待滅菌物品按照規定的裝載方式和滅菌條件使用脈動真空滅菌器進行滅菌效果的驗證,現將2014-2020年的驗證數據進行統計,結果報道如下。
1 材料和方法
1.1 實驗材料
SPF金黃倉鼠籠具:育種籠盒(53×38×19 cm)、運輸籠盒(50×35×20 cm)、繁殖籠盒(30×23×15 cm)、相應規格籠蓋;墊料(適量,預先鋪放在每一個籠盒中,重疊碼放,最上面一層籠盒內無墊料,裝織物等)、清潔用抹布、拖布、線手套、潔凈操作服、飲水瓶塞等干物。
飲水:預先灌裝入瓶(滿瓶),分為250 mL瓶裝、500 mL瓶裝。
1.2 主要試劑與儀器
B-D試紙(美國Mesalabs公司);生物指示劑(BI):嗜熱脂肪芽孢桿菌芽孢,最小含量2.0×106,D121℃值為2 min(美國Mesalabs公司);硫乙醇酸鹽流體培養基和胰酪大豆胨液體培養基(本公司培養基室制備)。
校準合格的Kaye溫度記錄儀(美國Amphenol公司);帶SIM和配備T型熱電偶;校準合格的溫度干井HTR-400(美國Amphenol公司);校準合格的標準鉑電阻,型號:IRTD-400(美國Amphenol公司);脈動真空滅菌器(山東新華醫療器械股份有限公司):型號XG1.GMM-2.0;恒溫培養箱:型號BPX-162(上海博訊實業有限公司醫療設備廠)。
1.3 實驗方法
1.3.1 滅菌參數和裝載方式
(1)循環B4(干物)的滅菌參數和裝載方式
滅菌程序:織物。
滅菌參數為:真空脈沖次數3次,脈動上下限±80 KPa,滅菌溫度122℃,滅菌時間1200 s,干燥時間240 s。
裝載方式有兩種:1、B4-1主要裝載物為育種籠盒、運輸籠盒、及籠蓋、飲水瓶塞、操作服,每疊13個育種籠盒,最上一個盒子裝有瓶塞,共4疊;每疊13個運輸籠盒,最上一個盒子裝有操作服,共2疊;1疊育種盒蓋,48個,具體的裝載方式和溫度探頭分布見圖1。2、B4-2主要裝載物為繁殖籠盒、籠蓋、操作服、毛巾、抹布、雜物,每疊13個繁殖籠盒,最上一個盒子裝有操作服、毛巾、抹布等織物,共18疊;1疊13個繁殖籠盒,最上一個盒子裝有雜物;1疊82個繁殖盒蓋,2疊,具體的裝載方式和溫度探頭分布見圖2。
(2)循環A4(飲水)的滅菌參數和裝載方式
滅菌程序:液體。
滅菌參數:置換時間2400 s,滅菌溫度122℃,滅菌時間1800 s。
裝載方式有兩種:1、A4-1主要裝載物為250 mL瓶和500 mL瓶,具體的裝載方式和溫度探頭分布見圖3。2、A4-2主要裝載物為250 mL瓶,具體的裝載方式和溫度探頭分布見圖4。
1.3.2 驗證方法及評價標準
(1)真空保壓試驗
方法:空載狀態下,啟動脈動真空菌器保壓程序,參數設定如下:保壓限度-90 KPa,時間900 s,泄露限度≤2 KPa。
判定標準:真空保持15 min后,真空檢測終點壓力與起點壓力之差應≤2 KPa,則視為設備保壓合格。
(2)B-D試驗
方法:選用預真空122.0℃時滅菌498 s的B-D試紙,在滅菌器空載狀態下將BD試紙放在排水口上方10~20 cm處,標簽向上。設定BD程序參數:脈動3次,真空脈動下限-80 KPa,真空脈動上限80 KPa,滅菌時間498 s,滅菌溫度122.0℃。在完成滅菌操作程序后,取出試紙包并打開觀察B-D試紙。
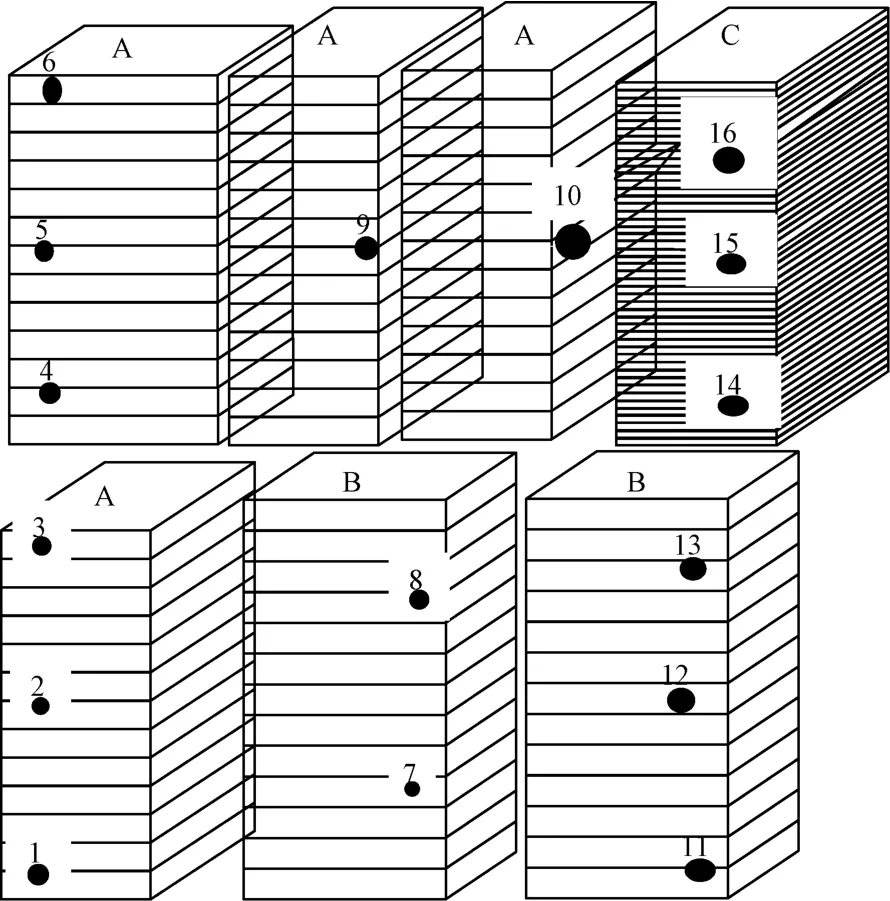
注:1~16:熱電偶布點,每個熱電偶旁放置一個生物指示劑。所有熱電偶均位于盒子中央。A:13個育種籠盒,最上一盒裝有瓶塞;B:13個運輸籠盒,最上一盒裝有操作服;C:48個育種盒蓋。圖1 循環B4-1(干物)裝載方式和熱穿透熱電偶布點圖Note.1~16,TC distribution points,and place one BI adjacent to the TC.All TCs are placed in the center sides of the boxes.A,13 breeding cage boxes,the top box contains the bottle stopper.B,13 transport cages,the uppermost containing operating suits.C,48 breeder cartons.Figure 1 Loading mode of cycle B4-1(dry matter)and distribution diagram of thermal penetration thermocouple
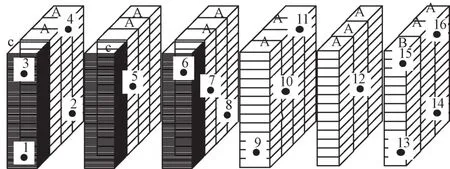
注:1~16:熱電偶布點,每個熱電偶旁放置一個生物指示劑。所有熱電偶均位于盒子中央。A:13個繁殖籠盒,最上一盒裝有織物;B:13個繁殖籠盒,最上一盒裝有雜物;C:82個繁殖盒蓋。圖2 循環B4-2(干物)裝載方式和熱穿透熱電偶布點圖Note.1~16,TC distribution points,and place one BI adjacent to the TC.All TCs are placed in the center sides of the boxes.A,13 breeding cages with fabric in the top box.B,13 breeding cages,the top box contains sundries.C,82 breeding cartridge LIDS.Figure 2 Loading mode of cycle B4-2(dry matter)and distribution diagram of thermal penetration thermocouple
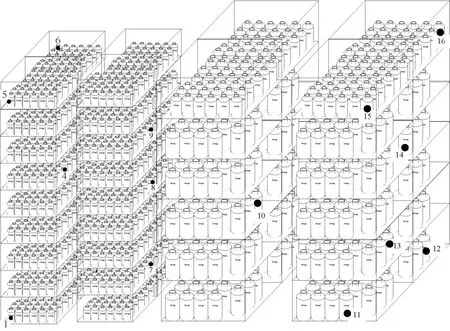
注:1~16:熱電偶布點,每個熱電偶旁放置一個生物指示劑。所有熱電偶布置在水瓶底部,保證頂端向上,距離底部不少于1 cm,不大于2 cm。圖3 循環A4-1(飲水)裝載方式和熱穿透熱電偶布點圖Note.1~16,TC distribution points,and place one BI Challenge Vials adjacent to the TC.All TCs are placed in the bottom of bottles,and verify that the top of the TC up to the bottom more than 1 cm,but less than 2 cm.Figure 3 Loading mode of cycle A4-1(drink water)and distribution diagram of thermal penetration thermocouple
判定標準:試紙顏色變成黑色(說明書給定滅菌后的合格顏色),且顏色分布均勻,提示脈動真空滅菌器能夠排除冷空氣99%以上,滅菌器真空性能合格。
(3)空載熱分布試驗
方法:滅菌器在空載狀態下,使用校準合格的帶SIM和T型熱電偶的Kaye溫度記錄儀,通過驗證孔將16根熱電偶插入蒸汽滅菌柜。將15支熱分布熱電偶按幾何分布在腔室內,熱電偶位置離腔室壁、地和頂不少于5 cm,不接觸腔室表面或架子(具體布點見圖5)。在滅菌器排水口主控溫度探頭附近布置1支熱分布熱電偶。設置Kaye驗證儀的熱電偶數據記錄時間間隔為30 s,每30 s對記錄的溫度數據進行統計分析(最小、最大、波動和平均)。同步Kaye記錄儀和滅菌器的時鐘。分別按照織物和液體程序進行滅菌。
判定標準:在滅菌階段,所有熱分布熱電偶溫度都在設定點0℃~+3.0℃范圍內,所有的熱電偶的溫度與同一時刻溫度平均值的差值在±1℃范圍內,滅菌器主控溫度探頭的顯示溫度和附近熱電偶溫度差值在±1.0℃內,提示滅菌室內的溫度分布可確定為均勻。
(4)滿載熱分布、熱穿透試驗
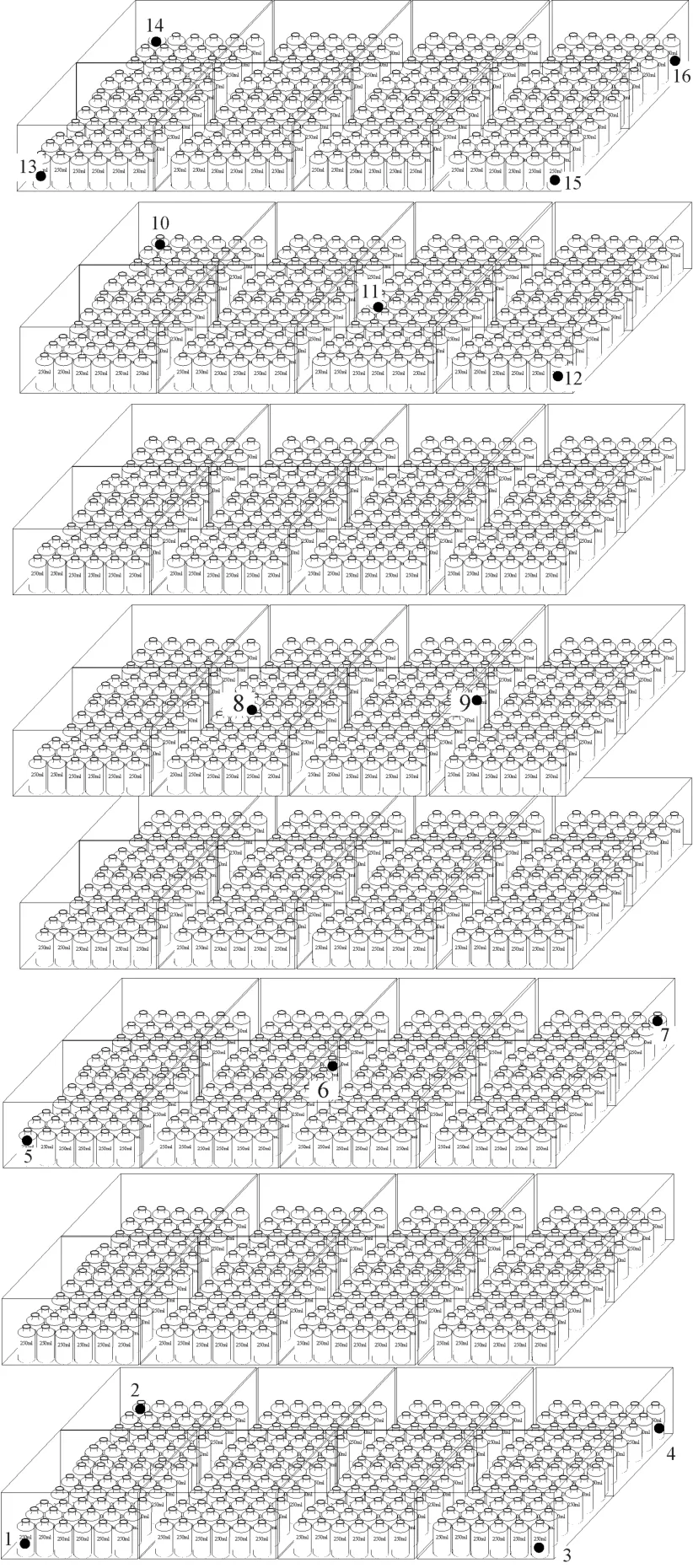
注:1-16:熱電偶布點,每個熱電偶旁放置一個生物指示劑。所有熱電偶布置在水瓶底部,保證頂端向上,距離底部不少于1 cm,不大于2 cm。圖4 循環A4-2(飲水)裝載方式和熱穿透熱電偶布點圖Note.1-16,TC distribution points,and place one BI Challenge Vials adjacent to the TC.All TCs are placed in the bottom of bottles,and verify that the top of the TC up to the bottom more than 1 cm,but less than 2 cm.Figure 4 Loading mode of cycle A4-2(drink water)and distribution diagram of thermal penetration thermocouple
方法:使用校準合格的帶SIM和T型熱電偶的Kaye溫度記錄儀,通過驗證孔將32根熱電偶插入蒸汽滅菌柜中。將待滅菌物品按規定的裝載方式擺放入腔室,同時將16根熱穿透熱電偶放在待滅菌物品中,具體的裝載方式和溫度探頭分布見圖1-圖4。再將15支熱分布熱電偶按幾何分布在腔室內(見圖5),熱電偶位置離腔室壁、地和頂不少于5 cm,不接觸腔室表面或架子。在蒸汽滅菌柜主控溫度探頭附近布置1支熱分布熱電偶。
判定標準:滅菌程序結束后進行結果判定,在滅菌暴露期間,所有熱分布熱電偶溫度都在設定點-1.0℃~+3.0℃范圍內,滅菌器主控溫度探頭的顯示溫度和附近熱電偶溫度差值在±1.0℃內,在滅菌階段所有的熱穿透熱電偶的標準滅菌時間(F0)≥18 min,提示滅菌器在規定的裝載方式和滅菌條件下滿足滅菌要求。
(5)微生物挑戰試驗
方法:將待滅菌物品按規定的裝載方式擺放,將生物指示劑按滿載熱穿透試驗所測試的每個點位的物品中放置1份生物指示劑(見圖1~圖4)。按照設定的滅菌程序進行滅菌操作,結束后將經過挑戰的生物指示劑和陽性對照(同批次未經滅菌的三份生物指示劑)同時在55℃~60℃下培養24 h。
判定標準:經滅菌挑戰后的所有嗜熱脂肪芽孢桿菌芽孢指示劑管內顏色呈現紫色(說明書給定滅菌后的合格顏色),即為培養陰性(-),且陽性對照管內的生物指示劑顏色不變(黃色),可判定滅菌效果合格。若被挑戰的生物指示劑有1支或多支指示劑的管內培養液仍為黃色,則判定滅菌效果驗證失敗。
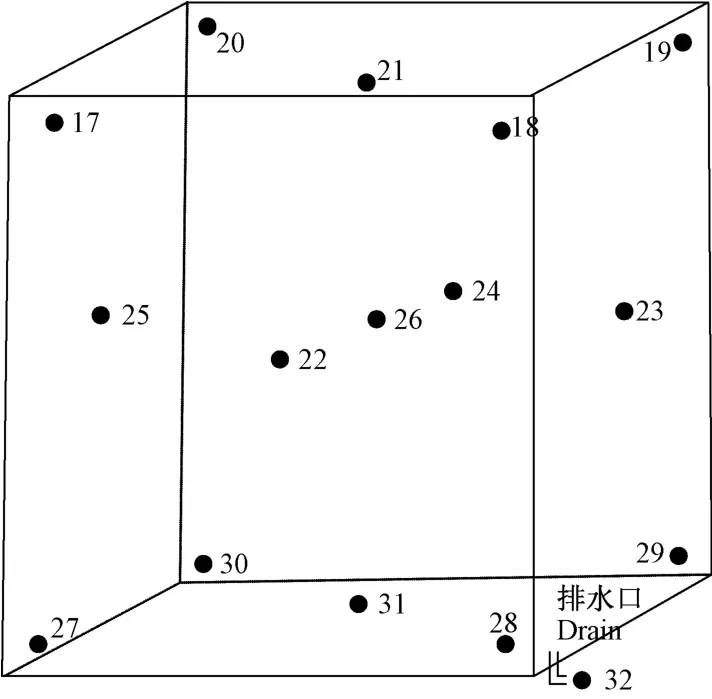
注:17~32:熱電偶布點。圖5 熱分布熱電偶布點圖Note.17~32,TC distribution points.Figure 5 Thermocouple placement of chamber heat distribution
(6)無菌試驗
方法:在滅菌結束后,分別抽取各裝載籠盒中的墊料和飲水送至本公司質量檢定部(QC)進行無菌試驗[7],采用硫乙醇酸鹽流體培養基和胰酪大豆胨液體培養基直接接種培養法,接種后的硫乙醇酸鹽流體培養基在30℃~35℃培養箱中培養14 d,接種后的胰酪大豆胨液體培養基在20℃~25℃培養箱中培養14 d。
判定標準:所有接種培養基的樣品在培養14 d后均無菌生長,則判定無菌驗證通過,若有1例樣品長菌則視為驗證失敗。
2 結果
2.1 真空保壓試驗結果
真空保持15 min后,真空檢測終點壓力與起點壓力之差≤2 KPa,保壓試驗合格(見表1)。
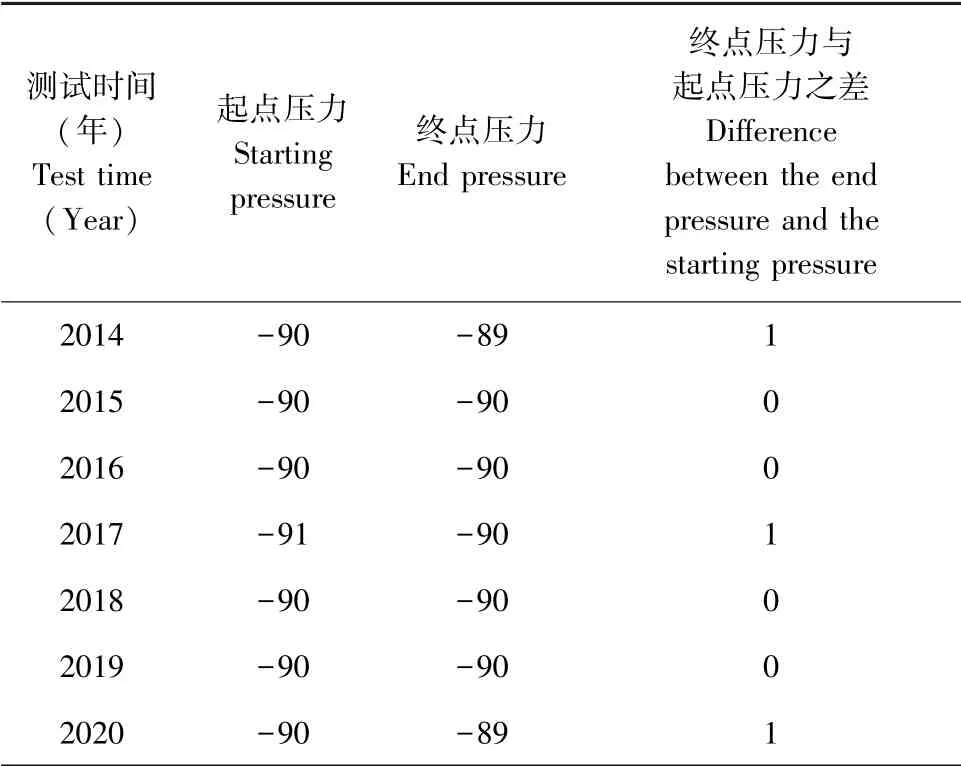
表1 真空保壓試驗結果(KPa)Table 1 Results of vacuum pressure holding test
2.2 B-D試驗結果
在完成滅菌操作后,取出測試包打開觀察B-D試紙。2014-2020年的B-D測試結果均是:試紙顏色變成黑色且顏色分布均勻,提示脈動真空滅菌器能夠排除冷空氣99%以上,滅菌器的真空性能試驗合格(見圖6)。
2.3 空載熱分布試驗結果
在完成每個滅菌周期后讀取溫度記錄儀。數據顯示(見表2),2014-2020年的驗證測試中,兩種循環在滅菌過程中,滅菌器主控溫度探頭顯示溫度和附近熱電偶溫度差值均在±1.0℃內,所有熱分布熱電偶溫度都在設定點0℃~+3.0℃范圍內,所有的熱電偶的溫度與同一時刻的溫度平均值的差值在±1℃范圍內,空載熱分布試驗合格。
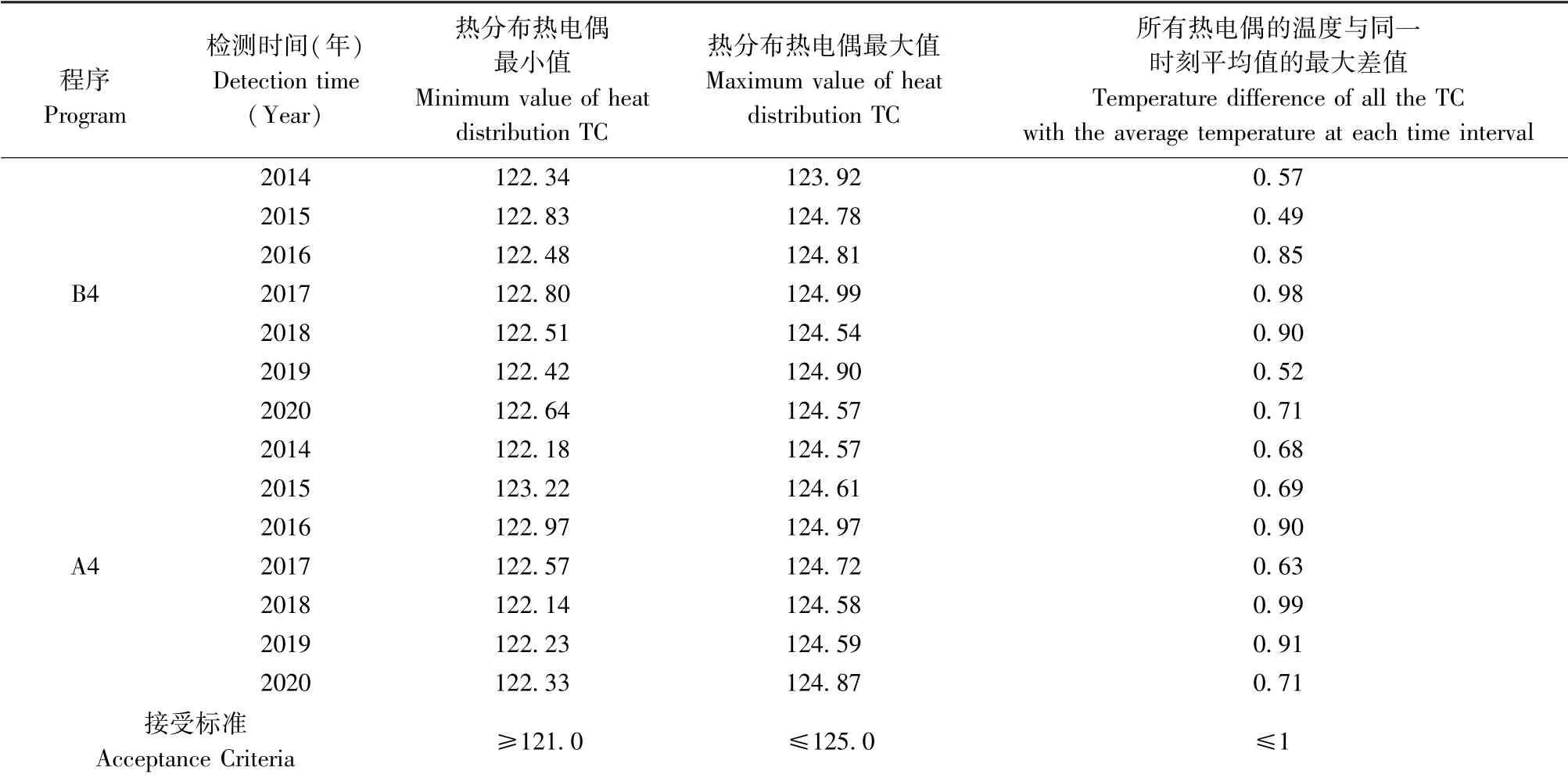
表2 空載熱分布測試結果(℃)Table 2 Results of empty chamber heat distribution test
2.4 滿載熱分布/熱穿透/微生物挑戰試驗結果
按規定的裝載方式進行裝載,并運行相應滅菌程序。滅菌程序結束后讀取溫度記錄儀,數據顯示(見表3),在滅菌暴露期間,2014-2020年的驗證測試中所有熱分布熱電偶溫度都在設定點-1.0℃~+3.0℃范圍內,滅菌器主控溫度探頭顯示溫度和附近熱電偶溫度差值在±1.0℃內,所有熱穿透熱電偶的F0值≥18 min,滿載熱分布試驗合格、熱穿透試驗合格。
滅菌程序操作完成后,取出所有被挑戰的生物指示劑觀察顏色并同陽性對照一起在55℃~60℃下培養24 h。被滅菌后的生物指示劑管內顏色呈現紫色,與說明書判定合格顏色一致,為培養陰性(-),同時陽性對照管內的生物指示劑顏色不變,說明55℃~60℃培養24 h后無細菌生長,微生物挑戰試驗合格(見表3)。
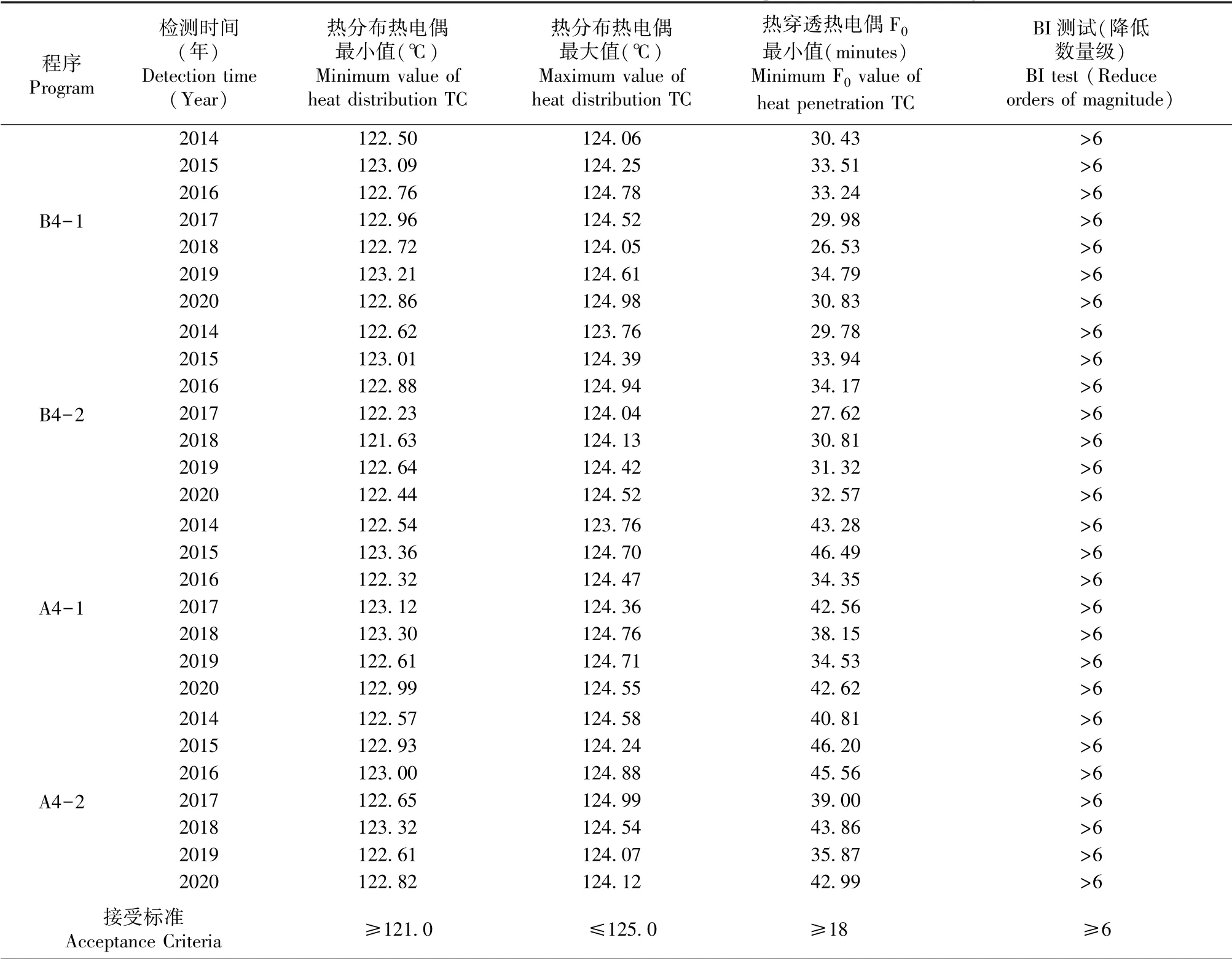
表3 負載熱分布/熱穿透/微生物挑戰測試結果Table 3 Results of loaded chamber heat distribution/Heat penetration/BI challenge test
2.5 無菌試驗結果
墊料和飲水在接種硫乙醇酸鹽流體培養基和胰酪大豆胨液體培養基后,放置在規定溫度培養14 d后觀察細菌生長情況。2014-2020年的無菌試驗結果均是:兩種培養基中均沒有菌落生長,無菌試驗合格。

注:a:滅菌前,b:滅菌后。圖6 B-D試紙滅菌前后變化Note.a,Before sterilization.b,After sterilization.Figure 6 Changes of B-D test paper before and after sterilization
3 討論
為保證高壓蒸汽滅菌物品的滅菌質量[8],滅菌后還需采取適當方法進行滅菌效果的驗證[9]。設備的驗證和裝載方法的驗證要定期化和常態化并且符合設備驗證的工藝要求[10]。本臺真空滅菌器從2010年啟用以來,每年均進行驗證。在設備的首次驗證及2014年之前的再驗證中,對每一種程序和裝載的滅菌性能,都采取了測試3次的策略,測試結果均符合標準、驗證合格。根據2010-2013年所積累的設備驗證及運行數據,決定從2014年開始,每年對真空滅菌器的歷史信息進行回顧性評估:收集、匯總、分析滅菌柜的驗證與再驗證情況、去年一年的運行情況、校準情況、變更情況以及維護保養情況確認設備運行穩定,從而確認該滅菌器本年度再驗證活動中采取的裝載運行次數,確認2014年到2020年驗證測試中每種程序裝載每年均測試1次。
對實驗動物籠盒、墊料、飲水等進行高壓滅菌,各研究采用的滅菌溫度、滅菌時間、墊料包裝方式等均有所不同[11-13],但通常溫度121.3℃,穩定持續1200 s即可殺死細菌的繁殖體及芽孢,達到滅菌效果[14]。本研究根據所需滅菌物品的具體特點,對于非液體類的物品采用122℃、1200 s的滅菌條件,墊料分裝到籠盒中,籠盒使用重疊法;液體類飲水122℃、1800 s的滅菌條件進行滅菌程序試驗。試驗結果顯示,不僅安全性能得到保障,而且非液體類物品滅菌效果合格、可靠,重疊籠盒(墊料)全部達到滅菌條件,干燥效果好,液體類飲水滅菌效果合格、可靠、液體損失量小。
單一品種物品的滅菌無論是滅菌過程還是滅菌程序的驗證都相對容易和簡單,但SPF金黃地鼠在飼養過程中所需要的物品種類較多,飼養籠盒及飲水瓶規格均不同,故本研究根據被滅菌物品的特性采用按照固定的多種物品組合裝載的方法進行滅菌。通過滅菌器的性能驗證、微生物挑戰試驗和無菌試驗,結合蒸汽滅菌的兩大基本要素,即作用時間、滅菌溫度[15],所有試驗結果表明各種SPF金黃倉鼠籠具及不同規格動物飲水在規定的裝載方式和滅菌條件下進行脈動真空滅菌驗證合格,且符合現行GMP關于對滅菌法的要求。不僅證明了本臺脈動真空滅菌器設備本身的可靠性,關鍵是對裝載方式和滅菌程序進行了驗證,保證了滅菌效果的有效性[7],為屏障設施安全與正常運行提供有力保障。因此,在日常工作中就必須嚴格按照驗證過程中的物品包裝方式和裝載位置進行包裝和裝載,嚴格按照驗證的裝載滅菌程序進行滅菌,以保證滅菌的有效性和均一性[16]。如果滅菌物品種類、裝載位置、或滅菌條件發生改變必須重新做滅菌效果驗證[17]。驗證后在日常生產中的每次滅菌也必須對各項參數和F0值進行監測[18]。

