試值代入法計算鹽水溶液的pH值
郝紹鵬
(金堆城鉬業股份有限公司化學分公司,陜西渭南,714000)
在教學、科研和化工生產中經常需要計算鹽水溶液的pH值,在已知各平衡常數和溶質濃度計算pH值時,通常采用消元整理后解關于[H+]一元高次方程。由于目前沒有精確表達高次方程根的方法,計算方法主要分為兩大類:一類是在解方程前先進行近似處理,然后由簡化的近似求解公式求解的粗略計算[1,2];另一類是依托高次方程使用二分法、迭代法等并借助計算機進行精確計算[3,4]。近似公式求解采用了近似處理前置的處理方式,在缺乏大量實驗數據印證的情形下,無法評估其計算結果的偏差。二分法、迭代法進行精確計算時,將化學問題高度抽象成數學運算,不易感知計算過程與化學原理之間的聯系,同時采用此類方法需要較高的數學邏輯認知或專業軟件輔助,在實際應用中也不易實施。
若將[H+]也看作是已知值,代入所有過程等式,則各等式應全部成立。此時的計算過程是一組數字簡單、大量的混合運算以及數量比較,不再涉及復雜的高次方程解法。
1 計算原理
1.1 主要運算式
設有正鹽或酸式鹽MzZm的水溶液體系,堿離子Mm+進行n級水解,強堿鹽n=0,弱堿鹽n=m;陰離子Zz-全部以Xx-、Yy-及其水解產物的形式存在,Yy-發生y級水解;Xx-發生a級水解,同多酸根體系a=x,體系無同多酸根a=0;Xx-、Yy-、Zz-中特征元素原子個數分別為s、t、r(如碳酸根、碳酸氫根中的碳元素)。建立其物料平衡式(MBE)和電荷平衡式(CBE),并將兩式中的各平衡濃度用[Xx-]、[Yy-]、[H+]表示,整理出方程組及其解的表達式;建立[Xx-]、[Yy-]之間關系式的通式(以下簡稱試算式)。如圖1。

圖1 主要算式及說明
對于給定的鹽,各參數和試算式確定。各平衡常數和溶質濃度已知時,每試選一個[H+]的猜測值,可算出方程組的解,代入試算式中可算出k的一個試算值(為了避免混淆,稱平衡常數k的實際值為目標常數,試值代入計算所得的k值稱為試算值)。與目標常數最接近的試算值所對應的[H+]猜測值,即為所要計算的氫離子平衡濃度,進而算得pH值。
1.2 試值選擇
分組選取pH值實現對[H+]的試值選擇。選取p組pH值,各組內pH值為等差數列,各組的公差依次減小且成等比數列,公比為1/q。第二組及其后各組均有2q-1個pH值,最后一組的公差小于所需精度,第一組結合第二組使全部選值可覆蓋pH值1至14。從第一組開始依次代入計算,選取最接近目標常數的試算值對應的pH值,作為后一組pH值的中位數。
第一組在理論pH值附近捕獲一個節點,其后各組在捕獲的節點附近提高計算精度并逼近理論值。上述選值中的重復取值,是為了便于文字描述和電子表格編輯,實際應用中可合理避免。
2 計算的實現
使用EXCEL電子表格作為工具,對水解不高于7級、pH值1至14范圍內的體系進行計算,計算流程、中間輔助計算值、主要函數公式見圖2。圖中指數差指試算值常用對數與目標常數常用對數的差的絕對值;獲得計算結果與獲取中位數所用函數相同,改變其計算單元格范圍即可。
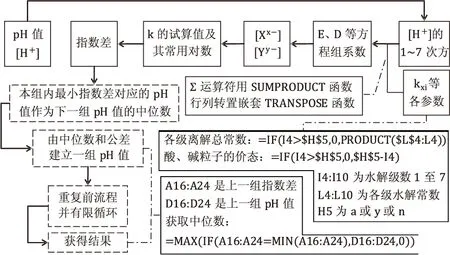
圖2 軟件計算流程示意圖
3 計算示例
示例中第一組9個pH值,中位數為7,公差1.458;各組公差之間的比例為3,共8組;pH值精度±0.000667。
3.1 同多酸鹽計算示例
鑒于同多酸鹽在水溶液中的平衡狀態比較復雜,這里將(NH4)6Mo7O24水溶液體系視為僅有兩種同多酸根,以此為模型介紹同多酸鹽水溶液pH值的計算,參數設置和水解見表1[5,6]。對1mol/l、0.1mol/l、0.01mol/l、0.001mol/l、0.0001mol/l(NH4)6Mo7O24水溶液pH值的計算結果分別約為5.855、5.461、5.045、4.614、4.26。

表1 同多酸鹽水解
3.2 正鹽、酸式鹽計算示例
分別以Na3PO4、Na2HPO4、NaH2PO4水溶液pH值的計算為例,參數設置和水解見表2[6],計算結果見表3[1]。

表2 正鹽、酸式鹽水解
計算多元弱酸正鹽和酸式鹽水溶液的pH值,不僅可以獲得相對精確的結果,而且從計算過程可以觀察到一些現象。如表2中三種鹽的參數設置只有z(陰離子價態)不同,結合表3數據可知,濃度相同時,參數z的變化引起計算結果的變化。再如表3中,比較指數差可以發現,在相同精度內,NaH2PO4的指數差明顯較大;通過增加計算行提高計算精度,pH值精度達到約±3.76×10-9時,指數差分別為0.03(1mol/l)、0.06(0.01mol/l)、0.003(0.0001mol/l)。
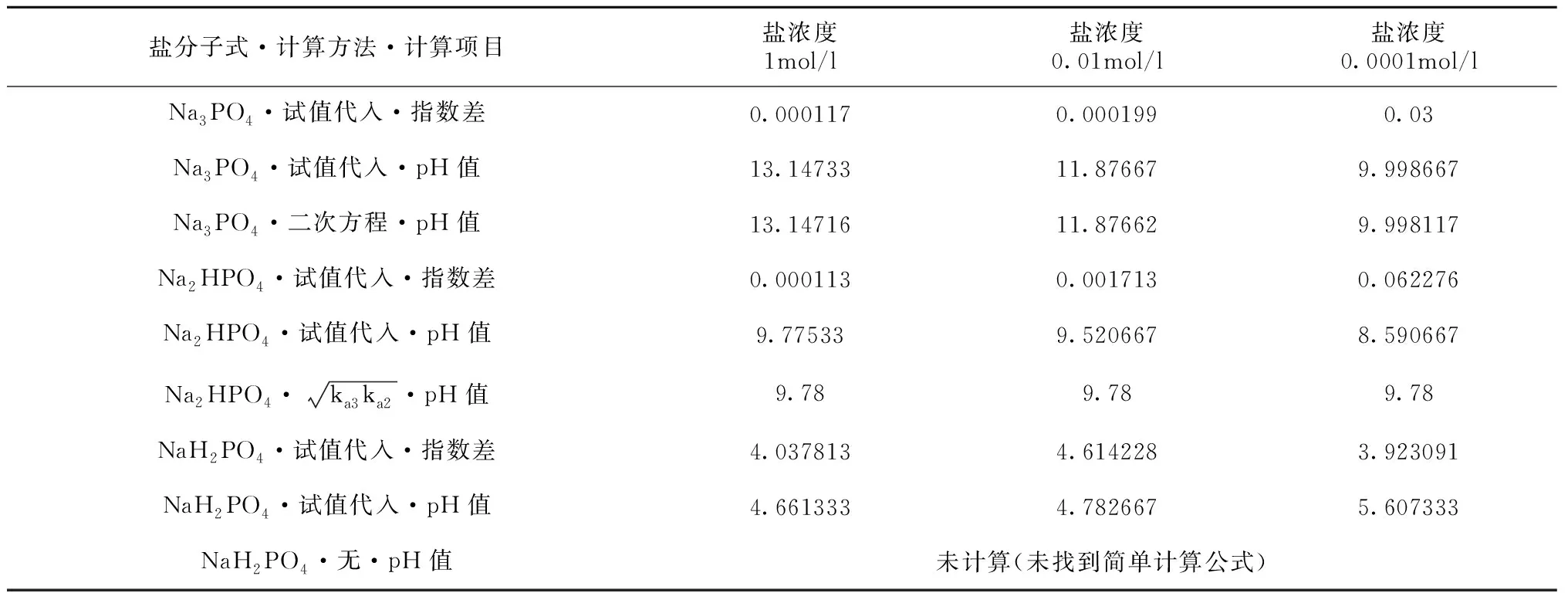
表3 正鹽、酸式鹽水溶液pH值計算對比
4 總結與結論
試值代入法為計算pH值提供了一種新的思路,將推導高次方程求根公式的難點轉化為大量簡單計算,再利用電子表格實現求值,獲得了良好的效果。
此方法計算范圍廣泛,可以完整地實現對正鹽、酸式鹽水溶液pH值的計算,可以嘗試對同多酸鹽水溶液pH值的計算。雖然在電子表格中的編輯和設置比較復雜,需要足夠的耐心和細致;但此方法的過程原理簡單,且可用日常辦公軟件實施,不需要高深的理論知識和專業軟件即可實現對pH值的高精度計算,仍然適用于廣大教學和技術研究人員使用。
除計算結果在所需精度內做近似處理外,計算過程中不做其他近似,完整考慮了水的離解和酸堿的各級水解,使計算結果獲得較高的精度。且從過程中可觀察到一些現象,如陰離子價態對pH值計算結果有影響;觀察指數差用以評估偏差等。

