分析化學經典內容是培養本科生創新能力的源泉
陳永雷,呂文娟,陳宏麗,陳興國
蘭州大學化學化工學院,蘭州 730000
分析化學經典內容是分析化學的核心,是分析化學長期科學研究和高水平應用成果的結晶,蘊含了豐富的創新思維和創新途徑,認真學習、熟練掌握和深刻理解這些內容對于培養本科生的創新思維和創新能力十分重要。分析化學的新理論、新方法、新技術和新應用對培養本科生的創新思維和創新能力同樣有著重要的作用。因此,采取卓有成效的方式講授分析化學經典內容、適時引導學生了解分析化學前沿領域和創新性研究成果,激發本科生創新思維、培養本科生創新能力,是分析化學課堂講授必須解決的重要問題之一[1]。為了解決這一問題,我們在長期的教學過程中進行了不懈的探索和實踐,結合分析化學經典內容的講授,以學生易于接受并有利于培養他們創新能力的方式將分析化學的新理論、新方法、新技術和新應用及時引入課堂,并鼓勵學生在學習中積極運用這些知識提高自身的創新能力,取得了良好效果。下面將通過實例進行介紹。
1 通過使極弱酸強化實現其準確滴定和Kjeldahl法測定蛋白質的講授培養本科生的創新思維和創新能力
通過某些特定的化學反應可使極弱酸強化以實現用強堿對其進行準確滴定的目的,現行分析化學教材中常以在水溶液中滴定硼酸(H3BO3)為例介紹本部分內容。由于H3BO3的解離常數很小(pKa=9.24),無法用強堿(如NaOH)標準溶液在水溶液中直接滴定,但基于其可與某些多元醇如甘露醇絡合而被強化,生成的甘露醇酸用酚酞作指示劑可通過NaOH標準溶液直接滴定。在講授這部分內容時,我們從分子結構出發仔細剖析甘露醇能使H3BO3強化的原因,引導學生認識到其本質是由于硼原子與甘露醇分子中的鄰二羥基絡合形成了穩定的絡離子所致(圖1)。
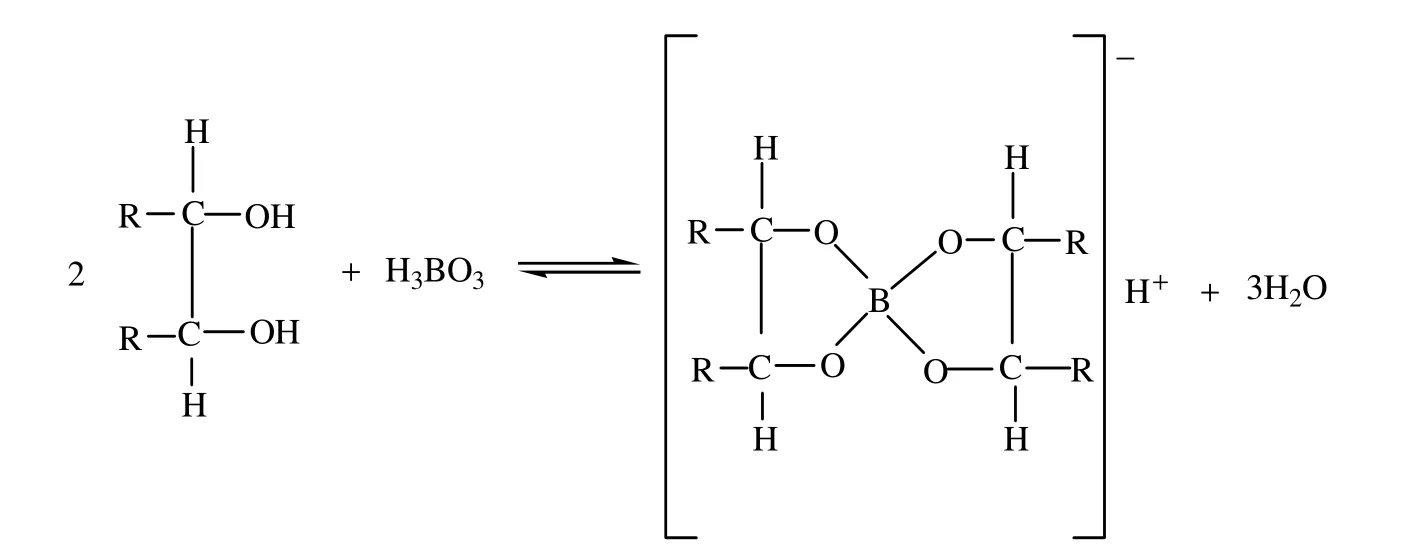
圖1 H3BO3與甘露醇的絡合反應[2]
進而我們啟發學生思考,能否將硼原子與甘露醇分子中的鄰二羥基絡合形成穩定絡離子的性質用于分析化學其他領域如手性藥物的分離,并要求通過查閱文獻回答這一問題。通過文獻調研,學生發現確實可以利用這一性質通過L-酒石酸二丁酯和硼酸緩沖液反應原位合成L-酒石酸二丁酯-硼酸絡合物手性選擇劑(圖2),使用該手性選擇劑建立的毛細管電泳方法可較好地實現普羅帕酮、布拉洛爾、普萘洛爾、阿普洛爾、丙萘洛爾、托利洛爾、吲哚洛爾、氧烯洛爾、比索洛爾、美托洛爾等十對手性藥物對映體的分離[3]。
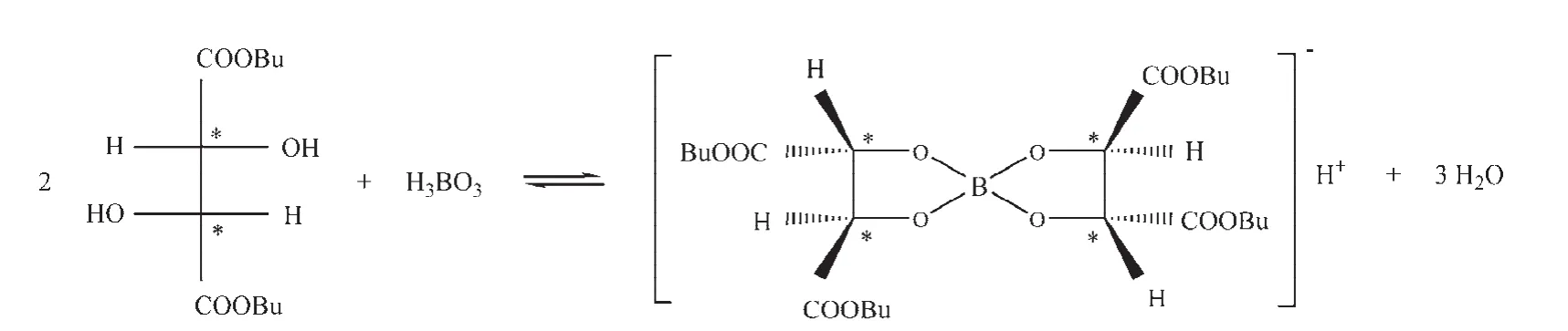
圖2 L-酒石酸二丁酯和硼酸的反應[3]
類似地,L-酒石酸二異丁酯分子中也有兩個相鄰的羥基,也可以和硼酸發生反應生成絡合物手性選擇劑L-酒石酸二異丁酯-硼酸,以其為手性選擇劑建立的毛細管電泳方法也可實現上述十對手性藥物對映體的分離[4]。
蛋白質是食品的重要組分之一,準確測定其含量對于食品安全是十分重要的。現有分析化學教材中介紹的測定蛋白質含量的方法主要是Kjeldahl法。我們在講授Kjeldahl法時,在介紹了其測定蛋白質含量的原理后,要求學生指出該方法存在的主要問題。學生經過思考和討論后認為該方法的主要問題是僅能測定食品中氮的含量而無法確定氮的來源,有可能給食品安全問題留下隱患。在“三聚氰胺”事件曝光后,我們要求學生思考如何測定食品如乳制品中非法添加的三聚氰胺的含量以確保食品中源于奶類的蛋白質含量測定的準確性。學生通過查閱文獻后發現,利用毛細管電泳技術不僅能在30 min內完成牛奶、酸奶、全脂奶等乳制品中三聚氰胺含量的測定,而且結果完全滿足國家標準[5]。
2 通過金屬離子指示劑的講授培養本科生的創新思維和創新能力
金屬離子指示劑(In)是絡合滴定的主要內容之一,迄今為止使用的金屬離子指示劑是基于In與被滴定金屬離子(M)反應形成與In本身顏色不同的絡合物(MIn)并使被滴定溶液呈現MIn的顏色。當滴入EDTA (Y)時,游離的M被逐步絡合。在化學計量點附近,MIn中的In被Y取代使In游離出來,溶液呈現In的顏色,指示終點已到達。由此可知,In的結構、性質等對指示劑的性能有著決定性的影響。現有的金屬離子指示劑雖然能滿足絡合滴定分析的要求,但仍存在封閉和僵化等現象。因此,在講授金屬離子指示劑時,我們要求學生在掌握其基本內容的基礎上思考近年來出現的新材料,如納米材料是否可以用作絡合滴定的指示劑。學生通過查閱文獻發現,離子選擇性納米球不僅可以用作絡合滴定的指示劑,而且其指示終點的原理與金屬離子指示劑在本質上是相同的,此外該指示劑放置一周后仍能很好地指示滴定終點(圖3)[6]。應指出的是,與傳統的絡合滴定法相比,以離子選擇性納米球作指示劑的絡合滴定法的選擇性更高。
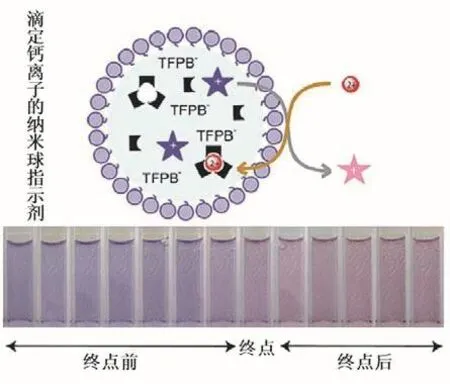
圖3 用于鈣離子滴定的納米球指示劑及滴定過程中溶液顏色的變化[6]
3 通過晶型沉淀形成過程的講授培養本科生的創新思維和創新能力
迄今為止,關于晶型沉淀的形成,一般認為在沉淀過程中構晶離子首先在過飽和溶液中形成晶核,然后進一步成長為按原定晶格排列的晶型沉淀。由此可知,通過合適的方式在溶液中形成數量適宜的晶核對于形成晶型沉淀是十分必要的。鑒于此,在講授沉淀形成的過程時,我們積極引導學生深入思考新型納米材料如金屬有機框架材料的形成過程,以培養學生的創新能力。學生查閱文獻后發現,通過在溶液中形成數量適宜的晶核不僅是制備金屬有機框架材料的方法之一,而且還可以制備具有手性的金屬有機框架材料[7–10]。進一步,我們鼓勵學生嘗試將這種方法用于制備手性涂層毛細管并考查它們在手性物質分離中的應用(圖4)。學生通過實驗,以ZnO納米顆粒為成核試劑成功制備了手性MOF [Zn(s-nip)2]n涂層毛細管,并以此為分離通道建立了分離單胺類神經遞質腎上腺素、異丙腎上腺素和脫氧腎上腺素對映體,麻黃堿和偽麻黃堿,硝基酚同分異構體,雙酚A類似物的開管毛細管電色譜新方法[11]。
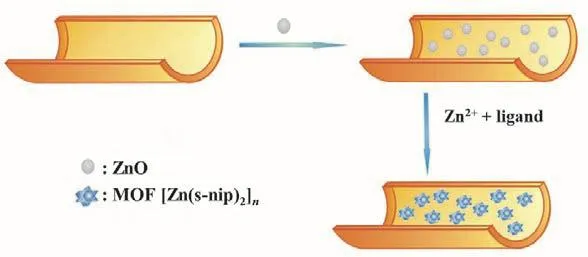
圖4 以ZnO為成核試劑制備手性MOF [Zn(s-nip)2]n涂層毛細管的過程[11]
眾所周知,通常都是在不斷攪拌下把沉淀劑緩慢加入溶液獲得沉淀,但這樣操作難以避免在沉淀劑加入瞬間出現的局部過濃現象。為解決這一問題,人們發展了均勻沉淀法以獲得完整的晶體沉淀。在講授過程中,我們要求學生思考能否將這種方法用于制備納米材料。學生通過查閱文獻發現,以硝酸鋅為原料、尿素為沉淀劑,基于反應溫度超過70 °C時尿素不斷發生水解產生的氨均勻分布于溶液中使得OH-濃度逐漸增大的現象,實現了在整個溶液中均勻生成氫氧化鋅沉淀的目的,而后經過洗滌、干燥、煅燒,即可得到20–80 nm的氧化鋅納米粉體[12]。
4 通過顯色劑的講授培養本科生的創新思維和創新能力
吸光光度法是分析化學經典內容之一。事實上,吸光光度法的發展和應用主要取決于新型顯色劑的發展。眾所周知,近十多年來,納米材料和納米科技有了突飛猛進的發展,許多性質優異的納米材料不斷涌現,這些材料可否作為顯色劑或顯色反應的催化劑用于建立新的靈敏度高、選擇性好的吸光光度法呢?基于此,我們在講授顯色反應和顯色劑的基礎上鼓勵學生深入思考這一問題并大膽探索將納米材料用作顯色劑或顯色反應的催化劑發展新的吸光光度法。學生經過查閱文獻發現,Fe3O4磁性納米顆粒具有類過氧化物酶的性質,可用于催化過氧化氫(H2O2)與2,2-連氮-雙(3-乙基苯并噻-6-磺酸)磷酸氫二銨鹽(2,2’-azino-bis (3-ethylbenzo-thiazoline-6-sulfonic acid) diammonium salt,ABTS)之間的氧化還原反應形成有色化合物[13]。利用Fe3O4磁性納米顆粒這一性質和三聚氰胺(C3H6N6)與H2O2形成包合物C3H6N6·H2O2降低了體系中H2O2的含量,導致生成的氧化態ABTS濃度降低、溶液顏色變淺的現象(圖5),建立了一種簡單、快捷、準確、無需復雜設備的測定乳制品中微量三聚氰胺的Fe3O4磁性納米顆粒吸光光度法[14]。
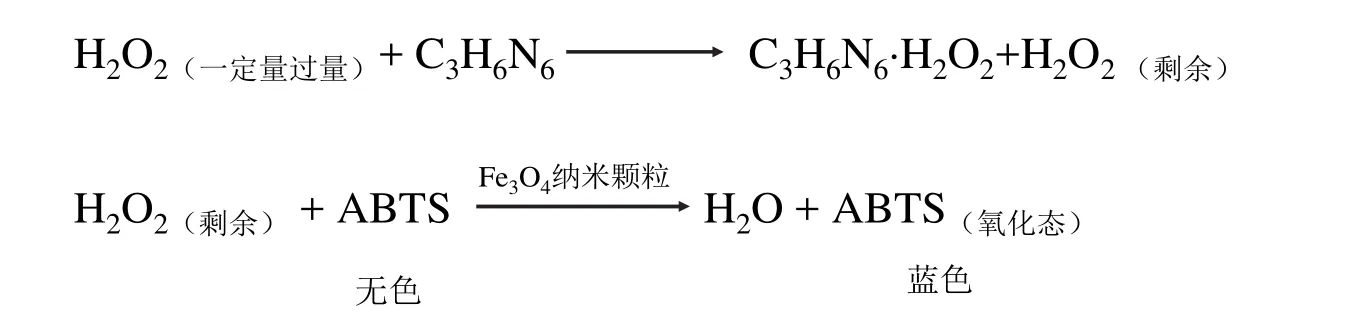
圖5 以Fe3O4納米顆粒為催化劑檢測三聚氰胺的原理[14]
在此基礎上,我們進一步啟發學生思考除了Fe3O4磁性納米顆粒外其他含有金屬的納米顆粒是否也可能具有類過氧化物酶的性質?學生思考后認為鐵酸鹽應該具有這種性質。而后通過實驗制備了ZnFe2O4磁性納米顆粒并發現其確實具有類過氧化物模擬酶性質。在此基礎上,利用ZnFe2O4磁性納米顆粒的這種性質建立了一種可視化檢測葡萄糖的新方法并將其成功用于糖尿病患者尿液中葡萄糖的測定[15](圖6)。進一步制備了MgFe2O4、NiFe2O4、CuFe2O4三種鐵酸鹽磁性納米顆粒并研究了其過氧化物模擬酶的性質,并基于NiFe2O4磁性納米顆粒的類過氧化物酶的性質建立了可視化測定尿液中葡萄糖的吸光光度新方法[16]。
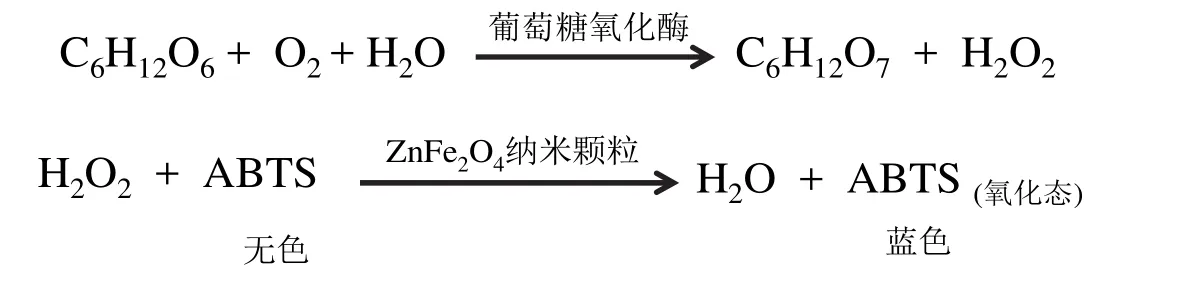
圖6 以ZnFe2O4納米顆粒為催化劑檢測葡萄糖的原理[15]
長期的教學實踐表明,這種講授方式深受學生歡迎,大家普遍反映這種講授方式不僅能使他們深刻地掌握并理解分析化學的經典內容和內涵,而且能強烈地激發他們的創新欲望和創新思維,對培養他們的創新能力起到了顯著的作用。學生還特別指出,這種講授方式使他們了解并初步掌握了開展創新性科學研究特別是分析化學創新性研究的選題、方案制定和實施、論文撰寫的方法和技能,為他們成功申請并高質量完成各類研究項目、取得具有一定創新性的研究結果奠定了堅實的基礎。
5 結語
從上述實例可以看出,分析化學經典內容不僅是分析化學的核心內容,而且是激發本科生創新思維、培養本科生創新能力的源泉。因此,在講授分析化學時,不能機械地、靜態地介紹這些內容,而應引導學生認真思考、發現與它們相關的分析化學的新理論、新方法、新技術和新應用,積極探究它們所包含的科學內容和創新思想,以此激發學生的創新思維,培養他們的創新能力,為他們今后進行創新性科學研究奠定堅實的基礎。

