多發性骨髓瘤合并腎損傷的實驗室特征
曲璟 肖斌 李林海 曾濤,3
1南方醫科大學南方醫院檢驗科(廣州510515);2中國人民解放軍南部戰區總醫院檢驗科(廣州510010);3廣東醫科大學附屬醫院醫學檢驗科(廣東湛江524001)
多發性骨髓瘤(multiple myeloma,MM)是一種惡性漿細胞疾病,常引起多種臨床并發癥,如貧血、骨損害、高鈣血癥、感染、腎損傷等。其中,比較常見的并發癥是腎功能不全。近年來,有研究報道,合并腎損害的MM 患者終末期腎病發生率及病死率均高于腎功能正常的MM 患者,且預后更差[1]。其中,由管型腎病導致的急性腎損傷是MM 的醫療急癥,具有較高的病死率[2]。現實驗室檢驗中多采用血清肌酐(creatinine,Cr)和肌酐清除率作為腎功能指標,但它們對腎功能的早期損害敏感度低[3]。目前較多研究證明實驗室指標與患者預后相關,與腎功能損傷的研究較少。因此,本研究通過進一步分析我院154 例MM 患者的臨床數據資料,探究影響腎臟損傷危險因素,以指導臨床早期干預。
1 資料與方法
1.1 病例資料 收集2018年6月至2021年3月南方醫科大學南方醫院及南部戰區總醫院血液內科收治的初診MM 患者的臨床資料。本研究共收集了157例MM患者臨床資料,其中男89例,女68例,年齡(60.28±9.92)歲。納入標準:(1)符合國際骨髓瘤工作組的最新診斷指標,且臨床資料完整;(2)未患有其他惡性腫瘤;(3)無其他血液相關疾病;(4)既往無腎損傷疾病,未進行相關性治療;(5)未接受化療及其他治療。
1.2 資料 根據國際骨髓瘤工作組的腎損傷的診斷標準:肌酐清除率<40 mL/min,或血清Cr>177 μmol/L,將患者分為兩組:合并腎損傷的MM 患者組與未合并腎損傷的MM 患者組。收集記錄患者的年齡、性別、Ig 分型、輕鏈類型、DS 分析、國際分期系統(ISS)分期等基本資料及相關實驗室檢查:總膽紅素(TBIL)、直接膽紅素(DBIL)、總蛋白(TP)、白蛋白(ALB)、球蛋白(Glo)、谷丙轉氨酶(ALT)、尿酸(UA)、Cr、尿素氮(BUN)、鈣離子(Ca)、β2?微球蛋白(β2?MG)、紅細胞(RBC)、血紅蛋白(Hb)、白細胞(WBC)、中性粒細胞(NEUT)、淋巴細胞(LYMPH)、單核細胞(MONO)、中性粒細胞/淋巴細胞(neutrophil/lymphocyte ratio,NLR)、血小板(PLT)、血小板/淋巴細胞(platelet/lymphocyte ratio,PLR)等指標。由于MM 患者較易出現血清白蛋白降低,影響鈣離子的檢測,本研究采用校正鈣離子(Calcium?Calibration),校正公式為:校正血清鈣(mmol/L)=血清總鈣(mmol/L)? 0.025×血清白蛋白濃度(g/L)+1.0。
1.3 統計學方法 用SPSS 25.0 軟件分析數據。正態分布計量資料用(±s)表示,t檢驗分析比較;非正態分布用M(P25,P75)表示,Mann?WhitneyU檢驗;計數資料采用χ2檢驗,相關分析采用Spearman分析,危險因素分析采用二元logistic 回歸分析,P<0.05 具有統計學意義。
2 結果
2.1 臨床資料分析 共納入MM 患者157 例,男89 例(56.68%),女68 例(43.32%),年齡(60.28 ±9.915)。其中以Cr 升高、蛋白尿、夜尿增多為首發癥狀的有30 例,腎損傷發生率為19.11%。根據Cr > 177 μmol/L 分為腎損傷組30 例(19.11 %)和非腎損傷組127 例(80.89 %)。腎損傷組年齡為(61.73 ± 11.432)歲;男19 例(63.33 %),女11 例(36.67%);IgG 型、IgA 型及其他類型(輕鏈型+IgD)分別為10 例(33.33%)、7 例(23.33%)和13 例(43.34%),κ 輕鏈15 例(50.00%),λ 輕鏈15 例(50.00%),DS?Ⅲ期為30 例(100%),ISS?Ⅲ期為30例(100%)。非腎損傷組年齡為(59.94±9.540)歲,男70 例(55.11%),女57 例(44.89%),IgG 型為74 例(58.26%),IgA 型為32 例(25.19%),其他類型為21 例(16.55%),κ 輕鏈為80 例(62.99%),λ 輕鏈為47 例(37.01%),DS?Ⅰ+Ⅱ期為29 例(22.84%),DS? Ⅲ期為98 例(77.16%),ISS? Ⅰ+Ⅱ為67 例(52.75%),ISS? Ⅲ為60 例(47.25%)。腎損傷組的BUN、UA、β2?MG、校正鈣離子、WBC、NEUT、MONO、NLR 高于非腎損傷組,TP、Glo、ALT、RBC 低于非腎損傷組(P<0.05,表1)。
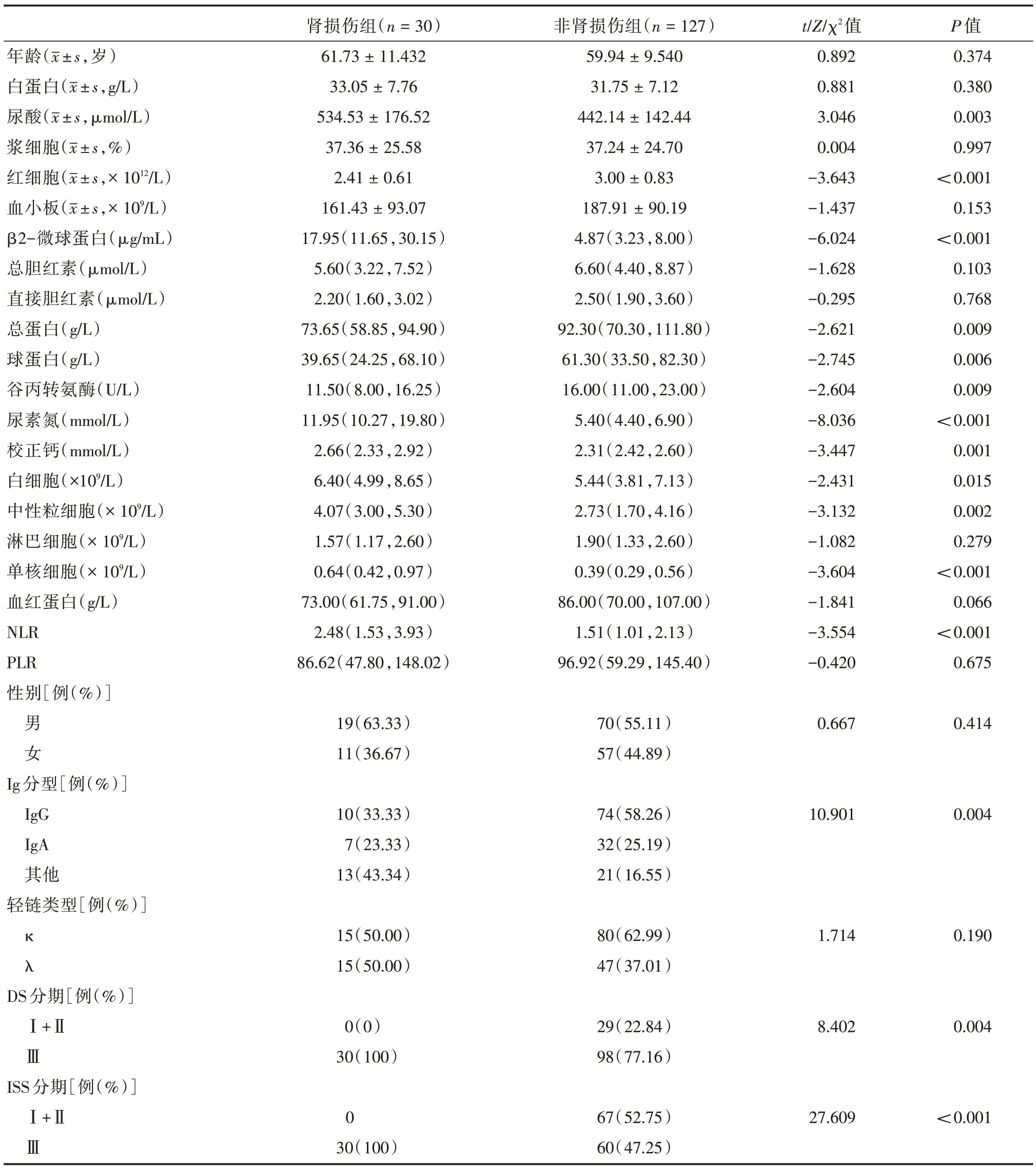
表1 MM 患者的臨床資料分析Tab.1 Clinical data analysis of MM patientsM(P25,P75)
2.2 腎損傷危險因素分析 對實驗室指標進行二元logistic 回歸分析,發現校正鈣離子升高(OR=5.174,95%CI:1.252~21.386,P=0.023)、β2?微球蛋白水平升高(OR= 1.209,95%CI:1.124 ~ 1.301,P< 0.05)、NLR 升高(OR= 1.691,95%CI:1.249 ~2.289,P< 0.05)為MM 合并腎損傷的獨立危險因素,見表2。
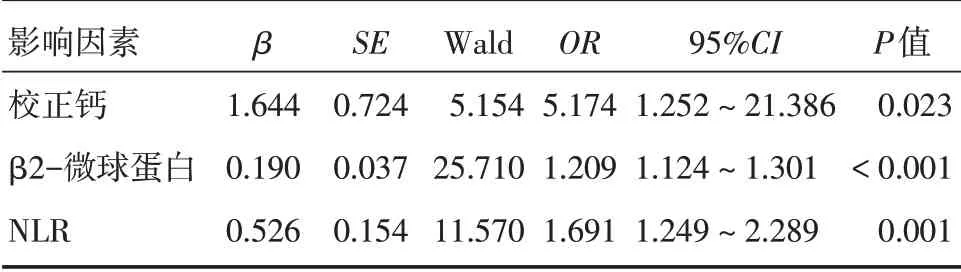
表2 校正鈣離子、β2?微球蛋白、NLR因素logistic回歸分析Tab.2 Calcium?Calibration,β2?microglobulin,NLR for logistic regression analysis
2.3 危險因素對MM 發生腎損傷的價值評估 通過獨立危險因素的ROC 曲線分析,結果β2?MG、校正鈣離子、NLR 具有較好的預測價值,進一步分析發現,三者聯合敏感度及特異度均較高,見表3、圖1。
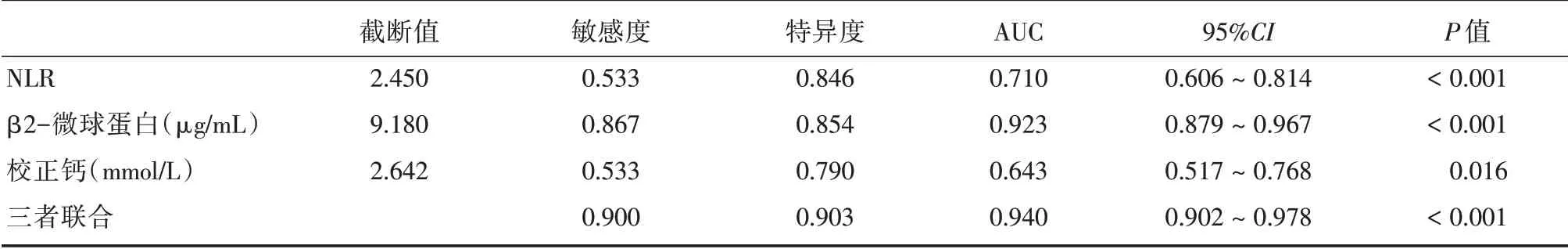
表3 危險因素校正鈣離子、NLR、β2?微球蛋白及聯合應用預測效能評價Tab.3 Evaluate the diagnostic efficacy of calibration calcium,NLR,β2?microglobulin and their combined application

圖1 危險因素校正鈣離子、NLR、β2?MG 及聯合應用ROC曲線分析Fig.1 Perform ROC curve analysis for calibrating calcium ,NLR,β2?microglobulin and their combined application
3 討論
腎損傷(renal injury,RI)是MM 的嚴重并發癥,被認為是預后的不良因素,COURANT 等[4]發現在以人群為基礎的研究中,24.6%的MM 患者出現RI(12.9%需要血液透析)。RI 患者中位生存期為21個月,RI是MM獨立危險因素[4]。本研究發現19.11%的新診斷MM 合并RI,可能為納入樣本較少及不符合標準的病例被剔除等原因。研究發現,MM 合并腎損傷以輕鏈型為主,骨髓瘤管型腎病通常會導致較嚴重的急性腎損傷,可能由于產生過量的單克隆輕鏈與Tamm?Horsfall 蛋白相互作用,導致輕鏈的沉積和遠端腎小管的堵塞[2,5]。多數MM 患者為輕度或中度RI,腎功能可恢復,腎臟恢復可延長患者生存時間,但嚴重的RI 患者,則需采用血液透析,快速診斷且及時抗骨髓瘤治療,可有助于腎臟恢復[6]。
本研究發現,腎損傷組與無腎損傷組MM 患者相比,UA、β2?MG、BUN、Ca、WBC、NLR 升高,球蛋白降低;通過logistic 回歸分析,發現鈣離子升高、β2?MG 升高、NLR 升高為MM 合并腎損傷的危險因素。目前較多研究發現,慢性炎癥與惡性腫瘤之間存在著密切的關系,為腫瘤的重要誘因,釋放大量的炎癥因子可損傷DNA,刺激細胞不斷增殖,促進血管和淋巴管的生成,刺激腫瘤細胞產生及惡化[7-8]。NLR 是炎癥指標,反應機體的免疫系統狀態,與多種惡性腫瘤的預后相關[9-11],劉春紅等[12]發現,高NLR 為MM 預后的獨立危險因素。LIU 等[13]發現,由NLR、RDW 和PLT 組成的炎癥預后評分指數在硼替佐米為主的化療時期對初步診斷的MM 患者的預后起著特定的作用。KIM 等[14]發現NLR、血小板計數及CRP 聯合可有效預測積極接受治療的MM 患者的生存期。除此之外,姜倩倩等[15]發現,NLR 可以作為MM 合并腎損傷的獨立危險因素,且具有較好的預測價值。蔣芬等[16]研究發現NLR 可以較好的預測重癥患者急性腎損傷的發生。目前NLR 在MM 的腎臟損方面的機制研究缺乏相關證明,需進一步的探究。本研究發現,NLR 可作為MM 患者合并腎損傷的獨立危險因素,其預測的敏感性卻只有0.533,可能為腎損傷組樣本量較少,需進一步擴大樣本量進行評估。
β2?MG由淋巴細胞等有核細胞分泌,參與體內免疫應答反應[17],體內合成增多或腎臟排出減少均會使血清β2?MG 增高。本研究顯示,Logistic 回歸分析發現β2?MG 可作為MM 的危險因素,可以較好的預測MM 患者是否合并腎損傷(AUC=0.946)。目前研究表明,β2?MG 相比血清Cr 和BUN 具有更好預測急性腎損傷的能力[3]。多項研究都已證實了β2?MG 在腎臟疾病中的重要指示性作用,根據β2?MG 和血清白蛋白計算的ISS 分期系統也是MM公認的預后評判標準[18-20]。β2?MG 可能為復發或難治性MM 患者硼替佐米治療預后的標志[21],其主要經腎臟進行排泄,與腎小球濾過率成負相關,為MM 合并腎功能損害的危險因素[22]。目前認為,β2?MG 參與腫瘤的調控與發展,但在體外β2?MG反而促進MM 細胞凋亡[23],可能骨髓瘤細胞在體內受白細胞介素?6 等細胞因子的保護,而避免了β 2?微球蛋白的凋亡作用。
MM 患者常伴有骨質損害和高鈣血癥等特點,血清中鈣分為游離鈣與結合鈣,目前臨床檢測為與血清白蛋白結合的結合鈣的濃度,MM 患者血清白蛋白降低,不能檢測出真實的鈣離子,因而采用校正鈣離子可真實的反映機體鈣離子的變化情況,可以更好地反映疾病嚴重程度[24]。多項研究證明,高鈣血癥為MM 合并腎損傷的危險因素,可增加腎臟損傷的發生率,可能由于鈣離子在腎臟的沉積所導致的不可逆的損傷[25]。本研究結果顯示,合并腎損傷的MM 的校正鈣離子濃度高于非腎損傷的MM 患者,為腎臟損傷的危險因素。
總之,當MM 患者出現血鈣增高,β2?MG 增高,NLR 增高等情況,需警惕是否發生腎臟損傷,通過實驗室指標指導臨床盡早進行腎臟保護,可逆轉腎臟損傷,延長患者的生存時間。

