溶劑萃取法凈化鹽酸法濕法磷酸的研究進展
冉瑞泉,金 央,劉 輝,李 軍,張 俊,陳 明
(1.甕福達州化工有限責任公司,四川達州635000;2.四川大學化學工程學院;3.教育部磷資源綜合利用與清潔加工工程研究中心)
磷酸是一種重要的無機酸化工原料,廣泛應用于肥料、飼料、食品和洗滌日用品等行業。磷酸的生產方法有兩大類,即熱法和濕法磷酸工藝。熱法磷酸生產存在產品能耗高、廢氣排放量大、污染重、對磷礦品位要求高等不足,面臨能源、環境和資源的多重壓力。世界上熱法工藝生產的磷酸占磷酸總產量的比例正在逐年下降。濕法磷酸是用無機酸分解磷礦,無機酸可以是硫酸、鹽酸或硝酸,最常使用的是硫酸。硫酸法二水硫酸鈣流程生產的濕法磷酸占全世界磷酸產量的80%以上。但是用硫酸法生產磷酸存在一個很大的問題——副產大量的磷石膏,每生產1 t磷酸(以P2O5計)就會產生4~5 t磷石膏[1]。由于磷石膏中含有多種雜質,使得其開發利用非常困難,特別是可溶的游離磷酸和氟化物會對環境造成嚴重污染[2]。此外,磷石膏分布集中,遠離消費市場,利用率完全受限于建材市場需求。從20世紀60年代起,研究人員就做了很多工作,以開發一種經濟有效的用鹽酸取代硫酸分解磷礦制取磷酸的辦法,即鹽酸法路線,該方法相比硫酸法,不會產生大量的磷石膏堆積,對環境的污染相對較小。鹽酸法路線可以使用中低品位磷礦,并且酸解反應速率快、反應完全,適合中國90%的磷礦為中低品位磷礦的國情[3]。此外,可以使用廉價的副產鹽酸,若與有副產鹽酸的工廠相鄰,幾乎可以獲得免費的鹽酸。
1 鹽酸法濕法磷酸凈化的典型流程——IMI流程
用鹽酸分解磷礦得到的酸解液主要含有磷酸和氯化鈣,以及少量的有機和無機雜質,必須經過凈化才能獲得較為純凈的磷酸。凈化過程的關鍵是將磷酸和極易溶解的氯化鈣分離開來。最早關于鹽酸法濕法磷酸路線的專利發表于1935年,但就當時的工業水平而言,沒法實現粗磷酸中磷酸與氯化鈣的分離。直至1957年Baniel、Blumberg提出了用溶劑萃取法分離磷酸與氯化鈣。之后,以色列礦業公司根據該專利開發了著名的IMI(Israel Mining Industries)法,成功實現了鹽酸法濕法磷酸中磷酸與氯化鈣的分離,將鹽酸法濕法磷酸凈化工業化。
IMI法凈化工藝主要由鹽酸分解磷礦和殘渣的分離、溶劑萃取分離磷酸、凈化稀磷酸的濃縮、萃余液中萃取劑的回收等4個部分組成,見圖1。
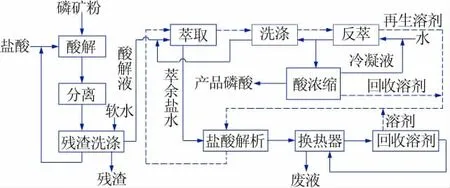
圖1 鹽酸法濕法磷酸凈化流程——IMI法Fig.1 Flow sheet for the purification of wet-process phosphoric acid by the hydrochloric acid route—IMI process
1)鹽酸分解磷礦和殘渣的分離。鹽酸分解磷礦的主要化學反應式為:

反應生成物溶于水,不存在生成物包裹反應物阻礙反應發生的情況。磷礦酸解反應速度很快,一般反應也比較完全[4]。鹽酸用量過小,則磷礦分解率會降低,殘渣量將會明顯增加;酸用量過大,則不利于殘渣的形成,且有更多的雜質進入酸解液。在酸解過程中會逸出較多的二氧化碳,在酸解槽中應設計有專門的機械消泡裝置。若產生的泡沫多且穩定,還應考慮在酸解過程中添加消泡劑。酸解后的料漿可以加入少量絮凝劑絮凝沉降,絮凝后的稠漿壓濾分離出殘渣。
2)溶劑萃取分離磷酸。溶劑萃取分離磷酸部分包括萃取、洗滌、反萃取和萃余液的鹽酸解析。酸解液與萃取劑相互接觸,磷酸進入有機相,大量的氯化鈣留在萃余水相中,實現磷酸與氯化鈣的分離。在萃取過程中有部分氯化鈣和其他雜質離子隨磷酸一同進入有機相。為了使產品磷酸更純凈,在反萃前用一部分經反萃得到的凈化磷酸洗滌萃取有機相,以除去氯化鈣和其他雜質離子。洗滌后的有機相用水或來自稀磷酸濃縮工段的餾出液進行反萃,得到凈化稀磷酸,同時萃取劑再生。再生的萃取劑與萃余水相接觸,因為萃余水相含有大量的氯化鈣,使萃余水相中的鹽酸進入萃取劑。然后萃取劑循環用于再次萃取。溶劑萃取過程是鹽酸法濕法磷酸凈化工藝的核心。
3)凈化稀磷酸的濃縮。反萃得到的凈化磷酸中含有磷酸、鹽酸和少量萃取劑。IMI流程采用的是三效負壓蒸發濃縮系統。在蒸發過程中,第三效的餾出液為醇與水,第二效的餾出液為稀鹽酸,第一效的餾出液為較濃鹽酸,底液為較純凈的濃磷酸。如果濃縮至磷酸質量分數為95%,氯化氫可以完全除盡[5]。該步驟的蒸發濃縮設備需要特殊材料制作,是整個工藝投資的主項。
4)萃余液中萃取劑的回收。在溶劑萃取過程中,有部分溶劑溶解在氯化鈣鹽水中。流程中萃取劑的消耗量直接關系到生產成本。因此必須對萃余水相中的萃取劑進行回收,最簡單的回收方法是精餾;但是需要加熱大量的氯化鈣鹽水,并對精餾塔釜排出的廢鹽水進行熱回收。
2 溶劑萃取法凈化鹽酸法濕法磷酸的進展與現狀
自以色列礦業公司IMI法工業化后,以色列海法化學公司在20世紀60年代、印度BILT公司在20世紀80年代建立的鹽酸法凈化磷酸工廠均采用該法。鹽酸法凈化磷酸經歷了短暫的興盛,但人們很快就將溶劑萃取法廣泛應用到了硫酸法濕法磷酸凈化,對鹽酸法濕法磷酸的凈化研究和工業應用并不多。原則上的IMI流程,一般采用正丁醇和/或異戊醇作為萃取劑。有文獻報道了正丁醇或異戊醇從鹽酸法濕法磷酸中萃取磷酸的性能研究。Bakr等[6]考察了以正丁醇或異戊醇為萃取劑、從鹽酸法濕法磷酸(埃及磷礦)中萃取磷酸時,磷酸、鹽酸和氯化鈣濃度及溫度和相比等條件對萃取過程的影響,找到了最佳操作條件;還研究了在萃取塔中正丁醇從磷酸/鹽酸混合液中逆流萃取磷酸的過程[7]。Shlewit[8]研究了以異戊醇為萃取劑、溶劑萃取凈化鹽酸法濕法磷酸(Syrian磷礦),得到了比較純凈的稀磷酸(P2O5質量分數為19.2%)。武漢化工學院研究了異戊醇從氯化物—磷酸中萃取磷酸的能力,以及各工藝條件對萃取分離性能的影響[9];還對異戊醇從該體系中萃取磷酸、鹽酸的動力學進行了研究[10-11]。
正丁醇或異戊醇等低碳醇微溶于水,必須回收萃取劑,不僅要回收溶解在凈化稀磷酸中的萃取劑,還需要回收溶解在萃余氯化鈣鹽水中的萃取劑。前者在稀磷酸濃縮過程中可以順道回收;而后者需要加熱大量的氯化鈣鹽水通過精餾方法回收。這兩個回收過程都需要換熱裝置并消耗大量熱量。此外,正丁醇或異戊醇易揮發,溶劑萃取和萃取劑回收過程的設備密封性要好。一旦溶劑回收不徹底或揮發,都會導致溶劑損失,使磷酸生產成本大幅增加。20世紀70年代,基于IMI法,上海骨膠廠與上海化工研究院合作,在中國設計投產了一個年產500 t 80%磷酸的生產車間。但是試驗生產線遭遇了溶劑損耗量大的問題。每生產1 t 80%磷酸要損耗150 kg丁醇,與IMI法報道的4~8 kg相差很大,這個試驗車間在運行了一段時間后就廢棄了。以低碳醇作為萃取劑,還需要注意低碳醇的閃點較低,在操作中容易引發安全問題。因此,用一種在水相中溶解度小、不易揮發且更安全的溶劑來代替低碳醇,是鹽酸法濕法磷酸凈化研究的最重要部分。
一些文獻報道了使用其他類型萃取劑來凈化鹽酸法濕法磷酸,如酮類、砜類、磷酸酯類等。馬敬中等[12]研究了環己酮對磷酸—鹽酸混合液中磷酸的萃取,發現隨著水相酸度的增加,萃取機理由中性結合萃取變成離子締合萃取,并提出了萃合物的可能結構。趙廷仁等[13]研究了S系列萃取劑的萃取性能,用混合萃取劑[S612~S610]對鹽酸分解磷礦酸解液中的磷酸進行單級和多級萃取,測定了等溫萃取平衡線,計算了多級錯流和逆流萃取的理論級數。磷酸三丁酯(TBP)作為一種磷酸酯類萃取劑,在溶劑萃取法凈化硫酸法磷酸領域已廣泛使用[14-15],但它在鹽酸法濕法磷酸凈化上的應用相對較少。文獻[16]公開了一種用鹽酸分解中低品位磷礦制造工業磷酸的方法。該方法先用磷酸三丁酯從鹽酸法濕法磷酸中萃取磷酸,洗滌、反萃、濃縮之后,再以磷酸三丁酯和異丙醚混合萃取劑萃取,濃縮脫色之后可以制成85%的工業磷酸。文獻[17]公開的用鹽酸分解中低品位磷礦制備工業級和食品級磷酸的方法中也采用磷酸三丁酯作為萃取劑。武漢化工學院歐陽貽德等[18]研究了磷酸三丁酯從氯化物—磷酸中萃取磷酸的能力及各工藝條件對萃取分離性能的影響;金士威等[19]研究了磷酸三丁酯從該體系中萃取磷酸的動力學;呂中等[20]研究了不同溫度下TBP—H3PO4—H2O三元體系的相平衡,以及氯化鈣含量對萃取平衡曲線的影響;柳丹等[21]將脈沖篩板萃取塔應用于鹽酸法濕法磷酸萃取過程,得到了最佳操作條件。Habashi等[22]研究了用磷酸三丁酯分離Florida磷礦酸解液中的磷酸與氯化鈣,用氨氣反萃經洗滌后的負載有機相生成磷酸銨鹽,同時實現萃取劑再生。Brazilian磷礦酸解所得粗磷酸也采用了磷酸三丁酯溶劑萃取來分離磷酸與氯化鈣[23]。四川大學磷資源綜合利用和清潔加工研究團隊Jin等[24]報道了磷酸三丁酯從磷酸—氯化鈣溶液中萃取磷酸時的相平衡數據,研究結果表明磷酸三丁酯相較低碳醇具有更好的選擇性,得到了萃取平衡方程,確定了萃合物的形式;Zhang等[25]表征了萃合物的組成,選擇了最佳的稀釋劑和有機相組成;Jin等[26]對萃取磷酸的動力學進行了研究,得到了萃取速率方程,確立了萃取過程的混合控制動力學機理,為磷酸萃取過程的強化指明了方向。總體來看,磷酸三丁酯在較寬的磷酸濃度范圍內對磷酸的萃取能力表現優異,選擇性高;在水中的溶解度很小,萃取劑損失小;化學性質非常穩定,閃點、沸點高,不易揮發,低毒性,操作安全,是一種比較適用于鹽酸法濕法磷酸凈化的萃取劑。2012年,由凱恩德利(北京)科貿有限公司自主研發、設計的1萬t/a鹽酸法食品級磷酸項目在埃及成功試車。這是首套采用磷酸三丁酯作為萃取劑的鹽酸法濕法磷酸凈化裝置。
用磷酸三丁酯作為鹽酸法濕法磷酸凈化過程的萃取劑,各方面優勢明顯,但因酸解液中存在大量氯化鈣,絕大部分Fe3+也會被磷酸三丁酯萃取,導致產品中Fe3+含量過高。因此,在磷酸三丁酯萃取H3PO4之前必須預先脫除Fe3+。易紹連等[27]采用ACPh作為萃取劑,脫除鹽酸法路線凈化反萃磷酸中的Fe3+,Fe3+脫除率較高,但會損失一定量的磷酸和游離鹽酸。用二(2-乙基己基)磷酸(D2EHPA)為萃取劑,煤油為稀釋劑,除鐵效果較好,不損失磷酸,但萃取過后的負載有機相必須用較高濃度的鹽酸反萃[28]。磷酸三丁酯亦可作為溶劑萃取法脫除Fe3+的萃取劑,Fe3+脫除率高,磷酸損失較少;但萃取后的有機相黏度大,分相比較困難,需要添加合適的稀釋劑以便于分相[29-30]。
3 溶劑萃取法凈化鹽酸法濕法磷酸的固有弊端和前景展望
不論萃取過程所用的萃取劑種類是什么,溶劑萃取法凈化鹽酸法濕法磷酸路線都會存在以下固有的弊端。
1)反萃得到的凈化磷酸濃度較低。因分解磷礦所用的是鹽酸,受鹽酸濃度限制,酸解液中的磷酸濃度較低,導致反萃得到的凈化磷酸濃度較低。若想作為濃磷酸出售,濃縮負荷很大,能耗很高。當然,凈化稀磷酸也可以制成磷酸鹽進行濃縮、結晶制得磷酸鹽產品。Habashi等[22]建議的流程用氨氣反萃負載有機相生成磷酸銨鹽,避免了稀磷酸或磷酸鹽溶液的濃縮。但若反萃—結晶在一常規反應器中進行,體系處于宏觀混合,局部點氨濃度較高,導致該點磷酸銨鹽的過飽和度較高,瞬間產生大量晶核并團聚,容易包藏萃取劑,造成萃取劑損失,影響磷酸銨鹽產品的質量。局部點氨濃度較高,還會造成與之接觸反應的有機相發生乳化和水解。此外,氨的利用率不高。上述問題是由于對多相體系的傳質過程控制精度較低而導致。四川大學磷資源綜合利用和清潔加工研究團隊提出可以用氨氣或較高濃度的堿溶液進行TBP再生[31],同時在反萃體系中加入相應的磷酸鹽飽和溶液來調節水相和萃取劑相的體積比,以保證兩相間的接觸面積;將反萃—結晶過程分解為液-液兩相穩定接觸、水相通堿、反應和結晶4個串聯過程。前3個過程在微通道中進行,利用微化工技術的可控和高效性實現氨的完全利用,同時精確控制反萃得到的水相鹽溶液濃度在結晶介穩區內。因前3個過程的精確調控,第四步鹽溶液在常規結晶器中結晶即可得到粒度分布窄、質量好的結晶產品,結晶母液循環用于反萃。如此可以有效解決控制精度低導致的爆發式成核、有機相乳化、水解和堿利用率低等問題。
2)反萃得到的凈化磷酸含有少量鹽酸。因萃取劑的選擇性問題,沒有辦法實現磷酸和Cl-完全分離的目的,即使充分洗滌也無法將Cl-完全洗脫。因此,反萃得到的凈化磷酸含有少量鹽酸。若想得到純度高的磷酸,需要在一個昂貴、能量消耗高的多效蒸發系統中蒸發、濃縮至磷酸質量分數為95%,才能完全除掉鹽酸[5]。凈化磷酸可以不經處理與氯化鉀/鈉/銨等反應,采用溶劑萃取法生產工業磷酸鹽,產品一般都能達到相應標準的一等品要求[32]。但目前工業磷酸鹽的生產絕大部分采用中和法,溶劑萃取法生產工藝的推廣還需要一定的時間。
3)CaCl2廢液高效綜合利用成難題。鹽酸法路線會副產大量的CaCl2廢液。在以色列,因其特殊的地理環境,CaCl2廢液直接排至死海,不存在CaCl2廢液處理問題。CaCl2廢液可經蒸發濃縮、冷卻、結晶、干燥制得氯化鈣產品,可用作干燥劑、制冷劑、建筑防凍劑、織物防火劑和空海港消霧劑等,但市場需求量有限、價格較低。Habashi等[22]建議的流程是往萃余CaCl2廢液中加入硫酸,產生可循環使用的氯化氫氣體和比較純凈的硫酸鈣晶體。四川大學磷資源綜合利用和清潔加工研究團隊開發了含磷CaCl2溶液與硫酸反應制備硫酸鈣晶須[33]、半水硫酸鈣[34]和超高強石膏[35]的技術。這幾種硫酸鈣產品的附加值升高,但仍受制于市場容量。
4)氯離子的存在對設備防腐提出更高要求。鹽酸法路線從始至終都有氯離子存在,設備防腐要求相對硫酸法路線更高,特別是系統中含有較高濃度氯離子或處于較高溫度狀態下,設備防腐任務更加嚴峻。這也限制了鹽酸法路線的工業化應用。
4 結束語
鹽酸法路線相比硫酸法具有一定的環保和低品位礦適應性優勢,但其固有弊端也限制了鹽酸法路線的工業化應用。鹽酸法路線生產的磷酸產品成本其實并不低;但若有廉價的鹽酸或副產鹽酸可利用,又不需要對大量的副產氯化鈣鹽水進行處理或副產氯化鈣及其衍生鈣鹽有目標市場需求,這個工藝就很有優勢。就目前中國的情況來看,鹽酸法路線的工業化應用任重而道遠。但隨著硫酸法磷石膏環保壓力加劇、磷礦貧化、防腐材料和技術的發展進步,鹽酸法路線將會得到推廣應用。

