有機氯對乙烯環氧化反應性能的影響
吳同旭,胡遠明,郭秋雙,孟廣瑩,李曉云,孫彥民,于海斌
(1.中海油天津化工研究設計院有限公司, 天津 300131;2.中國石油吉林石化公司化肥廠,吉林 吉林 132000)
環氧乙烷屬于一種雜環化合物,是重要的石油化工有機中間體[1],銀催化劑是目前用于乙烯不完全氧化制環氧乙烷的唯一催化劑。銀催化劑的選擇性對生產環氧乙烷的乙烯消耗起決定性的作用。由于環氧乙烷產量巨大,選擇性若提高1%,即可節省大量乙烯原料,意味著巨大的經濟效益。已有研究[2]認為,以有機氯化合物提供氯元素作為反應抑制劑,加入反應體系能夠顯著提高乙烯氧化反應的收率。
一些理論和實驗已經證明添加適量的1,2-二氯乙烷,可有效改變銀催化劑的表面吸附性能,有利于吸附氧與乙烯發生選擇性氧化反應的進行,提高生成目標產物環氧乙烷選擇性[3]。本文考察有機氯作為抑制劑對乙烯環氧化性能的影響,并且對抑制劑作用機理進行研究。
1 實驗部分
1.1 催化劑制備
篩選合適的氧化鋁前驅體,通過加入不同種類的造孔劑并篩選合適的添加方式,優化焙燒條件,實現構造出銀載體所需大孔的同時,優化載體孔分布,并提高載體強度。
銀載體物性:比表面積(1.5~1.8) m2·g-1;平均孔徑(1 200~1 500) nm;強度(55~70) N;孔容(0.5~0.6) cm3·g-1;吸水率80%~100%;堆積密度(0.5~0.6) g·cm-3。XRD晶型:α相。
稱取一定質量的硝酸銀溶解后與草酸溶液反應得白色草酸銀沉淀,采用負壓過濾取其沉淀物草酸銀濾餅。稱取適量水置于燒杯中,依次加入一定量的乙二胺、少量乙醇胺,之后緩慢加入草酸銀濾餅,得到銀胺絡合溶液。采用真空浸漬方法將所得銀胺溶液浸漬于α-Al2O3載體上,浸漬液體積為載體吸水率的2~4倍,瀝濾除去多余的溶液后,將其放入烘箱干燥,隨后在氮氣氣氛210 ℃活化制成銀催化劑。
1.2 催化劑表征
通過XRD、SEM、TEM、BET以及壓汞法等測試表征手段對載體及銀催化劑進行表征分析。圖1為銀催化劑載體XRD圖。由圖1的XRD峰形態可知,銀催化劑載體為純α-Al2O3晶相。
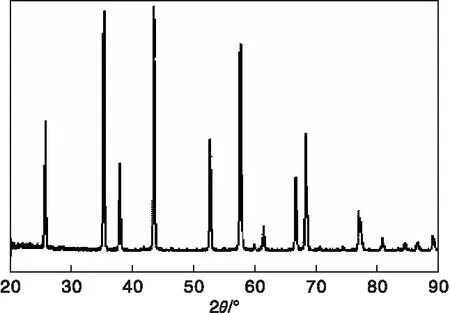
圖1 銀催化劑載體的XRD圖Figure 1 XRD pattern of silver based catalyst support
圖2為銀催化劑載體的SEM照片。

圖2 銀催化劑載體的SEM照片Figure 2 SEM image of silver based catalyst support
由圖2可以看出,銀催化劑載體具有疏松的大孔隙的蠕動蟲狀的結構。
硝酸銀與草酸銨在溶液中反應的反應方程式為:

由于銀催化劑制備使用惰性大孔氧化鋁材料,催化劑制備過程中要特別注意活性組分的負載。在銀催化劑上活性組分是以銀單質形式存在,銀顆粒均勻覆蓋于載體上,銀顆粒的大小對溫度影響較敏感。圖3和圖4分別為銀催化劑的SEM和TEM照片。由圖3和圖4可以看出,銀催化劑中的活性組分銀顆粒在載體上均勻分散。

圖3 銀催化劑SEM照片Figure 3 SEM image of silver based catalyst

圖4 銀催化劑TEM照片Figure 4 TEM image of silver based catalyst
1.3 催化劑性能評價
采用10 mL固定床反應器,在反應壓力(1.9~2.1) MPa、原料氣流量50 L·h-1、反應原料氣體積組成為乙烯13%、氧氣7%、甲烷為系統平衡氣的標準反應條件下,評價制備的銀催化劑對乙烯環氧化反應的催化性能。考察抑制劑種類及用量對乙烯環氧化性能的影響,進而對有機氯化合物作為抑制劑的作用機理進行研究。
圖5為銀催化劑微反評價流程。抑制劑進料方式為恒溫恒壓下采用鼓泡法使用甲烷氣帶入。采用安捷倫公司7890B氣相色譜儀對反應氣體組成進行定量分析,配備HP-PLOT Q毛細色譜柱和熱導池(TCD)檢測器,用以分離和檢測氣體組成。
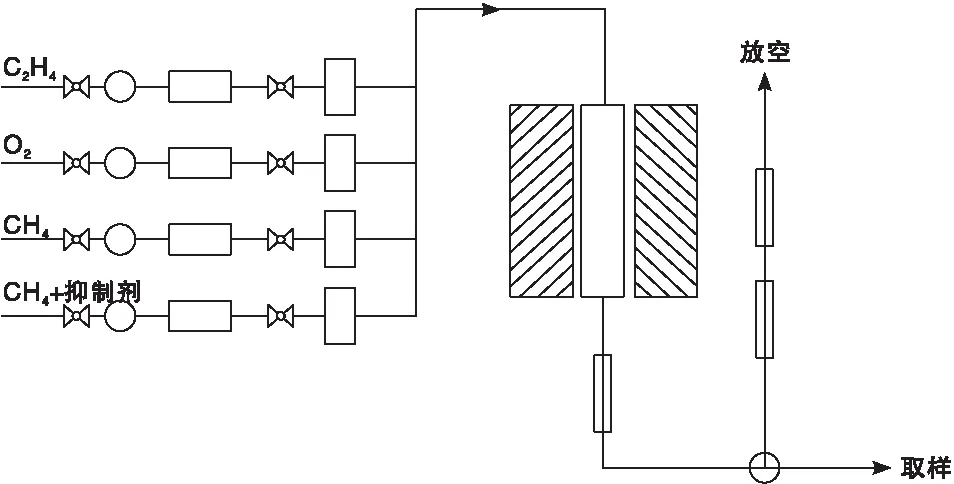
圖5 銀催化劑微反評價流程Figure 5 Micro reaction evaluation process of silver catalyst
2 結果與討論
2.1 氯含量
在乙烯環氧化制環氧乙烷的反應條件下,控制反應溫度225 ℃,加入四氯乙烯,考察氯含量對乙烯氧化性能的影響,結果如表1所示。
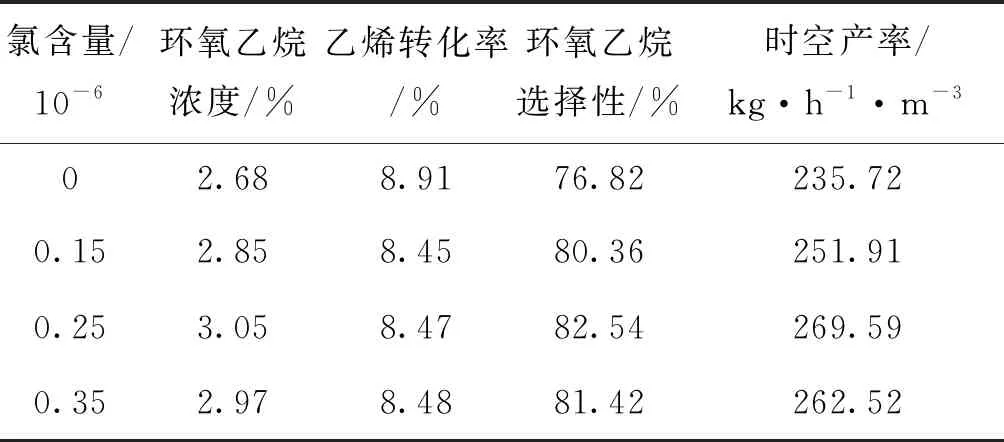
表1 不同氯含量對乙烯氧化性能的影響
由表1可以看出,以四氯乙烯為反應抑制劑,隨著氯含量升高,環氧乙烷選擇性和時空產率先升高后降低。當氯含量為0.25×10-6(以氯元素物質的量計,下同)時,目標產物環氧乙烷的選擇性及時空產率最高。這是因為氯離子表面修飾金屬銀,可提高乙烯環氧化反應中環氧乙烷選擇性,同時降低了催化劑的催化活性。因此,抑制劑的加入能夠明顯提高環氧乙烷選擇性,抑制反應速率。
2.2 抑制劑類型
其他反應條件不變,考察氯含量為0.25×10-6時,不同抑制劑對乙烯氧化性能的影響,結果如表2所示。
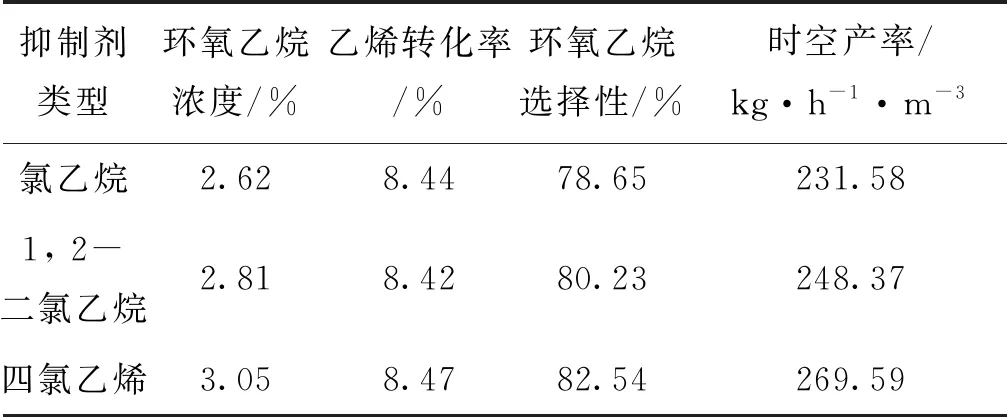
表2 不同抑制劑對乙烯氧化性能的影響
由表2可以看出,相同反應條件下,控制氯含量為0.25×10-6,分別選擇氯乙烷、1,2-二氯乙烷、四氯乙烯作為氯源,四氯乙烯的反應效果明顯優于氯乙烷和1,2-二氯乙烷。根據該實驗結果,以四氯乙烯為例,對其作為抑制劑的作用機理進行研究。
2.3 抑制劑四氯乙烯反應機理
2.3.1 四氯乙烯在銀催化劑及其載體上的反應
在反應器中裝入10 mL未負載活性組分的α-Al2O3載體,相同反應條件下,通入含有四氯乙烯物質的量為0.25×10-6的氣體(甲烷作平衡氣)。改變反應溫度,檢測反應器出口氣體中四氯乙烯含量,結果見表3。

表3 四氯乙烯在α- Al2O3載體上的分解反應
由表3可知,隨著反應溫度增加,反應器出口氣體中四氯乙烯含量未發生實質性變化。由此可見,在(200~260) ℃,四氯乙烯在未負載活性組分的α-Al2O3載體上幾乎不發生任何反應。
相同反應條件下,將同一氣體通入裝有相同粒度銀催化劑的10 mL反應器中,依次設定反應溫度為200 ℃、210 ℃、220 ℃、230 ℃、240 ℃、250 ℃、260 ℃,對反應器出口氣體進行連續48 h取樣分析。結果發現,反應器出口氣體中均未檢測到四氯乙烯,表明四氯乙烯在200 ℃時已在銀催化劑表面完全分解。
2.3.2 氧氣對四氯乙烯在銀催化劑表面吸附分解的影響
將四氯乙烯物質的量0.25×10-6、氧氣物質的量分數7%的氣體(甲烷作平衡氣)通入裝有銀催化劑的10 mL反應器中,在不同反應溫度下,檢測出口氣體中四氯乙烯含量,結果見表4所示。

表4 氧氣對四氯乙烯分解的影響
從表4可以看出,出口氣體中四氯乙烯含量隨反應溫度的升高而降低,結合2.3.1研究結果,表明在氧存在下,氧氣與四氯乙烯在銀催化劑表面發生競爭性吸附,占據了部分銀催化劑活性位,從而抑制四氯乙烯在催化劑表面的吸附及分解。隨著反應溫度升高,四氯乙烯的吸附作用越來越強。氧氣占據銀催化劑活性位的能力越來越弱,抑制四氯乙烯在銀催化劑表面吸附分解的能力也越來越弱。
2.3.3 乙烯對四氯乙烯在銀催化劑表面吸附分解的影響
相同實驗條件下,將四氯乙烯物質的量0.25×10-6、乙烯物質的量分數28%的氣體(甲烷作平衡氣)通入裝有銀催化劑的10 mL反應器中,依次改變反應溫度,檢測反應器出口氣體中四氯乙烯含量,結果見表5所示。

表5 乙烯對四氯乙烯分解的影響
由表5可以看出,乙烯存在下,反應器出口氣體中含有四氯乙烯,其含量隨反應溫度的升高而逐漸降低。
2.3.4 抑制劑分解可逆性的研究
為考察由于抑制劑的分解而新產生的氯是否會與乙烯發生化學反應,進行如下實驗:分別以氯乙烷、四氯乙烯及1,2-二氯乙烷為抑制劑,配制氧氣、乙烯、甲烷混和氣,抑制劑含量以氯元素計算,均為0.25×10-6,待完全混和均勻后,通入裝有10 mL銀催化劑的反應器中。在實驗條件下,分別連續測定反應器出口氣體中氯乙烷、四氯乙烯及1,2-二氯乙烷含量。結果發現,在反應溫度為200 ℃時,裝有銀催化劑的反應器出口氣中氯乙烷和四氯乙烯物質的量均為零,而1,2-二氯乙烷物質的量換算成氯元素的物質的量為0.23×10-6。由此證明,在乙烯環氧化制環氧乙烷反應條件下,由于有高濃度乙烯的存在,乙烯與游離氯發生加成反應,生成幾乎等量的1,2-二氯乙烷。相當于1,2-二氯乙烷的分解為可逆反應,而不能生成氯乙烷和四氯乙烯,相當于氯乙烷和四氯乙烯的分解是不可逆反應。這也是雖然四氯乙烯抑制乙烯完全氧化的作用效果優于氯乙烷和1,2-二氯乙烷,但工業上大多選用1,2-二氯乙烷的原因。
3 結 論
(1)在原料氣中添加微量的氯乙烷、1,2-二氯乙烷、四氯乙烯等含氯有機物作為抑制劑,可有效抑制乙烯完全氧化反應的進行,減少二氧化碳的生成,提高環氧乙烷選擇性。氯含量為0.25×10-6(以氯原子物質的量計)時的抑制作用效果最佳。
(2)在相同的氯含量下,四氯乙烯的抑制效果優于氯乙烷和1,2-二氯乙烷。
(3)在乙烯環氧化制環氧乙烷反應條件下,由于大量乙烯存在,1,2-二氯乙烷的分解是可逆反應,氯乙烷和四氯乙烯的分解是不可逆反應。

