基于磁微粒化學發光法的sST2檢測性能驗證*
熊夢秋,王旭鴻,潘蓓,聶俊杰,王書奎,何幫順(.南京市第一醫院中心實驗室,南京0006; .東南大學醫學院,南京89)
生長刺激表達基因2蛋白(growth stimulation expressed gene 2,ST2)基因片段大小約為4×104bp,編碼556個氨基酸的蛋白質,相對分子質量(Mr)約為63×103。ST2是白細胞介素-1(interleukin-1, IL-1)受體家族成員,具有2種異構體。研究表明,可溶性ST2(soluble ST2,sST2)在介導炎癥的過程發揮關鍵作用,其通過調控網絡影響相關細胞因子的表達,特別是在心臟損傷伴隨的炎癥過程中起著重要作用[1]。
sST2作為心衰標志物越來越受到基礎及臨床研究的關注,美國心臟病學院(ACC)和美國心臟協會(AHA)自2017年開始對sST2作為標志物在心衰中的臨床應用進行了評價,并評估其在病例管理中的臨床應用價值[2]。我國心臟疾病相關的診療指南中亦將該指標作為預測心衰預后的二級指標[3]。眾多的臨床研究亦表明,sST2、半乳糖凝集素-3(galectin-3,Gal-3)等被認為具有預測心衰患者的病程和死亡預后價值[4-6]。因此,本研究對一種基于磁微粒化學發光法檢測sST2的試劑盒進行性能評價,探討其臨床應用穩定性與可靠性。
1 資料與方法
1.1一般資料 收集2020年5至6月于南京市第一醫院體檢人群40例(男、女各20例,年齡:37.80±14.38歲)及60例臨床病例(男vs女:43例vs 17例,年齡:67.32±13.86歲),血清樣本用于不同方法學試劑的平行對比試驗。健康人群納入標準:體檢結果為正常;排除標準:(1)有免疫性疾病史;(2)近期有感冒及感染性疾病史;(3)有心血管及呼吸系統疾病史。臨床病例樣本為隨機檢測樣本,依對比試劑檢測結果,隨機選擇低、中、高值各20例。
1.2儀器與試劑 磁微粒化學發光法sST2測定試劑盒、CI2000S全自動化學發光免疫分析儀(北京利德曼生化公司), 膽紅素及血紅蛋白(上海信帆生物科技公司), 脂肪乳(西安立邦制藥公司),sST2蛋白檢測試劑盒(ELISA法,天津康爾克生物科技公司),ST-360酶聯儀(上海科華生物工程公司)。
2 實驗與結果
2.1精密度 按照CLSI-EP15-A2指南[7]要求,使用高、低2個水平的室內質控,質控品為廠家試劑盒提供的質控品及實驗室自制的血清樣本質控品,每個水平各分裝5管(冷凍保存),每天檢測1次,共測5 d。計算批內和總變異系數(CV)。所選擇的樣本經過批內以及批間精密度檢測結果顯示,低水平及高水平血清樣本的總CV值分別為2.2%和2.3%;低水平及高水平試劑盒質控品的總CV值分別為1.7%及1.5%;以上4組CV值均滿足≤10%的要求。見表1。

表1 精密度檢測結果

2.3線性范圍 實驗方法一:將接近線性范圍上限的高值樣本按比例稀釋(1、1/2……1/512),其中低值濃度的樣本接近線性區間的下限。每個稀釋濃度重復測試3次并求均值,計算線性相關系數r。認為合格標準的測量范圍在1.00~300.00 ng/mL內,r應≥0.99。檢測結果表明,在1.00~300.00 ng/mL范圍內,血清樣本r=0.999 9,試劑盒質控品線性范圍為6.40~200.00 ng/mL,試劑盒質控品r=0.999 9,符合≥0.990 0。實驗方法二:選擇低濃度(L)和高濃度(H)患者標本各1份,H和L混合成6個樣本,混合比例:L,4L+1H,3L+2H,2L+3H,1L+4H,H。每份混合樣本測定2次,將實測值與預期值作回歸分析。若r>0.95,a在0.97~1.03范圍內,b與0沒有顯著差異,則可判斷為線性,同時測定值與理論值偏差小于15%認為合格。檢測結果表明,血清樣本r=0.999 8,a=1.005 3;試劑盒質控品r=0.999 9,a=0.994 4。見圖1。

注:A,血清樣本方法學一線性范圍檢測結果;B,血清樣本方法學二線性范圍檢測結果;C,試劑盒質控品方法學一線性范圍檢測結果;D,試劑盒質控品方法學二線性范圍檢測結果。
2.4最低檢測限及靈敏度 最低檢測限:取待檢試劑盒中濃度為0的空白質控作為待測樣本,對樣本進行20次測定。同時取試劑盒中低濃度點標準品及血清進行2次測定。計算20次發光強度測量值的標準差(s),通過內插法從標準曲線上讀取sST2含量,即為空白檢測限。若計算的靈敏度不能滿足要求,需依據4倍均值法檢查有無離群點,若有離群點,則允許刪除1個點,并根據剩余19個數據計算最低檢測限。結果表明,以待檢試劑盒中0濃度點作為待測樣本,20次重復測定的最低檢測限為0.028 ng/mL,滿足≤1 ng/mL的要求,對比試劑要求≤2 ng/mL。靈敏度檢測:獲得1份略低于廠商給定的定量限(limit of detection,LoQ)濃度的樣本(用參考方法或已通過驗證的方法確定該樣本的靶值濃度A),重復測定20次,計算CV值應<目標CV(通常是20%)。結果表明,低于試劑盒給定的LoQ濃度的樣本經過20次重復測定,測定值<1 ng/mL,樣本CV= 1.1%,最低檢測限及靈敏度驗證均符合要求。
2.5臨床可報告范圍 選取線性范圍附近的高值樣本,分別進行倍數稀釋后,連同原濃度一起進行測試,重復檢測2次取平均值。稀釋后樣本結果和原濃度樣本結果進行比較,計算回收率。通過對高值樣本血清以及試劑盒質控品進行稀釋,計算回收率,結果表明,原倍、2倍(97.6%、98.9%)、5倍(101.2%、97.0%)、10倍(104.2%、98.2%)、20倍(100.3%、98.0%)、40倍(98.7%、103.4%),證實血清樣本及試劑盒質控品的40倍稀釋結果可靠。
2.6參考區間驗證 收集體檢結果為正常的男、女各20份參考個體樣本按要求各檢測1次,如果40例參考個體中不超過4例的觀測值在原始報告的參考區間之外則符合要求。使用磁微粒化學發光法試劑盒對收集的體檢健康人群臨床樣本進行檢測,結果表明,40例樣本sST2檢測最小值為0.45 ng/mL,最大值為29.43 ng/mL,平均值為8.26 ng/mL,所有樣本檢測值均在原始報告的參考區間之內,參考區間驗證符合要求。
2.7臨床樣本測試 將磁微粒化學發光法sST2測定試劑盒與對照酶聯免疫法試劑盒對同一臨床樣本進行平行測定,分別記錄2種試劑盒的測定值,并使用配對t檢驗進行統計分析。使用2種不同方法學試劑盒對樣本進行對比測試,2種方法陰、陽性不一致共3例,發生率為5%,陽性符合率為96.88%,陰性符合率96.55%,總符合率96.72%,配對t檢驗結果差異無統計學意義(t=0.582,P=0.563),樣本比對相關系數r為0.916 2。
2.8穩定性測試 設置3個條件分別對高低水平濃度的樣本進行測試:(1)室溫條件下:檢測時間總長為72 h。間隔24 h測試1次,重復測試2次;(2)2~8 ℃條件下:將樣本分裝為7管,每天每濃度連續測試2次,連續測試7 d;(3)-20 ℃條件下:將樣本分裝為7管,每天每濃度連續測試2次,連續測試7 d。室溫條件下樣本在不同時間的檢測結果表明,儲存樣本在室溫間隔72 h后,測試高、低兩水平樣本與初始測試結果的相對偏差分別為-15.3%及-14.6%。2~8 ℃冰箱內儲存樣本在7 d后,測試高、低水平樣本與初始測試結果的相對偏差分別為-0.44%及0.39%。-20 ℃冰箱內儲存樣本在7 d后,測試高、低水平樣本與初始測試結果的相對偏差分別為-2.08%及-0.72%。見圖2。

注:A,血清-20 ℃儲存時不同靜置天數下sST2檢測結果;B,血清2~8 ℃儲存時不同天數下sST2檢測結果;C,血清室溫儲存時不同天數下sST2檢測結果。
2.9干擾實驗 分別取高、低濃度血清樣本,分別加入膽紅素(0.25 mmol/L、0.5 mmol/L、1 mmol/L)、血紅蛋白(2.5 g/L、5 g/L、10 g/L)、脂肪乳(5 g/L、10 g/L、20 g/L)等3個梯度的干擾物質,以加入基質的樣本作為對照,按照常規檢驗程序進行平行測定,計算加之前與加之后的相對偏差,以偏差不超過15%認為合格。結果表明加入不同濃度的膽紅素、血紅蛋白、脂肪乳后的標本相對偏差均不超過15%。見圖3。
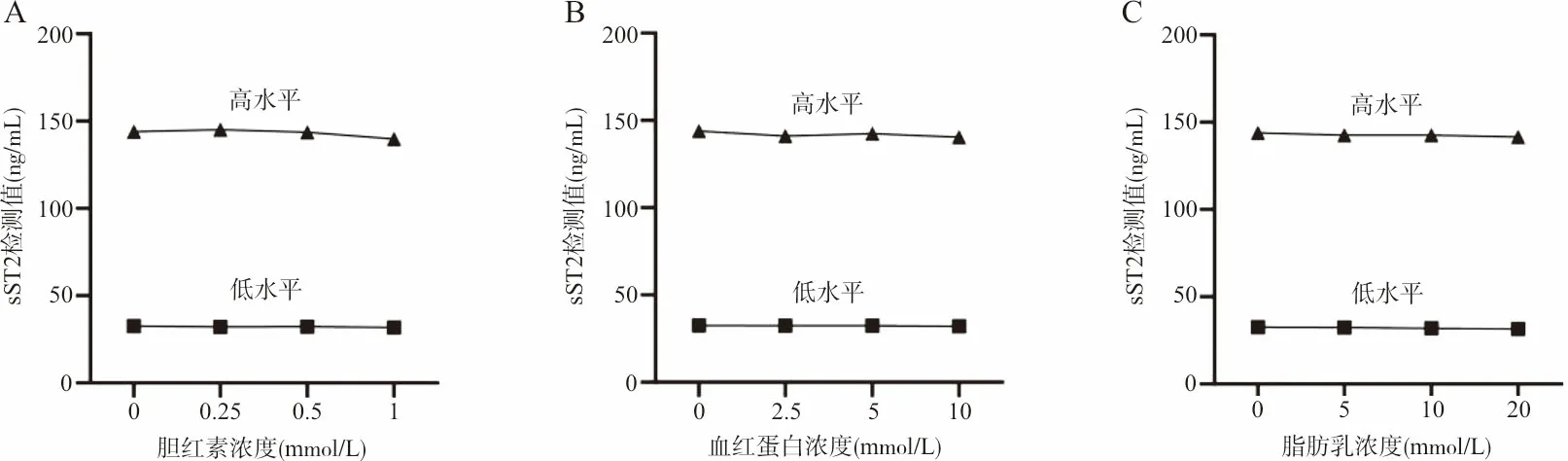
注:A,血清樣本中不同濃度膽紅素干擾實驗結果;B,血清樣本中不同濃度血紅蛋白干擾實驗結果;C,血清樣本中不同濃度脂肪乳干擾實驗結果。
3 討論
sST2臨床應用的優勢在于其變異度受到心衰人群中普遍合并癥的影響較小,與炎癥狀態和合并癥高度相關的sST2在射血分數保留的心力衰竭病程監測中具有獨特的應用優勢。研究表明,sST2連續監測可以作為療效監測及預后判斷的指標,對于制定治療方案及心衰精細化的管理顯示出良好的應用前景[8]。故本研究對基于磁微粒化學發光法的試劑盒從精密度、重復性、線性范圍、最低檢測限、臨床可報告范圍、參考區間驗證、臨床樣本對比測試、樣本穩定性測試、干擾實驗等9個方面對sST2檢驗試劑盒進行了驗證,結果顯示,該試劑盒檢測效能均符合臨床需求。
磁微粒化學發光法是將磁性分離技術、化學發光技術、免疫分析技術三者結合起來的一種新型分析方法[9],利用磁微粒包被相應的抗原抗體,結合酶標抗體以檢測目的抗原或抗體。該法具有高靈敏度,高準確性及穩定性好等特點,已經在臨床廣泛應用,如:乙肝表面抗原、丙型肝炎病毒抗體、梅毒螺旋體(TP)抗體、人類免疫缺陷病毒抗體定量檢測等方面[10]。此外,該法還可用于25-羥基維生素D的檢測且被證實具有較高的準確性及靈敏度[11]。ELISA法在臨床試驗中廣泛使用,因此,筆者將本研究建立的方法與ELISA法試劑盒同時測定40例臨床樣本,比對結果表明,2種方法結果差異不具有統計學意義,2種方法相比較而言,磁微粒化學發光法克服了ELISA法受反應溫度、反應時間及加樣等因素的影響。本實驗中發現有3例樣本存在兩試劑盒檢驗陰陽性不一致的結果,其中1例患者為左心耳介入封堵術后,ELISA法測值高于參考值1 ng/mL,位于臨界值附近,磁微粒化學發光法檢測的ST2水平較參考值低5 ng/mL,這可能與兩方法所設定的cut-off值不同有關。2例患者采用兩方法檢測結果相差較大,可能由兩試劑盒選定的抗體不同或2種試劑盒抗體的標記方法不同從而導致敏感性不同;此外,磁微粒化學發光主要是用磁珠做載體,ELISA是固相載體,這也可能導致ST2檢測結果有差異。因此,建議患者臨床檢測結果出現可疑值時需結合病史,必要時進行多次檢測,為臨床治療提供可靠依據。
sST2目前臨床開展應用較少,鮮有研究從方法學角度對該指標進行評價,本研究雖從多個角度闡述基于磁微粒化學發光法檢測sST2的可靠性,但本研究檢測的樣本還相對較少,還未完全評價涉及的影響臨床樣本結果的因素,因此,本研究結果還有待于更多的臨床試驗結果的驗證。
綜上,本研究對基于磁微粒化學發光法的sST2檢測試劑盒進行性能驗證,結果顯示精密度、重復性、線性范圍、最低檢測限、臨床可報告范圍、參考區間驗證、臨床樣本測試、樣本穩定性測試、干擾實驗驗證均符合的要求。本研究可供其他sST2檢測性能驗證的設計作為參考。

