高通量測序技術檢測早期自然流產組織染色體非整倍體及拷貝數變異的臨床意義
鄭蕓蕓,李 佳,萬陜寧,鄭 嬌,黨穎慧,張建芳,楊 紅
(空軍軍醫(yī)大學西京醫(yī)院婦產科,西安 710032;*通訊作者,E-mail:yanghongfck@163.com)
自然流產(spontaneous abortion,SA)為婦產科常見疾病,在妊娠中的發(fā)生率為10%-15%[1],其中早期流產(孕6-12周)約占80%。自然流產的病因十分復雜,包括胚胎因素、免疫因素、母體因素、環(huán)境因素等,而因為胚胎染色體數目異常原因導致的早期流產約占50%[2,3]。發(fā)生自然流產時的孕周越短,染色體異常的可能性會越大。目前國內外有關流產組織染色體異常檢測的方法有很多,如絨毛培養(yǎng)染色體核型分析、FISH檢測技術、染色體微陣列分析及高通量測序技術,極大地提高了流產組織染色體的分辨率和檢測成功率。其中高通量測序技術發(fā)展迅速,通過對樣本進行全基因組快速掃描,檢測出染色體小片段的缺失、重復,用于檢測染色體拷貝數變異的優(yōu)勢越來越明顯,具有高準確性、高通量、高靈敏度、低成本等優(yōu)勢。本研究應用高通量測序技術檢測流產胚胎及絨毛組織,評估該技術的應用價值及臨床意義。
1 對象與方法
1.1 研究對象
選擇2019年1月至2020年8月期間在空軍軍醫(yī)大學西京醫(yī)院婦產科就診的不明原因早期胚胎停止發(fā)育的91例孕婦,年齡22-41歲,平均年齡31歲,平均孕周6-12周,經B超提示胚胎停止發(fā)育(無心管搏動)。排除孕期感染及有害物質接觸史。自愿要求流產絨毛組織染色體檢測者,簽署知情同意書。本研究經中國人民解放軍總醫(yī)院醫(yī)學倫理委員會批準。
1.2 染色體拷貝數變異檢測
根據倫理要求,按照程序采集流產物組織,取3-5 mg組織研磨,將研磨好的組織放入56 ℃水浴鍋中消化過夜。通過試劑盒提取基因組DNA,純化,得到濃度為20 mg/μl的基因組DNA。根據建庫流程進行文庫構建(gDNA打斷,末端修復,末端加“A”,接頭連接)。使用PCR技術擴增兩端帶有接頭的DNA片段。最后將一定量的文庫按照等物質的量混合,上機測序。基于染色體拷貝數變異的檢測方法,將每個讀長的測序堿基與人類基因組參考序列(hg19)進行比對,通過唯一比對的讀長數據進行染色體異常分析。
1.3 統(tǒng)計學方法
使用SPSS19.0統(tǒng)計軟件進行分析,計數資料的組間比較采用χ2檢驗,P<0.05差異有統(tǒng)計學意義。
2 結果
2.1 染色體異常的類型與分布情況
共檢測胚胎總數91例,檢測結果中50例染色體正常,41例染色體異常。檢出有非整倍體的染色體有2,8,9,12,13,14,15,16,19,22號染色體,以15,16,22,X為高發(fā)。檢出CNV中,其中片段≥5 Mb的CNV(5-26 Mb)6例(54.55%),主要有1,2,7,8,19號染色體上的重復/缺失,重復的片段有25.92 Mb和19.38 Mb;缺失的片段有14.82,14.96,19.36,24.32 Mb。片段<5 Mb的CNV(0.18-5 Mb)6例(54.55%),包括1,7,15,X號染色體上的微重復/微缺失,微重復的片段有1.70 Mb,微缺失的片段有0.50,0.64,0.20,0.42,0.18 Mb(見表1)。陽性樣本的分布情況見圖1。

表1 91例流產組織高通量測序檢測結果 (未完待續(xù))
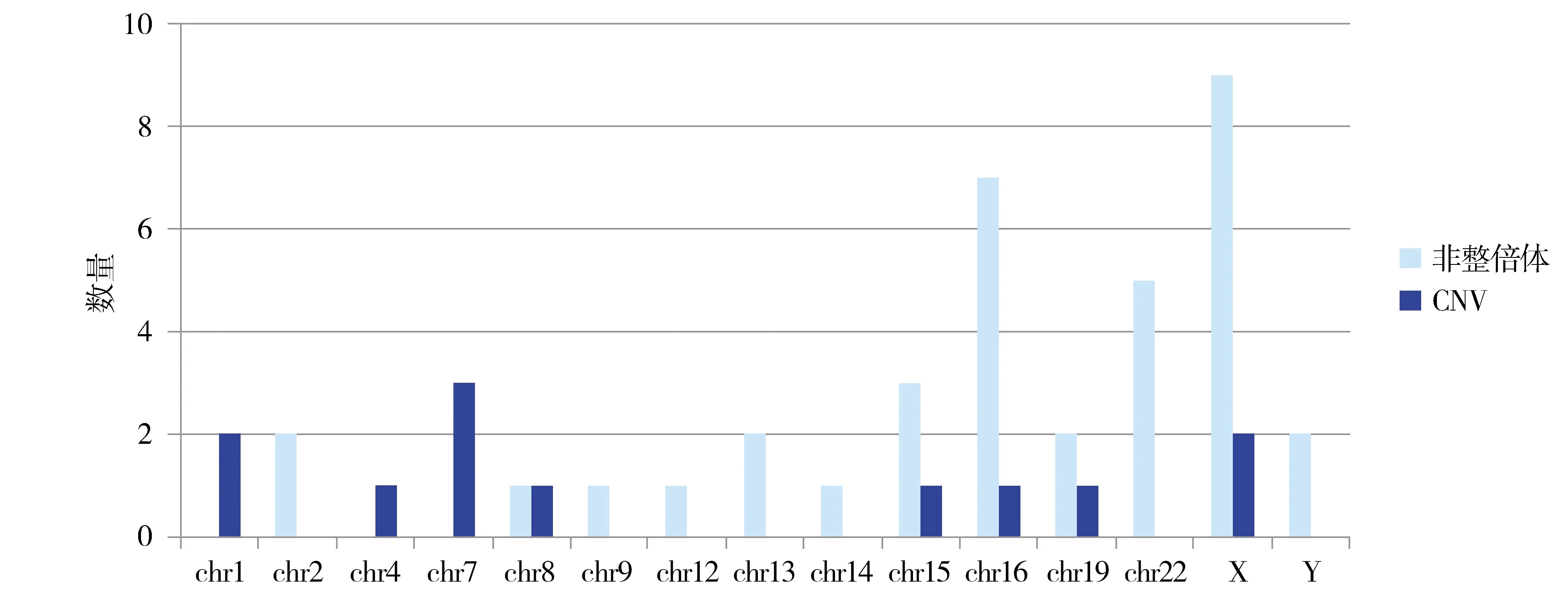
圖1 41例陽性樣本染色體異常分布情況
2.2 流產樣本特征分布情況
所有患者中,發(fā)生流產事件主要集中在孕早期(9-10周),不同孕周間的卡方檢驗得出差異無統(tǒng)計學意義(χ2=7.941,P=0.242)。91例患者中,檢出異常者41例,異常率為45.05%;將早期胚胎停育流產樣本依據年齡分為4組:25-29歲38例;30-34歲26例;35-40歲19例;>40歲8例。產婦年齡超過35歲,染色體數目異常的發(fā)生率更高,但經卡方檢驗得出差異無統(tǒng)計學意義(χ2=3.885,P=0.274);復發(fā)性流產者41例(含連續(xù)兩次自然流產者25例,連續(xù)3次及以上流產者16例),染色體數目異常高于初次流產患者,經卡方檢驗得出差異無統(tǒng)計學意義(χ2=2.231,P=0.135,見表2)。

表2 不同組別的流產組織染色體異常率比較 例(%)
3 討論
流產與多種因素有關,比較常見的有產婦生殖系統(tǒng)發(fā)育異常、病原微生物感染等,其中最主要原因是胚胎染色體異常[4,5]。孕婦及其家庭的悲傷與焦慮情緒迫切要求進行流產原因的診斷,并指導下一胎的妊娠,所以對妊娠早期流產胚胎進行遺傳學診斷,分析是否存在染色體異常,對探討孕婦在早期發(fā)生流產的病因及相應的遺傳咨詢具有重要的意義。
目前,對于流產胚胎染色體方面的檢測,最常用的方法是FISH技術,針對常見的染色體非整倍體(13,16,18,21,22三體及性染色體數目異常),及發(fā)現低比例嵌合,具有高效、特異性強等特點[6]。
細菌人工染色體標記-磁珠分離法(BoSsTM)亦是針對流產胚胎染色體數目異常的一種檢測方式,可發(fā)現所有的非整倍體(除多倍體),具有高通量、快速等特點[7]。
染色體微陣列分析技術(CMA)是對整體基因組拷貝數的單次、高通量、高敏感性、高分辨率的檢測[8,9]。可檢出所有的染色體非整倍體、多倍體,還有部分三體,對染色體多處重復、缺失及染色體微缺失/微重復綜合征能有效檢出,能發(fā)現>20%的嵌合。相較其他方法有較大優(yōu)勢。
在本研究中我們應用高通量測序技術來檢測流產組織的非整倍體和拷貝數變異,此技術具有高靈敏度、高特異度、高準確度,能夠對全基因組進行快速掃描[10]。成本相對低廉,具有臨床實際應用價值,實驗中檢出流產組織染色體CNV共91例,檢出異常41例,主要高發(fā)在8-9周,孕婦年齡30-40歲。陽性樣本中,以16,22,XO染色體發(fā)生異常幾率高,有文獻報道T16,T22是常染色體三體中導致習慣性流產最為常見的三體,會引起孕早期胎兒死亡、宮內生長受限、先天性心臟缺損、嚴重的臟器畸形等癥狀[11,12]。雙重三體較為少見,約占流產胚胎所有核型的0.21%-2.8%[13]。本研究發(fā)現1例既有雙重三體又有單體的樣本,47,XN,+16,+22,-19,7q11.1-q11.23 del 14.96 Mb;及1例2號三體和19單體,46,XN,+2,-19,7q11.1-q11.23 del 14.82 Mb。主要發(fā)生原因是雙親之一的配子形成時或妊娠受精卵卵裂時出現染色體不分離。X染色體單體發(fā)生率越高越易造成復發(fā)性流產,XO綜合征,也稱特納綜合征(Turner syndrome),患者通常表現為身材矮小、性腺發(fā)育不良、胚胎早期停育等[14],并且性染色體單體流產兒多見于年輕孕婦。染色體病發(fā)生率與染色體長度及其基因數量有關[15]。
檢出CNV 11例,根據檢測結果發(fā)現CNV的片段中包含了一些臨床意義明確的功能性基因。例如1例檢測出4號染色體p16.3-p15.31區(qū)域有約19.38 Mb的重復,此重復區(qū)域包括MKS3,CC2D2A和RPGRIP1L三個基因,這3個基因會引起眼-腦-肝-腎綜合征(COACH syndrome),數據庫Decipher、UCSC等顯示該區(qū)域重復的患者可能有智力發(fā)育遲緩、小腦發(fā)育不良、肺發(fā)育不良等臨床表現[16]。1例檢出15號染色體15q11.2區(qū)域有約0.64 Mb的缺失,該區(qū)域為致病區(qū)域,患者可能有異位腎、宮內生長遲緩、小頭畸形等臨床表現[17]。2例檢出7號染色體7q36.1區(qū)域有缺失,包含了劑量敏感基因:KMT2C,經查詢ClinGen數據庫資源,劑量致病性有充分證據(Haploinsufficiency Score:3)。該區(qū)域缺失的患者可能有精神運動發(fā)育遲緩、智力障礙多變和輕度畸形等臨床表現[18]。
本研究結果顯示復發(fā)性流產和初次流產的發(fā)生率分別為53.7%和38.0%,差異無統(tǒng)計學意義。Grande等[19]復發(fā)性流產者的異常率為60%,初次流產者的異常率為68%,差異也無統(tǒng)計學意義,與本研究結果基本一致,表示流產組織核型異常的風險與流產次數無關。隨著女性年齡的增長,卵細胞在逐漸地衰老退化,受精卵細胞內的紡錘絲老化,導致功能不全或部分喪失,易導致受精卵在減數或有絲分裂時染色體不分離,從而導致發(fā)生染色體數目異常或結構異常。本研究的數據顯示年齡≥35歲組的異常發(fā)生率高于其他組,表明女方年齡越大,發(fā)生染色體異常的幾率越大。
綜上所述,高通量測序技術應用于檢測孕早期流產組織的非整倍體及拷貝數變異具有較高的靈敏度、特異性和檢出率高,有明顯的技術優(yōu)勢,孕婦年齡越大,染色體非整倍體及拷貝數變異異常更易導致胎兒畸形、胚胎早期停育等。所以對自然流產的夫婦進行染色體異常的檢測并進行遺傳學病因分析,從而為幫助再次妊娠提供更多的指導,相信隨著技術的發(fā)展,高通量測序技術必將為早期自然流產病因診斷提供更有意義的指導信息。

