有機酸與鈣質砂反應過程及其動力學研究
潘杰,李鵬飛,李越煊,王萍,董元華,劉云
(1.中國科學院南京土壤研究所土壤環境與污染修復重點實驗室,江蘇 南京 210008;2.蘭州交通大學 化學與生物工程學院,甘肅 蘭州 730070;3.中國科學院大學,北京 100049)
碳酸鹽礦物在自然界中的形態呈現多樣化[1-2],它的溶蝕與環境問題緊密聯系[3-4]。碳酸鹽礦物的溶蝕影響礦物與土壤間的轉化[5-9]和油氣儲存與開采[10-12]。熱帶海洋區域的珊瑚島礁,主要成分為珊瑚砂,俗稱鈣質砂,屬于碳酸鹽礦物的一種[13-15],研究鈣質砂溶蝕中不同組分的溶蝕順序及速率對于深入了解島礁的演變具有重要意義。小分子有機酸可由植物根系、植物殘體及土壤中微生物分泌產生[16-19],可電離產生H+,也可為微生物提供更多碳源[20-23]。目前已有文獻報道小分子有機酸對碳酸鹽礦物的溶蝕[24-25],且在溶蝕過程中,Ca2+、Mg2+等金屬離子的析出較為明顯,在微生物固化[26-29]、工程建筑領域也有應用[30]。
本研究選取不同濃度乙酸、蘋果酸對鈣質砂進行溶蝕,通過浸泡、淋溶模擬實驗,比較鈣質砂的溶蝕速率,并分析溶蝕后的鈣質砂的組成,探討溶蝕過程及機理。
1 實驗部分
1.1 材料與儀器
HCl、乙酸、蘋果酸均為分析純;鈣質砂,取自南海某島礁。
QHZ-12B組合式型全溫度恒溫振蕩箱;BSA124S型分析天平;Optima 8000 型原子發射光譜儀;Nicolet 8700型紅外光譜儀;isss-120644 型X射線衍射儀;MERLIM型掃描電子顯微鏡。
1.2 實驗方法
1.2.1 鈣質砂的預處理 鈣質砂用自來水和去離子水反復浸泡清洗,直到浸泡液的電導低于30 μS/cm。 在70 ℃烘干,篩取1~2 mm的鈣質砂備用。
1.2.2 溶蝕實驗 稱取鈣質砂5.00 g,加入到250 mL,錐形瓶中,分別與濃度為1,10,100 mmol/L的100 mL乙酸、蘋果酸溶液混合,加蓋硅膠塞,隔絕空氣。于30 ℃、185 r/min的搖床振蕩,不同時間點取出錐形瓶,用隔膜真空泵(50 μm濾膜)快速過濾,測定濾液的pH和Ca2+、Mg2+的濃度,對溶蝕后的鈣質砂進行XRD及SEM分析。
Ca2+、Mg2+濃度采用原子發射光譜儀進行測定,使用Origin 6.5繪制曲線,Mg2+溶出動力學使用軟件Matlab擬合。
1.2.3 淋溶實驗 采用內徑3.94 cm,高12.32 cm的100 mL注射器作為淋溶柱,將烘干后130 g的鈣質砂(2~4 mm)放置于淋溶柱內,將孔徑為75 μm的尼龍布平鋪底部。以250 mL一次性輸液瓶作為儲液瓶,安裝流速調節閥,儲液瓶中乙酸、蘋果酸的濃度分別為100,10,1 mmol/L。以去離子水、通入空氣的去離子水以及1 mmol/L的鹽酸溶液作對照。每50 mL取一次樣,測定溶液中Ca2+、Mg2+濃度。采用間歇淋濾法,每24 h淋溶1次,每次250 mL,每50 mL收集一次淋出液,淋溶速率控制在20 mL/h,累積淋溶量1 050 mL。淋溶結束后,將剩余鈣質砂在75 ℃下烘72 h稱重量,與未淋溶前比較,計算損失量。
2 結果與討論
2.1 有機酸對鈣質砂的溶蝕
2.1.1 乙酸對鈣質砂的溶蝕 圖1為不同濃度乙酸與鈣質砂反應時溶液中Ca2+、Mg2+濃度隨時間的變化。

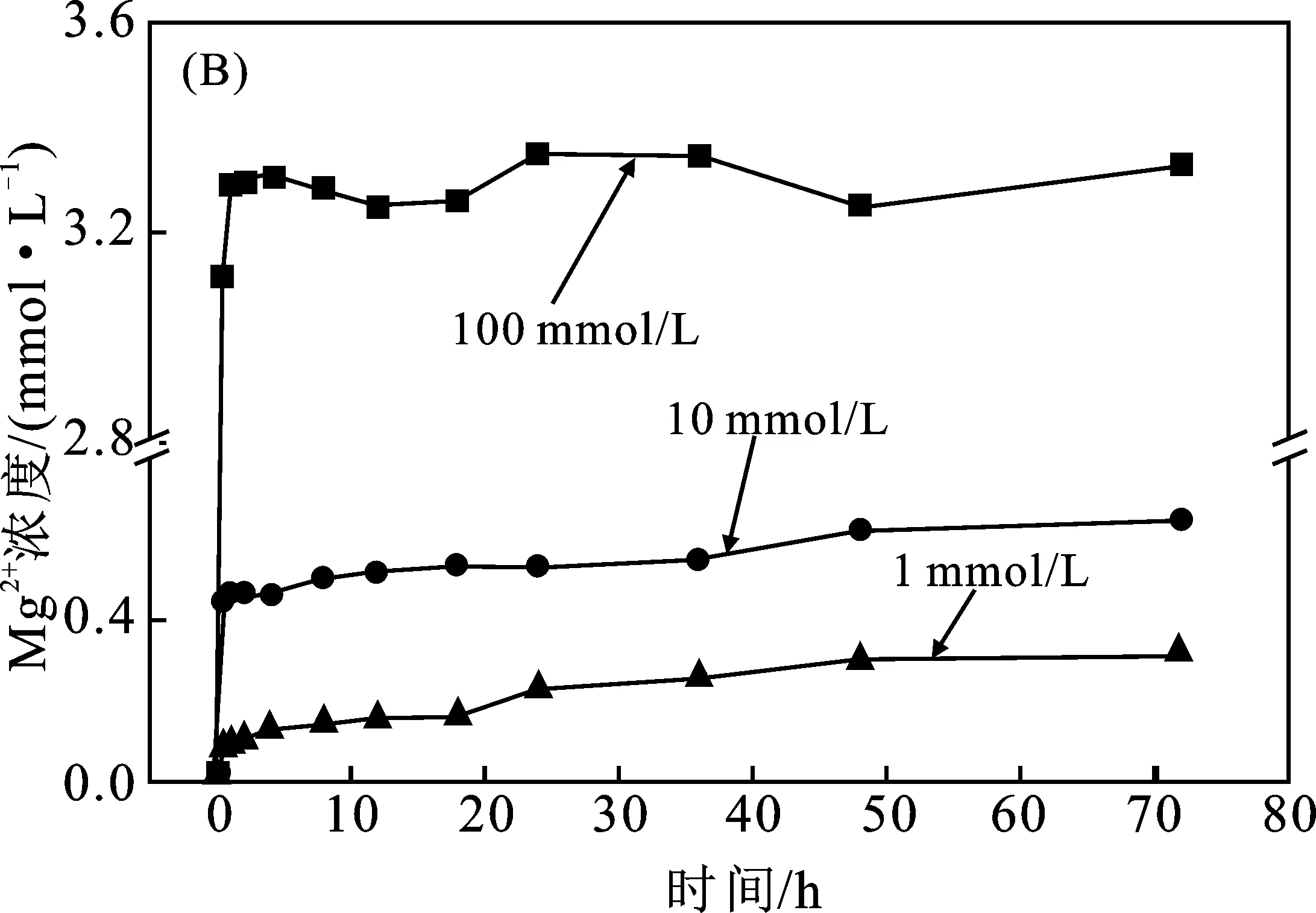
圖1 不同濃度乙酸溶蝕鈣質砂中Ca2+(A)和Mg2+(B)溶出反應動力學Fig.1 Dissolution kinetics of Ca2+(A) and Mg2+(B) respectively in calcium sands corroded by acetic acid at different concentrations
由圖1(A)可知,乙酸濃度為100 mmol/L時,溶液中Ca2+濃度在0~1 h迅速上升,1~4 h小幅降低,而4~12 h緩慢增大,隨后逐漸下降達到平衡濃度,72 h 時濃度為33.35 mmol/L;乙酸反應濃度為10 mmol/L時,溶液中Ca2+濃度在0~0.5 h迅速上升,在0.5~4 h緩慢上升達到峰值,后緩慢降低至平衡濃度,72 h 時,濃度為3.59 mmol/L;乙酸反應濃度為1 mmol/L時,Ca2+在0~2 h迅速攀升,后緩慢上升至平衡濃度,在72 h時,濃度為0.79 mmol/L。
由圖1(B)可知,乙酸濃度為100 mmol/L時,Mg2+濃度在0~1 h迅速上升,后漸至平衡濃度,72 h時濃度為3.33 mmol/L;乙酸濃度為10 mmol/L和1 mmol/L時,Mg2+濃度在0~0.5 h急劇升高,后逐漸緩慢上升至平衡,72 h時濃度分別為0.64 mmol/L和0.32 mmol/L。
2.1.2 蘋果酸對鈣質砂的溶蝕 圖2為不同濃度蘋果酸與鈣質砂反應時溶液中Ca2+、Mg2+濃度隨時間的變化。
由圖2(A)可知,蘋果酸濃度為100 mmol/L時,溶液中Ca2+濃度在0~2 h時迅速上升,2~7 h時緩慢上升隨后達到平衡,在72 h時濃度為72.26 mmol/L;當蘋果酸濃度為10 mmol/L時,Ca2+濃度在0~2 h時迅速上升,2~10 h時緩慢上升隨后達到平衡,其在72 h時濃度為9.82 mmol/L;蘋果酸濃度為1 mmol/L時,Ca2+濃度在0~0.3 h時迅速上升,0.3~10 h時緩慢上升隨后達到平衡,在72 h 時,其濃度為1.39 mmol/L。
由圖2(B)可知,蘋果酸濃度為100 mmol/L時,Mg2+濃度在0~4 h內迅速上升,4~10 h時緩慢上升隨后達到平衡,在72 h時濃度為6.81 mmol/L;蘋果酸濃度為10 mmol/L時,Mg2+濃度在0~0.67 h時迅速上升,在0.67~10 h時緩慢上升隨后達到平衡,其在72 h時濃度為1.00 mmol/L;蘋果酸濃度為1 mmol/L時,Mg2+在0~2 h時迅速上升,在2~48 h時緩慢上升逐漸達到平衡,在72 h時,其濃度為0.18 mmol/L。

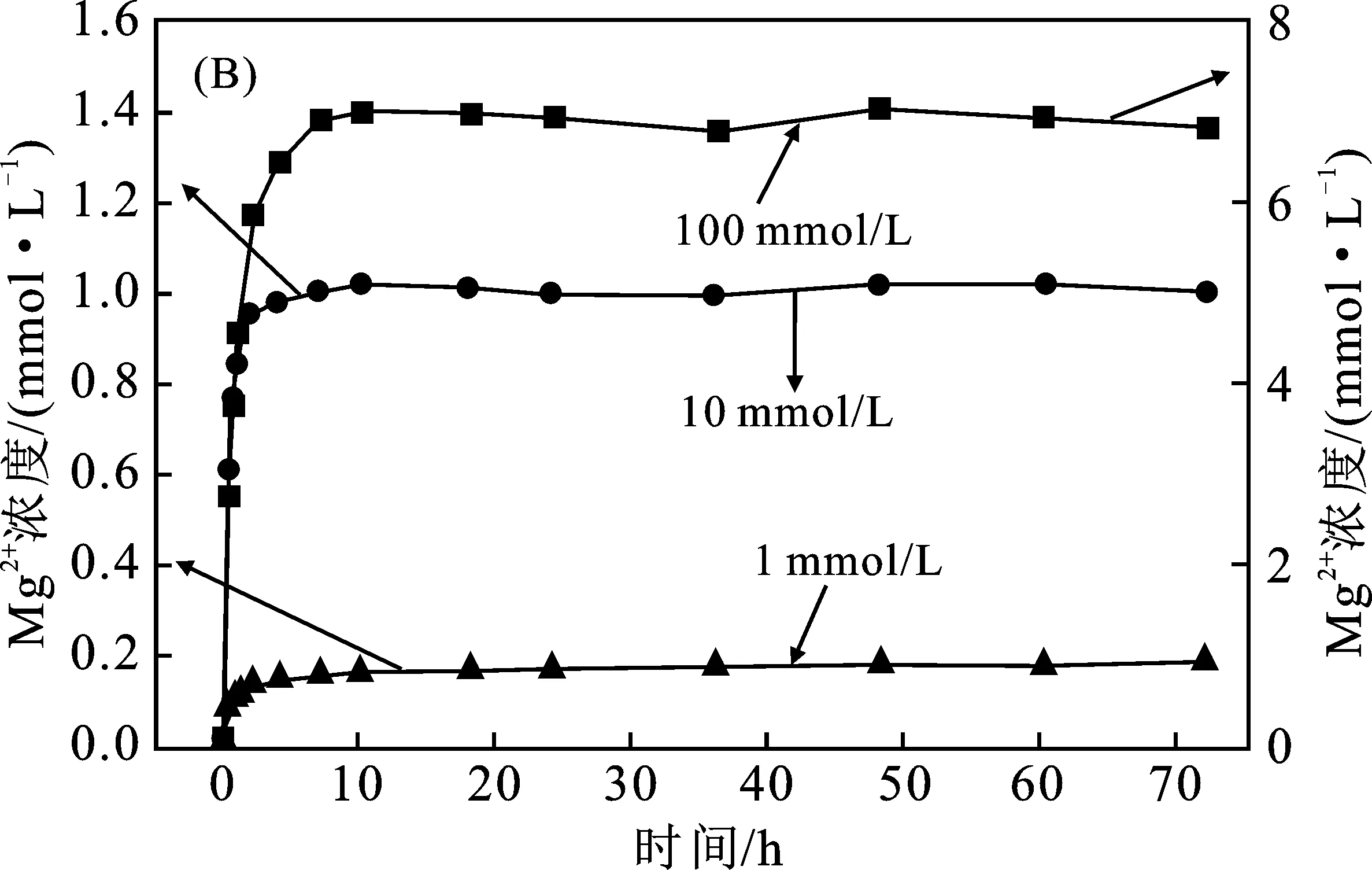
圖2 不同濃度蘋果酸溶蝕鈣質砂中Ca2+(A)和Mg2+(B)溶出反應動力學Fig.2 Kinetics of the dissolution of Ca2+(A) and Mg2+(B)respectively in calcareous sand corroded by malic acid at different concentrations
2.2 有機酸對鈣質砂的淋溶
由于不同淋溶液淋出的Ca2+、Mg2+總量相差較多,為更加方便直觀的比較不同處理組間的差異,分別將溶液中Ca2+、Mg2+淋出總量進行對數函數處理。
2.2.1 乙酸對鈣質砂的淋溶 圖3為不同濃度乙酸對鈣質砂淋溶后Ca2+、Mg2+累積淋出量隨淋溶量變化。
由圖3可知,隨著乙酸濃度的增加,Ca2+、Mg2+淋出量逐漸增大,1 mmol/L的HCl對鈣質砂中Ca2+、Mg2+的淋出量遠大于1 mmol/L乙酸淋出量,且與10 mmol/L乙酸淋出量相當。1,10,100 mmol/L乙酸對Ca2+的累積淋出量分別為39.72,235.10,1 345.43 mg, 對Mg2+的累積淋出量分別為3.60,11.24,62.30 mg。


圖3 不同濃度乙酸淋溶鈣質砂中Ca2+(A)和Mg2+(B)總量隨淋溶量的變化圖Fig.3 The change curves of the total Ca2+(A) and Mg2+(B)in acetic acid leached calcareous sand at different concentrations with the leached amount
2.2.2 蘋果酸對鈣質砂的淋溶 圖4為不同濃度蘋果酸對鈣質砂淋溶后Ca2+、Mg2+累積淋出量隨淋溶量變化。
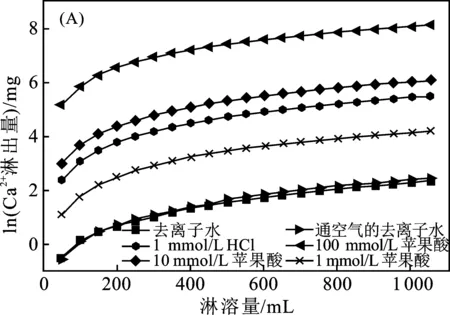
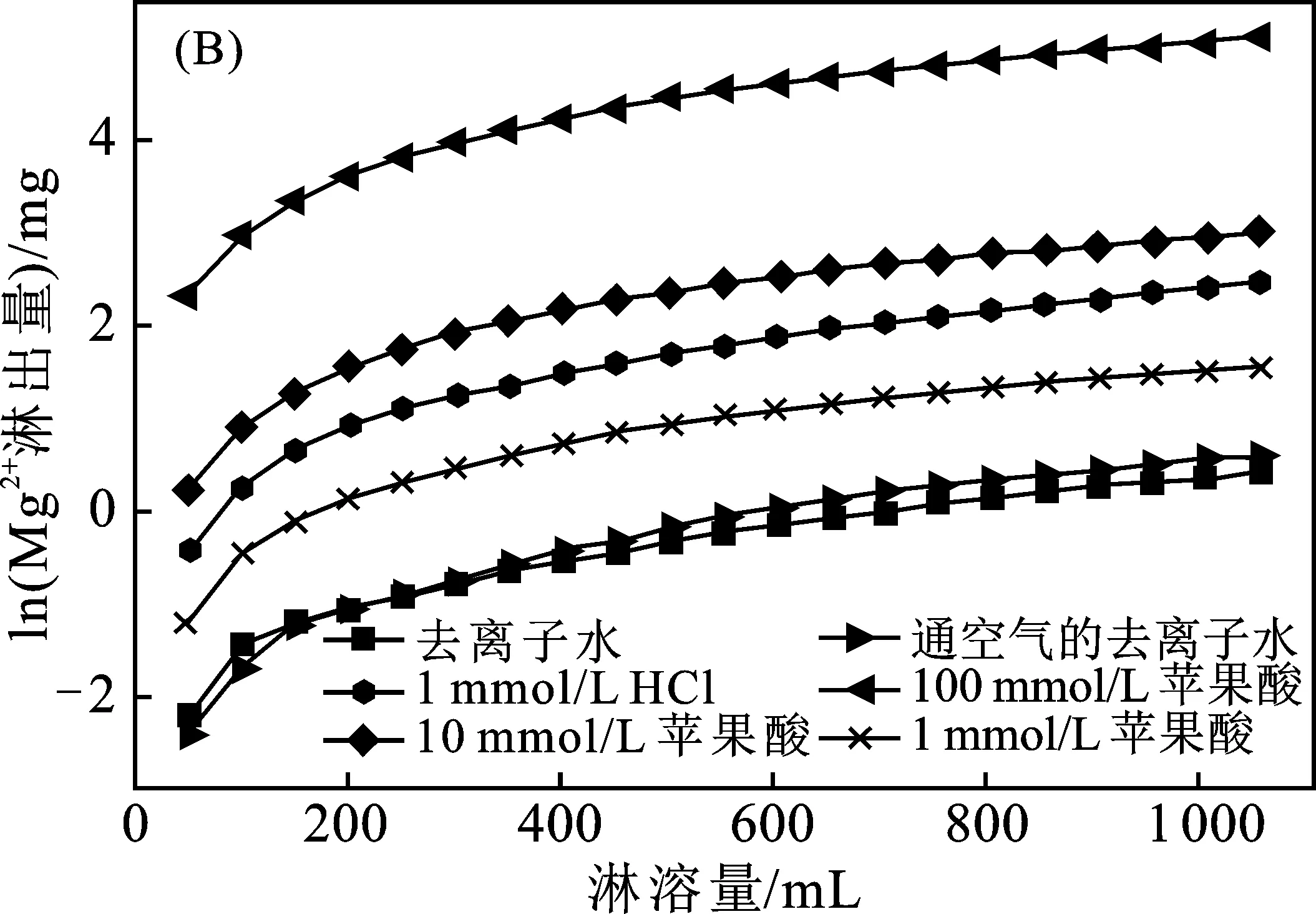
圖4 不同濃度蘋果酸淋溶鈣質砂中Ca2+(A)和Mg2+(B)總量隨淋溶量的變化曲線圖Fig.4 The change curves of the total Ca2+(A)and Mg2+(B) in malic acid leached calcareous sand at different concentrations with the leached amount
由圖4可知,隨著蘋果酸濃度的增加,淋出Ca2+、Mg2+的量逐漸增大,且由于蘋果酸為二元有機羧酸,因此蘋果酸對Ca2+、Mg2+的淋出量都高于相同濃度乙酸對Ca2+、Mg2+的淋出量。1,10,100 mmol/L蘋果酸對Ca2+的累積淋出量分別為66.86,437.28,3 353.75 mg,對Mg2+的累積淋出量分別為4.74,20.09,164.72 mg。
2.2.3 淋溶后的質量變化 將淋溶后鈣質砂烘干、稱重,與淋溶前比較,計算質量損失率,結果見表1。
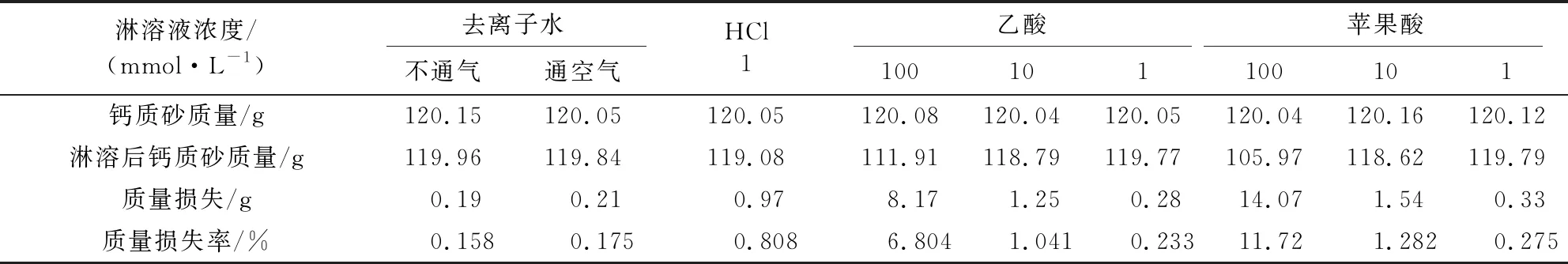
表1 淋溶后鈣質砂的質量損失Table 1 Quality loss of calcareous sand after leaching
由表1可知,隨著蘋果酸與乙酸濃度的增加,淋溶后鈣質砂的質量損失率逐漸增大,且在相同濃度的情況下,蘋果酸淋溶后的鈣質砂質量損失率均高于乙酸淋溶后的鈣質砂質量損失率。1 mmol/L的HCl淋溶后鈣質砂的質量損失率大于相同濃度的乙酸與蘋果酸淋溶后鈣質砂的質量損失率。由于通入空氣的去離子水中溶入CO2產生H2CO3,導致通空氣的去離子水淋溶后鈣質砂的質量損失率高于不通空氣的去離子水淋溶后的質量損失率。
2.3 反應前后鈣質砂的變化
2.3.1 反應前鈣質砂表面分析
2.3.1.1 XRD 用 X 射線衍射儀對反應前的鈣質砂進行物相分析,結果見圖5。

圖5 鈣質砂的X射線衍射譜圖Fig.5 X-ray diffraction spectra of calcareous sand
采用Jade 6.5分析軟件將其與PDF卡片庫中譜圖對比,可知特征譜線3.408 5(111),3.285 1(021),2.708 9(012),2.491 2(102),2.379 1(112),1.980 5(221),1.884 9(202),1.817 9(132),1.745 9(113)與文石的譜圖較為匹配;特征峰2.995 7(104)與鎂方解石的特征峰符合;少量的雜峰表明,鈣質砂中還含有少量的方解石。具體礦物組成見表2。
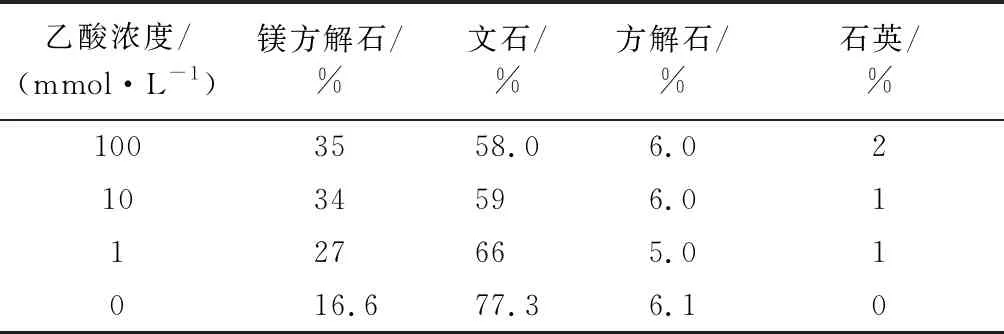
表2 不同濃度乙酸與鈣質砂反應72 h后固相部分組成Table 2 Solid phase fractionation after reaction of acetic acidand calcareous sand for 72 h
2.3.1.2 SEM 圖6為鈣質砂放大不同倍數的SEM圖片。

圖6 鈣質砂的掃描SEM圖Fig.6 SEM of calcareous sand放大1 000倍圖(A)和放大10 000倍圖(B)
由圖6可知,鈣質砂表面凹凸不平,具有多孔結構,表面有許多條狀物堆積在一起。
2.3.2 與乙酸反應后鈣質砂的變化
2.3.2.1 XRD 圖7為鈣質砂與乙酸振蕩溶蝕72 h后的XRD譜圖。
與PDF卡片庫對比可知,特征峰3.385 8(111),3.261 9(021),2.694 7(012),2.478 1(102),2.413 7(031),2.368 3(112),2.336 2(130),2.102 6(220),1.974 5(221),1.879 0(041),1.812 4(132),1.704 0(113)與文石卡片(99-0013)的特征峰相符;2.993 7(104),2.255 4(113)與鎂方解石卡片(86-2336)特征峰相符;3.037 5(104)與方解石卡片(85-1108)的特征峰相符。相較于未反應前鈣質砂組分無變化,但各組分間含量發生變化,見表2。
由表2可知,隨著乙酸濃度的增加,文石的相對含量減小,鎂方解石的相對含量增加。乙酸濃度為100 mmol/L時,文石含量減少了19.3%,鎂方解石含量增加了19.4%。故對于乙酸溶蝕鈣質砂,文石為主要的溶蝕對象。
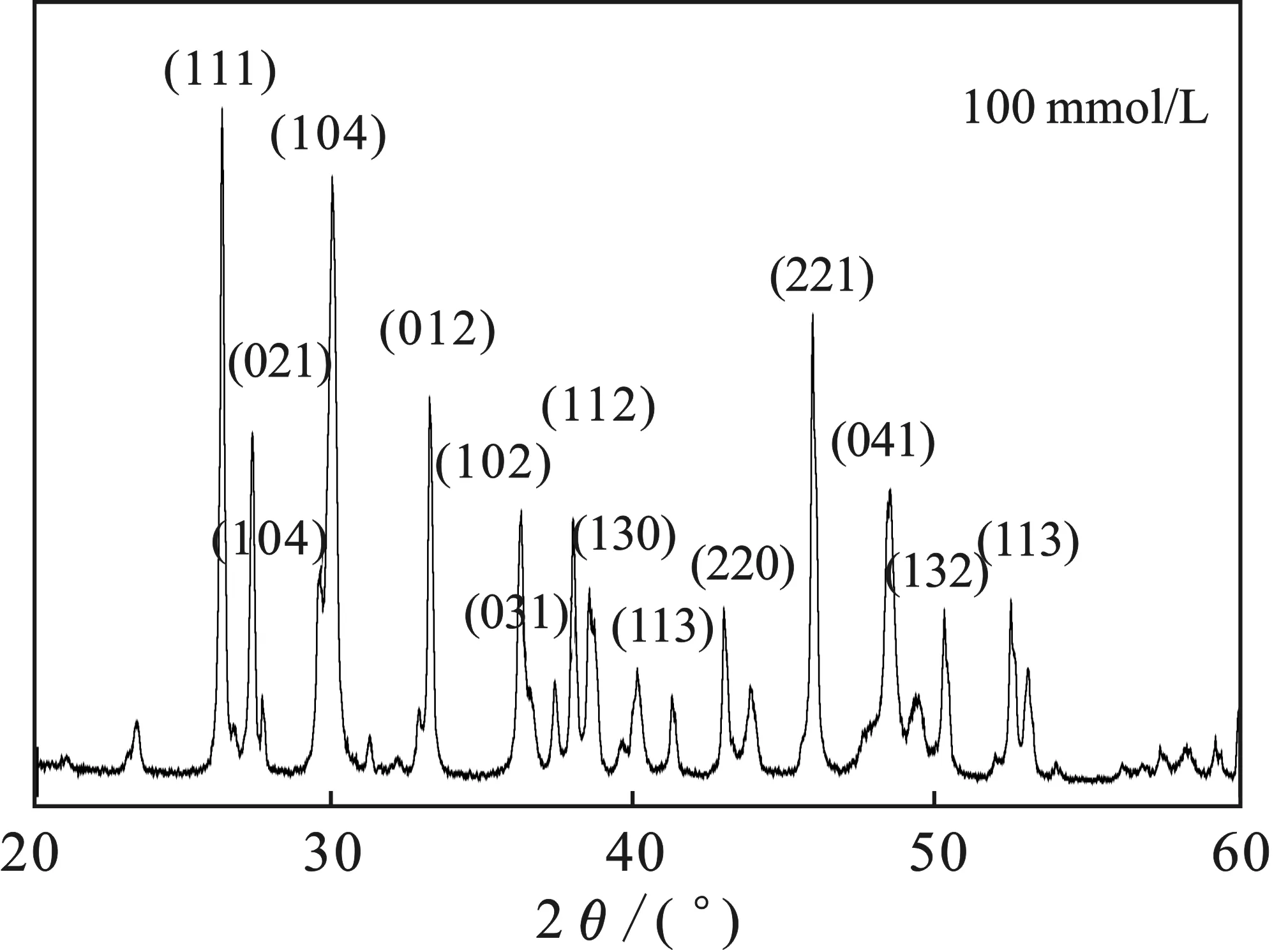


圖7 乙酸與鈣質砂反應72 h后固體部分XRD譜圖Fig.7 XRD of solids after reaction of acetic acid and calcareous sand for 72 h
2.3.2.2 SEM 圖8為鈣質砂與乙酸溶液振蕩反應72 h后固相部分的SEM圖片(放大10 000倍)。

圖8 乙酸與鈣質砂反應72 h后固體部分XRD譜圖和SEM圖Fig.8 XRD and SEM of solids after reaction of acetic acid and calcareous sand for 72 h
由圖8可知,溶蝕后的鈣質砂表面較原先平整,可能為乙酸溶蝕了文石組分,而溶蝕的鎂方解石組分較少,生成少量的CaCO3沉淀,難以觀察。
2.3.3 與蘋果酸反應后鈣質砂的變化
2.3.3.1 XRD 圖9為鈣質砂與不同濃度蘋果酸振蕩反應72 h后的XRD譜圖。
與PDF卡片庫對比可知,特征峰3.393 3(111),3.271 0(021),2.689 4(012),2.480 7(102),2.371 9(112),2.339 8(130),2.105 3(220),1.976 3(221),1.878 3(041),1.813 9(132),1.742 8(113)與文石卡片(99-0013)的特征峰匹配,特征峰2.983 9(104),2.250 0(113)與鎂方解石卡片(86-2336)的特征峰匹配;特征峰3.029 5(104)為方解石的特征峰。同乙酸溶蝕總體趨勢相同,鈣質砂組分未發生變化,但組分含量發生了變化,見表3。

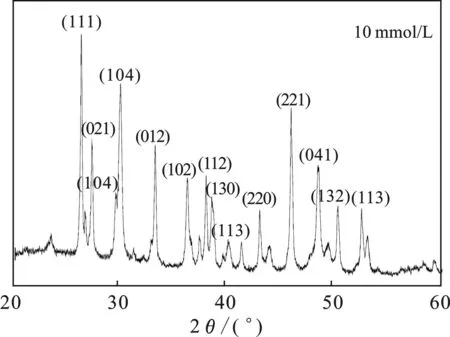
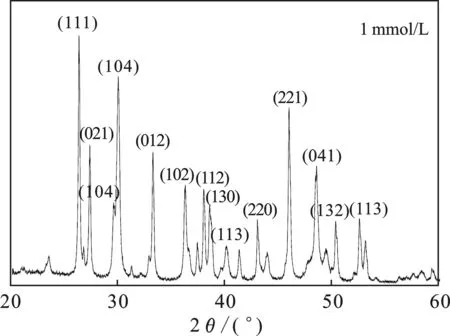
圖9 蘋果酸與鈣質砂反應72 h后固體部分XRD譜圖Fig.9 XRD of solids after reaction of malic acid and calcareous sand for 72 h
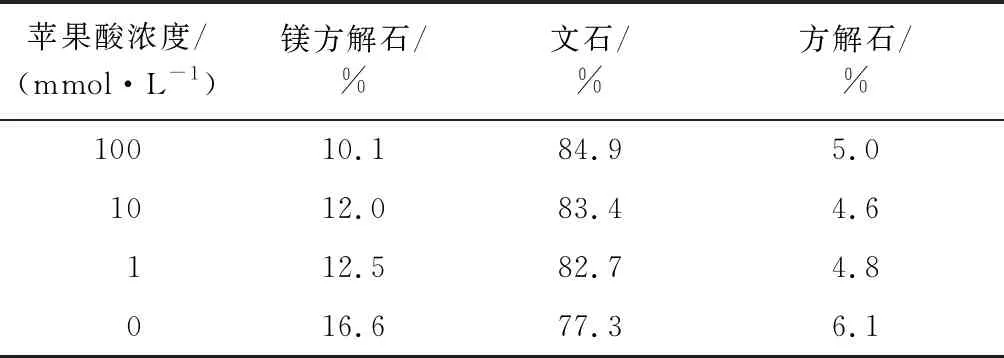
表3 不同濃度蘋果酸與鈣質砂反應72 h后固相部分組成Table 3 Solid phase fractionation after reaction of malic acid and calcareous sand for 72 h
由表3可知,隨著蘋果酸濃度的增加,鈣質砂中的鎂方解石含量逐漸降低,文石的含量逐漸增加。蘋果酸濃度為100 mmol/L時,文石的含量增加了7.6%,鎂方解石減少了6.5%,鎂方解石為反應過程中主要溶蝕對象。
2.3.3.2 SEM 圖10為蘋果酸與鈣質砂振蕩反應72 h后固相部分放大5 000倍的SEM圖。

圖10 不同濃度蘋果酸與鈣質砂反應72 h后固相部分的SEM圖Fig.10 SEM of solid phase fractions after reaction of malic acid and calcareous sand for 72 h(A)1 mmol/L;(B)10 mmol/L;(C)100 mmol/L
由圖9(C)可知,較同等濃度的乙酸溶蝕SEM圖,表面更為規則,且10(A)和10(B)表面較未溶蝕前變化不明顯。
2.3.4 有機酸溶蝕的紅外譜圖 對有機酸濃度為100 mmol/L鈣質砂溶蝕后的產物進行紅外分析,結果見圖11。
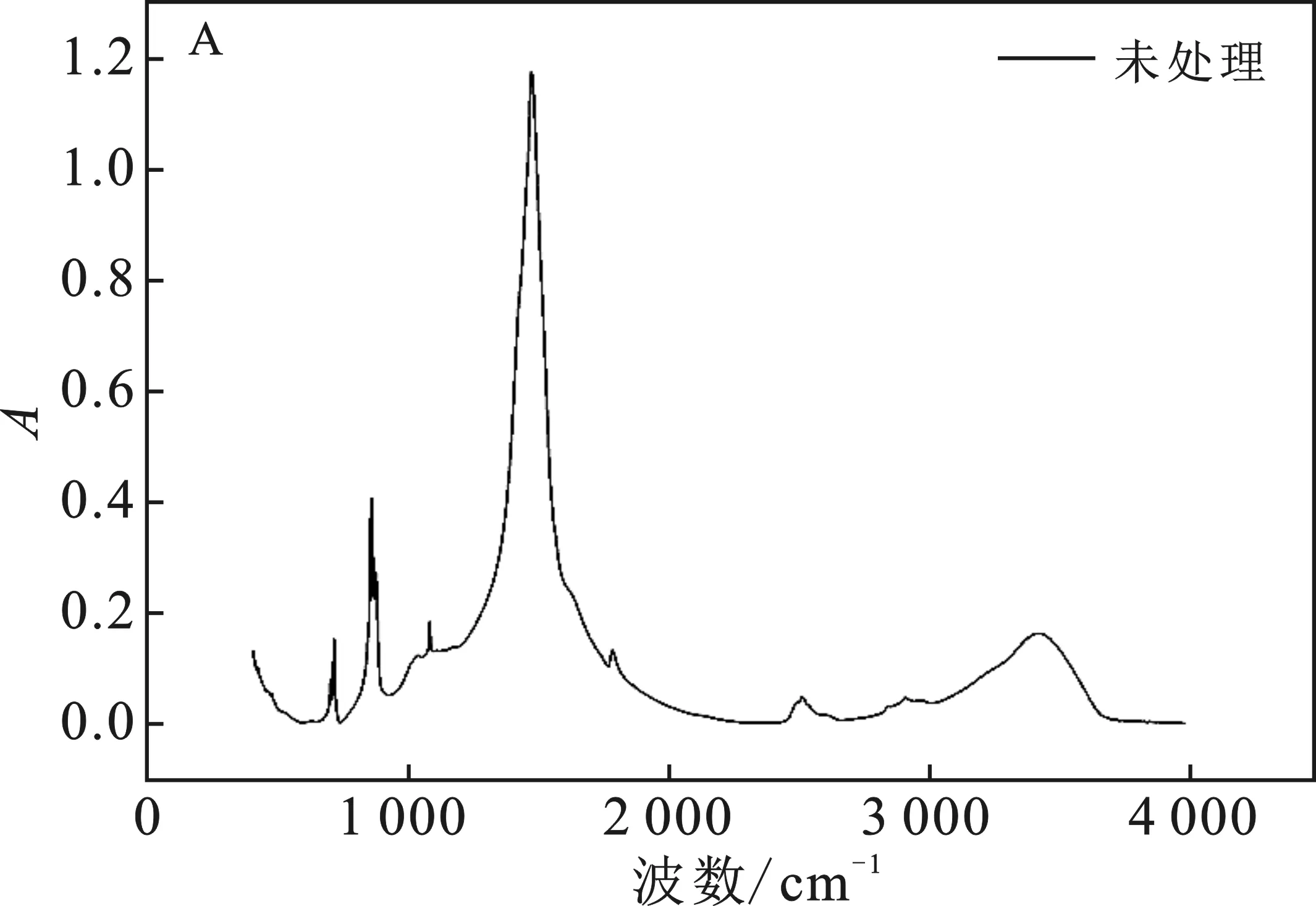
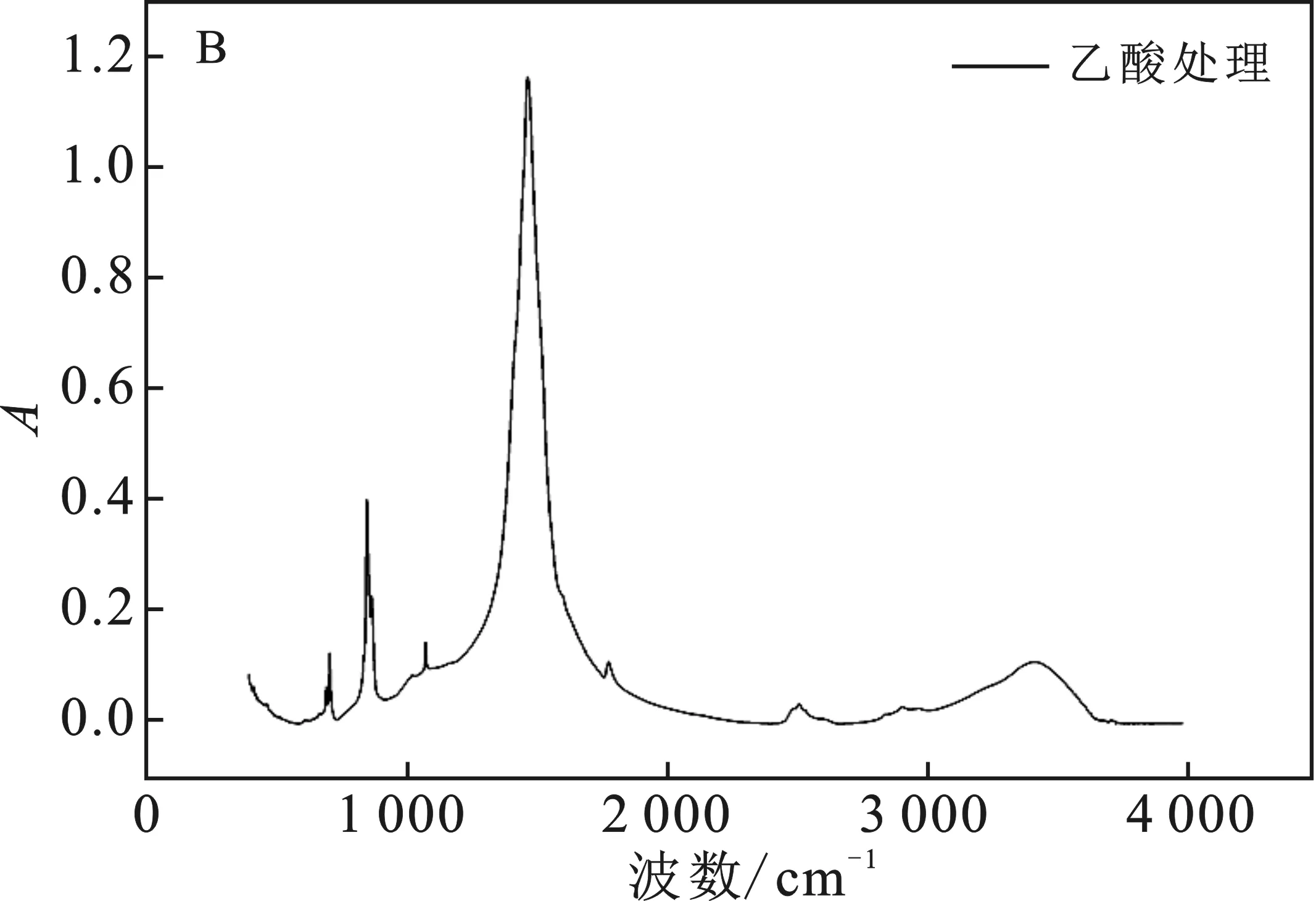
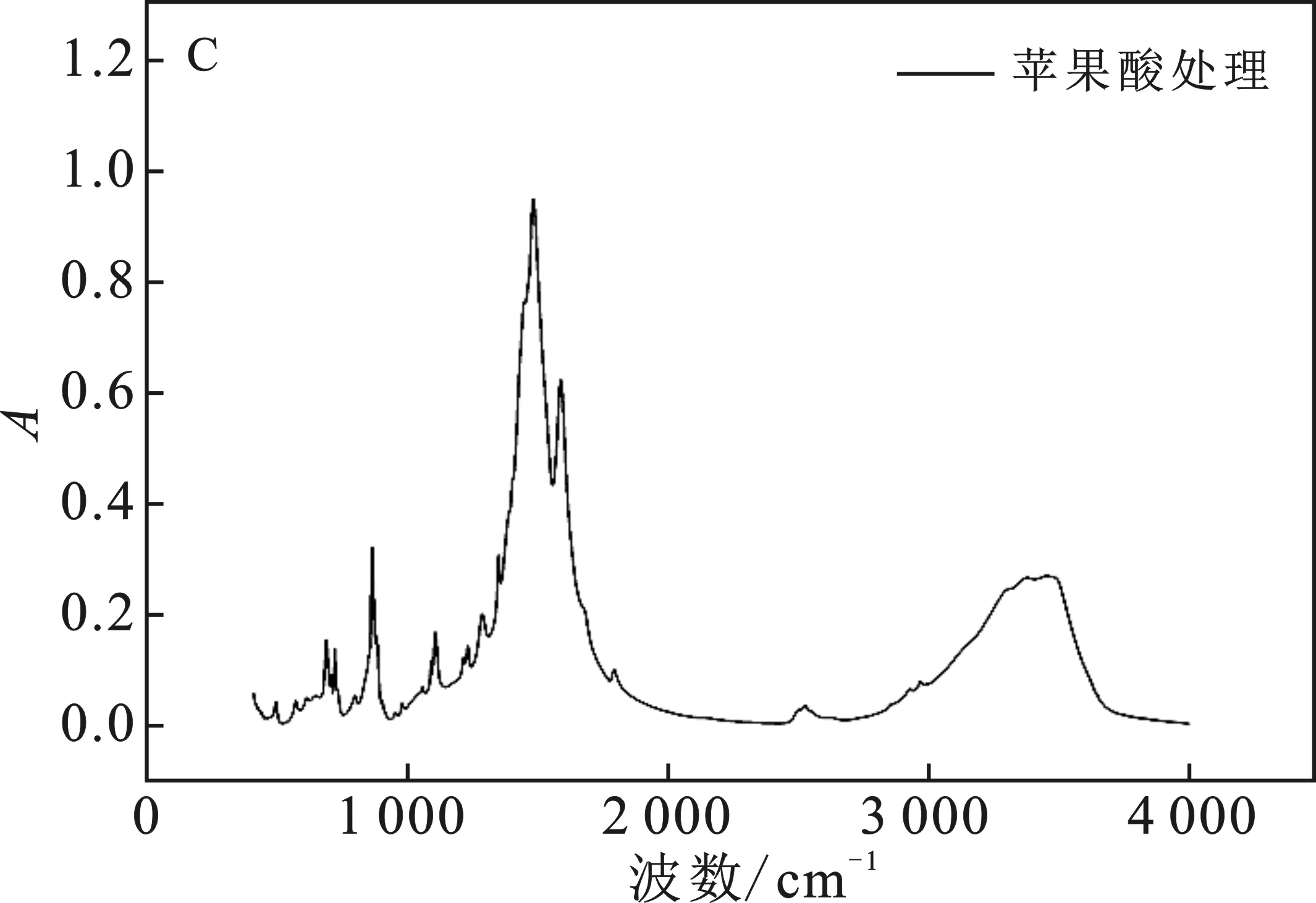
圖11 不同處理鈣質砂的紅外譜圖Fig.11 Infrared spectra of carbonate rocks treated with different organic reefs(A)未處理;(B)100 mmol/L乙酸;(C)100 mmol/L蘋果酸
由圖11可知,100 mmol/L的乙酸對鈣質砂溶蝕后產物的紅外譜圖與未處理的基本一致,而蘋果酸的溶蝕產物的檢測中,在639,680,1 582,3 454 cm-1處有不同的特征吸收峰,其中3 454 cm-1是O—H伸縮振動吸收峰;1 582 cm-1為羧酸根的對稱伸縮振動吸收峰,而DL-蘋果酸的羰基吸收峰為1 739~1 701 cm-1,此處向低波數偏移,表明與鈣形成了絡合物。
2.4 討論
鈣質砂的主要成分為CaCO3及MgCaCO3。由浸泡溶蝕實驗的Ca2+、Mg2+變化圖可知,隨著兩種酸濃度的增加,溶出的Ca2+、Mg2+濃度增大,而在初始反應的1 h內,酸的濃度很高,電離產生的H+較多,溶蝕作用最為強烈,而后Ca2+、Mg2+濃度無大的變化,表明反應趨于平衡,此過程中極少有沉淀生成。淋溶實驗中,鈣質砂經蘋果酸溶蝕后的質量損失大于乙酸,這是由于在同等濃度下,蘋果酸電離產生的H+多于乙酸的,溶蝕作用也就更加顯著。以上數據表明,溶蝕過程中,H+發揮著主要的作用,乙酸、蘋果酸與鈣質砂主要發生如下反應:

Ca2+(aq)+H2O(l)+CO2
(1)

Ca2+(aq)+ Mg2+(aq)+H2O(l)+CO2
(2)
在溶蝕過程中,乙酸與蘋果酸根離子會與Ca2+產生絡合物,溶蝕后產物X衍射分析表明,3種濃度乙酸溶液溶蝕的產物中并未找到乙酸鈣的特征峰,且定量分析后也未發現乙酸鈣沉淀的成分,可能是由于乙酸鈣溶解度大,在水溶液中很難會產生沉淀,或產生極少量沉淀,難以檢測到,對產物進行紅外分析也未發現乙酸鈣的存在。在蘋果酸溶蝕產物的XRD譜圖中也未發現與蘋果酸鈣相符的特征峰,隨后對其濃度為100 mmol/L的蘋果酸溶蝕產物進行紅外分析,觀察到了蘋果酸鈣官能團的特征吸收峰。
在小分子有機酸溶蝕鈣質砂的過程中不僅存在Ca2+離子的溶出反應,而且存在Ca2+被酸根離子固定絡合的反應以及碳酸鈣的重結晶的反應,溶液中測得的Ca2+濃度不能代表鈣質砂溶出Ca2+的實際濃度,因此不能簡單的通過數學模型對溶液中Ca2+離子濃度進行動力學模擬,故本研究中只對溶液中Mg2+濃度進行了動力學模擬。通常,鹽類礦物溶解動力學多數受擴散過程、表面反應過程以及擴散過程和表面反應過程的綜合影響[31-32]。當體系中溶解的離子濃度主要受擴散作用的影響時,可以用Stumm微分方程(方程3)來表示[33],當溶解過程同時受擴散過程和界面反應過程影響并伴有化學反應時,可用Srumm的修正方程(方程4~6)來表示。通過在matlab程序中運用方程(3~6)對鈣質砂中Mg2+溶出的溶解動力學進行計算擬合發現,方程(3)對Mg2+濃度隨時間的變化曲線的擬合度較高,因此我們推測Mg2+的溶出主要受擴散過程的影響。對溶出曲線進行擬合[34-35],具體動力學方程見表4,由動力學方程可知,隨著乙酸濃度的逐漸增大,表觀速率常數逐漸增加,隨著蘋果酸濃度的逐漸增大,表觀速率常數逐漸減小。
dC/dt=K(Cs-Ct)n
(3)
dC/dt=K(Cs-Ct) +K2
(4)
dC/dt=K(Cs-Ct)n+Ct-K2
(5)
dC/dt=K(Cs-Ct)n(Ct-K2)
(6)
式中,Cs為溶液中溶解離子平衡時濃度,Ct為t時刻溶解離子的濃度,K為表觀速率常數,n為反應級數。

表4 不同體系中Mg2+的溶解動力學方程Table 4 Dissolution kinetics equation of Mg2+ in different concentrations of oxalic acid system
3 結論
(1)有機酸溶蝕鈣質砂的過程中,Ca2+、Mg2+為主要的溶出物,且Ca2+、Mg2+的溶出速率及程度隨乙酸、蘋果酸濃度的增加而增大;蘋果酸對鈣質砂的溶蝕速率及程度強于乙酸。
(2)Ca2+、Mg2+的溶出過程中,主要受擴散過程的控制,可通過Stumm微分方程對其中的Mg2+進行擬合。
(3)在模擬溶蝕過程中,鈣質砂中的文石、鎂方解石組分含量發生主要的變化。
(4)不同濃度乙酸與蘋果酸對鈣質砂的淋溶模擬實驗發現,這一過程能夠顯著地減少鈣質砂的質量比例,且隨著酸濃度的增大,淋溶導致的質量損失也會逐漸變大。

