漆籽油納米乳液的制備及其抗氧化、防紫外輻射活性研究
周 昊,薛興穎,陳虹霞,葉建中,王成章
(中國林業科學研究院 林產化學工業研究所;生物質化學利用國家工程實驗室;國家林業和草原局林產化學工程重點實驗室;江蘇省生物質能源與材料重點實驗室;江蘇省林業資源高效加工利用協同創新中心,江蘇 南京 210042)
漆籽是我國重要經濟林樹種漆樹(Toxicodendronvernicifluum)的種子[1]。漆籽油是從漆籽種仁中提取的油脂,為黃色透明狀的液體油脂,具有特有的香氣。漆籽油是一種富含不飽和脂肪酸的功能性油脂,其含亞油酸≥63%,含油酸≥23%[2-3],具有調節血脂、消炎止痛、降低膽固醇、延緩衰老等保健功能和護膚功效,其在功能食品和化妝品領域具有很好的應用前景[4-5]。然而由于漆籽油中不飽和脂肪酸含量極高,在貯藏加工過程中極易被氧化,且水溶性差、生物利用率低等特點,限制了其產品開發與應用。近年來,納米乳液作為一種簡單有效的制劑,已被廣泛應用于功能性油脂的包埋與傳遞,能夠防止油脂的功能營養成分被氧化,并提高其水溶性和生物利用率[6-7]。納米乳液平均粒徑在50~500 nm,是由水相、油相、表面活性劑及助表面活性劑等按照一定比例混合所形成的熱力學穩定的膠體分散體系。納米乳液的制備方法包括高能乳化法和低能乳化法,其中高壓均質乳化技術是最常用的一種制備納米乳液的高能乳化法,高壓均質法具有乳化時間短、乳液粒徑小、體系穩定、表面活性劑的用量少等優勢[8-10]。目前,已有文獻報道通過高壓均質乳化技術制備乳木果油、沙棘果油、紫蘇籽油、核桃油等納米乳液,但是還未見通過高壓均質乳化法制備漆籽油納米乳液的相關報道[11-13]。本研究采用高壓均質法制備漆籽油納米乳液,考察壓力、均質次數、乳化劑用量及油添加量等參數對納米乳液平均粒徑及 Zeta電位的影響,優化納米乳液制備工藝條件,并對制得的漆籽油納米乳液特性及穩定性、抗氧化和抗紫外輻射活性進行研究,以期為漆籽油日化產品及保健品開發應用提供理論基礎。
1 實 驗
1.1 材料與試劑
漆籽油,購于陜西秦喬農林生物科技有限公司;酪蛋白酸鈉、1,1-二苯基-2-三硝基苯肼(DPPH)、2,2′-聯氮-雙-3-乙基苯并噻唑啉-6-磺酸(ABTS)、VC、二甲基亞砜(DMSO),購于阿拉丁試劑上海有限公司;改良伊格爾(DMEM)液體培養基、四甲基偶氮唑藍(MTT)溶液,購于南京諾爾曼生物技術有限公司;小鼠成纖維細胞 NIH 3T3,購于中國醫學科學院細胞中心;其他試劑均為分析純。
1.2 漆籽油納米乳液的制備
以酪蛋白酸鈉為乳化劑,取一定量的乳化劑溶解于去離子水中,磁力攪拌器室溫下攪拌過夜,作為水相,漆籽油為油相,將油相與水相溶液按質量比6 ∶100混合均一,用高速分散機在20 000 r/min 下剪切5 min,形成粗乳液。然后將粗乳液用高壓均質機進行均質,在一定均質壓力和均質次數條件下,制備得到漆籽油納米乳液。
制備過程中分別以乳化劑質量分數、漆籽油質量分數、均質壓力、均質次數為考察因素進行單因素試驗,測定不同條件下制備的漆籽油納米乳液的平均粒徑和Zeta電位。
1.3 漆籽油納米乳液的表征
1.3.1穩定性考察 將制備的漆籽油納米乳液分別于4,25和60 ℃條件下放置30 d,每5 d測定1次乳液的平均粒徑和Zeta電位值。
1.3.2平均粒徑、PDI及Zeta電位的測定 取適量的待測納米乳液用去離子水稀釋1 000倍后,搖晃均勻,用英國Malvern公司ZS90型納米粒度及Zeta電位分析儀,分別測定制備的漆籽油納米乳液的平均粒徑、多分散指數(PDI)及Zeta電位。
1.4 漆籽油納米乳液的抗氧化活性
1.4.1DPPH 自由基(DPPH·)清除能力 配制質量濃度分別為5、10、20、40、60、80和100 mg/L的漆籽油納米乳液,精密吸取0.2 mL的漆籽油納米乳液與4 mL的0.2 mmol/L的DPPH乙醇溶液混合均勻,于暗處反應30 min后,在517 nm下測吸光度A1。空白實驗組以0.2 mL乙醇溶液代替漆籽油納米乳液,其他操作不變,所得吸光度為A2;陽性對照組以0.2 mL系列濃度的VC溶液替代漆籽油納米乳液,其他操作不變。計算樣品對DPPH·的清除能力,清除率=(1-A1/A2)×100%,并求出有效中濃度(EC50)。
1.4.2ABTS 自由基(ABTS+)清除能力 取7 mmol/L ABTS 溶液5 mL與88 μL 的140 mmol/L過硫酸鉀溶液混合,室溫、避光靜置,15 h后用超純水稀釋至溶液在734 nm波長下吸光度約為0.7,所得溶液即為ABTS+溶液。配制質量濃度分別為5、10、20、40、60、80和100 mg/L的漆籽油納米乳液,精密吸取0.2 mL的漆籽油納米乳液與2 mL配制好的ABTS+溶液混合均勻,避光反應10 min后,在734 nm下測吸光度A′1。空白實驗組以0.2 mL乙醇溶液代替漆籽油納米乳液,其他操作不變,所得吸光度為A′2;陽性對照組以0.2 mL系列濃度的VC溶液替代漆籽油納米乳液,其他操作不變。計算樣品對ABTS+的清除能力,清除率=(1-A′1/A′2)×100%,并求出EC50。
1.4.3羥基自由基(OH·)清除能力 配制質量濃度分別為5、10、20、40、60、80和100 mg/L的漆籽油納米乳液。在10 mL比色管中分別加入1.0 mL的漆籽油納米乳液,1.0 mL濃度為 2 mmol/L的水楊酸乙醇溶液,1.2 mL濃度為 1.0 mmol/L的FeSO4溶液以及1.0 mL濃度為2.0 mmol/L的H2O2溶液,反應0.5 h后,在580 nm測其吸光值A″1。空白實驗組以1.0 mL蒸餾水代替漆籽油納米乳液,其他操作不變,所得吸光度為A″2;陽性對照組以1.0 mL系列濃度的VC溶液替代漆籽油納米乳液,其他操作不變。不加H2O2時580 nm處的吸光值為A″3。計算樣品對OH·的清除能力,清除率=[1-(A″1-A″3)/A″2]×100%,并求出EC50。
1.5 漆籽油納米乳液的抗紫外輻射活性
1.5.1對NIH 3T3細胞生長的影響 將小鼠成纖維細胞 NIH 3T3 以6 000個/孔接種至96孔細胞培養板中,置于體積分數為5%的CO2培養箱中在37 ℃下培養24 h,棄去上清液,用DMEM培養基配制質量濃度為20 mg/L的漆籽油納米乳液,然后再用DMEM培養基進行逐級稀釋成系列質量濃度的漆籽油納米乳液(10、5、2.5、1.25、0.625和0.312 5 mg/L),分別加入培養板中,對照組加入DMEM培養基,每孔100 μL,孵育24 h后,采用MTT法進行檢測。
1.5.2UVA輻射NIH 3T3細胞損傷模型 將NIH 3T3細胞分為6組:正常細胞對照組和5個UVA損傷組。用DMEM培養基將NIH 3T3細胞培養至融合度 70%~80%,置于96孔板中,每孔加入100 μL細胞懸液,每組4個復孔,孵育24 h后,各UVA 損傷組進行紫外輻照處理,細胞距輻照光源15 cm,輻照強度5.4 W/m2,輻照時間分別為15、20、30、60和120 min,繼續培養24 h后,采用MTT法進行檢測。
1.5.3體外抗UVA輻射實驗 將細胞隨機分為3組:細胞對照組、UVA損傷組、UVA損傷+漆籽油納米乳液組。將NIH 3T3細胞接種至96孔細胞培養板中(6 000個/孔),置于體積分數為5%的CO2培養箱中在37 ℃下培養24 h,先將UVA損傷組、UVA損傷+漆籽油納米乳液組按損傷模型結果接受UVA 輻射,然后UVA損傷+漆籽油納米乳液組分別加入系列質量濃度(10、5、2.5、1.25、0.625和0.312 5 mg/L)的漆籽油納米乳液,細胞對照組和UVA損傷組則加入DMEM培養基,孵育24 h后,采用MTT法進行檢測。
1.5.4MTT法檢測 參照文獻[16],在細胞培養板每孔加入20 μL的質量濃度為5 g/L的MTT溶液,繼續培養4 h后,棄去上清液,加入100 μL/孔的DMSO,避光振蕩15 min,酶標儀檢測光密度(OD)值,檢測波長為570 nm時的吸光值,計算細胞存活率。細胞存活率=實驗吸光值÷空白對照吸光值×100%。
2 結果與討論
2.1 漆籽油納米乳液的制備工藝優化
2.1.1乳化劑用量 分別配制質量分數為1.5%、2.0%、2.5%、3.0%和3.5%的酪蛋白酸鈉水溶液,室溫下攪拌過夜,然后緩慢加入水相質量6%的漆籽油,用高速分散機按1.2節條件進行制備,均質壓力選擇100 MPa,均質4次得漆籽油納米乳液。乳液的平均粒徑及Zeta電位絕對值見圖1(a)。
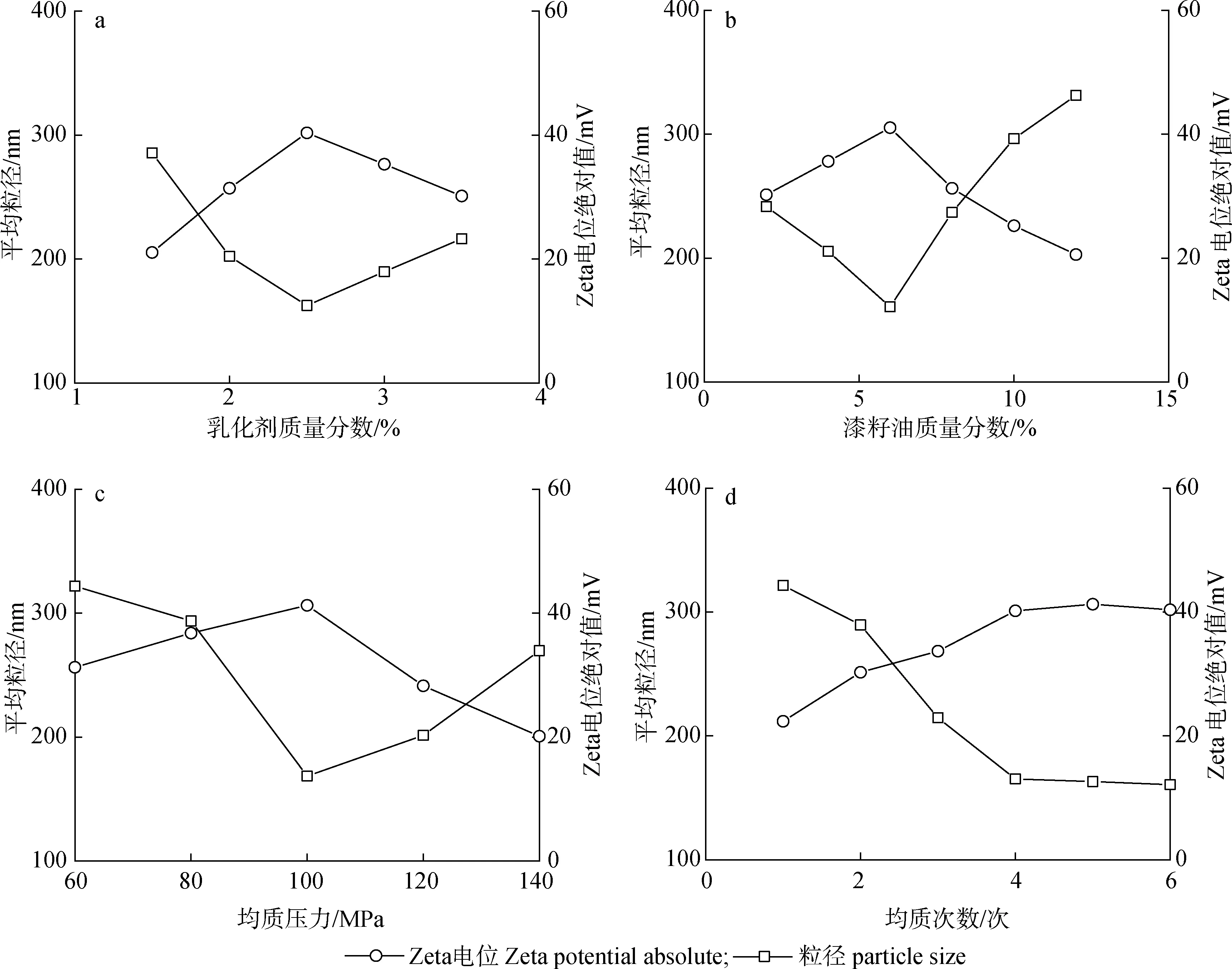
a.乳化劑質量分數mass fraction of emulsifier;b.漆籽油質量分數mass fraction of lacquer oil;c.均質壓力homogeneous pressure;d.均質次數number of homogen圖1 不同工藝條件下乳液的平均粒徑及Zeta電位絕對值Fig.1 Average particle size and Zeta potential absolute value of nanoemulsion under different process condition
由圖可知,隨著乳化劑用量的增加,漆籽油納米乳液的平均粒徑先減小后增大,Zeta電位絕對值先逐漸升高后又降低。當乳化劑質量分數為2.5%時,乳液具有最小的平均粒徑為162.5 nm,最大的Zeta電位絕對值為40.36 mV,此時乳液的穩定性最好。隨著乳化劑用量增加,它可以包裹更多的油滴,降低表面張力,減小乳化時能量的消耗,提高乳化效率,從而使平均粒徑減小;但是當乳化劑用量進一步增加時,納米乳液的平均粒徑反而增大,因為體系中沒有足夠的油滴被乳化劑吸附,多余的乳化劑部分以膠束的形式存在于體系中,使得乳液微粒發生聚合現象,粒徑增大,穩定性也會降低[10-11]。因此,選擇乳化劑質量分數為2.5%。
2.1.2漆籽油質量分數 配制質量分數為2.5%的酪蛋白酸鈉水溶液,室溫下攪拌過夜,然后分別緩慢加入質量分數2%、4%、6%、8%、10%和12%的漆籽油,用高速分散機按1.2節條件進行制備,均質壓力選擇100 MPa,均質4次得漆籽油納米乳液。乳液的平均粒徑及Zeta電位絕對值見圖1(b)。由圖可知,隨著漆籽油質量分數的增加,漆籽油納米乳液的粒徑呈現先下降后上升的趨勢,Zeta電位絕對值呈現先上升后下降的趨勢。油脂含量在一定范圍內,乳化劑可較好地乳化所加入的油脂,形成穩定的納米乳液,而當油脂加入量過大時,相同乳化劑為了乳化更多的油脂,則需要増大所乳化的油滴體積,降低油滴與水相的接觸面積,導致體系粒徑的增大,穩定性也變差,因此油脂含量過大不利于形成粒徑小且穩定的納米乳液[12-13]。漆籽油質量分數為6%時,乳液的粒徑最小,Zeta電位絕對值最大,乳液最穩定,因此最佳的漆籽油添加量為6%。
2.1.3均質壓力 配制質量分數為2.5%的酪蛋白酸鈉水溶液,室溫下攪拌過夜,然后緩慢加入6%的漆籽油,用高速分散機按1.2節條件進行制備,設定均質壓力分別為60、80、100、120和140 MPa,均質4次得漆籽油納米乳液。乳液的平均粒徑及Zeta電位絕對值見圖1(c)。由圖可知,隨著均質壓力的增加,漆籽油納米乳液的粒徑呈現先下降后上升的趨勢,Zeta電位絕對值呈現先上升后下降的趨勢。高壓均質過程中,乳液分散相顆粒在巨大剪切、撞擊空穴效應的作用下,逐漸形成納米乳滴。隨著均質壓力的增加,機械力輸出強度增大,顆粒粒徑變小。當均質壓力高于100 MPa時,此時機械輸出作用過強,分散相粒徑的比表面積急劇增加,有限的乳化劑不能被有效吸附到所有液滴表面上,乳化作用下降,液滴相互聚集,粒徑會變大,乳液體系也會變得不穩定[14-15]。均質壓力為100 MPa時,乳液的粒徑最小,Zeta電位絕對值最大,乳液最穩定,因此最佳的均質壓力為100 MPa。
2.1.4均質次數 配制質量分數為2.5%的酪蛋白酸鈉水溶液,室溫下攪拌過夜,然后緩慢加入6%的漆籽油,用高速分散機按1.2節條件進行制備,均質壓力選擇100 MPa,設定均質次數分別為1、2、3、4、5和6次,制得不同的漆籽油納米乳液。不同均質次數條件下乳液的平均粒徑及Zeta電位絕對值見圖1(d)。由圖可知,隨著均質次數的增加,漆籽油納米乳液的粒徑呈現下降趨勢,Zeta電位絕對值呈現上升趨勢。但是當均質次數超過4次時,乳液粒徑和Zeta電位絕對值變化不大。高壓均質過程中,在一定均質壓力下,隨著均質次數的增加,乳液粒徑大小會下降,隨著均質循環次數的增加,其機械作用時間變長,之前未被均質細化的大顆粒或小顆粒聚集體在多次均質后粒徑減小,乳液乳滴也更加穩定[15]。在實際應用中,均質次數的選擇對節約成本、減少機器工作時間有重要作用,綜合考慮,選擇均質次數為4次。
2.1.5驗證實驗 通過單因素試驗,確定漆籽油納米乳液的較佳工藝條件為:乳化劑質量分數2.5%,漆籽油質量分數6%,均質壓力為100 MPa,均質次數4次。按此工藝條件制備 3 批漆籽油納米乳液,測定平均粒徑分別為162.5、165.3和161.2 nm,平均值為163.0 nm;PDI分別為0.215、0.228和0.232,平均值為0.225;Zeta電位分別為-40.36、-41.39和-41.28 mV,平均值為-41.01 mV;由數據可知,漆籽油納米乳液分布均一,說明該制備方法可行,工藝的重復性良好。
2.2 漆籽油納米乳液的穩定性
乳液在運輸貯藏過程中,溫度對其理化穩定性具有顯著影響[6]。溫度升高會引起納米乳液體系內的粒子受熱吸收能量,遷移活動加劇,布朗運動增強,進而引起乳液的破乳或液滴聚合等現象。因此,如何使乳液在保質期內保持良好的物理穩定性是其應用于食品、化妝品等領域的重要問題。將漆籽油納米乳液在 4、25和60 ℃條件下貯藏 30 d,結果如表1所示。
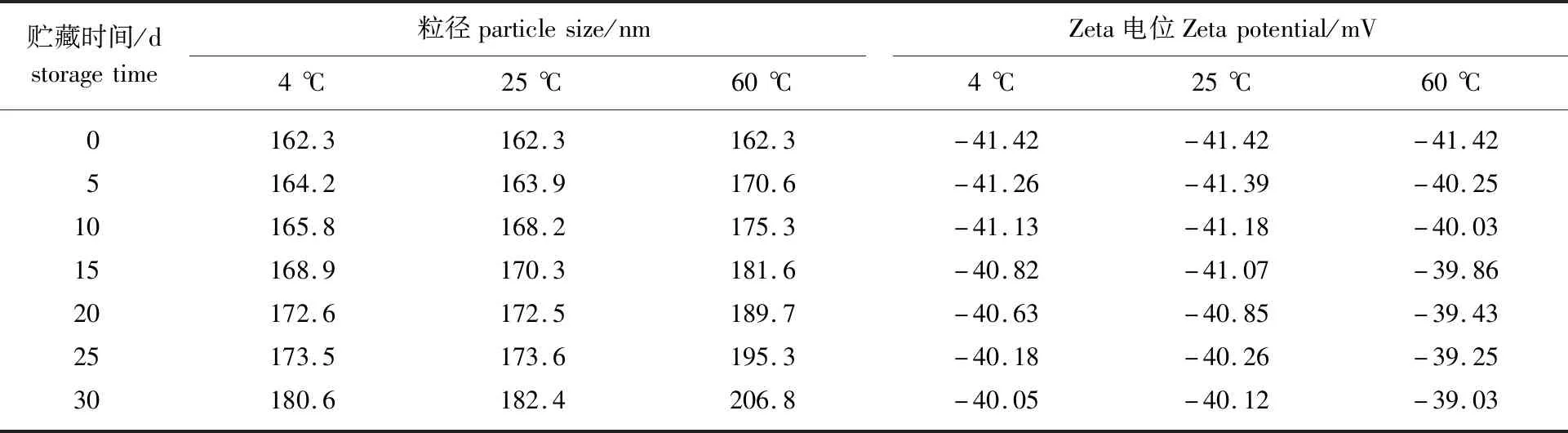
表1 不同溫度貯藏過程中漆籽油納米乳液的穩定性Table 1 The stability of lacquer seed oil during different temperature storage
在4和25 ℃貯藏溫度下,30 d內漆籽油納米乳液平均粒徑和 Zeta電位值變化較小。在4 ℃貯藏30 d后,乳液的平均粒徑由162.3 nm增加到 180.6 nm,增長率為11.3%;在25 ℃貯藏30 d后,漆籽油納米乳液的平均粒徑由162.3 nm增加到182.4 nm,增長率為12.4%;而在60 ℃時,乳液的平均粒徑增長較大,由162.3 nm增加到206.8 nm,增長率為27.4%。這是因為較高的環境溫度破壞了納米乳液內部結構,分子運動速率增加,粒子相互碰撞聚集,導致粒徑變大。然而漆籽油納米乳液在4、25和60 ℃條件下貯藏30 d,平均粒徑仍能保持在200 nm級的液滴范圍內且未出現破乳或相分離現象,同時漆籽油納米乳液的Zeta電位均處于-41~-39 mV,維持在乳液穩定的范圍內,表明漆籽油納米乳液在長期貯藏過程中具有良好的物理穩定性。
2.3 漆籽油納米乳液的抗氧化活性
漆籽油納米乳液對DPPH、ABTS及羥基自由基的清除能力如圖2所示,可以看出漆籽油納米乳液對3種自由基均具有很好的清除作用,清除率隨著質量濃度的增加而變高。有效中濃度(EC50)是指自由基被清除50%時所需要的抗氧化劑的質量濃度,常用來表征抗氧化能力的大小,EC50越小,抗氧化劑的抗氧化效果越強。漆籽油納米乳液對DPPH、ABTS及羥基自由基的EC50分別為24.26、23.77和21.10 mg/L,而漆籽油對DPPH、ABTS及羥基自由基的EC50分別為35.38、41.29和38.52 mg/L,說明漆籽油制備成納米乳液后可顯著增強抗氧化活性。同時本試驗也采用VC為陽性對照,VC對DPPH、ABTS及羥基自由基的EC50分別為38.48、43.25和40.56 mg/L。通過比較看出,漆籽油納米乳液對3種自由基的清除率明顯高于VC(P<0.05),表明漆籽油納米乳液具有比VC更好的抗氧化活性。
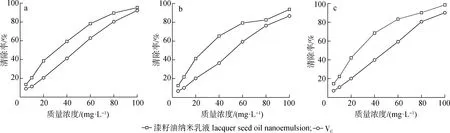
a.DPPH·;b.ABTS+;c.OH·圖2 不同質量濃度的漆籽油納米乳液和VC的抗氧化活性Fig.2 Antioxidant activity of lacquer seed oil nanoemulsion and VC at different concentrations
2.4 漆籽油納米乳液的抗紫外輻射活性
將NIH 3T3正常細胞對照組的相對細胞存活率設定為 100%,漆籽油納米乳液對NIH3T3細胞生長的作用見表2。由表2數據可知,與正常細胞對比,漆籽油納米乳液對 NIH 3T3細胞無明顯的細胞毒性,NIH 3T3細胞的存活率隨著漆籽油納米乳液濃度的增加而升高,表明漆籽油納米乳液對 NIH 3T3細胞有促增殖的作用。NIH 3T3細胞在接受不同時間 UVA 輻照后,細胞均受到不同程度的損傷,隨著輻照時間的延長,細胞損傷的程度越高。UVA 不同輻照時間對NIH 3T3細胞的損傷較大,在15、20、30、60和120 min的輻射時間下,細胞存活率分別為(92.6±1.5)%、(79.5±1.3)%、(58.2±1.2)%、(6.5±0.3%)和(0.0±0.0)%。由此可知,當UVA 輻照時間在30 min時,細胞死亡率處在半數死亡值左右,是建模的理想劑量,因此后續UVA損傷建模實驗選擇30 min的輻照時間。漆籽油納米乳液對UVA輻射損傷NIH 3T3的修復作用結果亦見表2,表中數據表明漆籽油納米乳液對UVA損傷的NIH 3T3細胞有顯著的修復作用,當漆籽油納米乳液質量濃度大于等于5 mg/L時對UVA損傷的NIH 3T3細胞修復作用更明顯,細胞的存活率可高于正常NIH 3T3細胞的存活率(P<0.05)。因此漆籽油納米乳液具有很好的抗紫外輻射活性。

表2 漆籽油納米乳液的抗紫外輻射活性Table 2 Anti-UV radiation activity of lacquer seed oil nanoemulsion
3 結 論
3.1以漆籽油為原料,酪蛋白酸鈉為乳化劑,以高壓均質法制備了漆籽油納米乳液,采用單因素試驗對制備條件進行了優化,得到較佳工藝條件為:乳化劑質量分數2.5%,漆籽油質量分數6%,均質壓力100 MPa,均質次數4次。優化條件下制備的漆籽油納米乳液平均粒徑為163.0 nm,Zeta電位為-41.01 mV,PDI為0.225;乳液的貯藏穩定性很好,在4、25和60 ℃條件下貯藏 30 d,平均粒徑保持在210 nm以內。
3.2漆籽油納米乳液對DPPH、ABTS及羥基自由基的EC50分別為24.26、23.77和21.10 mg/L,顯示出比陽性對照VC更好的抗氧化活性(EC50分別為38.48、43.25和40.56 mg/L)。
3.3漆籽油納米乳液對NIH 3T3細胞無明顯的細胞毒性,對正常NIH 3T3細胞有促增殖的作用。漆籽油納米乳液對UVA損傷的NIH 3T3細胞有顯著的修復作用,在質量濃度大于5 mg/L時,細胞的存活率可高于正常NIH 3T3細胞的存活率。因此漆籽油納米乳液具有很好的抗紫外輻射活性。

