扶正化瘀片聯合恩替卡韋治療慢性乙型肝炎肝纖維化的效果觀察
顧宏圖, 桂紅蓮, 徐列明, 郭 清, 謝 青, 趙長青
1 上海中醫藥大學附屬曙光醫院 肝硬化科, 上海 201203; 2 上海市中醫臨床重點實驗室, 上海 201203;
3 上海中醫藥大學肝腎疾病病證教育部重點實驗室, 上海 201203;
4 上海交通大學醫學院附屬瑞金醫院 感染科, 上海 200025
乙型肝炎是21世紀全世界共同面臨的難題,盡管通過應用乙型肝炎疫苗,我國HBV感染者已減少,但是數據[1]顯示,我國現存HBV感染者仍有約7000萬,其中2000萬~3000萬人處于慢性階段。肝纖維化是疾病從慢性肝炎進展為肝硬化的必經病理過程,因缺乏治療肝纖維化的化學、生物藥物和手段,目前慢性乙型肝炎(CHB)的西醫治療專注于抗病毒。針對病因治療的抗病毒藥物能減輕肝細胞的炎癥損傷,從而減少引起肝纖維化的刺激因素,進而一定程度上抑制肝纖維化的形成[2],但是CHB患者的病毒載量與肝纖維化程度不一致,單純抗肝炎病毒治療并不能有效抑制肝纖維化向肝硬化發展,部分患者病毒抑制后,肝纖維化仍會持續存在甚至進展[3],因此抗肝纖維化是慢性肝病治療中的一大難點。由于肝纖維化的形成機制較為復雜,故尚未研制出針對單一作用靶點的有效抗肝纖維化的化學或生物藥物。中藥雖成分復雜,但有多靶點作用的綜合治療優勢,經過幾十年來的基礎研究和臨床實踐,目前已有數個經國家食品藥品監督管理局批準的治療肝纖維化的中成藥在臨床中應用[4]。
中醫藥治療可以減輕CHB肝纖維化,已得到證實[5-6]。以西藥抗病毒,抑制肝臟炎癥、減少肝纖維化的刺激因素為基礎,輔以中藥抗肝纖維化,可阻止肝星狀細胞受炎癥刺激的活化和自我活化,減少纖維組織生成和促進纖維組織降解,改善肝臟的微循環,有助于提高抗病毒療效。兩種醫療技術聯合應用的優勢,有待更多的符合循證醫學的臨床試驗所證實。
1 資料與方法
1.1 研究對象 選取2011年4月—2013年1月在上海交通大學附屬瑞金醫院和上海中醫藥大學附屬曙光醫院2個中心的乙型肝炎肝纖維化患者。納入標準:(1)年齡18~65歲,性別不限。(2)CHB病史,HBsAg陽性≥6個月,ALT<5倍正常值上限。(3)肝活檢確認顯著肝纖維化,Ishak分期≥F3。(4)HBeAg陽性患者,HBV DNA>1.0×105拷貝/ml。HBeAg陰性患者,HBV DNA>1.0×104拷貝/ml。(5)半年內未曾接受抗病毒治療,或半年前曾服用拉米夫定/替比夫定經耐藥位點檢測證實無耐藥者。(6)觀察前1個月內未服用抗肝纖維化藥物。(7)有能力理解和簽署知情同意書。排除標準:(1)入選前3個月內曾有上消化道大出血者。(2)TBil>2倍正常值上限。(3)AFP>50 μg/L。(4)B超顯示肝內明顯占位性病變。(5)BMI>30 kg/m2。(6)診斷為CHB重型或有重型肝炎傾向者。(7)失代償期肝硬化及肝臟腫瘤患者。(8)酒精性、藥物性、遺傳性、免疫性、其他病毒性和非病毒性慢性肝炎患者。(9)合并心血管、肺、腎、內分泌、神經及血液系統嚴重疾病者以及精神病患者。(10)活動性消化性潰瘍。(11)妊娠及哺乳期婦女。
1.2 隨機方案 本研究采用中央隨機、雙盲、雙中心、安慰劑平行對照的研究設計。為保證隨機化和雙盲,運用中央隨機系統(DAS for IWRS),采用動態隨機的最小化,通過系統對不同影響因素(纖維化、炎癥程度和病毒水平)的不同水平實時計算,達到二組間1∶1均衡分配,自動分配隨機號。每個隨機號,配對一個相應的藥物號。
1.3 治療方法 研究期間,所有患者口服恩替卡韋(entecavir,ETV),1片/次,1次/d;聯合組口服扶正化瘀片(FZHY,國藥準字:Z20050546),4片/次,3次/d;對照組口服安慰劑片(內含1%扶正化瘀片全浸膏),4片/次,3次/d。治療48周。FZHY及相應的安慰劑片均0.4 g/片,由上海現代中醫藥股份有限公司黃海制藥有限責任公司生產。ETV(商品名潤眾)0.5 mg/片,由江蘇正大天晴藥業股份有限公司生產。
1.4 觀察指標、隨訪、有效性及安全性評估 入組前4周篩選期內行首次肝穿刺檢查,48周治療結束時,行第二次肝穿刺檢查。入組后每12周隨訪1次,分別進行肝功能、血常規、乙型肝炎五項、HBV DNA、AFP、腹部超聲等檢測。每24周進行FibroScan檢查,以及健康狀況調查簡表(SF-36)評估。研究期間血液生化及病理等檢查由各中心實驗室進行。所有病理片評分由2位病理專家分別獨立雙盲打分。
主要療效評估指標:肝纖維化Ishak分期治療后比治療前下降1級及以上的比例。次要療效評估指標:(1)治療后HBV DNA陰轉率(HBV DNA<50拷貝/ml)和下降幅度;(2)肝臟病理炎癥組織學活動指數(HAI)分級治療后下降1級或以上的比例。
1.5 倫理學審查 本研究方案經由上海交通大學附屬瑞金醫院和上海中醫藥大學附屬曙光醫院倫理委員會審批,批號:(2011)倫審第(20),所有患者入選前均簽署知情同意書。本臨床試驗注冊號為ChiCTR-TRC-11001377。
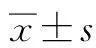
2 結果
2.1 一般資料 2個中心共52例患者納入本研究,隨機分入聯合組和對照組,每組各26例。有1例聯合組患者因AFP 228 μg/L,未進入FAS分析;2例聯合組患者因工作地點變動,退出研究;1例聯合組患者未完成第二次肝穿刺;2例對照組患者未完成第二次肝穿刺。最終,共有46例患者完成了兩次肝穿刺,進入PPS分析;所有52例受試者,均進入SS分析。其中聯合組入組26例,PPS 22例,FAS 25例,SS 26例;對照組入組26例,PPS 24例,FAS 26例,SS 26例。治療前兩組的年齡、性別、身高、體質量等一般資料比較,差異均無統計學意義(P值均>0.05)(表1)。兩組患者治療前乙型肝炎病程比較,差異有統計學意義(P<0.05);其他指標如疾病診斷、肝硬化病程、既往治療史、過敏史、患有其他疾病及用藥情況方面差異均無統計學意義(P值均>0.05)。治療前肝臟炎癥各單項評分(界面性炎癥,融合性壞死,灶性壞死、凋亡和灶性炎癥,匯管區炎癥)、肝臟炎癥HAI分級、纖維化Ishak分期、肝臟硬度測定(liver stiffness measurement,LSM)值、實驗室檢測指標等兩組比較,差異均無統計學意義(P值均>0.05)(表1)。兩組患者治療前SF-36評分表中除精神健康評分比較差異有統計學意義[(89.60±20.23)分 vs (75.54±19.31)分,t=2.540,P=0.014],其余各項SF-36評分(生理機能、生理職能、軀體疼痛、一般健康狀況、精力、社會功能、情感職能和健康變化)差異均無統計學意義(P值均>0.05)。兩組依從性均良好,研究期間在合并其他用藥方面差異無統計學意義(P值均>0.05)。

表1 兩組患者主要基線資料比較
2.2 藥物安全性 用藥后兩組受試者生命體征均平穩,尿常規、血常規、腎功能、心電圖等均未見異常,聯合組和對照組各有1例出現不良事件,不良事件發生率均為3.8%,聯合組發生1例嚴重不良事件(肝癌死亡)。兩組均無不良反應發生。兩組不良事件發生率、嚴重不良事件發生率、不良反應發生率、生命體征安全性分析、實驗室安全性指標等比較,差異均無統計學意義(P值均>0.05)。
2.3 療效 采用FAS進行生化、病毒學和血清學比較。兩組48周生化終點無明顯差異。聯合組和對照組48周時較0周ALT改變分別為-4.00(-23.00~2.63) U/L和-5.00(-14.83~8.00) U/L,AST改變分別為-1.00(-13.45~4.33) U/L和-2.83(-13.64~1.00) U/L,TBil改變分別為0.05(-3.75~3.30) μmol/L和0.70(-2.98~5.40) μmol/L,白蛋白改變分別為-1.00(-3.00~1.00) g/L和-1.37(-3.52~0) g/L,球蛋白改變分別為-1.40(-3.00~1.00) g/L和0(-3.00~2.00) g/L,PT改變分別為0.15(-0.70~1.10) s和-0.25(-0.85~0.70) s,各項指標兩組間均無統計學意義(P值均>0.05)。
在48周內,聯合組和對照組中分別有91%(21/23)、92%(23/25)的患者實現了完全病毒應答(HBV DNA<1×103拷貝/ml);聯合組有30.8%(4/13),對照組有35.7%(5/14)在48周時發生HBeAg血清陰轉;聯合組有7.7%(1/13),對照組有28.6%(4/14)發生HBeAg血清轉化成抗-HBe陽性,兩組間HBeAg血清轉化方面均無統計學意義(P值均>0.05)。兩組均無HBsAg血清轉換發生。
對SF-36評分表進行FAS歷時性分析,兩組治療前后在生理機能、生理職能、軀體疼痛、一般健康狀況、精力、社會功能、情感職能等方面均無明顯差異。在精神健康方面,聯合組評分較治療前改變幅度為-8.00(-16.00~4.00)分,對照組改變幅度為8.00(-12.00~16.00)分,兩組間差異有統計學意義(Z=2.043,P=0.047)。
對PPS進行Ishak分期治療前后比較,聯合組22例患者中,較治療前Ishak分期下降≥1期的有18例,對照組24例患者中僅有13例下降,兩組比較差異有統計學意義(P<0.05);對照組有4例發生Ishak分期較治療前升高,聯合組無Ishak分期加重情況發生(表2)。
對PPS進行HAI分級治療前后比較,聯合組22例患者中,有13例在48周內較基線改善了HAI分級,對照組24例患者中僅有6例下降,兩組在HAI分級改變上治療前后差異有統計學意義(P<0.05);對照組有3例發生HAI分級較治療前升高,聯合組無壞死性炎癥惡化情況發生(表2)。
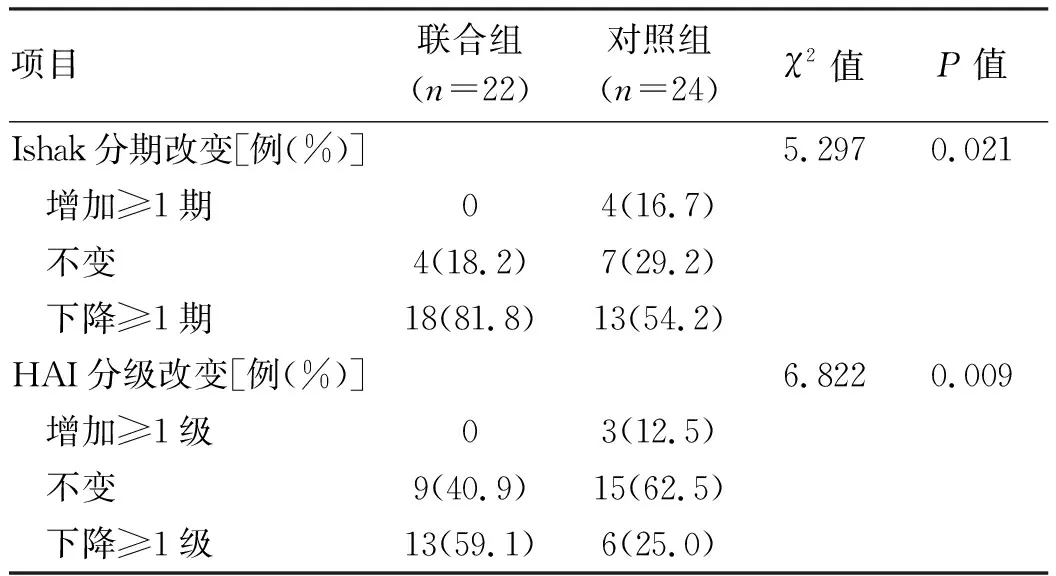
表2 治療前后肝纖維化Ishak分期和肝臟炎癥HAI分級改變情況
3 討論
抗病毒治療可以持續抑制HBV復制,降低肝細胞癌(HCC)的發病率,然而有研究[7]顯示,接受ETV等抗病毒藥物治療的CHB患者一旦已經發生肝硬化,仍有較高的HCC患病風險。雖然近半個世紀以來中醫藥專家總結前人經驗,通過探索,在抗肝纖維化治療方面取得了很多進展,但是中醫藥抗肝纖維化的療效,尚未被國際廣泛承認,有待依靠更多的大樣本隨機對照、以肝穿刺病理為診斷和評判療效“金標準”的臨床多中心研究來加以驗證和支持。
《肝纖維化中西醫結合診療指南(2019年版)》[4]的發布,提高了業界對中醫藥抗肝纖維化的認識。FZHY是一種抗肝纖維化的中成藥,由丹參、發酵蟲草菌粉、絞股藍、桃仁、松花粉、五味子(制)組成,以CHB肝纖維化為適應證,作用于肝纖維化病理過程的11個環節,達到消除或減輕肝臟炎癥,減輕或去除肝纖維化,防治肝硬化的目的。既往動物和臨床研究均未發現該藥物有明顯的毒副作用。經過多項基礎和臨床試驗也已證實其在抗肝纖維化方面有一定的療效[8]。國內Ⅱ期臨床研究[5]證明其肝纖維化組織學逆轉率達52%。一項回顧性研究[9]顯示,服用FZHY的肝硬化患者中位生存時間為351.6周,對照組(服用和絡舒肝膠囊)為112.1周,兩組5年生存率差異顯著(P<0.001)。然而,此前尚無通過治療前后肝組織活檢來評判比較聯合應用FZHY、核苷和核苷酸類藥物在減輕肝纖維化方面療效的隨機對照雙盲臨床試驗。
在CHB的治療中,組織病理學結果仍然是療效評估的一個重要方面,有助于確定療程。盡管存在肝穿刺樣本誤差和觀察者間的差異,但肝活檢仍是評估慢性肝炎分級和肝纖維化分期的最佳標準。本研究獲得肝纖維化改善的結果是建立在組織病理學客觀基礎之上,而不是單純依靠對肝纖維化的無創評估。本研究表明,與ETV單藥治療相比,FZHY和ETV 48周聯合治療在壞死性炎癥活動度和纖維化方面有明顯改善。治療后HAI分級降低的患者比例,聯合組(59.1%)是對照組(25.0%)的2.36倍(P<0.05),且對照組有12.5%的患者HAI分級較治療前升高,聯合組則為0;治療后Ishak分期下降的患者比例,聯合組為81.8%,對照組為54.2%,聯合用藥較單用ETV提高肝纖維化的逆轉率27.6%(P<0.05),且對照組亦有16.7%的患者Ishak分期較治療前升高,而聯合組為0。
最近有薈萃分析[10]顯示,相比傳統乙型肝炎肝硬化的療法,FZHY能更有效改善肝功能(ALT、AST、TBil等),在降低Child-Pugh評分、提高HBV DNA陰轉率等方面更有效,且無嚴重不良反應。本研究觀察到,在第24周和第48周,聯合組與對照組在生化、病毒學和血清學應答等方面的改善程度差異并無統計學意義。本研究與薈萃分析結果不同的原因可能有:一是本研究入組患者中,肝硬化只占半數左右;二是薈萃分析納入的研究中,FZHY的劑量每日0.6~4.5 g不等,療程6~12個月不等。不可否認的是,在生化、病毒學和血清學反應等方面獲得近期療效,抗病毒藥物可能發揮了主要作用[2,11-12]。
本研究以治療前后的肝穿刺病理評定結果作為臨床抗纖維化療效評價指標,相對以理化檢查等其他指標評價纖維化改變更為客觀,但本研究最大的缺陷在于樣本量相對較小。為獲得更詳實可靠的臨床研究結果,上海中醫藥大學肝病研究所后續將開展列為國家科技部“十二·五”重點項目的一項多中心隨機雙盲對照大樣本臨床試驗(NCT02241590),預期此研究結果能為中醫藥抗肝纖維化療效提供強有力的循證醫學依據。本研究為上述大樣本臨床試驗提供了可靠的預初試驗結果,并提供了計算樣本量的統計依據。
綜上所述,本研究表明,與ETV單藥治療相比,FZHY聯合ETV治療方案對于有明顯纖維化/肝硬化的CHB患者是一種較好的治療方案。入組的大多數CHB患者在48周的治療中獲得持續的生化應答、病毒學抑制和肝臟組織學改善等方面的療效。為推廣應用抗病毒和抗肝纖維化的“雙抗療法”提供了可靠證據。
利益沖突聲明:本研究不存在研究者、倫理委員會成員、受試者監護人以及與公開研究成果有關的利益沖突,特此聲明。
作者貢獻聲明:顧宏圖、桂紅蓮、郭清參與收集數據;徐列明、謝青負責課題設計,擬定寫作思路,指導撰寫文章;趙長青負責資料分析,撰寫論文并最后定稿。

