活性血炭的制備及其吸附性能測定
張興萍,李海朝
(青海民族大學 青藏高原資源化學與生態環境保護國家民委重點實驗室,青海 西寧 810007)
近年來,水體污染嚴重,吸附法作為一種低能耗、易操作、易再生的固體萃取技術,在水處理方面有著不可比擬的優勢。活性炭是最常見的吸附劑[1],是由含碳原料經熱解、活化而成,是特異性吸附能力較強的炭材料的統稱[2],具有比表面積大、孔隙結構發達、吸附效率高、化學穩定性好等優點[3],能夠吸附水中的有機物,且無二次污染,是廢水回用處理的理想材料。制備活性炭的原料來源廣泛,所有含碳材料包括石油、煤、果殼、活性污泥等都可以用來制備活性炭。
畜禽血液是肉類生產的副產物,一般在屠宰時收集。畜禽血液含量因畜禽種類而異,屠宰后所能收集到的血液約占血液總量的80%[4]。若將收集到的血液制成血粉,再通過化學方法制成活性血炭,不僅可有效利用畜禽血液資源,還可減少環境污染。目前,禽血粉、豬血粉年產量分別約40萬t、95萬t,制備的活性血炭具有廣闊的發展前景[5]。為此,作者利用豬血粉為原料,分別以磷酸、氯化鋅和氯化鎂為活化劑,采用化學活化法制備活性血炭,通過BET、SEM對3種活性血炭進行表征,通過亞甲基藍吸附實驗、碘吸附實驗和酸性品紅吸附實驗評價3種活性血炭的吸附性能。
1 實驗
1.1 材料、試劑與儀器
豬血粉,購于廣西南寧西鄉屠宰廠。將豬血粉置于95 ℃干燥箱中干燥8 h,冷卻至室溫,備用。
磷酸、氯化鎂、普通顆粒活性炭,分析純,天津大茂化學試劑廠;氯化鋅,分析純,天津永大化學試劑廠;生物染色劑亞甲基藍、酸性品紅,北京化工廠;碘,分析純,上海廣諾化學科技有限公司;實驗用水為去離子水。
SX型箱式電阻爐,沈陽節能電爐廠;PL203型電子天平,梅特勒-托利多儀器(上海)有限公司;Autosor iQ Station 2型全自動比表面積及孔徑分布測定儀,美國Quantachrome公司;JSM-5610LV型掃描電子顯微鏡,日本電子株式會社。
1.2 活性血炭的制備
采用化學活化法制備活性血炭,工藝流程如圖1所示。

圖1 活性血炭的制備工藝流程
稱取50 g豬血粉于500 mL坩堝中,按浸漬比2∶1加入100 g活化劑,混合均勻,放置24 h;然后放入馬弗爐中煅燒,在N2氣氛下以6 ℃·min-1的升溫速率從室溫升至550 ℃左右(依據活化劑調節活化溫度),煅燒停止后恒溫1 h,再關閉馬弗爐電源;待坩鍋冷卻至室溫后用去離子水清洗以去除活化過程中殘留的活化劑和其它無機物;待清洗至中性后,用布氏漏斗過濾,置于105 ℃真空干燥箱中干燥24 h,研磨,即得活性血炭。
活化溫度按活化劑的不同有所差異,以磷酸、氯化鋅、氯化鎂為活化劑時,活化溫度分別為500 ℃、550 ℃、600 ℃,制備的磷酸活性血炭(H-AC)、氯化鋅活性血炭(Zn-AC)和氯化鎂活性血炭(Mg-AC)的得率分別為27.52%、34.66%、40.32%。
1.2 活性血炭的表征和吸附性能評價
通過BET、SEM對3種活性血炭進行表征。
亞甲基藍吸附實驗:參照GB/T 12496.10-1999《木質活性炭試驗方法 亞甲基藍吸附值的測定》測定活性血炭的亞甲基藍吸附值。稱取1.500 0 g亞甲基藍,加入500 mL去離子水中,攪拌使之充分溶解,用去離子水定容至1 000 mL,配制成亞甲基藍溶液;稱取 0.100 0 g 活性血炭置于100 mL磨口錐形瓶中,用標簽標記后每2 min加入適量的亞甲基藍溶液,測定活性血炭的亞甲基藍吸附值,同時觀察溶液顏色變化。每組實驗平行3次,繪制活性血炭的亞甲基藍吸附值與吸附時間的關系曲線。
碘吸附實驗:參照GB/T 12496.8-2015《木質活性炭試驗方法 碘吸附值的測定》測定活性血炭的碘吸附值。稱取活性血炭0.500 0 g置于250 mL磨口錐形瓶中,加入50 mL碘標準溶液,振蕩均勻,靜置;用干濾紙過濾;取50.00 mL濾液,用硫代硫酸鈉標準溶液進行滴定,每2 min取一定的標定液測定活性血炭的碘吸附值,繪制活性血炭的碘吸附值與吸附時間的關系曲線。
酸性品紅吸附實驗:稱取酸性品紅0.200 0 g置于500 mL容量瓶中,加入2 mL稀硫酸,用去離子水稀釋至刻度,配制成酸性品紅溶液;稱取0.506 3 g活性血炭置于100 mL錐形瓶中,標記后每2 min加入適量酸性品紅溶液,測定活性血炭的酸性品紅吸附值,同時觀察溶液顏色變化,繪制活性血炭的酸性品紅吸附值與吸附時間的關系曲線。
2 結果與討論
2.1 活性血炭的比表面積及孔徑分布
采用BET法測定活性血炭的比表面積、總孔容及平均孔徑,結果見表1。
由表1可知,3種活性血炭均具有較大的比表面積和發達的微孔結構,為吸附提供了通道。
用Origin 2018軟件對3種活性血炭的N2吸附-脫附數據進行分析,繪制N2吸附-脫附曲線,結果如圖2所示。
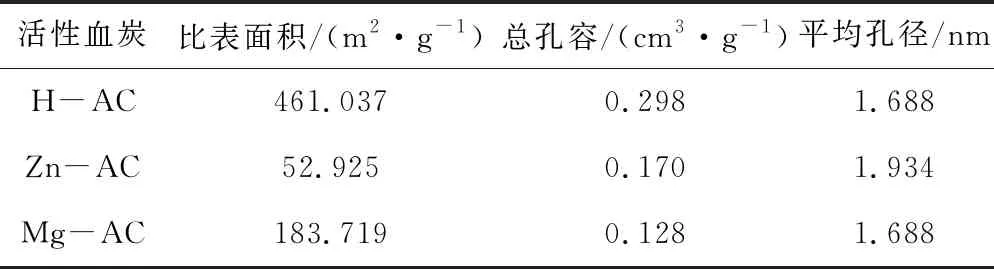
表1 活性血炭的比表面積、總孔容及平均孔徑
由圖2可以看出,3種活性血炭的N2吸附-脫附等溫線均屬于Ⅳ型。其中,H-AC的等溫線在相對壓力為0~0.4區域較平緩表明吸附行為屬單分子層吸附,在相對壓力大于0.4后的小坡度表明有多層彌散的形成;Zn-AC、Mg-AC的等溫線在相對壓力為0.2~0.8區域呈現明顯的上升趨勢,吸附量增加很快,這是因為Zn-AC、Mg-AC具有較高的介孔率和較多的微孔結構;活性血炭在相對壓力較低時表現為單分子層吸附,在相對壓力較高時出現明顯滯后現象,是因為毛細管凝聚所致。
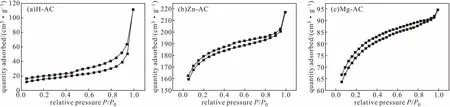
圖2 3種活性血炭的N2吸附-脫附曲線
2.2 活性血炭的外觀形貌
3種活性血炭的SEM照片如圖3所示。
由圖3a可以看出,H-AC的表面凹凸不平,顆粒較小且分布不均,有少量的團聚現象,表面結構疏松呈絮狀,微孔結構發達。這是因為,磷酸與碳反應,損失碳原子產生大量的微孔,導致H-AC表面含有許多大小不一、形狀各異的孔隙。由圖3b可以看出,Zn-AC的表面凹凸不平,顆粒較大且分布均勻,孔道豐富。由圖3c可以看出,Mg-AC的顆粒較小且形狀不規整,表面結構疏松,小顆粒較多,有少量的團聚現象。這和N2吸附-脫附曲線結果一致。
2.3 活性血炭的吸附性能
2.3.1 對亞甲基藍的吸附能力
3種活性血炭的亞甲基藍吸附值與吸附時間的關系如圖4所示。
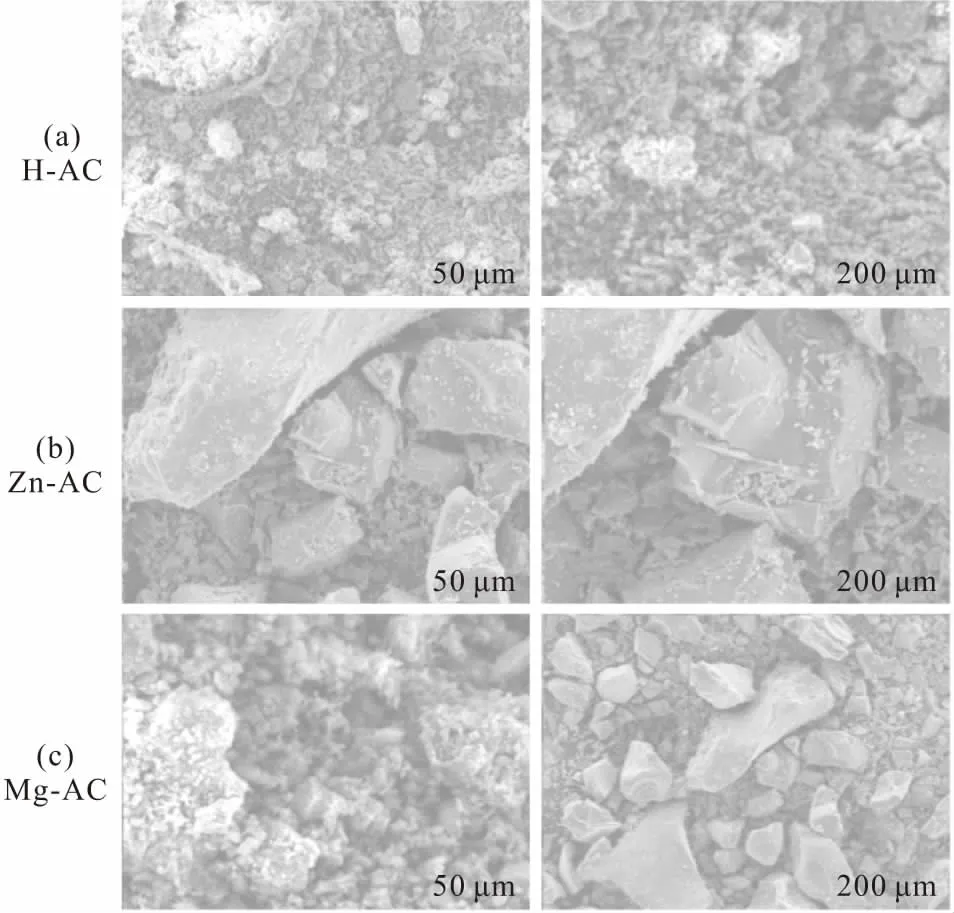
圖3 3種活性血炭的SEM照片
由圖4可以看出,3種活性血炭在吸附初始對亞甲基藍的吸附速度較快,隨著吸附時間的延長,亞甲基藍吸附值不斷升高;在16~22 min時吸附達到平衡,吸附值基本不變,H-AC、Zn-AC、Mg-AC的亞甲基藍吸附值分別為1 900.00 mg·g-1、400.00 mg·g-1、600.00 mg·g-1。表明,H-AC對亞甲基藍的吸附能力較好,Mg-AC對亞甲基藍的吸附能力一般,Zn-AC對亞甲基藍的吸附能力較差。
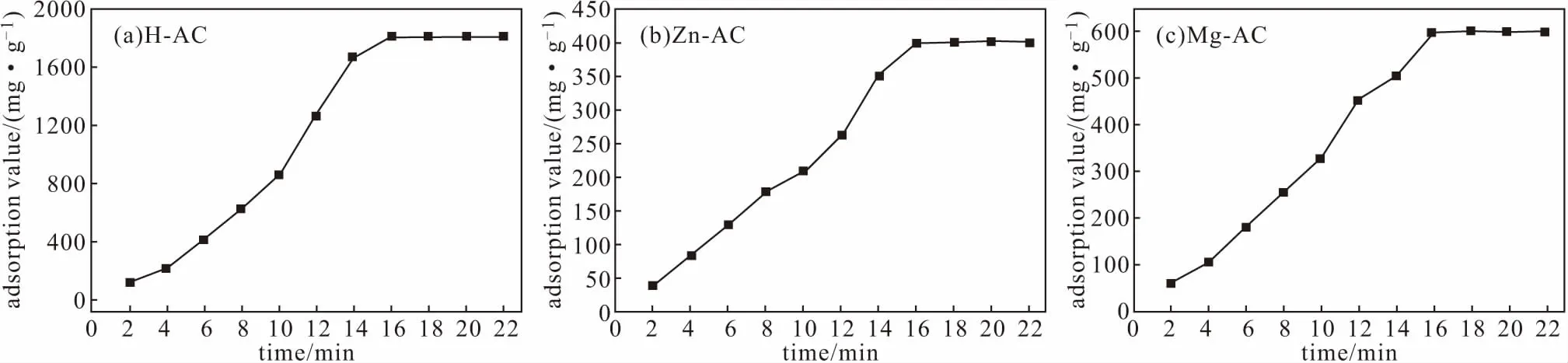
圖4 3種活性血炭的亞甲基藍吸附值與吸附時間的關系
2.3.2 對碘的吸附能力
3種活性血炭的碘吸附值與吸附時間的關系如圖5所示。
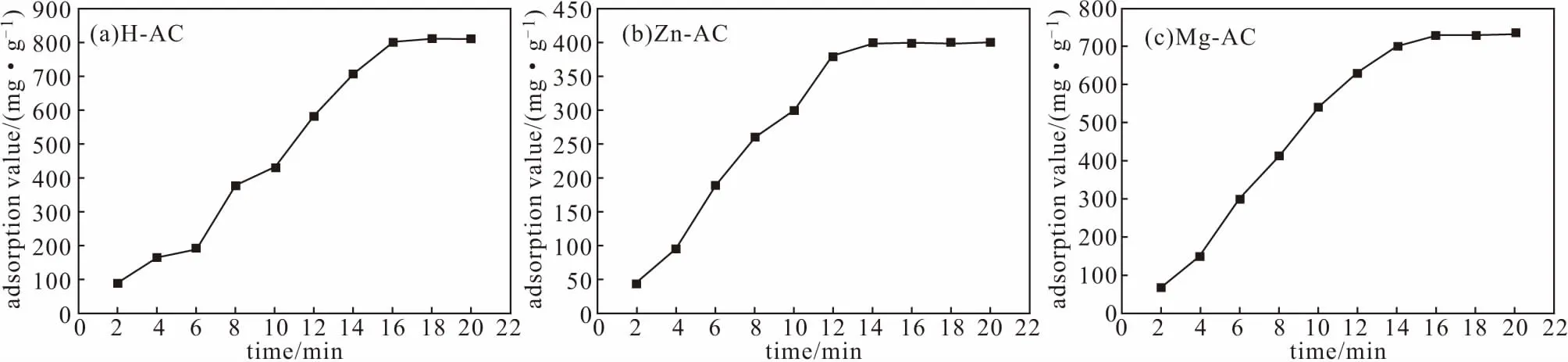
圖5 3種活性血炭的碘吸附值與吸附時間的關系
由圖5可以看出,3種活性血炭在吸附初始對碘的吸附速度較快,隨著吸附時間的延長,碘吸附值不斷升高;在14~20 min時吸附達到平衡,吸附值基本不變,H-AC、Zn-AC、Mg-AC的碘吸附值分別為810.00 mg·g-1、400.94 mg·g-1、734.95 mg·g-1。表明,H-AC對碘的吸附能力較好,Mg-AC對碘的吸附能力一般,Zn-AC對碘的吸附能力較差。
2.3.3 對酸性品紅的吸附能力
3種活性血炭的酸性品紅吸附值與吸附時間的關系如圖6所示。
由圖6可以看出,3種活性血炭在吸附初始對酸性品紅的吸附速度較快,隨著吸附時間的延長,酸性品紅吸附值不斷升高;在16~22 min時吸附達到平衡,吸附值基本不變,H-AC、Zn-AC、Mg-AC的酸性品紅吸附值分別為2 200.00 mg·g-1、1 700.00 mg·g-1、1 300.00 mg·g-1。表明,H-AC對酸性品紅的吸附能力較好,Zn-AC對酸性品紅的吸附能力一般,Mg-AC對酸性品紅的吸附能力較差。同時可以看出,3種活性血炭的酸性品紅吸附值明顯高于亞甲基藍吸附值和碘吸附值,可能是因為酸性品紅溶液呈酸性,活性血炭更易吸附。
2.4 討論
3種活性血炭與普通活性炭的亞甲基藍吸附值、碘吸附值和酸性品紅吸附值比較見表2。
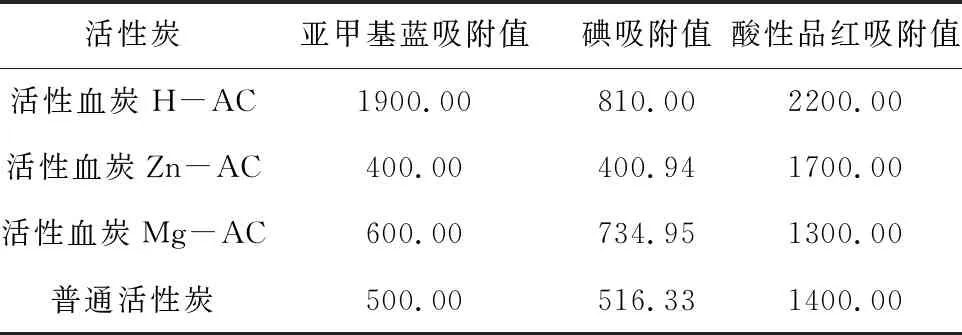
表2 吸附值比較/(mg·g-1)
由表2可知,活性血炭H-AC的亞甲基藍吸附值、碘吸附值和酸性品紅吸附值最高;除活性血炭Mg-AC對酸性品紅的吸附值較低外,與普通活性炭相比,3種活性血炭的吸附值相對較高。表明3種活性血炭具有發達的微孔結構,且孔容較大,吸附性能相對穩定。
3 結論
以豬血粉為原料,以磷酸、氯化鋅和氯化鎂為活化劑制備的3種活性血炭均具有較好的吸附性能,其中以磷酸為活化劑制備的活性血炭H-AC的吸附性能最好,其亞甲基藍吸附值為1 900.00 mg·g-1、碘吸附值為810.00 mg·g-1、酸性品紅吸附值為2 200.00 mg·g-1,可開發應用于食品、建筑、環保等行業。活性血炭的研究為充分利用畜禽血液資源提供了有效途經。

