骨密度和骨代謝指標在強直性脊柱炎合并骨質疏松患者中的水平變化*
李玉琳,趙 虬
(天津醫科大學總醫院骨科 300052)
強直性脊柱炎(ankylosing spondylitis,AS)是風濕免疫科常見的以新骨形成為特征,主要累及中軸關節的風濕性疾病,可通過侵蝕、破壞關節導致患者勞動能力和自主生活能力的喪失[1]。骨質疏松(osteoporosis,OP)是臨床常見的以骨組織微結構退化、骨量減少為特征的系統性骨病,可使骨脆性及骨折風險增加[2]。AS患者多伴有不同程度的骨量減少甚至OP。報道顯示,AS合并OP的發生率高達50%~92%[3]。AS合并OP患者常出現駝背畸形或者脊柱僵硬,甚至可能發生脊柱骨折,嚴重影響患者的健康和生命質量[4]。早期診斷并及時治療對提高患者生命質量與改善預后有重要意義。本研究通過測定AS合并OP患者的骨密度及骨代謝指標水平變化情況,評估患者的病情活動度及脊柱功能,旨在為臨床早期診治、評估患者病情提供指導,現報道如下。
1 資料與方法
1.1 一般資料
選取2017年1月至2018年12月本院收治的65例AS合并OP患者為AS+OP組,納入標準:(1)符合1984年美國風濕病學會修訂的關于AS的診斷標準[5];(2)符合OP診斷標準[6]。排除標準:(1)妊娠期及哺乳期的婦女;(2)心臟功能不全者;(3)肝、腎功能障礙者;(4)近期接受過糖皮質激素或其他可能影響骨代謝的藥物治療者;(5)重度營養不良者;(6)合并內分泌疾病者;(7)合并其他可能影響本研究結果的疾病者。AS+OP組中男45例,女20例;年齡26~55歲,平均(26.3±5.6)歲;病程3個月至8年,平均(2.6±0.4)年。于同期選取70例單純AS患者為AS組,同樣符合1984年美國風濕病學會修訂的關于AS的診斷標準[5],排除標準同AS+OP組,其中男46例,女24例;年齡23~57歲,平均(26.1±6.2)歲;病程8個月至12年,平均(1.9±0.6)年。另選取40例健康志愿者為對照組,其中男26例,女14例;年齡23~46歲,平均(24.5±6.1)歲。本研究獲得本院倫理委員會的批準,所有研究對象均簽署知情同意書。
1.2 方法
1.2.1骨密度測定
采用雙能X線吸收法對3組研究對象的腰椎、股骨頸、股骨粗隆、Ward′s三角區的骨密度進行檢測,DPX-L型骨密度儀由美國GE公司提供。
1.2.2骨代謝指標測定
分別于清晨空腹收集3組受試者肘靜脈血5 mL,2 000 r/min離心10 min,收集上清液用于測定骨代謝指標,包括Ⅰ型膠原羧基端前肽(CICP)、Ⅰ型膠原羧基端交聯肽(CTX-Ⅰ)、骨堿性磷酸酶(BALP)、甲狀旁腺激素(PTH)、骨鈣素(BGP)、尿脫氧膠原吡啶交聯(D-Pyr)。其中CICP、CTX-Ⅰ、BALP水平采用酶聯免疫法進行測定,PTH、BGP水平采用放射免疫法進行測定,D-Pyr水平采用ELISA進行測定。
1.3 統計學處理
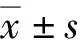
2 結 果
2.1 3組臨床資料特征比較
3組性別構成比、年齡比較,差異無統計學意義(P>0.05);AS+OP組AS病程比AS組長,累及外周關節數、骶髂關節CT分級高于AS組,差異均有統計學意義(P<0.05),見表1。

表1 3組臨床資料特征比較
2.2 3組骨密度比較
3組腰椎、股骨頸、股骨粗隆、Ward′s三角區骨密度經方差分析,差異均有統計學意義(P<0.05);組間兩兩比較,AS+OP組、AS組腰椎、股骨頸、股骨粗隆、Ward′s三角區骨密度均低于對照組,且AS+OP組各部位骨密度均低于AS組,差異有統計學意義(P<0.05),見表2。

表2 3組骨密度比較
2.3 3組骨代謝指標水平比較
3組骨代謝指標水平經方差分析,差異均有統計學意義(P<0.05);組間兩兩比較,AS+OP組、AS組CICP、CTX-Ⅰ、D-Pyr水平高于對照組,PTH、BGP水平低于對照組,且AS+OP組CICP、CTX-Ⅰ、D-Pyr水平高于AS組,PTH、BGP水平低于AS組,差異均有統計學意義(P<0.05);3組BALP水平比較,差異無統計學意義(P>0.05),見表3。
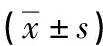
表3 3組骨代謝指標水平比較
2.4 AS+OP患者骨密度與骨代謝指標的相關性分析
Pearson相關分析顯示,腰椎、股骨頸、股骨粗隆、Ward′s三角區骨密度與CICP、CTX-Ⅰ、D-Pyr水平呈負相關(P<0.05),與PTH、BGP水平呈正相關(P<0.05),與BALP水平無明顯相關性(P>0.05),見表4。

表4 AS+OP患者骨密度與骨代謝指標的相關性分析(r)
3 討 論
AS是臨床常見的,以外周關節、骶髂關節的慢性炎癥為主要表現的疾病,好發于青壯年人群,尤其多見于男性。研究顯示,AS患者普遍存在骨量減少甚至OP癥狀[7]。AS合并OP極易造成骨折,嚴重威脅患者的健康和生命質量,早期診治并及時干預對改善患者預后有重要價值。關于AS合并OP的發病機制,目前尚無統一定論。研究表明,骨代謝失衡、機械因素、炎性反應及藥物不良反應等與其發生密切相關[8-9]。
本研究通過檢測骨密度和骨代謝指標,探討其在AS患者中的表達水平及臨床意義。結果顯示,AS合并OP患者累及外周關節的數量、骶髂關節CT分級高于AS患者。AS是以骶髂關節和中軸關節無菌性炎性反應為特征的進展性免疫介導炎性疾病,炎性反應貫穿AS發病的整個過程。而AS合并OP患者炎性反應加劇,因此累及的外周關節數量更多,影像學分級更高,推測可能是由于炎性反應加快骨吸收速度,導致骨量減少,最終誘發OP,與相關研究結果相似[10-11]。因此,臨床應高度重視AS患者的炎性反應,采取有效的干預措施盡早控制炎癥,從而阻斷或延緩骨量下降,減少OP發生風險。此外,本研究結果顯示,AS患者腰椎、股骨頸、股骨粗隆、Ward′s三角區骨密度均低于對照組,并且AS+OP患者各部位骨密度均低于AS組患者,與相關研究結果一致[4],即AS患者存在不同程度骨量丟失,尤其是AS合并OP患者骨密度下降尤為明顯。
骨代謝過程是指成骨細胞新骨的形成及破骨細胞舊骨的吸收,其中,新骨形成和舊骨吸收的平衡性是同一骨骨量的決定性因素,新骨形成速度大于舊骨吸收速度則骨量增加,反之則骨量減少[12-13]。研究骨代謝指標水平變化,可以了解機體骨量,其中骨Ⅰ型膠原形成的降解產物(CICP、CTX-Ⅰ)作為特異性指標能有效反映骨的吸收過程;BALP是成骨細胞中直接反映成骨細胞活性及功能的表型標志物;PTH是參與人體許多重要生理過程的激素,可促進骨的形成;BGP由成骨細胞合成和分泌,血清BGP水平可反映成骨細胞的活動狀態,尤其是新形成的成骨細胞的活動狀態;D-Pyr也是反映骨吸收的重要指標[14-17]。本研究結果發現,與健康志愿者比較,AS組患者CICP、CTX-Ⅰ、D-Pyr水平明顯升高,PTH、BGP水平明顯降低,并且AS合并OP患者上述指標異常改變較單純AS患者更為明顯,提示AS患者成骨細胞活性相對較差,患者舊骨吸收速度大于新骨形成速度,骨量減少,而這種現象尤其多見于AS合并OP患者。因此,早期檢測骨代謝指標有助于臨床評估AS患者骨代謝能力,從而判斷病情嚴重程度,以指導臨床制訂針對性的治療方案。Pearson相關分析表明,腰椎、股骨頸、股骨粗隆、Ward′s三角區骨密度與CICP、CTX-Ⅰ、D-Pyr水平呈負相關,與PTH、BGP水平呈正相關,提示早期檢測不同部位骨密度與骨代謝指標,有助于臨床及時有效地評估患者病情。
綜上所述,AS合并OP患者存在明顯的骨密度下降和不同程度的骨代謝異常,早期聯合檢測骨密度及骨代謝指標對輔助臨床評估患者病情,以及采取針對性的治療措施具有重要的指導意義。

