多靶標(biāo)受體酪氨酸激酶抑制劑的合成與初步活性篩選
單媛媛,劉婷婷,馬瑛,王茂義
(西安交通大學(xué)第一附屬醫(yī)院藥學(xué)部,陜西 西安 710061)
查爾酮是一種重要的活性天然產(chǎn)物,其結(jié)構(gòu)為1,3-二苯基-2-丙烯基-1-酮,廣泛存在于甘草、紅花等藥用植物[1],具有抗真菌、抗炎、抗腫瘤等生物活性[2],其抗腫瘤活性主要是對(duì)受體酪氨酸激酶(receptor tyrosine kinases,RTKs)的抑制[3]。RTK在腫瘤發(fā)生、發(fā)展中發(fā)揮關(guān)鍵的作用,其中,表皮生長(zhǎng)因子受體(EGFR)、血管內(nèi)皮細(xì)胞生長(zhǎng)因子受體2(VEGFR-2)、成纖維細(xì)胞生長(zhǎng)因子受體-1(FGFR1)3種RTKs的表達(dá)異常與多種腫瘤密切相關(guān),已成為抗腫瘤藥物研究的有效靶標(biāo)[4]。尤為重要的是,這3種RTKs具有高度保守的一級(jí)序列和三維結(jié)構(gòu),其配體結(jié)合位點(diǎn)和酪氨酸激酶催化區(qū)域高度相似,使得設(shè)計(jì)同時(shí)針對(duì)這3種RTKs的多靶標(biāo)抑制劑成為可能,也有利于解決單靶標(biāo)抑制劑的耐藥性的缺陷[5]。
基于查爾酮為先導(dǎo)化合物,設(shè)計(jì)并合成新型查爾酮衍生物類多靶標(biāo)RTKs抑制劑,通過(guò)體外活性篩選有望發(fā)現(xiàn)具有抗腫瘤活性的新型查爾酮衍生物[6]。基于已報(bào)道對(duì)RTKs有抑制活性且結(jié)構(gòu)對(duì)稱的聯(lián)苯化合物為先導(dǎo)物,首先采用分子剖裂原理將對(duì)稱的聯(lián)苯化合物破裂為兩分子苯氧基乙酰苯胺結(jié)構(gòu)[7],分析其結(jié)構(gòu)發(fā)現(xiàn):苯氧基乙酰苯胺結(jié)構(gòu)與查爾酮的結(jié)構(gòu)母核類似,而且其結(jié)構(gòu)中不存在α,β-不飽和羰基共軛結(jié)構(gòu)片段,因此不會(huì)與體內(nèi)谷胱甘肽的硫醇發(fā)生親電反應(yīng)[8],被谷胱甘肽還原,所以保留了查爾酮本身的藥效結(jié)構(gòu)特征與生物活性[9]。在此基礎(chǔ)上,引入含有氫鍵供受體網(wǎng)絡(luò)的苯甲酰胺、溴代苯甲酰胺結(jié)構(gòu)作為RTKs抑制劑的鉸鏈區(qū)結(jié)合基團(tuán)[10],并重點(diǎn)考察末端苯胺上不同取代基對(duì)活性的影響[11],設(shè)計(jì)了查爾酮苯甲酰胺系列衍生物(查爾酮-BAA)(見圖1)。
1 實(shí)驗(yàn)部分
1.1 儀器與試劑 化合物合成所需的試劑按照標(biāo)準(zhǔn)操作流程處理,常用有機(jī)溶劑主要購(gòu)自天津科密歐試劑公司、青島海洋化工有限公司、國(guó)藥集團(tuán)試劑公司等。所用試劑除了有特殊說(shuō)明之外均為分析純,合成操作中除水相反應(yīng)外,其他實(shí)驗(yàn)操作按照標(biāo)準(zhǔn)操作程序除水,無(wú)氧反應(yīng)操作均在氮?dú)獾榷栊詺怏w保護(hù)下進(jìn)行。化合物合成中所有反應(yīng)通過(guò)薄層色譜(TLC)監(jiān)測(cè)反應(yīng)進(jìn)程。目標(biāo)化合物及關(guān)鍵中間體的熔點(diǎn)采用予華儀器有限責(zé)任公司的X-4型數(shù)顯熔點(diǎn)測(cè)定儀測(cè)定(溫度未經(jīng)校正)。目標(biāo)化合物的1H-NMR(400 MHz)由西安交通大學(xué)理學(xué)院核磁共振儀(Bruker Advance AC 400)測(cè)定,測(cè)試所用氘代溶劑為DMSO-d6和CDCl3,采用四甲基硅烷(TMS)為內(nèi)標(biāo),化學(xué)位移值δ單位為ppm。目標(biāo)化合物的EI-MS由西安交通大學(xué)藥學(xué)院HPLC-MS-QP2010測(cè)定。
1.2 方法與結(jié)果
1.2.1 化合物的制備[12]基于以上結(jié)構(gòu)優(yōu)化策略,完成了共35個(gè)查爾酮衍生物(查爾酮BAA1~35)的合成(合成路線1與合成路線2)。該系列化合物以異香草醛(1)為起始原料,首先以NaOH/KOH為氧化劑將異香草醛氧化為異香草酸(2),然后將其羥基以芐基保護(hù)得到中間體(3),再與氯化亞砜反應(yīng)生成酰氯,將得到的酰氯分別與甲胺、異丙胺、二乙胺反應(yīng)得到相應(yīng)的苯甲酰胺關(guān)鍵中間體(4)。此外,將各種取代苯胺與氯乙酰氯反應(yīng)得到相應(yīng)的氯乙酰苯胺(6)。最后將前面制備的苯甲酰胺關(guān)鍵中間體(5)與取代氯乙酰苯胺(6)反應(yīng)制得相應(yīng)的查爾酮苯甲酰胺系列衍生物(查爾酮BAA1~21),見圖2。
化合物2的合成:稱取1.0 g氫氧化鈉,1.5 g氫氧化鉀加入三頸瓶中,加入0.3 mL蒸餾水,混合物加熱至160 ℃使其熔融。分5批緩慢加入3.0 g異香草醛,熔融狀態(tài)下繼續(xù)反應(yīng)10 min,停止加熱待反應(yīng)混合物溫度降至室溫后,加水100 mL使混合物全部溶解,冰浴條件下用2 mol·L-1鹽酸將混合物調(diào)pH至1~2。混合物溶液直接抽濾,用水洗滌濾餅2~3次既得產(chǎn)物,將產(chǎn)物放入真空干燥箱干燥。
化合物3的合成:化合物2(3.47 g,15 mmol)溶于70 mL無(wú)水乙醇中,加入無(wú)水碳酸鉀(6.22 g,45 mmol)和氯化芐(2.30 mL,20 mmol),回流反應(yīng)6 h,除去碳酸鉀,減壓蒸除乙醇,乙酸乙酯(30 mL×3)提取,分別用H2O (3×30 mL),2 mol·L-1NaOH 水溶液(3×30 mL),2 mol·L-1HCl 水溶液(3×30 mL),飽和氯化鈉水溶液 (2×30 mL)洗滌,無(wú)水硫酸鈉干燥,柱層析分離得到產(chǎn)物(4.56 g,95%) 。
化合物4的合成:將化合物3(6.72 g,26 mmol)溶于10 mL無(wú)水二氯甲烷中,冰浴條件下緩慢滴加5.82 mL氯化亞砜的二氯甲烷溶液和5滴催化量的二甲基甲酰胺(DMF),室溫條件下3 h。待反應(yīng)完全后減壓蒸除溶劑,將產(chǎn)物溶于無(wú)水二氯甲烷中備用。冰浴條件下,將上述酰氯的無(wú)水二氯甲烷溶液(25 mL)緩慢逐滴加入22.91 mL 30%的甲胺水溶液中,冰浴反應(yīng)2 h后升溫至室溫反應(yīng)。反應(yīng)完全后,加入10 mL水,分液,水相用二氯甲烷(3×30 mL)提取,合并有機(jī)相,有機(jī)相分別用2 mol·L-1的鹽酸(3×25 mL),水(2×25 mL),飽和碳酸氫鈉(2×25 mL),飽和氯化鈉(2×20 mL)洗滌,無(wú)水硫酸鈉干燥,柱層析分析得到產(chǎn)物(3.16 g,84%)。
化合物5的合成:化合物4(3.49 g,10 mmol)溶于100 mL無(wú)水甲醇中,加入10%的Pd/C(0.10 g)。通入氫氣還原反應(yīng),室溫條件下攪拌反應(yīng)。反應(yīng)完全后,過(guò)濾,回收Pd/C,減壓蒸除甲醇,得到產(chǎn)物(2.58 g,97%)。
目標(biāo)化合物(BAA1)的合成:將化合物5(1.58 g,5.90 mmol)溶于70 mL無(wú)水乙醇中,加入無(wú)水碳酸鉀(2.45 g,17.70 mmol)。反應(yīng)混合物室溫條件下攪拌反應(yīng)30 min,加入化合物6 (1.54 g,6.49 mmol)。混合物回流反應(yīng)10 h,TLC監(jiān)測(cè)反應(yīng)進(jìn)程,待反應(yīng)完全后,過(guò)濾除去碳酸鉀,減壓蒸除乙醇,乙酸乙酯(3×20 mL)提取,有機(jī)相依次用H2O (3×10 mL)、2 mol·L-1NaOH(3×10 mL)、2 mol·L-1HCl (3 ×10 mL) 和飽和氯化鈉水溶液 (2×10 mL)洗滌,無(wú)水硫酸鈉干燥。柱層析分離得到目標(biāo)化合物BAA1(2.13 g,78%)。mp:197~198 ℃。EI-MS(m/z):366.1 (M+)。1H-NMR (400 MHz,CDCl3) δ 8.88 (s,1H),7.80 (d,J=4.7 Hz,1H),7.51(s,1H),7.46(d,J=8.4 Hz,2H),7.17-7.12 (m,1H),6.97 (d,J=8.4 Hz,1H),6.27 (s,1H),4.69 (s,2H),4.00(s,3H)。3.03 (s,3H)。化合物BAA2~21的制備方法與BAA1相同。
查爾酮衍生物(查爾酮BAA22~35)的合成見合成路線2,該系列化合物同樣以異香草醛為起始原料,首先以液溴為溴化試劑制備溴代異香草醛,將其羥基以芐基保護(hù),然后以次氯酸鈉為氧化劑將醛基氧化為羧基制備溴代異香草酸。再與氯化亞砜反應(yīng)生成酰氯,將得到的酰氯分別與甲胺、異丙胺、二乙胺反應(yīng)得到相應(yīng)的苯甲酰胺關(guān)鍵中間體。此外,將各種取代苯胺與氯乙酰氯反應(yīng)得到相應(yīng)的氯乙酰苯胺。最后將前面制備的苯甲酰胺關(guān)鍵中間體與取代氯乙酰苯胺反應(yīng)制得相應(yīng)的查爾酮苯甲酰胺系列衍生物(查爾酮BAA22~35)(見圖3)。
1.2.2 體外抗腫瘤活性篩選[13-14]體外篩選了目標(biāo)化合物對(duì)EGFR(表皮生長(zhǎng)因子受體)、VEGFR-2(血管內(nèi)皮細(xì)胞生長(zhǎng)因子受體-2)和FGFR1(成纖維細(xì)胞生長(zhǎng)因子受體-1)3種受體酪氨酸激酶的抑制活性;細(xì)胞水平篩選了目標(biāo)化合物對(duì)乳腺癌細(xì)胞(MCF-7)、非小細(xì)胞肺癌細(xì)胞(A549)、白血病細(xì)胞(K562)3種腫瘤細(xì)胞的增殖抑制活性[14];尋找基于EGFR/VEGFR-2/FGFR1多靶標(biāo)的抗腫瘤候選化合物。目標(biāo)化合物對(duì)受體酪氨酸激酶抑制活性篩選所用的試劑盒為ADP-Glo Kinase Assay檢測(cè)試劑盒(Promega),實(shí)驗(yàn)對(duì)照藥物選用吉非替尼(Gefitinib);腫瘤細(xì)胞增殖抑制活性篩選采用經(jīng)典的噻唑藍(lán)(MTT)方法,對(duì)照藥物選用吉非替尼(Gefitinib)。
查爾酮衍生物對(duì)EGFR、VEGFR-2和FGFR1 3種RTI抑制活性結(jié)果(見表1)可以看出,與陽(yáng)性藥吉非替尼相比,大部分化合物對(duì)EGFR、VEGFR-2和FGFR1具有一定程度的抑制活性。對(duì)EGFR抑制活性中,化合物BAA22、BAA23、BAA30和BAA31的活性結(jié)果接近(IC50小于20 nmol·L-1)吉非替尼(IC50=4.07 nmol·L-1),這4個(gè)化合物的結(jié)構(gòu)特征是結(jié)構(gòu)母核為溴代苯甲酰胺結(jié)構(gòu),末端苯胺為3-氯-4-氟苯胺或者3-三氟甲基苯胺;化合物BAA25對(duì)EGFR無(wú)抑制活性,說(shuō)明溴代苯甲酰胺是EGFR的有效結(jié)構(gòu)片段,而3-氯-4-氟苯胺或者3-三氟甲基苯胺對(duì)EGFR的抑制活性是必需的;有11個(gè)化合物的IC50值在1~30 nmol·L-1,其中有4個(gè)化合物的活性在20 nmol·L-1以下,值得深入研究。對(duì)于VEGFR-2,4個(gè)化合物的活性結(jié)果較好,分別是BAA10(IC50=17.09 nmol·L-1),BAA16(IC50=14.65 nmol·L-1),BAA19(IC50=15.50 nmol·L-1)和BAA30(IC50=12.44 nmol·L-1);對(duì)于FGFR1,目標(biāo)化合物的抑制活性普遍低于對(duì)EGFR和VEGFR-2的抑制活性,說(shuō)明該系列化合物對(duì)FGFR1的選擇性不如EGFR和VEGFR-2,其次,化合物BAA1(IC50=19.54 nmol·L-1),BAA3(IC50=13.69 nmol·L-1)和BAA29(IC50=19.23 nmol·L-1)的活性較好。從整體活性結(jié)果顯示,化合物BAA30對(duì)EGFR、VEGFR-2和FGFR1的抑制活性均較好,特別是對(duì)EGFR和VEGFR-2的抑制活性明顯高于其他化合物,說(shuō)明BAA30結(jié)構(gòu)中的溴代苯甲酰胺是較為理想的多靶標(biāo)酪氨酸激酶抑制劑鉸鏈區(qū)結(jié)合基團(tuán),其末端的3-三氟甲基取代基對(duì)于保持化合物的多靶標(biāo)抑制活性是必需的。
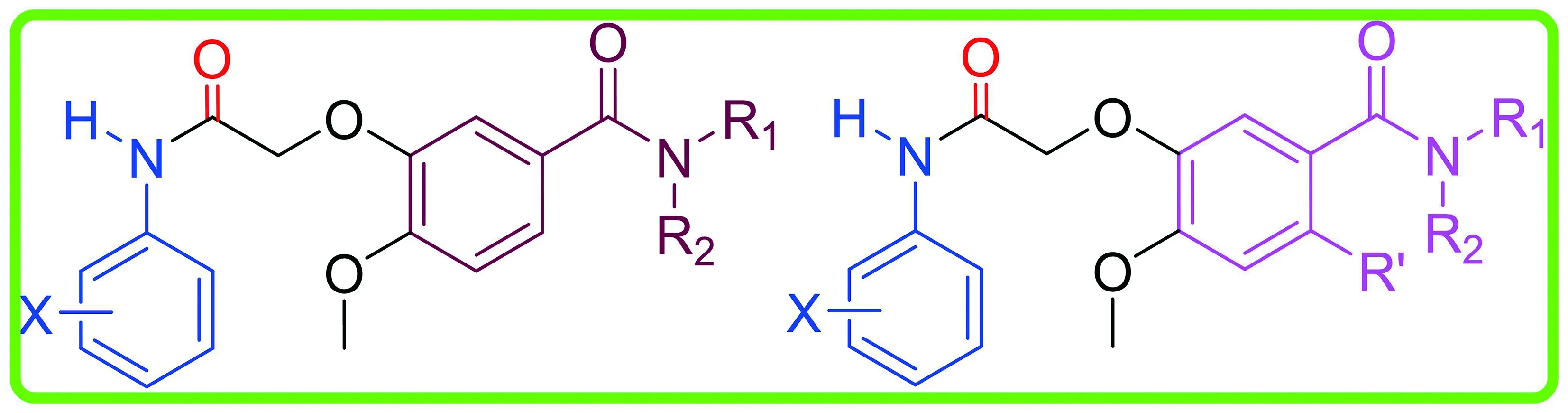
表1 查爾酮衍生物對(duì)受體酪氨酸激酶的抑制活性結(jié)果(IC50,nmol·L-1)
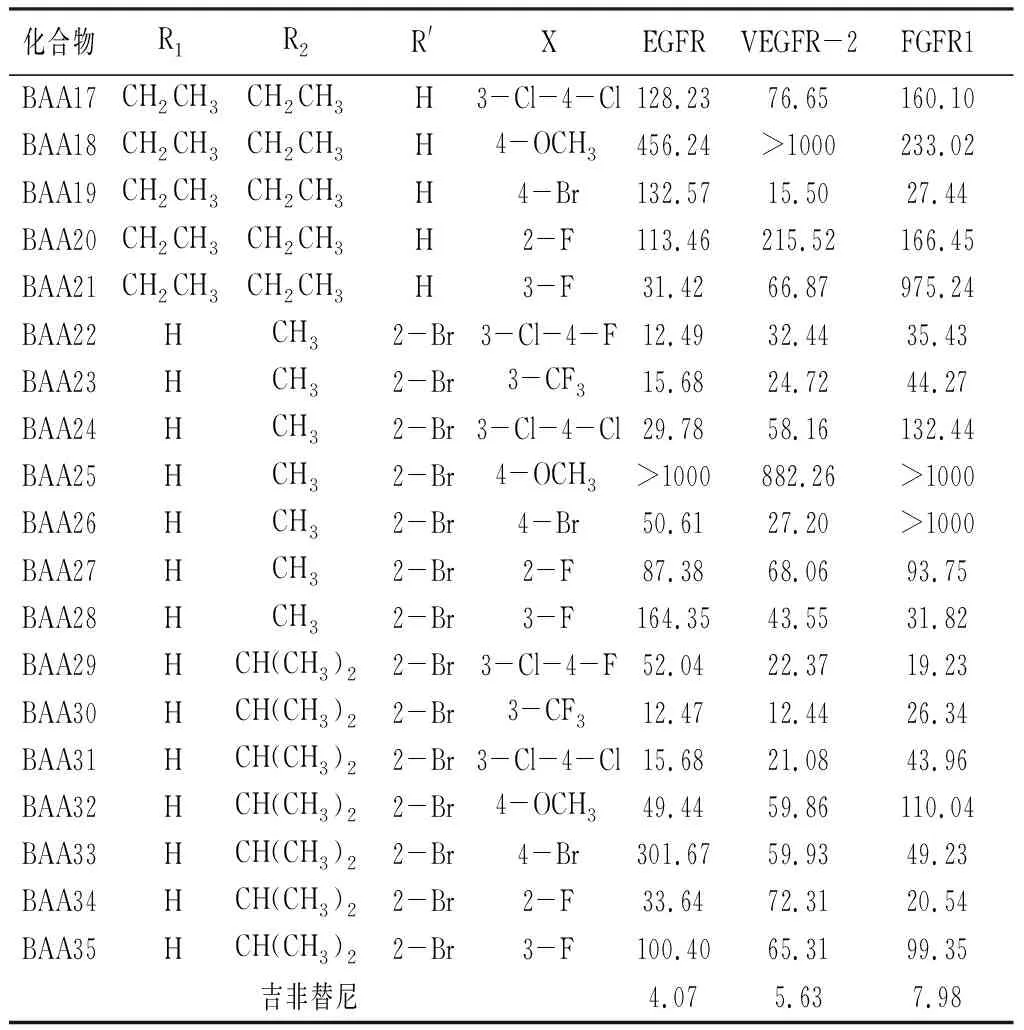
表1(續(xù))
查爾酮衍生物對(duì)乳腺癌細(xì)胞(MCF-7)、非小細(xì)胞肺癌細(xì)胞(A549)、白血病細(xì)胞(K562)的增殖抑制活性見表2。大部分衍生物對(duì)3種腫瘤細(xì)胞均具有一定的增殖抑制活性,其中活性最高的化合物是BAA23,其結(jié)構(gòu)特征為苯甲酰胺母核上2-位為溴取代基,末端苯胺為3-三氟甲基苯胺,對(duì)MCF-7、A549、K562的抑制活性IC50值分別為5.42、8.27、9.82 μmol·L-1。對(duì)于不含溴的苯甲酰甲胺類衍生物,活性最高的是BAA5(末端為4-溴苯胺),對(duì)3種腫瘤細(xì)胞增殖抑制活性IC50值分別為12.7、15.2、13.3 μmol·L-1。對(duì)于不含溴的苯甲酰異丙胺類衍生物,活性最高的是BAA8(末端為3-三氟甲基苯胺),對(duì)3種腫瘤細(xì)胞增殖抑制活性IC50值分別為21.7、10.4、8.93 μmol·L-1;該系列中對(duì)MCF-7抑制活性最高的是BAA14(末端為3-氟苯胺)。對(duì)于不含溴的苯甲酰二乙胺類衍生物,活性最高的是BAA16(末端為3-三氟甲基苯胺),對(duì)3種腫瘤細(xì)胞增殖抑制活性IC50值分別為24.1、20.4、12.4 μmol·L-1。對(duì)于苯甲酰胺母核上含溴取代基的化合物(BAA22~BAA35),其抗腫瘤活性普遍優(yōu)于不含溴的衍生物,包括活性最高的化合物BAA23。苯甲酰甲胺類衍生物中BAA26和BAA27對(duì)3株腫瘤細(xì)胞的增殖抑制活性值在20~30 μmol·L-1之間,活性較好。苯甲酰異丙胺系列化合物中,BAA33和BAA36的活性較好,與BAA26接近。總結(jié)苯甲酰胺系列衍生物構(gòu)效關(guān)系發(fā)現(xiàn):苯甲酰胺母核上溴取代基有利于提高活性,末端苯胺上的三氟甲基與氟取代基有利于抗腫瘤活性。
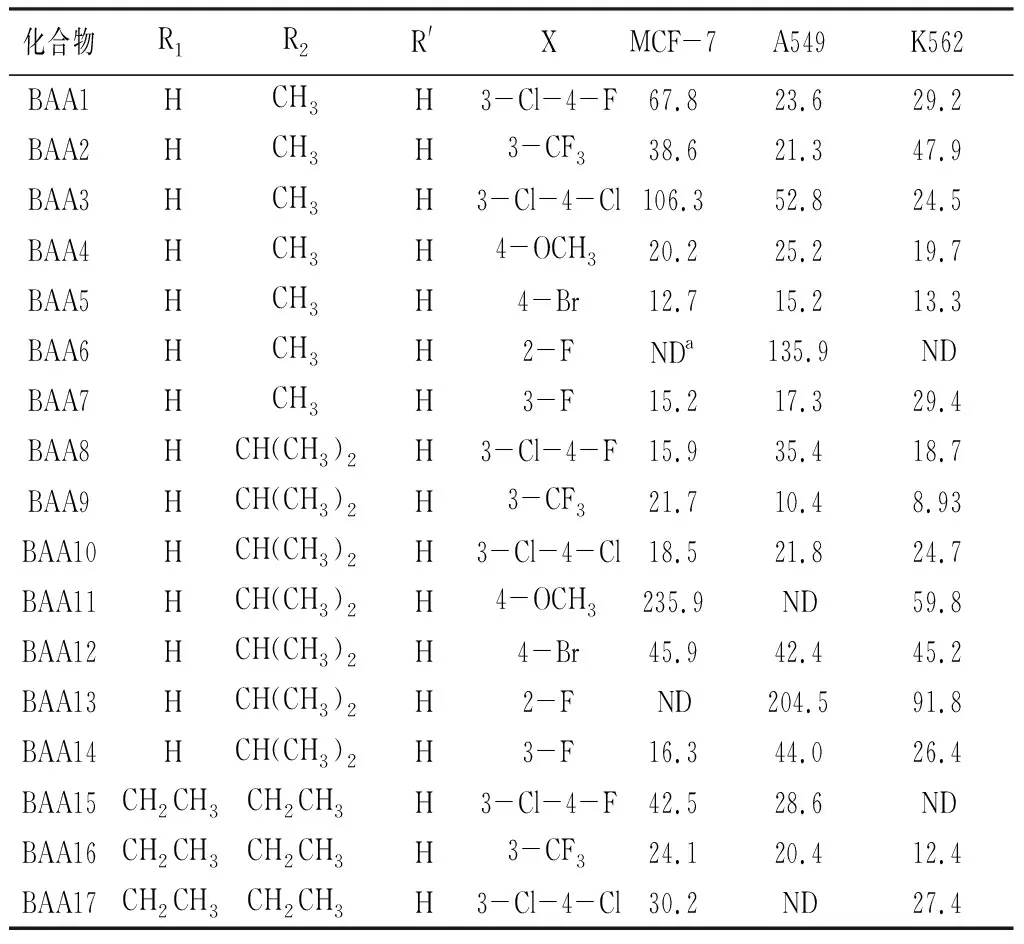
表2 查爾酮衍生物對(duì)不同腫瘤細(xì)胞株的抗增殖活性(IC50,μmol·L-1)
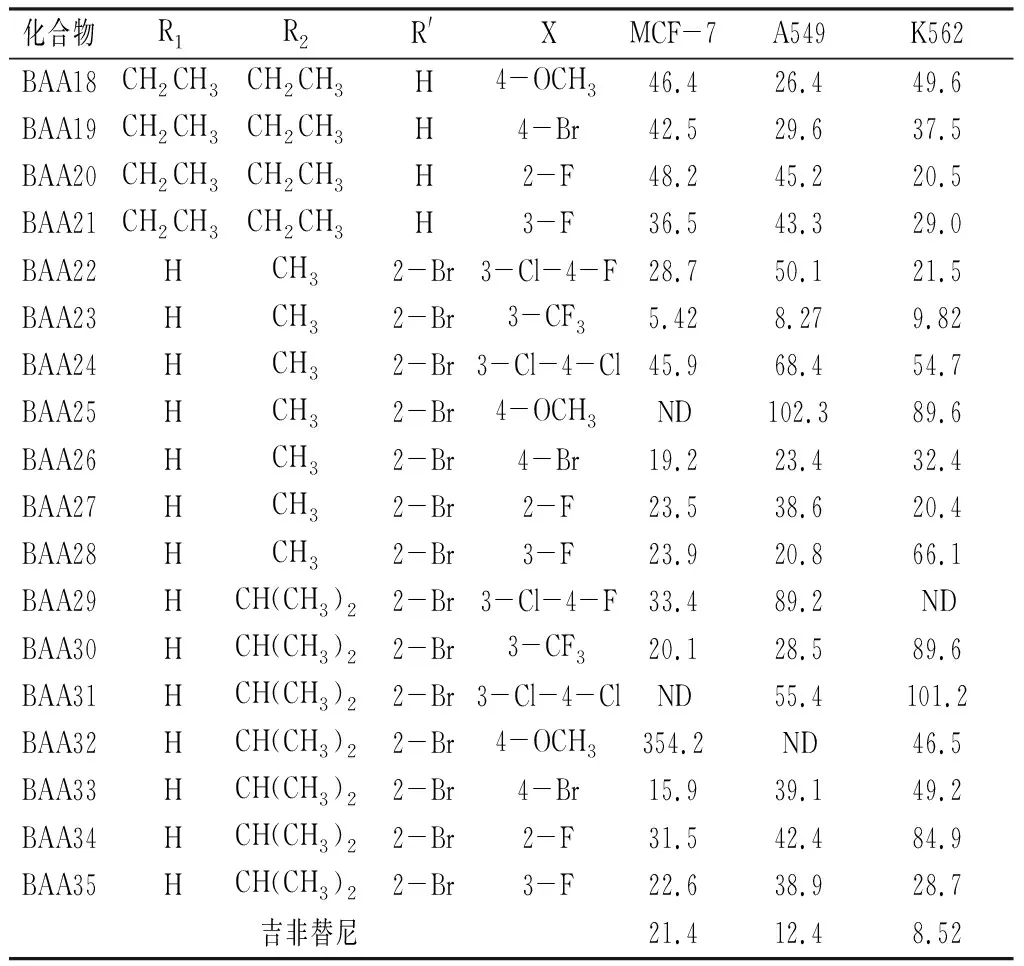
表2(續(xù))
2 討論
以查爾酮為先導(dǎo)化合物,針對(duì)查爾酮母核結(jié)構(gòu)中α,β-不飽和雙鍵的缺陷,共設(shè)計(jì)、合成了35個(gè)新型查爾酮衍生物。合成路線合理,反應(yīng)條件比較溫和,均由廉價(jià)易得的異香草醛為原料制備。體外活性實(shí)驗(yàn)表明,大部分化合物具有較好的RTK抑制與抗腫瘤活性,部分化合物的活性接近陽(yáng)性對(duì)照的水平。為新型查爾酮先導(dǎo)化合物的結(jié)構(gòu)優(yōu)化提供了依據(jù)。

