生物基聚對苯二甲酸丙二醇酯低聚物的提取及其熱性能
王晶晶,陳 詠,王朝生,王華平,,邊樹昌,烏 婧
(1. 東華大學 材料科學與工程學院,上海 201620; 2. 東華大學 紡織產業關鍵技術協同創新中心,上海 201620; 3. 江蘇國望高科纖維有限公司,江蘇 蘇州 215000)
熔融本體聚合制備逐步縮聚物的過程中,受熱力學驅動,聚合物中常含有一定比例的低聚物[1-2]。由于其相對分子質量較低,易在聚合物后續加工過程中遷移[3-5],會極大干擾聚合[6]、紡絲和染色等多個生產環節[7-9]。對纖維級聚酯切片所含低聚物進行定性、定量分析,并針對性地降低纖維生產加工過程中低聚物的含量,對于提升聚酯纖維的生產效率及后道產品品質具有重要研究意義。Franz等[10]在1967年首次對聚對苯二甲酸乙二醇酯(PET)中低聚物進行了提取分離工作。結果表明,PET切片中低聚物質量分數約為2%~3%,纖維中低聚物質量分數約為2.5%~3%[11-12];低聚物的主要成分為環狀三聚體。Weijers等[13]對聚對苯二甲酸丁二醇(PBT)中的低聚物進行定性定量分析發現,PBT中低聚物的總含量約為1%~2%,其中環狀二聚體為主要成分。隨著聚對苯二甲酸丙二醇酯(PTT)的成功產業化,研究人員也針對PTT所含低聚物進行了研究。Bumchan等[14]利用溶解-沉淀法對PTT進行提取發現,其低聚物主要由環狀二、四、五聚體組成,含量最高的為環狀二聚體,占總樣品質量的2.5%。與此相反,宛新華等[15]利用“假高稀”條件在冰水浴條件下合成了PTT環狀低聚物,產物主要由二、三、四、五、七聚體組成,其中三聚體含量最高,質量分數為34.9%。總體而言,基于已有研究工作,PTT中環狀低聚物的含量較PET(1%~3%)和PBT(1%~2%)更高,甚至可達3%~5%左右[16-17]。
近年來,隨著有機物提取分離技術的進一步發展,多種方法在芳香族聚酯低聚物的提取研究中均獲得了應用。主要包含基于傳統技術發展起來的溶劑溶解-沉淀法和索氏萃取法[18-19],以及基于現代技術發展起來的超聲波萃取法和超臨界流體萃取法等[13, 20-21]。然而,目前的所有方法都存在一定的局限性,且環狀低聚物的提取結果與所使用的提取方法密切相關。
生物基PTT作為我國新型聚酯品種,其大容量、高品質化生產對于我國生物基纖維產業的升級具有重要的戰略意義。鑒于前述低聚物,特別是環狀低聚物對于聚酯生產的多個環節均存在潛在影響,樣品的形態也會對聚酯樣品內部的低聚物遷移性有一定的影響。綜合考慮實驗成本及裝置的簡易性[22-23],本文采用溶解-沉淀法和索氏萃取法對生物基PTT進行提取。本文研究的生物基PTT樣品形態主要包括切片、粉末和纖維,對其所含低聚物進行定性定量分析,并研究其熱學性能,以期為深入理解生物基PTT中低聚物對于聚合、紡絲和后道加工的多個生產環節的影響提供參考。
1 實驗部分
1.1 主要原料
生物基PTT樣品(PTT-1,盛虹集團有限公司;PTT-2,美景榮化學工業有限公司;PTT-3,美國杜邦公司);氯仿、1,4-二氧六環(分析純,國藥集團化學試劑有限公司);六氟異丙醇(質量分數為99%,沃凱化工科技有限公司);甲醇、四氫呋喃(上海凌峰化學試劑有限公司);氘代氯仿、乙醇(質量分數為95%,上海金畔生物科技有限公司);二甲基甲酰胺(分析純,阿達瑪斯試劑有限公司)。3種生物基聚酯樣品的相關物理性能參數如表1所示。
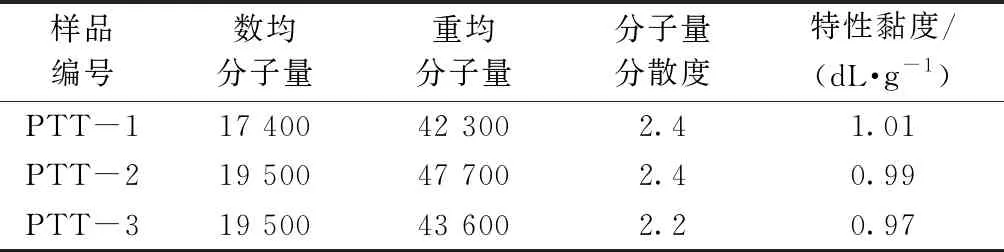
表1 生物基PTT物理性能參數Tab.1 Bio-based PTT polyester physical properties
1.2 生物基PTT纖維的制備
將3種生物基PTT切片進行熔融紡絲,設置噴絲板孔數為36,孔徑為0.5 mm,長徑比為1.5,紡絲速度為800 m/min,熱牽伸倍率為3.5,控制熱輥溫度為80 ℃,熱板溫度為160 ℃,牽伸速度為 200 m/min。 控制一區、二區、三區、四區溫度分別為270、280、275、275 ℃。將制得的纖維用乙醇洗去表面油劑,干燥后對生物基PTT纖維進行環狀低聚物提取。
1.3 生物基PTT粉末的制備
將3種生物基PTT切片置于粉碎機內,以液氮保護,打碎至直徑約為10 μm的粉末。
1.4 生物基PTT環狀低聚物提取方法
1.4.1 溶解-沉淀法
將約6 g生物基PTT樣品(切片、纖維)加入至120 mL的六氟異丙醇(HFIP)和氯仿(CHCl3)的混合溶劑中,二者體積比為1∶3,于50 ℃攪拌0.5 h至聚合物完全溶解后,冷卻至室溫,加入240 mL甲醇沉降劑,常溫攪拌0.5 h后,過濾并將濾液旋干得到白色環狀低聚物粉末,進一步于50 ℃真空干燥至質量恒定。
1.4.2 索氏提取法
將約5 g生物基PTT樣品(切片、粉末、纖維)置于索氏提取器中。分別以CHCl3、二氧六環及CHCl3/二氧六環(二者體積比為1∶2)混合溶劑為萃取溶劑體系,進行反復回流提取得到環狀低聚物粉末,探究不同萃取時間與萃取率的關系。
1.5 生物基PTT提取物表征
1.5.1 化學結構測試
采用Bruker Avance 3HD 600 Hz型核磁共振譜儀對樣品的化學結構進行表征,溶劑為含四甲基硅氧烷(TMS)內標物的氘代氯仿(CDCl3),測試溫度為25 ℃; 將溶解-沉淀法和索氏萃取法獲得的提取物干燥后,分別稱取5~10 mg樣品溶解在適量CDCl3中,待樣品溶解完全進行測試。
采用Nicolet 6700型傅里葉變換紅外光譜儀對樣品提取進行結構分析,使用ATR附件測試。
1.5.2 熱性能測試
采用TAQ-20型差示掃描量熱儀表征提取物的熱學性能。取5~10 mg樣品,測試溫度由30 ℃升溫至280 ℃,消除熱歷史后,以10 ℃/min降溫速率降溫至30 ℃,記錄焓值(ΔH)隨溫度的變化曲線。
采用TA-Q5000IR型熱重分析儀對低聚物熱穩定性進行分析,稱取1~3 mg聚酯粉末置于坩堝內,在氮氣氣氛(流速為50 mL/min)下,設定初始溫度40 ℃,以10 ℃/min的速率升溫至600 ℃。
1.5.3 高效液相色譜測試
采用C8-3型液相色譜柱(HPLC)進行測試,流動相溶劑體系為THF、CH3OH和H2O(三者體積比為5∶4∶1),紫外線(UV)檢測器波長為254 nm,稱取1 mg樣品溶解在1 mL四氫呋喃溶液中,待樣品完全溶解后,進樣體積為10 μL,流速為1 mL/min。
1.5.4 基質輔助激光解吸電離飛行時間質譜測試
采用LDI-1700型激光解吸電離飛行時間質譜儀(MALDI-TOF)進行測試,采用N2激光器,脈沖持續3 ns,激光波長為337 nm,檢測電壓為-4.75 kV,激光質譜圖采集約為200次掃描累加,以正離子譜測定,基質為1,8,9-蒽三酚(DHB),測試時吸取0.5 uL的混合溶液于樣品探頭靶心上,有機溶劑為二甲基甲酰胺。
2 結果和討論
2.1 生物基PTT低聚物的提取量分析
2.1.1 溶解-沉淀法提取生物基PTT低聚物
針對生物基PTT切片和纖維樣品,本文首先使用沉淀-溶解法對其進行環狀低聚物提取。前期實驗通過對HFIP和CHCl3混合溶劑體系的溶劑體積比為1∶1、1∶2、1∶3、1∶4、1∶5進行篩選發現,HFIP和CHCl3體積比小于1∶3時,PTT樣品能夠實現較好溶解,因此,以此溶劑體系作為溶解-沉淀法的溶劑。溶解-沉淀法的總體提取結果如表2所示。可知,生物基PTT纖維的低聚物提取量略高于切片,分別為2.7%~3.6%及2.6%~3.1%。縱向比較3種來源的生物基PTT,其低聚物提取量以PTT-3最高;經過熔融紡絲后低聚物的含量增加明顯,高達3.55%。
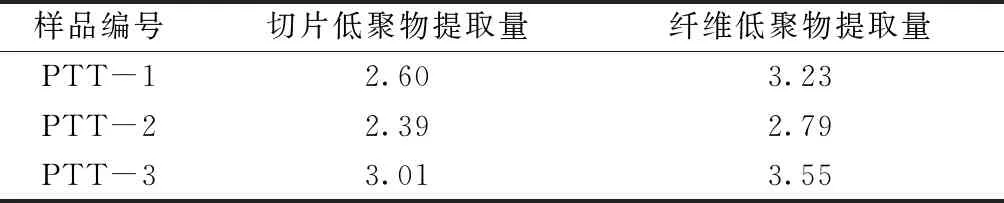
表2 生物基PTT切片和纖維樣品通過 溶解-沉淀法所得提取物含量Tab.2 Extraction content of bio-based PTT polyester chips and fiber samples by dissolution- precipitation method %
2.1.2 索氏提取法提取生物基PTT低聚物
對芳香聚酯環狀低聚物進行索氏萃取時,常用的溶劑為氯仿、二氧六環、苯酚、氯苯、二甲苯以及氯仿/二氧六環混合溶劑等。根據相似相容原理,理想的萃取溶劑可在最大程度上將低聚物溶解,而保持對高聚物的低溶解度。根據文獻[17]研究結果,較為高效的芳香聚酯環狀低聚物提取溶劑為氯仿或氯仿/二氧六環混合溶劑體系。本文分別使用氯仿、二氧六環,以及氯仿/二氧六環(體積比為1∶2)混合溶劑,通過索氏萃取法對不同形態的生物基PTT樣品(切片、粉末、纖維)所含低聚物進行定性、定量分析。圖1示出以不同溶劑萃取PTT切片、粉末及纖維提取物含量與時間的關系。
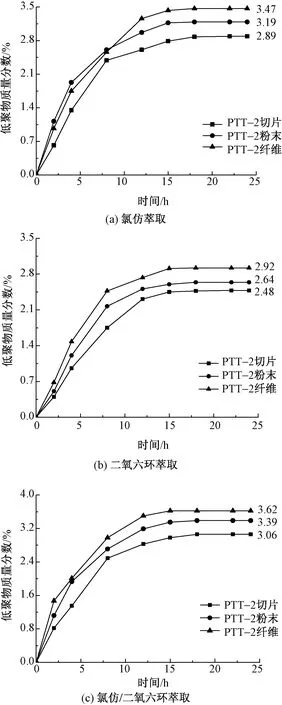
圖1 不同溶劑萃取PTT切片、粉末及 纖維提取物的質量分數與時間的關系Fig.1 Relationship between mass ratio of oligomer extracted from PTT chip, powder and fiber with different solvent. (a) Chloroform extraction;(b) Dioxane extraction;(c) Chloroform/dioxane extraction
根據圖1可知,溶劑體系對萃取平衡時間無明顯影響,而主要影響低聚物的萃取率。不同形態的樣品在不同溶劑和萃取溫度下,總體均可在15~18 h 達到萃取平衡。對比表2和圖1結果可以看出,低聚物提取量:溶解-沉淀法<索氏萃取法;切片<粉末<纖維。由于粉末比表面積較大,其與溶劑的接觸面積也較大,更有利于低聚物的萃取;溶解-沉淀法可提取所有的低聚物,其提取率理論上應該與多數文獻報道的結果一致,即高于萃取法的提取率,然而本文所獲得結果與之相反。其原因可能與溶解-沉淀提取過程中提取物的質量損失,以及PTT切片熔融紡絲過程中高溫(280 ℃)促進低聚物的形成有關。纖維表面的提取物總含量為2.5%~3.6%。進一步利用掃描電鏡(SEM)對PTT-2纖維表面形貌進行表征,結果如圖2所示。可以看出,相較于表面粗糙且有附著物的纖維原樣,溶劑萃取后的纖維表面更為光滑。

圖2 索氏提取前后生物基PTT-2纖維表面 形貌掃描電鏡照片Fig.2 Surface SEM images of bio-based PTT-2 polyester fiber before(a)and after (b) Soxhlet extraction
2.2 生物基PTT提取物組分分離結果
為對上述溶解-沉淀法和索氏萃取法提取的產物的組分進行定性定量分析,其高效液相色譜圖如圖3所示,對應各組分含量如圖4所示。可以看出,2種提取方法的提取物呈現相近的HPLC分離結果。提取物在保留時間分別為4.8、5.5、6.8、7.8、9.1、11.1 min時出現6個分離的峰,其中峰1為主要組分,含量高達85%~90%,其他5個峰所代表的組分總含量為10%~15%。
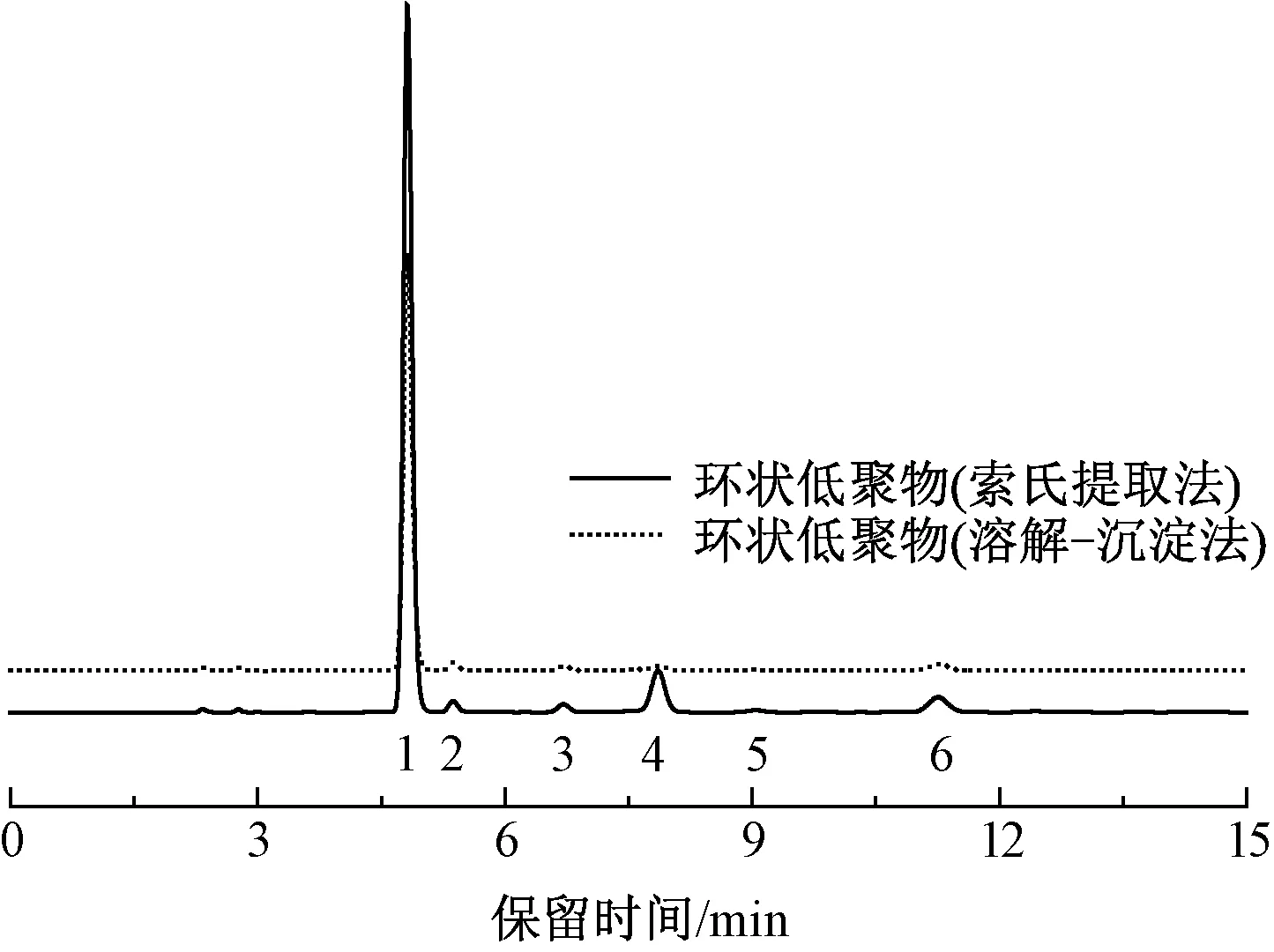
圖3 生物基PTT-2切片經溶解-沉淀法和 索氏萃取法獲得提取物的HPLC圖Fig.3 Liquid chromatographic separation of oligomers extracted from bio-based PTT-2 chips via Soxhlet extraction and dissolution-precipitation methods
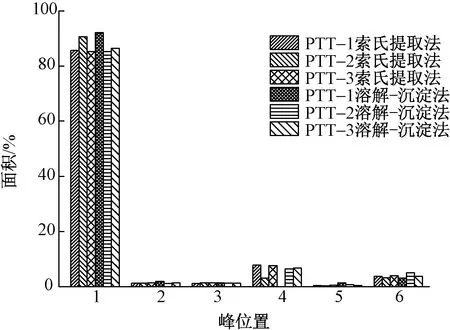
圖4 生物基PTT切片提取物6種組分比例圖Fig.4 Proportions of 6 extracted components of oligomers extracted from bio-based PTT polyester chips
2.3 環狀低聚物組分化學結構分析
2.3.1 提取物的核磁共振譜圖分析
對溶解-沉淀法和索氏萃取法提取物進行核磁共振表征,結果如圖5所示。可知,2種方法獲得的產物呈現較為類似的1HNMR譜圖,且與PTT高聚物的譜圖較為類似。化學位移δ為2.24~2.31處是1,3-PDO中間亞甲基氫的信號峰,δ在4.51~4.62范圍內對應1,3-PDO與氧相連的亞甲基上氫的信號峰,而7.64~8.06處則為苯環上氫的信號峰。由譜圖可以看出未出現活潑氫的核磁信號,提取物則較大可能為環狀結構,而非直鏈結構。
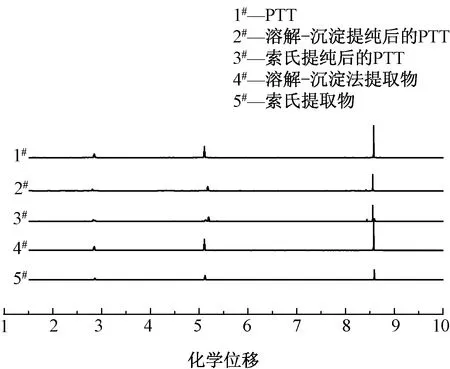
圖5 生物基PTT切片提取物的核磁氫譜圖Fig.5 1HNMR spectra of oligomers extracted from bio-based PTT polyester chips
2.3.2 提取物的紅外譜圖分析
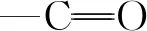

圖6 生物基PTT-2切片索氏萃取法提取物的紅外譜圖Fig.6 Infrared spectra of extracts from bio-based PTT-2 polyester chips by Soxhlet extraction
2.3.3 提取物的MALDI-TOF質譜分析
由于環狀低聚物化學結構特殊,其不具有直鏈低聚物和直鏈高聚物具有的羥基或羧基官能團,因而可利用質譜對其進行表征。本文以生物基PTT-2 切片經索氏萃取后的低聚物進行MALDI-TOF 分析,結果如圖7所示。可知,萃取物中含有PTT環狀二聚體(相對分子質量412)、環狀三聚體(相對分子質量618)、環狀四聚體(相對分子質量824)、環狀五聚體(相對分子質量1 030)和環狀七聚體(相對分子質量1 442)[24-26]。可能由于環狀六聚體含量太低或儀器分辨率不足的原因,檢測結果中無法判定其是否存在。盡管根據MALDI-TOF譜圖中所有信號的強度無法對每種成分進行準確的定量分析,然而,與前述HPLC分析結果相對應,本文認為PTT提取物中的6種組分很可能包括環狀二聚體(C2)、 環狀三聚體(C3)、環狀四聚體(C4)、環狀五聚體(C5)、環狀六聚體(C6)和環狀七聚體(C7)。
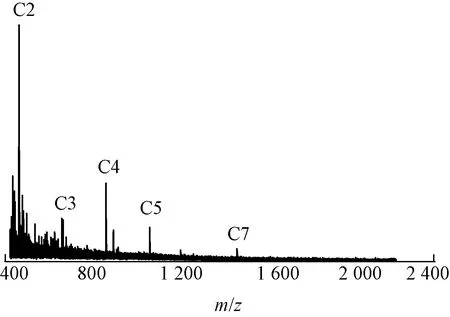
圖7 生物基PTT-2切片索氏提取物的 MALDI-TOF圖Fig.7 MALDI-TOF plot of Soxhlet extract from bio-based PTT-2 polyester chips
2.4 生物基PTT低聚物的熱穩定性分析
PTT主要應用于纖維以及工程塑料等,所以聚酯在加工過程(如紡絲、注塑等)中的熱穩定性極其重要。對生物基PTT、提純后的生物基PTT和提取物的熱穩定性進行比較分析,結果如圖8所示。可知,提取物的熱穩定性明顯低于未提純以及提純后的生物基PTT-2。提取物質量損失率約為5%時的溫度(Td,5%)為287 ℃,而高聚物的Td,5%值高達363 ℃。 未提純生物基PTT以及提純后的PTT-2的Td,5%值差別不大,其原因可能是由于環狀低聚物含量較少,其對熱穩定性的影響并不明顯。同時,低聚物呈現2個明顯的質量損失臺階(340、396 ℃)。這很大可能與低聚物是由一系列聚合度不同的環聚體組成有關。
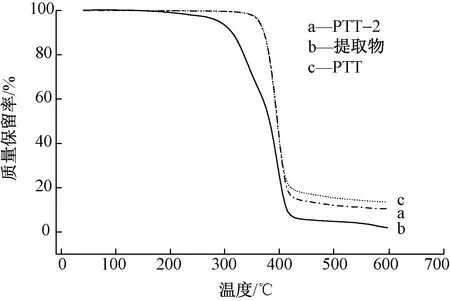
圖8 熱重分析曲線Fig.8 Thermogravimetric analysis curve
2.5 生物基PTT環狀低聚物熱學性能分析
生物基PTT環狀低聚物的相對分子質量通常在在幾百至1 000左右,與高聚物相對分子質量差異較大,其存在也會對聚酯的熱力學性能造成一定影響。使用差示掃描量熱法可表征環狀低聚物的熱學性能,從而進一步與PTT進行區分。由于生物基PTT主要的應用領域之一是作為纖維,且目前高低聚物含量的生物基PTT在紡絲過程中出現毛頭、斷絲現象嚴重,所以研究環狀低聚物在聚酯常規加工過程如擠出、注塑和紡絲等的熱學性能顯得十分重要。圖9示出生物基PTT-2索氏提取物的DSC曲線圖。
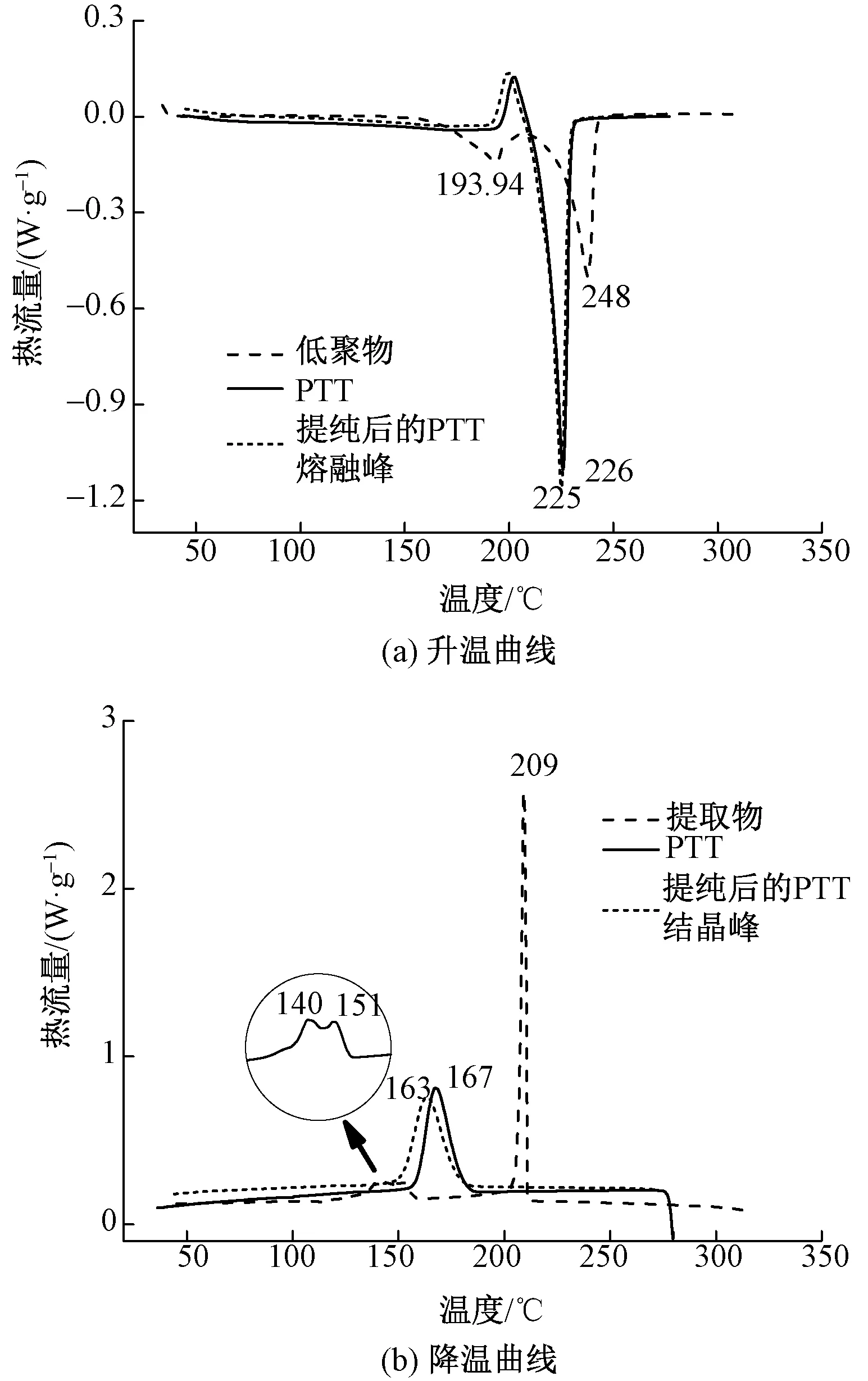
圖9 生物基PTT-2索氏提取物的DSC曲線圖Fig.9 DSC curves of oligomers extracted from bio-based PTT-2 polyester by Soxhlet extraction. (a) Heating curve; (b) Cooling curve
從圖9可以看出,生物基PTT-2切片經索氏萃取后的環狀低聚物在升溫過程中出現2處明顯的熔融峰,熔點分別為194和248 ℃,其中248 ℃為環狀二聚體的熔點,與文獻報道數據吻合[15],194 ℃熔融峰則推測為其他環狀低聚物混合物呈現的熔點。環狀二聚體熔點高于生物基PTT-2切片的熔點約20 ℃,熔融焓為67.23 J/g,低于PTT的熔融焓;生物基PTT-2的結晶溫度比提取物低約 41 ℃,結晶焓高于提取物;提取物玻璃化轉變溫度比PTT-2高出20 ℃,高達80 ℃。主要是因為環狀二聚體分子僅含有2個鏈段,分子鏈柔性較差,空間位阻較大。在結晶峰的曲線上,低聚物也有2處結晶峰,與熔融峰相對應。
3 結 論
本文以生物基PTT為原料,重點研究其所含低聚物的組分及其含量,并對提取的低聚物進行化學結構、熱穩定性及熱學性能分析,得出以下主要結論。
1)通過溶解-沉淀法和索氏提取法對生物基PTT進行提取發現,生物基PTT的低聚物質量分數約為3%,其中纖維樣品的低聚物質量分數(3.6%)高于切片及粉末樣品,其原因可能與紡絲高溫條件下促進環狀低聚物的生成有關。
2)對低聚物進行高效液相色譜分離及激光解吸電離飛行時間質譜分析發現,低聚物的主要組分為環狀二聚體,其質量分數約為低聚物總量的 85%~90%; 同時檢測出低含量的環狀三聚體、環狀四聚體、環狀五聚體及環狀七聚體,幾種組分總含量約為10%~15%。而目前檢測結果尚不能證實環狀六聚體的存在。
3)生物基PTT環狀低聚物的穩定性遠低于PTT高聚物,其大量存在時可能嚴重影響高聚物的熱穩定性,對PTT產品的品質產生較大影響。通過DSC方法對低聚物進行熱學分析發現,環狀低聚物具有比高聚物更高的熔融溫度,其存在充當成核劑的作用,促進高聚物的結晶。

