螺旋斷層動態(tài)鎢門技術在宮頸癌術后放療中的應用
吳駿翔,劉敏,康盛偉,王培,黎杰,唐斌,吳凡
四川省腫瘤醫(yī)院·研究所/四川省癌癥防治中心/電子科技大學醫(yī)學院/放射腫瘤學四川省重點實驗室,四川成都610041
前言
螺旋斷層調(diào)強放療(Helical Tomotherapy,TOMO)技術應用于宮頸癌術后放療相比于調(diào)強放療(Intensity Modulated Radiation Therapy, IMRT)和 旋轉(zhuǎn)容積調(diào)強放療(Volumetric Modulated Arc Therapy,VMAT)技術可以提高靶區(qū)的均勻性和適形度,以及給予危及器官更好的保護[1-3]。TOMO 技術在提高計劃質(zhì)量的同時,也將顯著增加機器跳數(shù)和照射時間,在楊波等[2]研究中,使用TOMO技術應用于宮頸癌術后患者得到的計劃機器跳數(shù)分別是IMRT 和VAMT技術的5 倍和11 倍;而在劉娟等[4]研究中,宮頸癌患者使用TOMO 技術得到的機器跳數(shù)是IMRT 技術的7.1倍。TOMO計劃優(yōu)化時為了平衡計劃質(zhì)量和治療效率,通常選用射野寬度2.5 cm,如果使用5.0 cm 的射野寬度則可以顯著降低機器跳數(shù)和照射時間,但是卻不能保證計劃質(zhì)量。TOMO 最新的動態(tài)鎢門技術已應用于臨床,該技術通過鎢門的運動減少靶區(qū)邊緣頭腳方向的射野半影,從而降低靶區(qū)頭腳方向危及器官的受照劑量[5-7]。本研究探討能否使用射野寬度5.0 cm 的動態(tài)鎢門技術代替2.5 cm 的固定鎢門技術應用于宮頸癌術后調(diào)強治療,保證計劃質(zhì)量的同時減少照射時間。
1 資料與方法
1.1 患者資料
選擇2019年3~5月四川省腫瘤醫(yī)院收治的25例宮頸癌術后患者,年齡46~64 歲,中位年齡50 歲,所有患者均無放療禁忌證。根據(jù)國際婦產(chǎn)科聯(lián)合會(International Federation of Gynecology and Obstetrics, FIGO)分期[8],其中IIA期10 例,IIB期15例。
1.2 CT定位和靶區(qū)危及器官勾畫
患者采用仰臥位,體部熱塑膜固定體位,雙手交叉抱肘置于額頭,采用Philips Brilliance TM CT BigBore 416 排大孔徑CT 掃描機,掃描層厚0.3 cm,掃描范圍從胸10至坐骨結(jié)節(jié)下5 cm。掃描后將患者CT 數(shù)據(jù)傳送至美國MIM Software 公司的MIM Maestro軟件由主管醫(yī)生勾畫計劃靶區(qū)(PTV)和危及器官。臨床靶區(qū)(CTV)由盆腔淋巴引流區(qū)(CTVln)、陰道殘端(CTV2)和陰道上段(CTV1)組成。CTV 在頭腳方向外擴0.6~0.8 cm,其余方向外放0.8~1.0 cm形成PTV。危及器官包括直腸、膀胱、小腸、骨髓、脊髓以及股骨頭。
1.3 處方劑量和計劃設計
PTV處方劑量50.4 Gy,28次,1.8 Gy/次。計劃要求處方劑量,即50.4 Gy劑量線至少要覆蓋95%的靶區(qū)體積,靶區(qū)內(nèi)Dmax<110%處方劑量。危及器官劑量限值為膀胱D40≤45 Gy,直腸D40≤45 Gy,小腸D40≤35 Gy,脊髓Dmax≤45 Gy,骨髓D40≤35 Gy,股骨頭D5≤50 Gy[9]。將勾畫好的結(jié)構(gòu)傳至美國Accuray公司的TomoTherapy治療計劃系統(tǒng),在相同優(yōu)化條件下分別設置射野寬度2.5 cm的固定鎢門(2.5F)、2.5 cm的動態(tài)鎢門(2.5D)和5.0 cm的動態(tài)鎢門(5.0D)計劃。劑量計算網(wǎng)格設為Fine,調(diào)制因子2.5,螺距設置為0.43。
1.4 計劃評價指標
靶區(qū)和危及器官的評估參考國際輻射單位和測量委員會(ICRU)83 號報告[10]建議,其中靶區(qū)評估采用95% PTV 體積的劑量D95、平均劑量Dmean、均勻性指數(shù)(HI)以及適形度指數(shù)(CI)。HI=(D2-D98)/D50,其中D2、D50和D98為2%、50%和98%靶區(qū)體積所對應的劑量;CI=(TVPV)2/(TV×PV),其中TVPV為處方劑量所覆蓋的PTV 的體積,TV 為PTV 的體積,PV 為處方劑量線所覆蓋的總體積。HI越接近0表示均勻性越好,CI越接近1 表示適形度越高。危及器官的評估指標包括直腸和膀胱的V20、V30、V40和Dmean;小腸的V20、V30和Dmean;骨髓的V20、V30和Dmean;股骨頭的V20和Dmean;脊髓的Dmax。另外,還統(tǒng)計3組計劃的機器跳數(shù)和照射時間。Vn<m表示nGy 劑量所包裹的危及器官的體積小于m%。
1.5 統(tǒng)計學方法
采用SPSS 23.0 統(tǒng)計軟件進行分析,計量資料用均數(shù)±標準差表示,采用配對t檢驗分析,P<0.05 為差異有統(tǒng)計學意義。
2 結(jié)果
2.1 靶區(qū)和危及器官劑量學比較
3組計劃靶區(qū)和危及器官劑量參數(shù)結(jié)果見表1。3組計劃得到的靶區(qū)和危及器官的劑量學參數(shù)均能滿足臨床要求。3組計劃得到的靶區(qū)D95和Dmean參數(shù)的差異無統(tǒng)計學意義(P>0.05)。2.5D組得到的CI和HI值優(yōu)于其他兩組,差異有統(tǒng)計學意義(P<0.05),2.5F和5.0D兩組之間差異無統(tǒng)計學意義(P>0.05)。2.5D組對于危及器官的保護整體均優(yōu)于2.5F和5.0D組,與2.5F組相比,其中直腸(V20、V40和Dmean)、膀胱(V20、V40和Dmean)、骨(Dmean)、小腸(V20和Dmean)均降低,差異有統(tǒng)計學意義(P<0.05);與5.0D 組相比,直腸(V20)、膀胱(V20)、骨(Dmean)、小腸(V20和Dmean)均降低,差異有統(tǒng)計學意義(P<0.05)。5.0D和2.5F組相比,直腸(V20、V40和Dmean)、膀胱(V20、V40和Dmean)、小腸(V20)均降低,差異有統(tǒng)計學意義(P<0.05);骨、股骨頭和小腸的Dmean均增加,差異有統(tǒng)計學意義(P<0.05)。
表1 3組計劃靶區(qū)和危及器官劑量參數(shù)結(jié)果(± s)Tab.1 Results of target and OARs for treatment plans of three groups(Mean±SD)
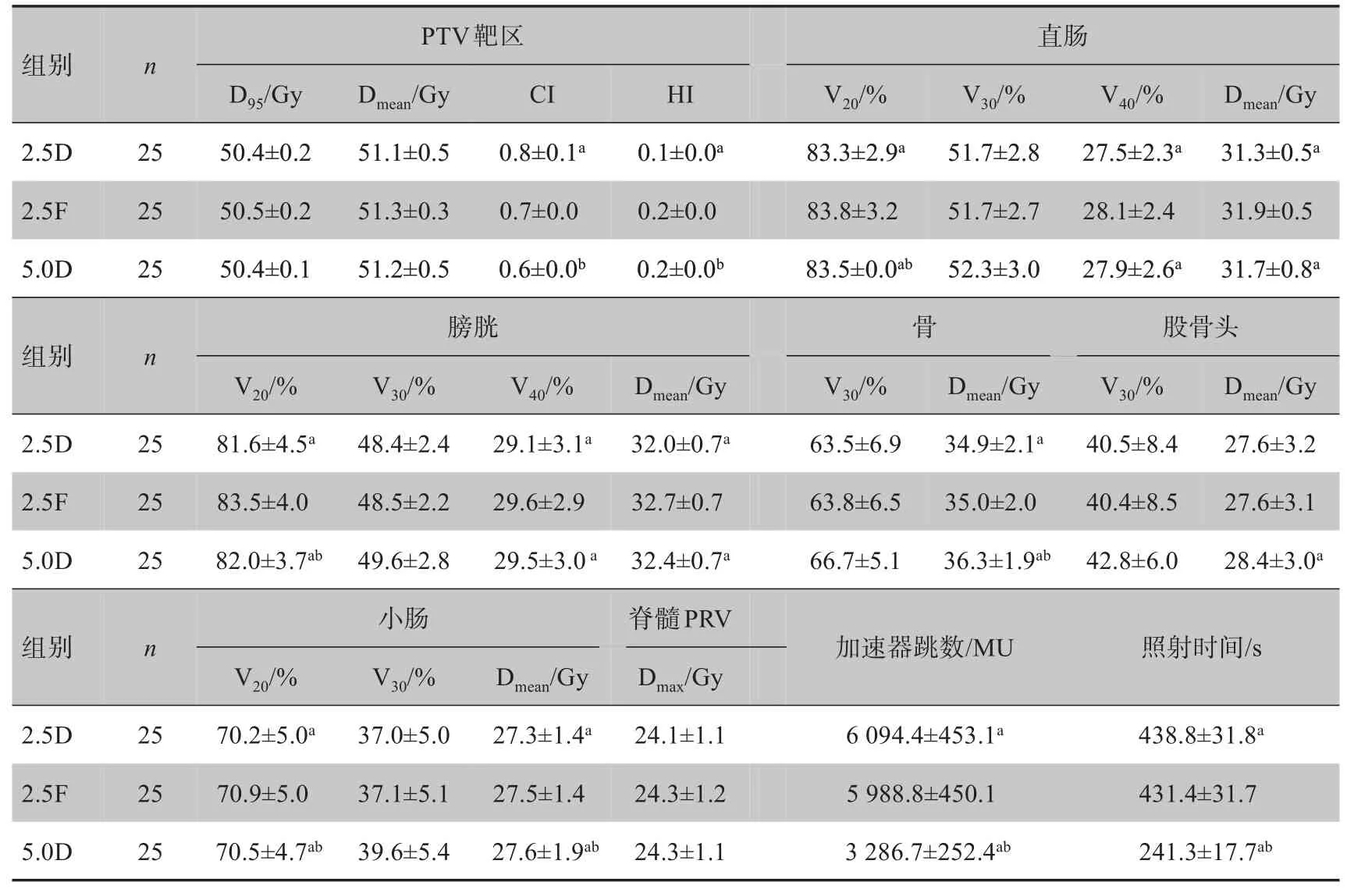
表1 3組計劃靶區(qū)和危及器官劑量參數(shù)結(jié)果(± s)Tab.1 Results of target and OARs for treatment plans of three groups(Mean±SD)
a與2.5F組相比,t=3.891、3.233、5.582、6.068、7.746、8.820、5.937、5.688、6.778、6.987、4.019、5.582、2.790、3.108、10.761、13.053、3.277、5.056、4.491、6.751、4.770、-41.638、-40.698、-41.574、-40.414,P<0.05;b與2.5D組相比,t=2.585、2.787、3.123、3.878、-2.813、-3.674、-2.419、17.703、17.654,P<0.05
組別n直腸Dmean/Gy CIHIV20/%V30/%Dmean/Gy PTV靶區(qū)D95/Gy V40/%2.5D 2.5F 5.0D 25 25 25 51.1±0.5 51.3±0.3 51.2±0.5 0.8±0.1a 0.7±0.0 0.6±0.0b 0.1±0.0a 0.2±0.0 0.2±0.0b 83.3±2.9a 83.8±3.2 83.5±0.0ab骨V30/%63.5±6.9 63.8±6.5 66.7±5.1組別n 2.5D 2.5F 5.0D 25 25 25 V30/%48.4±2.4 48.5±2.2 49.6±2.8 V40/%29.1±3.1a 29.6±2.9 29.5±3.0a照射時間/s Dmean/Gy 27.6±3.2 27.6±3.1 28.4±3.0a組別膀胱V20/%81.6±4.5a 83.5±4.0 82.0±3.7ab小腸V20/%70.2±5.0a 70.9±5.0 70.5±4.7ab n股骨頭V30/%40.5±8.4 40.4±8.5 42.8±6.0 V30/%37.0±5.0 37.1±5.1 39.6±5.4 Dmean/Gy 32.0±0.7a 32.7±0.7 32.4±0.7a脊髓PRV Dmax/Gy 24.1±1.1 24.3±1.2 24.3±1.1 2.5D 2.5F 5.0D Dmean/Gy 34.9±2.1a 35.0±2.0 36.3±1.9ab 25 25 25 Dmean/Gy 27.3±1.4a 27.5±1.4 27.6±1.9ab加速器跳數(shù)/MU 6 094.4±453.1a 5 988.8±450.1 3 286.7±252.4ab 438.8±31.8a 431.4±31.7 241.3±17.7ab 51.7±2.8 51.7±2.7 52.3±3.0 31.3±0.5a 31.9±0.5 31.7±0.8a 50.4±0.2 50.5±0.2 50.4±0.1 27.5±2.3a 28.1±2.4 27.9±2.6a
2.2 機器跳數(shù)和照射時間比較
2.5D、2.5F 和5.0D 組的機器跳數(shù)平均值分別為6 094、5 988和3 286 MU。5.0D組的機器跳數(shù)降低顯著,與2.5D 和2.5F 組相比分別降低46.1%和45.1%,差異有統(tǒng)計學意義(t=17.703、-40.698,P<0.05)。5.0D 組的照射時間與2.5D 和2.5F 組相比分別降低45.0%、44.1%,差異有統(tǒng)計學意義(t=17.654、-40.414,P<0.05)。另外,2.5D 和2.5F 組相比,在使用相同的射野寬度時動態(tài)鎢門技術將會增加機器跳數(shù)和照射時間,分別增加1.8%和1.7%,差異有統(tǒng)計學意義(t=-41.638、-41.574,P<0.05)。
3 討論
TOMO 通過64對二元化氣動多葉光柵給予靶區(qū)360°照射,其中每圈共51 個投影角度照射靶區(qū),每個子野100級以上的強度調(diào)制能力,調(diào)制能力遠高于常規(guī)IMRT 和VMAT 等技術[11-15]。對于宮頸癌患者使用TOMO 技術對于某些危及器官的保護優(yōu)于IMRT和VMAT 等技術[2,16]。楊波等[2]研究中,宮頸癌術后患者使用TOMO 技術靶區(qū)的CI和HI顯著提高,并且TOMO 得到的膀胱V40相比于IMRT 和VMAT 技術分別降低7%和4%,直腸V40分別降低8%和2%。但是TOMO 技術得到的機器跳數(shù)和照射時間與IMRT 和VMAT 等技術相比卻成倍增加,顯著降低治療效率[17-18]。
本研究比較了動態(tài)鎢門技術和固定鎢門技術在宮頸癌術后放療中的應用。研究結(jié)果表明,動態(tài)鎢門技術對于宮頸癌術后調(diào)強放療具有一定的劑量學優(yōu)勢,在相同射野寬度時,使用動態(tài)鎢門技術可以提高計劃質(zhì)量,其中直腸和膀胱(V20、V40和Dmean)、小腸(V20和Dmean)、骨(Dmean)等參數(shù)均降低,但是2.5D組的機器跳數(shù)和照射時間與2.5F 組相比,分別增加1.8%和1.7%;5.0D組的整體計劃質(zhì)量優(yōu)于2.5F組,5.0D組的直腸(V20、V40和Dmean)、膀胱(V20、V40和Dmean)、小腸(V20)均優(yōu)于2.5F組,而骨、股骨頭和小腸的Dmean高于2.5F 組。本研究結(jié)果與國內(nèi)外研究結(jié)果基本一致[7,19-20],在Manabe等[7]研究中,2.5 cm 動態(tài)鎢門得到的計劃質(zhì)量最好,其中2.5 cm 動態(tài)鎢門、2.5 cm 固定鎢門和5.0 cm 動態(tài)鎢門得到的肺V5分別為18.5%、21.8%和20.1%,V20為4.0%、4.7%和4.4%。動態(tài)鎢門技術在靶區(qū)縱向邊緣實現(xiàn)寬度調(diào)制,鎢門最小寬度縮短至1 cm,其實質(zhì)是可以縮短射野的半影寬度,通過胡志輝等[21]研究可知,1.0 cm固定鎢門的半影寬度為8.38 mm、2.5 cm 固定鎢門為17.92 mm、2.5 cm 動態(tài)鎢門為7.51 mm、5.0 cm 固定鎢門為33.73 mm 以及5.0 cm 動態(tài)鎢門為6.97 mm,射野寬度2.5 cm 和5.0 cm 的動態(tài)鎢門的半影寬度比固定鎢門相比分別減少10.41 和26.76 mm。另外,5.0D 組在計劃質(zhì)量優(yōu)于2.5F 組的同時,可以顯著降低機器跳數(shù)和照射時間,分別降低45.1%和44.1%。本研究選擇的是宮頸癌術后患者,靶區(qū)長度與常規(guī)宮頸癌相比較短,靶區(qū)周圍相鄰的危及器官有一定的差異,該研究結(jié)果具有一定的局限性。因此,本研究結(jié)果不一定適用于常規(guī)宮頸癌螺旋斷層放療,需要進一步研究。
總之,通過使用射野寬度5.0 cm的動態(tài)鎢門技術可以得到優(yōu)于射野寬度2.5 cm 固定鎢門的計劃質(zhì)量的同時有效地降低照射時間,提高治療效率。因此,綜合考慮計劃質(zhì)量和治療效率,推薦使用射野寬度5.0 cm 的動態(tài)鎢門技術替代升級前的射野寬度2.5 cm 固定鎢門技術應用于宮頸癌術后患者的放療應用。另外,通過本研究可知,射野寬度2.5 cm 的動態(tài)鎢門得到的計劃質(zhì)量最優(yōu),如果不考慮治療效率可以使用該照射技術。

