鉻取代針鐵礦異化鐵還原過程及鉻的環境行為研究
王春,童輝,華健,陳曼佳*,劉承帥,
1.廣東石油化工學院生物與食品工程學院,廣東 茂名 525000;2.廣東省科學院生態環境與土壤研究所/華南土壤污染控制與修復國家地方聯合工程研究中心/廣東省農業環境綜合治理重點實驗室,廣東 廣州 510650;3.中國科學院地球化學研究所/環境地球化學國家重點實驗室,貴州 貴陽 550001
鉻(Cr)自然環境中普遍存在的重金屬之一,環境中鉻的價態通常在-2到+6價之間,而+3價和+6價兩種價態相對穩定(Fendorf et al.,2000),且Cr(VI)的毒性遠遠大于 Cr(III),具有強烈的“三致性”(Han et al.,2004)。隨著我國工業化的快速發展,Cr及其化合物通過電鍍、冶金、皮革鞣制、紡織染色等方式排放到環境中,造成不同程度的土壤Cr污染,危害農產品安全及人類的健康(Dotaniya et al.,2014)。已有研究表明,Cr在土壤中的環境行為與含量豐富的鐵氧化物密切相關(Stewart et al.,2016),Cr可通過吸附鐵氧化物表面,形成表面絡合物或者沉淀物,影響Cr的遷移轉化(Singh et al.,2002)。同時,由于 Cr(III)和 Fe(III)的離子半徑十分接近(61.5 vs 64.5 pm),Cr(III)常與鐵氧化物結構中的 Fe(III)發生取代進入晶格中形成 Cr取代鐵氧化物,顯著影響了Cr(III)的移動性,生物可利用性以及 Cr(III)向有毒 Cr(VI)氧化轉化過程(Choppala et al.,2013)。因此,研究鐵Cr取代鐵氧化物的氧化還原、穩定性及 Cr的環境行為具有重要的土壤學和環境學研究意義。
鐵氧化物作為土壤中具有較高地球化學活性和高含量的重要礦物,其氧化還原循環過程需要微生物提供基本驅動力(Borch et al.,2010;Roden,2003)。在厭氧還原條件下,土壤中的鐵還原菌能以有機碳作為電子供體,以胞外不溶性鐵氧化物為末端電子受體,通過氧化電子供體耦聯Fe(III)還原,并從這一過程貯存能量(Kappler et al.,2005;Roden,2003),這一過程也稱為異化鐵還原過程。已有研究表明,土壤異化鐵還原過程可通過氧化還原、甲基化以及固定等作用顯著影響重金屬形態轉變、有效性以及遷移轉化等(Bousserrhine et al.,1999;Burton et al.,2019;Zachara et al.,2001;毛暉等,2005;司友斌等,2015)。Burton et al.(2019)對異化鐵還原過程中銻的遷移轉化進行研究,結果表明游離態的銻可被固定在新生成的鐵氧化物中,從而減少重金屬的危害。毛暉等(2005)研究不同Cr(VI)濃度壓迫下,水稻土的異化鐵還原過程,結果表明,Cr(VI)參與水稻土的鐵還原過程,在該過程中,Cr(VI)可被鐵氧化物或微生物吸附,降低了Cr的可利用性和生物有效性;且高濃度的Cr(VI)對土壤中鐵還原微生物具有毒害作用,從而抑制了水稻土的異化鐵還原過程。反之,金屬取代的鐵氧化物在異化鐵還原過程中,由于結構態Fe(III)的還原溶解,鐵氧化物結構發生變化,結構中的重金屬可被溶解釋放,提高了重金屬的移動性和可利用性(Zachara et al.,2001;張蕊等,2015)。Bousserrhine et al.(1999)研究表明,在Clostridiumbutyricum還原5% mol Cr取代針鐵礦([Cr]/([Cr]+[Fe])為0.05)時,針鐵礦發生還原溶解,固體中約8.46%的Cr釋放到環境中。
盡管重金屬取代鐵氧化物的異化鐵還原過程對重金屬的影響已引起廣泛關注和重視,但已有的研究仍集中在重金屬取代弱晶型的鐵氧化物(如Cr取代的聚合硫酸鐵和Cr取代施氏礦物)(Wan et al.,2018;Li et al.,2016),對重金屬取代的強晶型鐵氧化物的生物還原溶解過程中鐵物種和重金屬的環境行為、礦物結構變化等,仍缺乏系統性的研究。因此,本研究以土壤中常見的Cr(III)取代的針鐵礦(下文簡稱Cr取代針鐵礦,Cr-Goe)為研究對象,將不同 Cr取代比例的針鐵礦作為鐵還原菌的唯一電子受體,探究Cr取代針鐵礦的異化鐵過程中Fe、Cr以及礦物結構變化特征,為土壤環境中Cr的遷移轉化等行為提供理論依據。
1 材料與方法
1.1 針鐵礦及鉻取代針鐵礦的制備
針鐵礦和Cr取代針鐵礦的合成主要參考已有文獻報報道的方法(Schwertmann et al.,2000)。首先,將150 mL 5 mol·L-1的KOH溶液加入到250 mL 0.5 mol·L-1的 Cr(NO3)3溶液中在燒杯中混合均勻,制得堿性Cr溶液。分別量取0、3.3、8.4、8.4、30.5、75.3 mL上述配好的堿性Cr溶液,均依次加入 50 mL,1 mol·L-1Fe(NO3)3溶液和 5 mol·L-1KOH溶液(使得最終懸浮液中KOH的濃度為0.3 mol·L-1),最后加入超純水定容到1 L。混勻溶液,并在70 ℃下老化30 d。接著,將老化的混勻液取出離心去除上清液,保留固體,用 3 mol·L-1H2SO4,于50 ℃下浸提固體2 h,去除固體中的無定型雜質。同時,用超純水將固體樣品清洗5次,并在70℃烘箱中干燥過夜,最后用研缽研磨過篩,得到所需的不同Cr取代的針鐵礦,根據開始添加時[Cr]/([Cr]+[Fe])([Me]: mol·L-1)比例計算,其理論取代值分別為 0、2%,5%,16%和32%,并最終根據實際的Cr取代值,分別命名為Goe、1.4-Cr-Goe、3.5-Cr-Goe、9.03-Cr-Goe 以及10.3-Cr-Goe。
1.2 菌種來源和活化
本研究所采用的鐵還原菌為Shewanella oneidensisMR-1,ATCC70050。菌體購于北京百歐博偉生物技術有限公司。菌體在30 ℃的LB液體培養基(成分為 10 g·L-1蛋白胨,5 g·L-1酵母粉,10 g·L-1的 NaCl)中培養 16 h,于 4 ℃ 6000 r·min-1條件下離心10 min,用滅菌超純水洗滌重懸浮,重復3次,最終配成約1010cell·mL-1的菌懸液待用。
1.3 實驗設計
在本實驗開始前,對所有用到的實驗器具和溶液進行標準的高壓滅菌流程后在無菌超凈臺進行操作。在20.2 mL的西林瓶中依次加入哌嗪-1, 4-雙(2-乙烷磺酸)(PIPEs)緩沖溶液、乳酸鈉(電子供體)和鐵還原菌ShewanellaoneidensisMR-1,混勻之后,加入針鐵礦或不同Cr取代比例的針鐵礦,最終培養溶液的總體積為10 mL,各物種的終濃度分別為 0.02 g 針鐵礦,25 mmol·L-1(PIPEs)、10 mmol·L-1乳酸鈉以及約 108cell·mL-1的Shewanella oneidensisMR-1。實驗同時設置不添加鐵還原菌的對照處理(CK:滅菌針鐵礦+PIPEs+乳酸鈉)。為達到最優的鐵還原效果,本研究通過PIPES緩沖溶液將pH值控制在7.0左右。高純氮氣充氣30 min排氧,然后用橡膠塞壓緊,并用鋁蓋密封,置于厭氧培養箱中 (25±1) ℃靜置培養。反應進行到設定的時間點,在厭氧箱中取樣。首先取適量的樣品用同體積的0.4 mol·L-1HCl進行提取浸提90 min,取出在離心機中10000 r·min-1轉速下離心10 min,用針頭過濾器(0.22 μm)過濾上清液并收集,用于游離態物質含量分析(He et al.,2008),而固體繼續用同體積的濃HCl(約11.2 mol·L-1)進行溶解,待固體完全溶解之后進一步過濾收集液體,用于結構態物質含量分析(Hua et al.,2018)。上述兩種液體樣品進一步用于后續 Fe(II)和 Cr(III)物種的濃度分析。另取適量的樣品,進行固液分離,收集固體,用于后續礦物結構表征分析。
每個樣品設置3個重復,文中所示數據均為數據平均值。
1.4 測試與表征方法
游離態 Fe(II)物種的檢測采用鄰菲羅啉比色法,測試方法根據已有文獻(Tamura et al.,1974)報道進行改進,具體步驟如下:取1 mL上清液,先加入50 μL濃鹽酸進行酸化,依次加入50 μL 0.1 mol·L-1氟化銨,200 μL 1 g·L-1鄰菲羅啉和 200 μL 5 mol·L-1醋酸緩沖溶液,充分混勻之后顯色15 min,上機檢測。分析儀器為紫外可見分光光度計(TU-1800,北京普析通用)。游離態和結構態Cr(III)物種的檢測采用電感耦合等離子發射光譜儀(ICPOES,Perkin-Elmer optima 2000,USA)測定(Hua et al.,2018)。礦物的晶相結構分析,首先將礦物粉末壓片,在X’Pert Pro MPD X射線衍射儀上進行衍射分析(XRD)。測試要求條件:Ni濾波片,Bragg-Brentano幾何衍射,探測器為LynxBye陣列,Cu Ka(λ=0.154059 nm),管壓40 kV,管流40 mA,步長為 0.02°,掃描速度為 1°·min-1或步長為 0.04°,每步積分時間為10 s。
1.5 數據分析
采用微生物生長曲線Logistic方程擬合異化鐵還原過程(He et al.,2008)。所有數據采用Microsoft Office Excel 2010進行統計,SPSS 20.0進行方差分析,Origin 8.0進行做圖。
2 結果與討論
2.1 不同Cr取代針鐵礦的性質特征
為驗證合成不同Cr取代針鐵礦過程中,Cr(III)離子是否進入礦物的晶體結構中,及其 Cr的真實取代量,對合成得到的礦物進行化學分析測試。使用0.4 mol·L-1HCl將吸附在固相表面的洗掉,再用濃鹽酸完全溶解固體,測定固體中Cr濃度,并計算實際[Cr]/([Cr]+[Fe])比例(圖 1)。結果表明,不同Cr取代針鐵礦中 Cr的質量分數分別為 19.24、47.82、131.61 以及 152.15 mg·g-1,大部分 Cr離子進入到礦物結構中;同時計算 Cr取代的實際摩爾比例分別為1.4%,3.5%,9.03%以及10.3%,均小于理論計算值2%、5%、16%和32%。這是由于實驗合成針鐵礦的老化時間有限,Cr(III)離子不能全部進入固相中(Schwertmann et al.,1989)。
為驗證合成的礦物結構為針鐵礦,對礦物樣品進行了XRD結構分析(圖2)。通過與粉末衍射標準聯合委員會數據庫中針鐵礦的特征峰進行比較發現,本研究所合成的固體礦物均為針鐵礦;且隨著針鐵礦中越來越多的Fe(III)被Cr(III)取代,礦物XRD圖譜中主峰位置(2θ)向左偏移(2θ值越小),晶格參數和晶胞體積都比純針鐵礦小(Hua et al.,2018)。Sileo et al.(2004)研究表明,針鐵礦中Fe(III)周圍原先被兩個獨立的FeO3(OH)3配體所包圍,而當Fe(III)被Cr(III)取代之后,其周圍形成更加對稱的 Cr(OH0.5)6的多面體,從而縮小金屬離子之間的距離,進一步引起晶格和晶胞參數的變化。
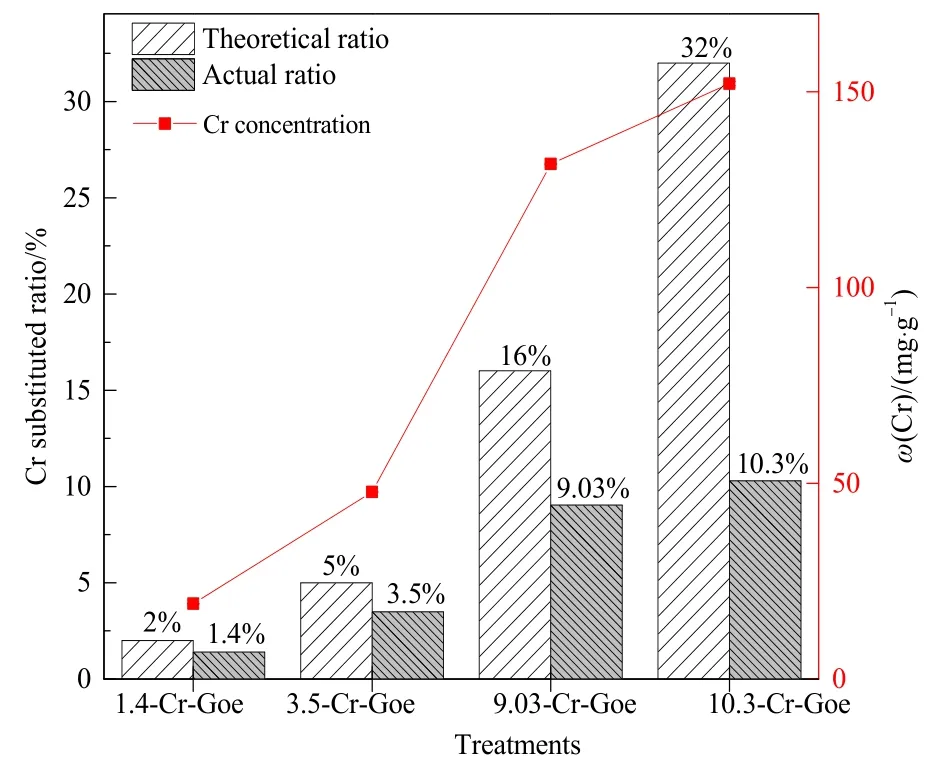
圖1 Cr取代針鐵礦的比例以及針鐵礦中Cr的含量Fig.1 The percentage of mol [Cr]/[Cr+Fe] and the concentration of Cr in the goethite
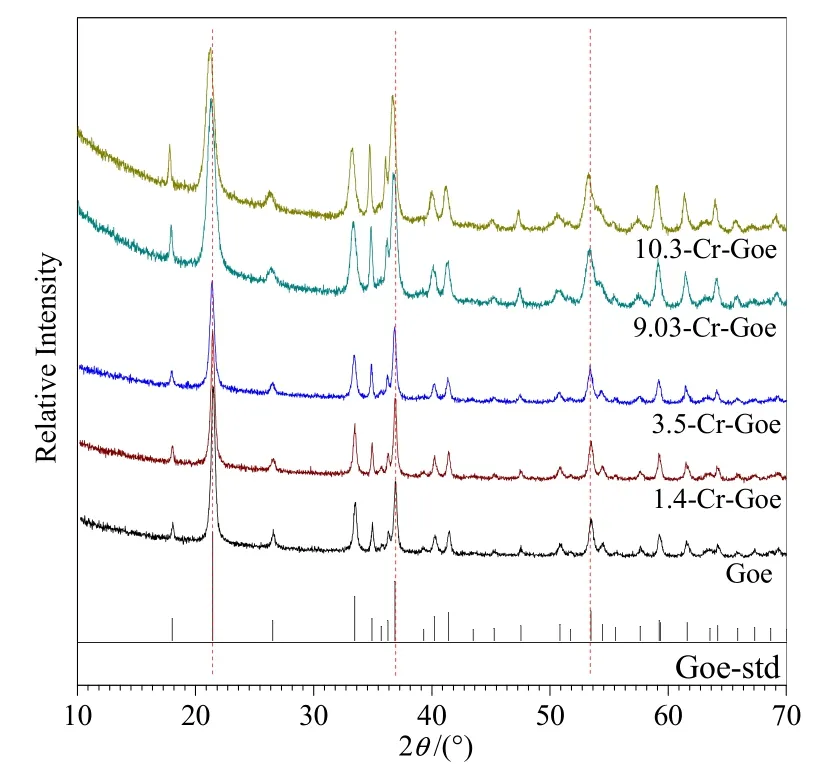
圖2 合成的針鐵礦及Cr取代針鐵礦XRD譜圖Fig.2 XRD patterns of the synthesized goethite and Cr substituted goethite
2.2 異化鐵還原動力學
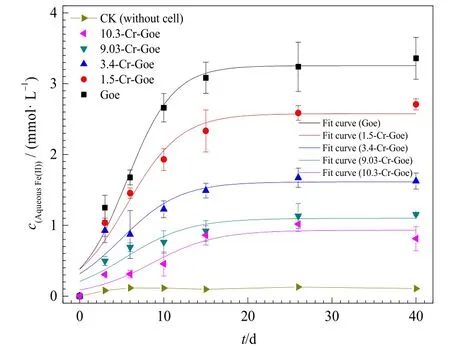
圖3 不同Cr取代針鐵礦的微生物鐵還原動力學及擬合曲線Fig.3 The rate of the total Fe(II) concentration profile for 5 Cr substituted goethite samples using logistic model fitting
體系中不同Cr取代針鐵礦的微生物還原動力學如圖3所示。不加菌的對照處理(CK)中,基本未檢測出Fe(II)的存在,說明沒有鐵還原菌Shewanella oneidensisMR-1作用時,針鐵礦未能發生還原溶解。在添加ShewanellaoneidensisMR-1(針鐵礦+菌)處理中,體系中游離態Fe(II)的含量在反應前15 d快速增長,隨后出現緩慢增加的趨勢。這可能是由于系統中的乳酸鈉電子供體被消耗,微生物未能持續快速生長(He et al.,2008;Liu et al.,2001)。在反應40 d 時,約 3.36 mmol·L-1的 Fe(III)被ShewanellaoneidensisMR-1 還原生成 Fe(II)。Liu et al.(2001)利用鐵還原菌Shewanellaputrefaciensstrain CN32還原針鐵礦發現,在10 mol·L-1乳酸作為電子供體的情況下,反應26 d之后,約11%的針鐵礦被還原,生成約 3.8 mol·L-1的 Fe(II)。與之相比,本研究中ShewanellaoneidensisMR-1鐵還原菌對針鐵礦具有相類似的還原能力。而隨著針鐵礦中的 Fe(III)被Cr(III)取代,游離態Fe(II)量受到限制,但不同處理異化鐵還原動力學仍呈現先快速增長后平緩趨勢(圖3)。在反應40 d之后,1.5%、3.4%、9.03%以及10.3% Cr取代的針鐵礦中分別僅有2.71、1.63、1.15和 0.81 mmol·L-1游離態 Fe(II)生成,說明鐵還原菌ShewanellaoneidensisMR-1具有還原Cr取代針鐵礦的能力,且鐵還原效率呈現 Goe>1.5-Cr-Goe>3.4-Cr-Goe>9.03-Cr-Goe>10.3-Cr-Goe的規律。
2.3 異化鐵還原過程中Cr的環境行為
為探究不同 Cr取代針鐵礦異化鐵還原過程中Cr(III)的賦存狀態,本研究同時測定反應過程中游離態和殘渣態Cr(III)濃度變化(圖4)。由于研究體系的pH值為7.0,在此條件下,Cr(III)未能以溶解態形態存在(Beverskog and Puigdomenech,1997)。結果表明,在反應的前15 d,1.5-Cr-Goe、3.4-Cr-Goe、9.03-Cr-Goe和 10.3-Cr-Goe反應體系中,游離態Cr(III)的濃度呈快速上升的趨勢,分別可達到1.22、2.28、21.20以及30.42 mg·g-1(圖4a);隨后趨向相對穩定,并逐漸下降;最終反應體系中分別有2.49%、3.10%、12.97%和13.69%的Cr(III)被釋放到環境中。這表明了在不同 Cr取代針鐵礦的異化鐵還原過程中,Cr(III)會隨著 Fe(III)還原溶解而從礦物結構中釋放。然而,不同Cr取代針鐵礦異化鐵還原過程中殘渣態Cr(III)的濃度呈現相反動力學趨勢(圖4b)。在反應的前15 d,殘渣態Cr(III)的濃度快速降低,隨后趨向相對穩定,并逐漸上升趨勢。前人研究指出,金屬取代的鐵氧化物在鐵還原菌作用下,礦物會發生還原溶解從而釋放出重金屬離子(Bousserrhine et al.,1999;Li et al.,2016);同時,在礦物進一步二次成礦過程中,游離態的重金屬會再次被固定到礦物當中(Burton et al.,2019;Li et al.,2016)。近些年研究也表明,游離態Fe(II)可催化鐵氧化物晶相重組,鐵氧化物晶體結構中取代的重金屬可隨礦物的晶相重組過程釋放到環境中,形成游離態重金屬。同時,游離態重金屬離子(如Cd、Al、As、Cr等)在礦物晶相重組過程中,可通過化學鍵形式吸附固定或者是重金屬取代新生成鐵氧化物結構中的部分Fe(III)位,被穩定/固定在新生成的礦物結構中(Hua et al.,2018;Liu et al.,2019;劉亞楠等,2018)。而在本研究當中,以10.3-Cr-Goe體系為例,可發現游離態Cr(III)質量分數從0增加到20.84 mg·g-1;而固體中(結構態)Cr(III)的質量分數則從 149.34 mg·g-1降低到 124.55 mg·g-1。其他體系與之類似,其游離態 Cr(III)與結構態Cr(III)濃度變化動力學呈現相反規律,且二者之和呈現穩定不變的趨勢(圖4c),即游離態Cr(III)增加或減少的量約等于結構態中(III)減少或增加的量。由此可推測,Shewanella oneidensisMR-1還原不同Cr取代針鐵礦過程中,結構態Cr(III)逐漸從針鐵礦結構中釋放,吸附在針鐵礦表面,形成游離態Cr(III);隨著異化鐵還原的進行,游離態Fe(II)可催化針鐵礦二次成礦,而釋放出來的Cr(III)部分可被重新固定在針鐵礦結構中。
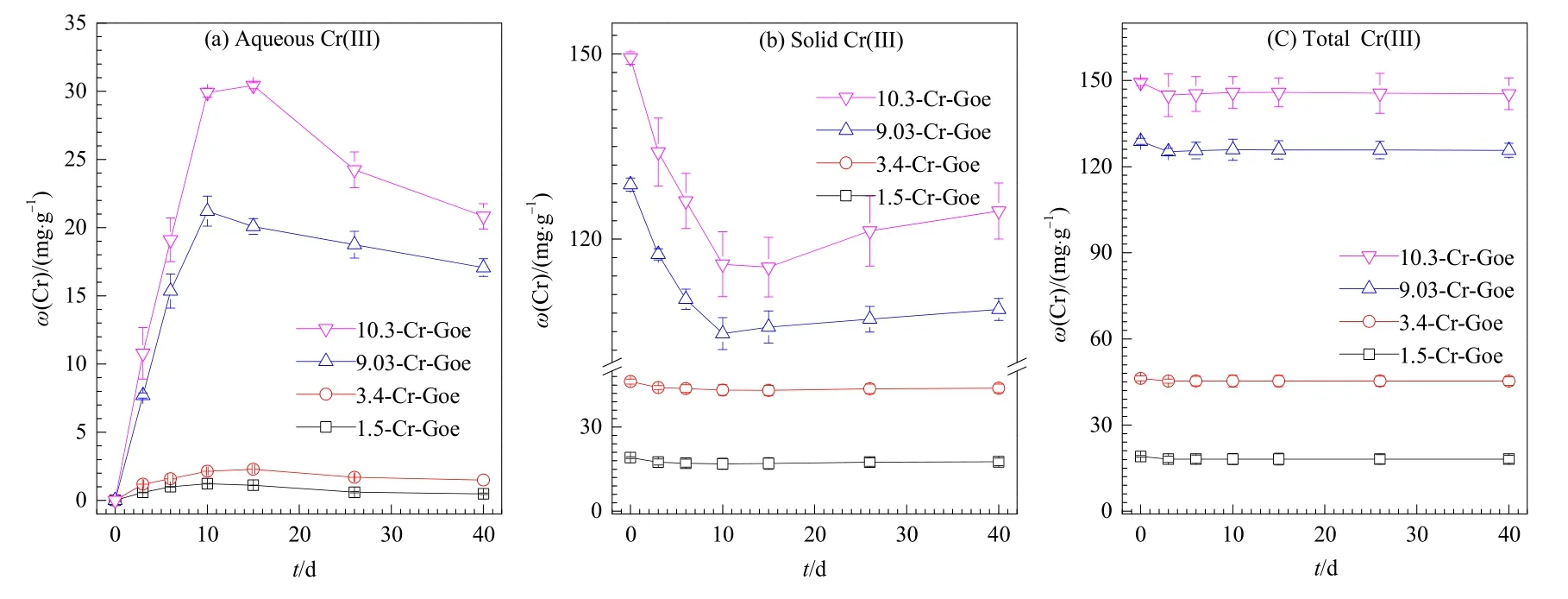
圖4 不同Cr 取代針鐵礦異化鐵還原過程中游離態、結構態和總Cr(III)濃度變化動力學Fig.4 The concentrations of (a) extracted, (b) solid, and (c) total Cr(III) during microbial reduction of 0.02 Cr-goethite, 0.05 Cr-goethite,0.16 Cr-goethite, and 0.32 Cr-goethite over 40 d
2.4 礦物結構變化
為考察不同 Cr取代針鐵礦異化鐵還原過程中礦物結構的變化,本研究采用 XRD對不同反應時間下(10 d和40 d)礦物的結構進行表征(圖5)。由圖可知,反應中期(10 d)和反應后期(40 d),Goe、1.5-Cr-Goe、3.4-Cr-Goe、9.03-Cr-Goe和10.3-Cr-Goe反應體系中,礦物的XRD圖譜中衍射峰均為針鐵礦的特征衍射峰,具有較高的結晶度;同時,并未觀察到新的礦物特征衍射峰出現。Liu et al.(2001)研究表明,針鐵礦在鐵還原菌Shewanella putrefaciensstrain CN32作用下可二次成礦生成菱鐵礦(FeCO3)和針鐵礦。游離態Fe(II)催化針鐵礦晶相重組過程,針鐵礦晶相重組新生成的礦物仍為針鐵礦(Handler et al.,2009;Hua et al.,2018)。由此可推測,本研究中不同 Cr取代針鐵礦在鐵還原菌Shewanella oneidensisMR-1作用下可能發生二次成礦,新生成的礦物仍為針鐵礦。
2.5 Cr取代量對針鐵礦穩定性影響
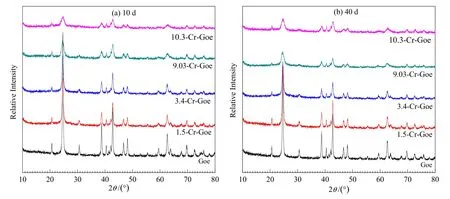
圖5 不同Cr取代針鐵礦異化鐵還原過程中礦物結構XRD圖譜Fig.5 XRD patterns of the Cr substituted goethite during microbial reduction
前人研究表明,土壤的微生物鐵還原過程符合微生物生長曲線,常采用 Logistic方程(Nt=a/(1+be-kt))進行模擬,以便更準備計算異化鐵還原速率等信息(Chen et al.,2014;He et al.,2008)。本研究采用 Logistic方程對鐵還原菌Shewanella oneidensisMR-1還原不同Cr取代針鐵礦過程進行擬合分析(圖3),其中a代表游離態Fe(II)的最大生成量,b是一個擬合參數,k是異化鐵還原速率,Nt代表體系中t時刻體系中游離態Fe(II)的含量。擬合數據表明,Goe、1.5-Cr-Goe、3.4-Cr-Goe、9.03-Cr-Goe和10.3-Cr-Goe反應體系中異化鐵還原速率k分別為 0.3596、0.3135、0.2866、0.2638以及0.2637 d-1(圖6)。與無Cr取代針鐵礦相比較,Cr取代針鐵礦的鐵還原速率顯著降低(P<0.05),其生物穩定性提高。對鐵還原速率與 Cr的取代量進一步統計分析發現,不同 Cr取代針鐵礦的異化鐵還原速率與 Cr的摩爾取代量呈指數關系(R2=0.9995,P<0.001)(圖 6)。Sileo et al.(2004)對人工合成的 Cr取代針鐵礦進行熱力學性質分析發現,隨著Cr取代量的增加,礦物會形成更加穩定的團聚體,使得針鐵礦的結構更加穩定,難以向赤鐵礦轉化。Wan et al.(2018)利用Shewanella oneidensisMR-1對Cr(VI)-施氏礦物進行還原表明,礦物中附載的Cr(VI)量增高時,施氏礦物表面由原本的粗糙云狀變成刺猬狀,顆粒團聚變大,從而提高了礦物的生物穩定性。由此推測,在本研究中,隨著Fe(III)被Cr(III)取代,針鐵礦的結構越來越穩定,其生物穩定性也大大提高。當Cr(III)離子的取代量達到9.03%時,微生物還原Cr取代針鐵礦生成Fe(II)的速率趨向穩定,可達0.26 d-1。在不同Cr取代針鐵礦異化鐵還原過程中,隨著 Cr取代量的增加,礦物生物穩定性更高,釋放到環境中Cr(III)的濃度將會達到一個最大平衡值。
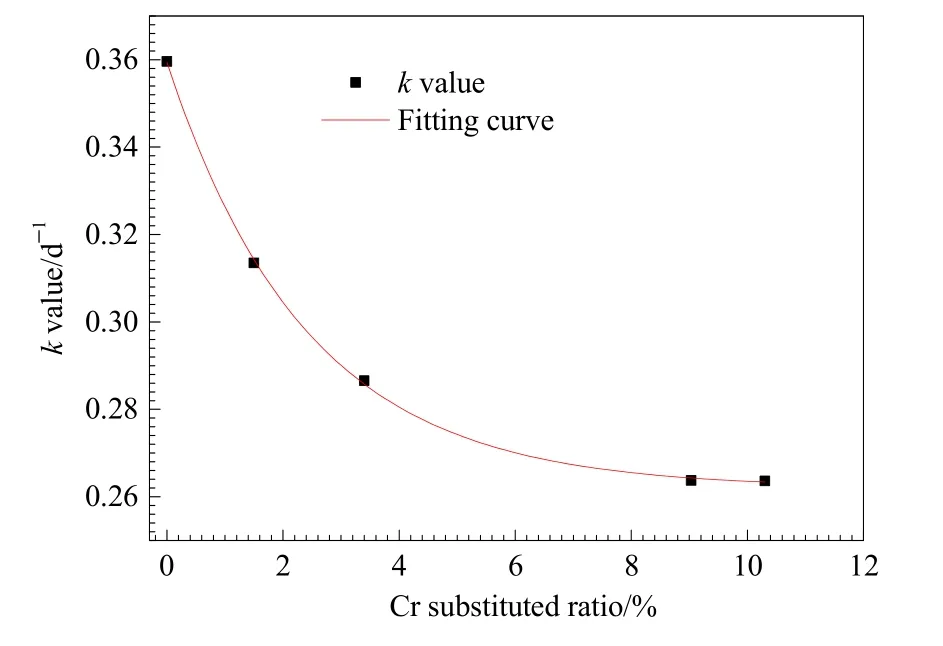
圖6 鐵還原速率與針鐵礦中Cr取代量的關系Fig.6 The relation between iron reduction rate and the mol ratio of Cr substituted in goethite
3 結論
本研究以不同 Cr取代針鐵礦為電子受體,以乳酸鈉為電子供體,研究鐵還原菌Shewanella oneidensisMR-1對不同Cr取代針鐵礦的還原作用及過程中Cr(III)的釋放固定行為,實驗結果表明,ShewanellaoneidensisMR-1對純針鐵礦或Cr取代針鐵礦菌均具有還原能力,且隨著針鐵礦中Cr(III)的取代量增加,還原作用效果越來越弱。在反應時間內,不同Cr取代針鐵礦反應體系中,游離態Fe(II)含量呈快速增長后平穩的趨勢,且鐵還原速率k的大小順序為 Goe>1.5-Cr-Goe>3.4-Cr-Goe>9.03-Cr-Goe>10.3-Cr-Goe。同時,游離態Cr(III)的含量則呈快速增長后降低的趨勢;殘渣態中Cr(III)的含量則與游離態 Cr(III)呈相反規律,說明不同 Cr取代針鐵礦異化鐵還原過程中,礦物結構中的Cr(III)可被釋放并重新固定到礦物中。

