短肽型腸內(nèi)營(yíng)養(yǎng)制劑對(duì)胃癌根治術(shù)后患者胃腸功能及營(yíng)養(yǎng)狀態(tài)的改善作用研究
田俊梅,趙永飛,郅文娟
(鄭州大學(xué)附屬洛陽(yáng)中心醫(yī)院,洛陽(yáng) 471000)
胃癌為消化系統(tǒng)常見(jiàn)的惡性腫瘤,已成為國(guó)內(nèi)發(fā)病率第二高的惡性腫瘤,發(fā)病率與病死率均較高。因該病早期癥狀隱匿,患者就診時(shí)多為進(jìn)展期,對(duì)于具有手術(shù)指征的患者施行根治術(shù)仍是目前的首選治療方案[1-2]。胃癌根治術(shù)涉及消化道的重建,可能對(duì)患者造成大面積創(chuàng)傷,提升基礎(chǔ)代謝率;加之患者術(shù)后需長(zhǎng)時(shí)間禁食,營(yíng)養(yǎng)不良的發(fā)生率增加,營(yíng)養(yǎng)支持可為患者提供營(yíng)養(yǎng)底物,從而改善機(jī)體代謝狀態(tài),以促進(jìn)機(jī)體的功能恢復(fù)[3]。胃癌術(shù)后早期腸內(nèi)營(yíng)養(yǎng)支持更符合人體的正常生理,有利于機(jī)體生理功能恢復(fù);同時(shí),腸內(nèi)營(yíng)養(yǎng)還有助于維持腸黏膜細(xì)胞結(jié)構(gòu)與功能的穩(wěn)定,防止腸道菌群易位而加速患者恢復(fù)[4]。目前,腸內(nèi)營(yíng)養(yǎng)制劑種類較多,不同劑型的應(yīng)用效果可能有較大差異。短肽型腸內(nèi)營(yíng)養(yǎng)制劑與整蛋白型腸內(nèi)營(yíng)養(yǎng)制劑均為臨床上常用的腸內(nèi)營(yíng)養(yǎng)制劑,關(guān)于兩種營(yíng)養(yǎng)制劑對(duì)胃癌根治術(shù)后患者療效均有報(bào)道,但關(guān)于兩種劑型對(duì)患者胃腸功能指標(biāo)影響方面的報(bào)道不多。本研究對(duì)此進(jìn)行了比較,現(xiàn)報(bào)道如下。
1 資料與方法
1.1 一般資料
選擇2018年1月~2020年1月在本院行胃癌根治術(shù)的患者184例進(jìn)行研究。納入標(biāo)準(zhǔn):① 經(jīng)病理學(xué)確診為胃癌者。② 術(shù)前未進(jìn)行放化療者。③ 在術(shù)前2周無(wú)白蛋白及免疫增強(qiáng)劑使用史者。④ 智力正常,可配合進(jìn)行相關(guān)治療者。⑤ 已簽署知情同意書(shū)者。排除標(biāo)準(zhǔn):① 有明確的腸內(nèi)營(yíng)養(yǎng)禁忌癥者。② 長(zhǎng)期貧血或代謝性疾病者。③ 肝腎功能異常者。④ 妊娠期及哺乳期婦女。
采用隨機(jī)數(shù)字表法將患者分為2組,每組92例。對(duì)照組:男48例,女44例;年齡32~72歲,平均(57.19±6.08)歲;遠(yuǎn)端胃切除33例,近端胃切除39例,全胃切除20例;病理分期Ⅰ期34例,Ⅱ期31例,Ⅲ期27例。觀察組:男41例,女51例;年齡31~74歲,平均(57.80±6.11)歲;遠(yuǎn)端胃切除31例,近端胃切除36例,全胃切除25例;病理分期Ⅰ期34例,Ⅱ期30例,Ⅲ期28例。兩組患者一般資料差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。
1.2 治療方法
兩組患者均在手術(shù)重建消化道時(shí)由吻合口將鼻飼管送至空腸距離吻合口約30 cm處,術(shù)后給予腸內(nèi)營(yíng)養(yǎng)制劑輸注,對(duì)照組給予整蛋白型腸內(nèi)營(yíng)養(yǎng)劑(粉劑,商品名:能全素,德國(guó)Milupa GmbH,注冊(cè)證號(hào):H20170172,規(guī)格:320 g/聽(tīng)),稀釋方法:在潔凈容器中注入500 ml溫開(kāi)水后加入本品320 g,待粉劑完全溶解后加溫開(kāi)水稀釋至1500 ml,混勻備用。觀察組則給予短肽型腸內(nèi)營(yíng)養(yǎng)制劑(粉劑,商品名:百普素,德國(guó)Milupa GmbH,注冊(cè)證號(hào):H20170170,規(guī)格:125 g/袋),稀釋方法:在潔凈容器中注入50 ml溫開(kāi)水,加入本品180 g,待粉劑完全溶解后加溫開(kāi)水稀釋至800 ml,混勻備用。兩組患者在術(shù)后首日均給予0.9%氯化鈉溶液鼻飼管緩慢滴入,若無(wú)明顯的腹脹、腹痛等表現(xiàn)則在術(shù)后d 2開(kāi)始進(jìn)行腸內(nèi)營(yíng)養(yǎng)支持。將腸內(nèi)營(yíng)養(yǎng)液溫度控制在37~39 ℃,術(shù)后d 2腸內(nèi)營(yíng)養(yǎng)制劑量為500 ml,速度控制在10~20 ml/h;d 3 則將劑量增加至1000 ml,速度控制在50 ml/h以內(nèi);d 4劑量增加至1500 ml,速度控制在120 ml/h以內(nèi),直至術(shù)后d 8;術(shù)后前3天能量不足者由腸外營(yíng)養(yǎng)補(bǔ)充。
1.3 評(píng)價(jià)指標(biāo)
比較兩組患者胃腸功能、營(yíng)養(yǎng)狀態(tài)及不良反應(yīng)。① 胃腸功能、營(yíng)養(yǎng)狀態(tài):在營(yíng)養(yǎng)支持前及營(yíng)養(yǎng)支持8天后抽取患者空腹外周靜脈血5 ml,以3000 r/min轉(zhuǎn)速離心5 min后采用酶聯(lián)免疫吸附法對(duì)患者胃腸功能指標(biāo)(胃動(dòng)素、胃泌素)及營(yíng)養(yǎng)狀態(tài)指標(biāo)[總蛋白(TP)、運(yùn)鐵蛋白(TFN)、白蛋白(ALB)]進(jìn)行檢測(cè)。② 記錄兩組患者治療期間不良反應(yīng)發(fā)生情況。
1.4 統(tǒng)計(jì)學(xué)方法

2 結(jié)果
2.1 兩組患者胃腸功能指標(biāo)比較
治療后,兩組患者胃動(dòng)素、胃泌素水平均明顯升高,且觀察組高于對(duì)照組(P<0.05),見(jiàn)表1。

表1 兩組患者胃腸功能指標(biāo)比較
2.2 兩組患者營(yíng)養(yǎng)狀態(tài)指標(biāo)比較
治療后,兩組患者TP、TFN及ALB水平均升高,見(jiàn)表2。
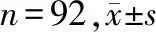
表2 兩組患者營(yíng)養(yǎng)狀態(tài)表比較
2.3 兩組患者不良反應(yīng)發(fā)生情況比較
對(duì)照組不良反應(yīng)總發(fā)生率為31.52%,高于觀察組(14.13%,P<0.05),見(jiàn)表3。

表3 兩組患者不良反應(yīng)發(fā)生情況比較n=92,n(%)
3 討論
胃癌患者為營(yíng)養(yǎng)不良的高危人群,腫瘤本身可造成機(jī)體營(yíng)養(yǎng)物質(zhì)消耗及代謝水平升高,還可對(duì)機(jī)體的消化與吸收功能造成影響,加重營(yíng)養(yǎng)不良[5]。同時(shí),惡性腫瘤細(xì)胞還可釋放出多種毒素,導(dǎo)致機(jī)體出現(xiàn)消瘦、無(wú)力、食欲不振等表現(xiàn)。對(duì)于行根治術(shù)治療的患者而言,術(shù)后無(wú)法正常進(jìn)食更增加了患者營(yíng)養(yǎng)不良的發(fā)生概率[6-7]。因此,有必要通過(guò)營(yíng)養(yǎng)支持以最大限度滿足患者的營(yíng)養(yǎng)所需,并促進(jìn)機(jī)體功能的恢復(fù)。
早期腸內(nèi)營(yíng)養(yǎng)支持是近年來(lái)較為推崇的營(yíng)養(yǎng)支持方式,符合當(dāng)前較流行的快速康復(fù)理念,早期腸內(nèi)營(yíng)養(yǎng)支持可有效降低高分解代謝而促進(jìn)患者康復(fù)。接受胃腸道手術(shù)的患者,可因麻醉及手術(shù)應(yīng)激等原因?qū)е鲁霈F(xiàn)不同程度的胃腸功能癱瘓。因此,對(duì)于此類患者的治療,盡快恢復(fù)患者胃腸道功能是關(guān)鍵[8]。胃癌根治術(shù)后胃腸道功能癱瘓的發(fā)生機(jī)制尚未完全明確,目前認(rèn)為可能與手術(shù)過(guò)程對(duì)患者胃腸神經(jīng)及迷走神經(jīng)造成損傷,胃腸道激素分泌失調(diào)、心理因素及微血管病變等多方面的因素有關(guān)[9]。其中,以胃動(dòng)素、胃泌素為主的胃腸激素分泌異常在胃癌根治術(shù)后胃腸功能癱瘓中的作用日益受到重視。胃動(dòng)素由十二指腸近端空腸黏膜合成及分泌,該激素可提高細(xì)胞內(nèi)鈣離子水平并加快胃腸道蠕動(dòng),從而加速胃腸道排空。胃泌素則主要由胃竇及小腸上部細(xì)胞合成與分泌,胃泌素除可增加胃酸分泌外,對(duì)胃的運(yùn)動(dòng)同樣具有中等程度的刺激,同時(shí)還可提高幽門(mén)泵的活動(dòng)[10]。本研究結(jié)果顯示:治療后兩組患者胃動(dòng)素、胃泌素水平均明顯升高,且觀察組高于對(duì)照組(P<0.05),提示短肽型腸內(nèi)營(yíng)養(yǎng)制劑可有效提高胃腸激素的分泌。胃癌根治術(shù)后患者常可出現(xiàn)低蛋白血癥,血漿蛋白是維持機(jī)體滲透壓的主要成分,但胃癌患者術(shù)后血漿內(nèi)蛋白含量遠(yuǎn)低于正常水平,導(dǎo)致細(xì)胞內(nèi)外滲透壓差過(guò)大而出現(xiàn)腸黏膜水腫,致小腸絨毛吸收能力下降從而影響營(yíng)養(yǎng)物質(zhì)的運(yùn)輸。既往認(rèn)為,蛋白質(zhì)被分解成氨基酸后才可被機(jī)體吸收,但近年來(lái)越來(lái)越多的研究證實(shí)蛋白質(zhì)分解過(guò)程的中間產(chǎn)物同樣可被人體吸收[11-13]。短肽型腸內(nèi)營(yíng)養(yǎng)制劑營(yíng)養(yǎng)成分是經(jīng)水解處理的預(yù)消化型營(yíng)養(yǎng)制劑,其氮源為乳清蛋白水解物(短肽)。短肽除分解為氨基酸而被人體所吸收外,其自身也可被吸收,可有效提高患者對(duì)營(yíng)養(yǎng)物質(zhì)的吸收,為胃腸道激素的分泌提供更多的能量及底物,提高機(jī)體胃動(dòng)素及胃泌素水平。腸內(nèi)營(yíng)養(yǎng)支持的根本目的在于改善患者營(yíng)養(yǎng)狀況,本研究選取TP、TFN和ALB水平作為評(píng)估患者營(yíng)養(yǎng)狀況的指標(biāo),本研究結(jié)果顯示:治療后兩組患者TP、TFN和ALB水平均明顯升高,但觀察組升高幅度更大(P<0.05),可能因短肽型腸內(nèi)營(yíng)養(yǎng)制劑更容易被機(jī)體吸收,從而使患者營(yíng)養(yǎng)狀況指標(biāo)迅速改善。不良反應(yīng)方面:對(duì)照組不良反應(yīng)總發(fā)生率為31.52%,高于對(duì)照組(14.13%,P<0.05),可能因整蛋白型營(yíng)養(yǎng)制劑含有膳食纖維,此類物質(zhì)無(wú)法在小腸吸收,但可通過(guò)大腸部分發(fā)酵為可食用的植物性成分、碳水化合物等。對(duì)于胃癌等消化功能薄弱者,膳食纖維經(jīng)細(xì)菌分解產(chǎn)生大量氣體,而胃腸道蠕動(dòng)功能尚未完全恢復(fù),因而可導(dǎo)致患者出現(xiàn)腹脹[14]。與整蛋白型相比,短肽型腸內(nèi)營(yíng)養(yǎng)制劑所含脂肪含量明顯更低,使用后導(dǎo)致患者脂肪瀉的概率更低[15]。
綜上所述,短肽型腸內(nèi)營(yíng)養(yǎng)制劑對(duì)胃癌根治術(shù)后患者胃腸功能及營(yíng)養(yǎng)狀態(tài)的改善效果優(yōu)于整蛋白型腸內(nèi)營(yíng)養(yǎng)制劑,且短肽型腸內(nèi)營(yíng)養(yǎng)制劑還可有效降低術(shù)后不良反應(yīng)發(fā)生率。

