Ⅱ型胸部神經阻滯對乳腺癌改良根治術患者圍術期應激反應的影響
許奎斌 張霄蓓 舒瑞辰 周鵬 趙洪偉 王凱元
全身麻醉是乳腺癌手術的主要麻醉方式,但手術、麻醉等強烈刺激不可避免地激活機體神經內分泌系統,誘發應激反應[1]。如何對圍術期炎性反應進行早期干預,減少術后慢性疼痛的發生,改善患者術后恢復,是臨床麻醉研究的熱點領域。研究顯示,區域麻醉鎮痛可通過阻滯傳入神經信號傳遞,阻止有害信息傳入到達中樞神經系統,從而減輕應激反應發生的程度[2]。
目前,臨床上多采用胸椎旁神經阻滯或者高位硬膜外阻滯鎮痛來抑制圍術期應激反應[3]。但上述操作可能導致患者氣出現血氣胸、高位脊髓損傷等風險,限制了其廣泛應用。Ⅱ型胸部神經(pectoral nerves Ⅱ,PECSⅡ)阻滯是一種新型的胸部神經阻滯方法,由于其操作創傷小、并發癥等風險低,且能有效減少阿片類藥物用量,利于患者恢復,已初步應用于圍術期鎮痛[4]。但PECSⅡ阻滯是否可抑制圍術期炎性細胞因子釋放,降低機體應激反應尚不明確。本研究旨在對乳腺癌改良根治術患者進行全身麻醉復合PECSⅡ阻滯與單純全身麻醉比較,探討其對圍術期應激反應的影響。
1 材料與方法
1.1 一般資料
選擇2018年1月至2019年5月于天津醫科大學腫瘤醫院擇期行乳腺癌改良根治術患者60例,隨機分成全身麻醉組(G組)和全身麻醉復合PECSⅡ阻滯組(P組),每組各30 例。所有患者采用美國麻醉醫師協會(American society of anesthesiologists,ASA)分級為Ⅰ~Ⅱ級,年齡39~62歲,體質量指數(body mass index,BMI)為18.1~22.5。排除標準:局麻藥過敏史、心肺功能障礙、肝腎功能異常、凝血功能異常、術前新輔助化療或放療、穿刺點皮膚感染等外周神經阻滯禁忌癥等。剔除標準:術后出血、肺感染等嚴重并發癥,患者拒絕接受疼痛評估。本研究經天津醫科大學腫瘤醫院倫理委員會批準(批號:bc2017022),患者均簽署知情同意書。
1.2 方法
1.2.1 穿刺步驟 患者入手術室后,監測心電圖、血壓、脈搏血氧飽和度、腦電雙頻指數(bispectral index,BIS)、體溫,開通靜脈通路,輸入乳酸鈉格林氏液。麻醉誘導:咪達唑侖0.03 mg/kg,芬太尼3 μg/kg,依托咪脂0.3 mg/kg,羅庫溴銨0.6 mg/kg。喉罩通氣,采用容量控制性通氣,潮氣量8×10 mL/kg,呼吸頻率定為12 次/min,維持二氧化碳分壓30×40 mmHg。P組患者在麻醉誘導后在超聲引導下行PECSⅡ阻滯,患者取仰臥位,手臂外展,將超聲探頭放于鎖骨外三分之一處,找到位于其下側的腋動脈和腋靜脈,然后橫向移動定位到胸大肌和胸小肌。在探頭平面,從近端內側向遠端外側斜刺入22G 外周神經叢穿刺針(德國Braun公司),當針尖到達胸大肌和胸小肌平面時,回抽無血后,注射0.5%羅哌卡因10 mL;然后將超聲探頭由第一肋移到第三肋,定位到胸小肌和前鋸肌,從探頭內側進針,局部浸潤麻醉后,繼續進針,使針尖到達胸小肌和前鋸肌之間,回抽無血后,注射0.5%羅哌卡因20 mL,拔出穿刺針,超聲下確定穿刺側有無血氣胸。密切觀察患者心率、血壓變化及外周神經阻滯相關并發癥,如過敏、局麻藥物的不良反應等,及時給予對癥處理。
1.2.2 麻醉維持 靶控輸注丙泊酚和瑞芬太尼,維持BIS 在45~55。圍術期低血壓(收縮壓<80 mmHg或平均動脈壓<60 mmHg)時使用適量麻黃堿糾正,高血壓(收縮壓>180 mmHg 或舒張壓>100 mmHg)注射適量烏拉地爾糾正。合并心動過速(心率>100次/min和/或心率的變化>20%基礎值)時注射艾司洛爾處理,心動過緩(心率<50次/min和/或心率的變化>20%基礎值)注射適量阿托品治療。術畢自主呼吸恢復、意識清醒、肌松藥代謝完全后拔出喉罩后轉入術后加強病房(postoperative intensive care unit,PICU)。在PICU 采用視覺模擬評分(visual analog scale,VAS)評估患者術后疼痛程度,記錄患者轉入PICU即刻、術后2、6和12 h的VAS評分,如果VAS>4分給與靜脈嗎啡滴定治療除痛。分別于麻醉誘導前(T0)、手術結束時(T1)、術后24 h(T2)、術后48 h(T3)取患者靜脈血3 mL,ELISA 法測定血清皮質醇(cortisol,Cor)、白細胞介素(interleukin,IL)-6、IL-10 及腫瘤壞死因子(tumor necrosis factor,TNF-α)水平。
1.3 統計學分析
采用SPSS 13.0軟件進行統計分析。為檢測兩組血清Cor濃度30%的區別,按照P組∶G組比例1∶1,設定檢驗功效0.8,α為0.05,計算得出兩組至少需要25例患者。計量資料采用±s表示,采用Shapiro-Wilk法進行正態分布檢驗。組間比較采用Student′st檢驗或Mann-Whitney U 檢驗;多時間點兩組比較采用雙因素重復測量的方差分析,兩兩比較采用Bonferroni法。P<0.05為差異具有統計學意義。
2 結果
2.1 一般資料比較
60例患者中,因3例拒絕接受術后評估或術后出血共57例入組。P組29例患者的ASA分級中Ⅰ級20例、Ⅱ級9例,腫瘤TNM分期中Ⅰ期21例、Ⅱ期8例;G組28例患者的ASA分級中Ⅰ級19例、Ⅱ級9例,腫瘤TNM分期中Ⅰ期22例、Ⅱ期6例。兩組患者的年齡、ASA、體質量、BMI、手術時間、腫瘤TNM分期、術中補液量、失血量及尿量均無顯著性差異(P>0.05,表1)。
表1 一般資料比較 (±s)
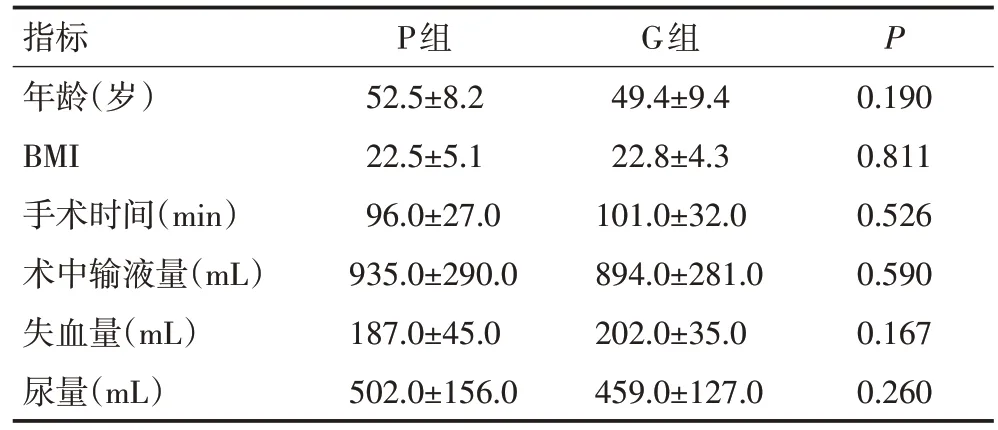
表1 一般資料比較 (±s)
指標年齡(歲)BMI手術時間(min)術中輸液量(mL)失血量(mL)尿量(mL)P組52.5±8.2 22.5±5.1 96.0±27.0 935.0±290.0 187.0±45.0 502.0±156.0 G組49.4±9.4 22.8±4.3 101.0±32.0 894.0±281.0 202.0±35.0 459.0±127.0 P 0.190 0.811 0.526 0.590 0.167 0.260
2.2 血清Cor水平比較
麻醉誘導前兩組患者血清Cor 濃度相比無顯著性差異(P>0.05);與麻醉誘導前相比手術結束時兩組患者血清Cor 濃度均顯著性升高(P<0.05);兩組患者術后24、48 h的血清Cor濃度逐漸下降至麻醉誘導前水平,手術結束時,與G組相比P組患者的血清Cor濃度降低(P<0.05,表2)。
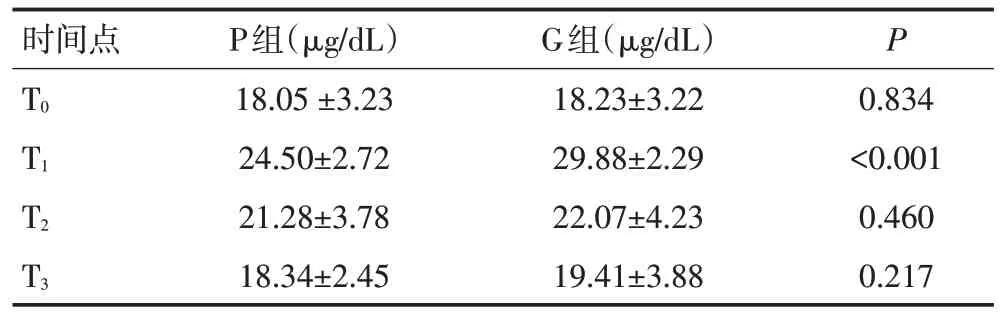
表2 兩組患者各時間點血清Cor濃度的比較
2.3 血清炎性因子變化
麻醉誘導前兩組患者血清IL-6、IL-10、TNF-α濃度相比無顯著性差異(P>0.05);與麻醉誘導前相比,手術結束時和術后24 h 兩組患者血清IL-6、IL-10、TNF-α 濃度升高(P<0.05)、術后48 h 無顯著性差異(P>0.05);在手術結束和術后24 h,與G 組相比P組患者血清IL-6、IL-10、TNF-α濃度均顯著降低(P<0.05,表3)。

表3 兩組患者各時間點IL-6、IL-10、TNF-α的比較
2.4 VAS評分比較
P 組患者進入PICU 即刻、術后2 h 及術后6 h 的VAS評分明顯低于G組(P<0.05),兩組患者術后12 h的VAS 評分進行比較差異無統計學意義(P>0.05,表4)。

表4 兩組患者各時間點VAS比較
3 討論
本研究發現,全身麻醉復合PECSⅡ阻滯可顯著降低乳腺癌改良根治術患者圍術期的應激反應。圍術期應激反應是嚴重影響乳腺癌患者術后恢復的重要因素。疼痛、手術及麻醉等因素可激活機體神經內分泌系統,導致血中應激激素(如兒茶酚胺、Cor等)和炎性細胞因子(TNF-α、IL-6、IL-10)大量釋放,引起心肌做功及耗氧量增加,易誘發心肌缺血及惡性心律失常。應激激素如Cor 水平增高還可引起腎臟、腸道以及肝臟等器官的缺血缺氧性損害,使機體呈高凝狀態,增加血栓栓塞風險[5]。TNF-α 與IL-6為經典的促炎因子,與受體結合后可直接或間接激活與乳腺癌生存相關的多條細胞信號通路,在腫瘤的增殖、遷移、侵襲和血管生成中起關鍵性作用[6]。同時,TNF-α、IL-6也是腫瘤微環境及神經系統中常見的致痛因子,可與神經元細胞中相應受體結合,傳遞疼痛信號并參與痛覺過敏及慢性疼痛的發生和發展[7-8]。IL-10為體內主要的抗炎細胞因子,但研究表明IL-10 可增強肺腺癌細胞的侵襲性,并通過PD-1/PD-L1通路抵消IFN-γ的抗瘤作用,從而減弱免疫治療的效果[9]。
PECSⅡ阻滯是一種改良的胸部神經阻滯法[10-11],在胸大肌與胸小肌之間筋膜層平面注入一定量的局麻藥物,阻滯第2~6肋間神經外側皮支、肋間臂神經、胸長神經等胸部神經而產生區域麻醉作用。本研究結果顯示,兩組患者在手術結束時血清Cor、IL-6、IL-10及TNF-α水平雖均升高,但全身麻醉復合PECSⅡ阻滯組與單純全身麻醉組相比,血清Cor、IL-6、IL-10及TNFα水平顯著下降,說明PECSⅡ阻滯用于乳腺癌改良根治術可有效阻斷局部痛覺等傷害性刺激信號向中樞神經系統傳遞,從而抑制Cor及炎性細胞因子的釋放,減輕機體的應激反應。同時,PECSⅡ阻滯的有效鎮痛,降低了由于早期組織損傷導致的血清TNF-α、IL-6及IL-10濃度升高,通過抑制炎癥因子對腫瘤的增殖、遷移、侵襲和血管生成的不良影響,可降低腫瘤復發率,有利于乳腺癌患者的遠期預后[12-14]。
本研究證實,超聲引導下PECSⅡ阻滯鎮痛效果確切。與G 組患者相比,P 組患者VAS 評分在轉入PICU即刻、術后2 h以及術后6 h顯著降低,表明患者術后疼痛明顯減輕,且呼吸、循環系統無顯著變化,進一步證實在乳腺癌改良根治術中應用PECSⅡ阻滯鎮痛的有效性。與以往乳腺癌手術實施全身麻醉或復合椎旁阻滯以及高位硬膜外阻滯相比,本研究中P組患者均未發生神經損傷、血氣胸等穿刺并發癥,且無高位硬膜外麻醉時交感神經過度阻滯引起的嚴重低血壓、高位脊髓損傷等風險[15-16],表明超聲可視引導下PECSⅡ阻滯優勢突出,其定位準確,操作簡單且安全有效,便于臨床推廣。
綜上所述,全麻復合PECSⅡ阻滯能夠有效抑制乳腺癌改良根治術患者圍術期血清中的Cor、IL-6、IL-10 和TNF-α 釋放,降低應激反應程度,有效緩解術后疼痛,有利于患者恢復,是一種安全、有效的鎮痛方法,具有臨床意義。

