基于顯色法的紙基微流控芯片用于水中的三氮檢測
徐榕 楊葉欣 林敏 李曉東 馮愛玲

摘?要?硝酸鹽、亞硝酸鹽和氨氮 (簡稱“三氮”) 是水體中的主要污染物,目前我國的地表水和淺層地下水中普遍存在三氮污染問題。本研究將顯色法與紙基微流控技術結合,制備了單通道紙基微流控芯片,在優化的反應條件下,分別對3種含氮化合物進行檢測,亞硝酸鹽、硝酸鹽和氨氮的檢出限分別為0.001 mmol/L、 1 mmol/L和1 mg/L; 在實際樣本的檢測中,3種樣本的加標回收率均在95.4%~114.9%之內。其次,通過合理的結構設計將分別用于3種含氮化合物檢測的單通道紙基微流控芯片集成于一體,制備出用于三氮同時檢測的多通道紙基微流控芯片,多通道紙基微流控芯片的檢測結果與單通道紙基微流控芯片的檢測結果具有良好的一致性。本研究提出的基于顯色法的多通道紙基微流控芯片可對水中的三氮進行同時檢測,并且,此芯片具有成本低廉、靈敏度高和便于操作等特點,適用于現場快速檢測,有望在資源匱乏的水源污染地區推廣。
關鍵詞?顯色法; 三氮檢測; 紙基微流控
1?引 言
水質安全與人類的生命健康息息相關,污染水的攝入會引發各類疾病,甚至導致死亡[1,2]。水體中的硝酸鹽、亞硝酸鹽和氨氮 (簡稱“三氮”) 作為主要的無機非金屬含氮污染化合物,是水質安全檢測的重要指標之一。通過對水體中三氮含量的檢測,可有效監測水質安全,防止污染水的攝入,并能夠準確判斷水體污染的特征,采取及時有效的治理措施。目前,三氮的檢測方法主要有分光光度法[3]、光譜法[4]和電化學法[5]。分光光度法是一種較為精確的水質檢測方法,但該方法對儀器的要求通常較高,并且所用的檢測試劑苯酚含有劇毒。光譜法檢測水質安全時常需要復雜的樣本預處理過程,以及專業的操作人員。電化學法操作簡單,檢測速度快,適用于水質安全的實時監測,但是,當水體成分復雜時,電極易受到其它離子的干擾,造成檢測不穩定和檢出限高等問題。化學顯色法通過顯色劑顏色的變化對檢測結果進行直觀快速的判斷,具有操作簡單、成本低廉、適合現場快速檢測等特點[6]。目前,化學顯色法已廣泛應用于水體中含氮污染物的檢測。如Cho等[7]提出以多孔濾紙為載體的檢測策略,無需借助專業的實驗室儀器,僅通過改進的Berthelot反應即可對水樣中的氨氮含量進行比色檢測,檢測范圍在10~1020 mg/L之間,但該方法僅實現了水樣中氨氮的檢測,無法對三氮進行同時檢測。發展便攜式的多目標物同時檢測的裝置可有效解決現存水質中三氮檢測方案的缺陷,有利于偏遠地區和野外的水質安全的實時監測。
紙基微流控分析器件 (Microfluidic paper-based analytical devices,μPADs) 是一種以紙為基體材料的微流控裝置,因其成本低廉、質量輕巧、修飾簡便等優勢,成為近年檢測分析的研究熱點和有力手段[8,9]。通過結合不同的疏水試劑和圖案化工具,紙基微流控分析器件可通過構建多樣化的通道實現多目標物檢測[10]。Jayawardane等[11]以紙基微流控芯片為檢測平臺,利用顯色劑與目標物之間的化學反應,實現了對硝酸鹽和亞硝酸鹽的同時檢測。但是,該檢測平臺僅可對兩種含氮化合物進行同時檢測,并且使用的紙基芯片需借助噴蠟打印機制備親疏水通道,操作過程繁瑣。目前,利用紙基微流控芯片對水體中三氮進行同時檢測的文獻鮮有報道。
本研究設計了一種基于顯色反應的紙基微流控芯片,用于對水體中三氮的同時檢測。首先利用單一通道的紙基微流控芯片分別驗證每種含氮化合物的檢測方案,并對反應條件進行優化; 其次,通過將3種單通道紙基微流控芯片的加樣區進行集成,制備出多通道紙基微流控芯片,用于三氮同時檢測。在本研究中,硝酸鹽和亞硝酸鹽的檢測利用Griess試劑的偶氮反應,通過在相應的檢測區產生洋紅色的顏色變化判斷檢測結果; 通過Berthlot顯色試劑與底物相互作用生成藍綠色絡合物反映氨氮的檢測結果。結合顯色反應與紙基微流控芯片的優勢,本研究可對實際水樣中的亞硝酸鹽、硝酸鹽和氨氮進行同時檢測,檢出限分別為0.001 mmol/L、1 mmol/L和1 mg/L,滿足國標[12]對于飲用水中三氮檢測的要求。
2?實驗部分
2.1?儀器與試劑
VLS2.30激光切割機(美國Universal公司); DPX-9082B電熱恒溫培養箱(上海南榮實驗設備有限公司); DZ-1BC II真空干燥箱(上海飛越實驗室儀器有限公司) ; PVC背膠板(上海捷寧生物科技有限公司); 高速定量濾紙(上海捷寧生物科技有限公司); 打孔器和濾網篩(0.15 mm孔徑)。
磺胺(純度>99.5%)、檸檬酸(純度>99.5%)、H2SO4(分析純)、鋅粉(分析純)、LiOH(分析純)、NaNO2(純度99.9%)、NaNO3(純度99.9%)、NH4Cl(純度99.5%)、蔗糖(分析純)、無水乙醇(分析純)、無水乙醚(分析純)均購于天津致遠化學試劑公司; N-1萘基乙二胺鹽酸鹽(純度>98%)、水楊酸鈉(分析純)、硝普鈉(純度99.98%)、二氯異氰尿酸鈉(純度98%)、甲基纖維素(純度BR)均購于阿拉丁試劑有限公司; 實驗用水為二次蒸餾水(18.2 MΩ·cm,IQ 7003Milli-Q 純水儀(美國 Millipore 公司) 制備)。
2.2?實驗方法
2.2.1?單通道紙基微流控芯片的構建?紙基微流控芯片主要由PVC背膠板、加樣區、流道和檢測區組成,加樣區、流道和檢測區均由高速定量濾紙構建。其中,亞硝酸鹽通道和硝酸鹽通道的構建方法: 使用CoreDraw軟件繪制出加樣區、流道和檢測區的輪廓,再使用激光切割機對每一部分進行切割,以PVC背膠板為支撐基底將加樣區、流道和檢測區進行組裝,得到單一通道的紙基微流控芯片。氨氮通道的構建方法: 首先使用濾網篩將所用試劑均勻分布在濾紙上,再使用乙醇潤濕,室溫放置30 min后,將其剪裁成直徑為5 mm的顯色區,同樣以PVC背膠板為基底,依次將加樣區、流道和檢測區進行組裝,其中檢測區和流道之間有2 mm的重疊。
2.2.2?亞硝酸鹽的單通道紙基微流控檢測方法?亞硝酸鹽中NO2的檢測過程: 首先,在組裝完成的單通道微流控芯片的檢測區滴加1 μL 2% HCl 溶液,室溫放置10 min; 然后,在檢測區內滴加0.8 μL Griess試劑,將芯片置于60℃真空干燥箱中干燥15 min; 將10 μL樣品梯度液滴加在單通道紙基微流控芯片的檢測區,室溫放置3 min后,將芯片置于內置固定光源的暗箱中,使用CCD相機對芯片的檢測區進行顯色結果的拍攝。其中,Griess試劑的配制方法參照文獻[13],試劑配比為:檸檬酸鈉330 mmol/L,磺胺 30 mmol/L 和1-2萘乙二胺鹽酸鹽 10 mmol/L,溶劑為超純水。本實驗中梯度液的NO2來源于NaNO2,首先使用超純水配制10 mol/L NaNO2母液,再將其按照10∶1的比例稀釋為10、1、0.1、0.01和0.001 mmol/L的濃度梯度樣本溶液。
對實際水樣進行檢測和加標回收實驗時,首先使用單通道紙基微流控芯片對隨機選取的湖水樣進行初始濃度的測量,然后進行標準加入實驗,加標水平分別為0.025、0.05和0.1 mmol/L,在單通道芯片的加樣區滴加每種濃度的梯度加標溶液10 μL,室溫放置3 min后,使用CCD相機對芯片的檢測區進行顯色結果的拍攝,每個加標水平重復檢測3次。
顯色結果使用Image J軟件進行分析:將檢測結果照片導入到軟件中,使用軟件對圖片進行分通道,處理選取綠色通道(檢測結果的顏色變化在綠色通道中最為明顯),選中顯色區域,進行平均灰度值計算,將目標物濃度與檢測結果的灰度值相對應,繪制標準曲線。
2.2.3?硝酸鹽的單通道紙基微流控檢測方法?金屬鋅可將硝酸鹽還原為亞硝酸鹽,在進行硝酸鹽檢測時,首先使用鋅粉將其還原為亞硝酸鹽,再采用2.2.2節的方法進行檢測。鋅粉還原硝酸鹽分為兩步: 第一步需要對鋅粉進行活化,將3 mL 2% (w/V) HCl 與1.2 g 鋅粉混合攪拌1 min,分別使用超純水洗滌3次,無水乙醇洗滌2次,無水乙醚洗滌1次,洗滌完成之后的鋅粉置于37℃烘箱中徹底干燥后,于真空干燥箱進行保存; 第二步將活化后的鋅粉用于還原硝酸鹽,在制備完成的單通道紙基微流控芯片的檢測區上滴加1 μL 2% (w/V) HCl,室溫放置10 min,然后在檢測區內滴加0.8 μL Griess試劑,并在60℃真空干燥箱中干燥15 min,稱取0.1 g活化后的鋅粉溶于500 μL蔗糖溶液中 (飽和度為50%) 配制鋅粉蔗糖溶液,混勻后靜置,直至鋅粉完全沉淀,再使用移液槍吸取鋅粉蔗糖溶液的沉淀物在單通道芯片的流道上劃線2次 (1 μL/次),室溫放置15 min后,將樣本梯度濃度液和梯度加標溶液滴加在檢測區進行檢測。本實驗中標準樣本的NO3來自于NaNO3,稱取101.1 mg NaNO3溶于10 mL超純水中,然后將其稀釋為1000、500、100、50、10和5 mmol/L的濃度梯度樣本溶液,在單通道芯片的加樣區滴加每種梯度加標溶液10 μL,每個加標溶液重復檢測3次,室溫放置3 min后,使用CCD相機對芯片的檢測區進行顯色結果的拍攝。
在對實際樣本進行檢測時,首先使用單通道微流控芯片對隨機選取的湖水樣本中的硝酸鹽進行初始濃度的測定,然后進行加標回收實驗,實際樣本的梯度加標溶液的檢測和檢測結果分析同2.2.2節。
2.2.4?氨氮的單通道紙基微流控檢測方法?氨氮的單通道紙基微流控檢測分為兩步: (1)加入顯色劑。 稱取甲基纖維素38.2 mg、蔗糖60 mg、水楊酸鈉38.2 mg、二氯異氰尿酸鈉15.2 mg、LiOH 7.6 mg和硝普鈉20 mg于瑪瑙研缽中混合,研磨均勻,使用孔徑為0.15 mm的濾網篩將粉末均勻分散在乙醇潤濕的高速定量濾紙上,在濾紙表面均勻噴灑乙醇,直至粉末完全濕潤,室溫放置30 min后,將其剪裁成5 mm的檢測區; (2)將加樣區、流道和檢測區組裝后用于樣本檢測,組裝時檢測區與流道之間有2 mm重疊。
用于氨氮檢測的標準樣品由NH4Cl配制,將NH4Cl試劑置于105℃烘箱中干燥2 h后,配制成氨氮濃度為1 mg/mL的母液,再稀釋為50、20、10、5和1 mg/L的梯度濃度樣本溶液,在單通道芯片的加樣區滴加每種濃度的加標溶液20 μL,重復檢測3次,室溫放置15 min后,使用CCD相機對芯片的檢測區進行顯色結果的拍攝。
在對實際樣本進行檢測時,用單通道芯片對隨機選取的湖水樣本進行初始濃度測量,然后取3份樣品,分別加入干燥處理后的NH4Cl,進行標準添加實驗,實際樣本梯度加標溶液的檢測和檢測結果分析同2.2.2節。
2.2.5?多通道紙基微流控芯片的構建及三氮同時檢測?多通道紙基微流控芯片的構建是通過合理的結構設計將3個單通道紙基微流控芯片進行集成,實現三氮同時檢測。多通道紙基微流控芯片主要由1個PVC基底、3條流道、3個檢測區和1個加樣區構成,首先使用激光切割機將PVC背膠板切割成直徑為4 cm的圓形基底,再在圓形基底上切割出裝配通道,然后將高速定量濾紙分別切割成加樣區、流道和檢測區,分別使用單通道紙基微流控芯片中檢測區的處理方法,對多通道紙基微流控芯片的3個檢測區進行處理。處理完成之后,將圓形基底上裝配通道的膠面撕下,依次將流道、檢測區和加樣區進行粘貼,其中,檢測區和加樣區分別與流道有2 mm的重疊,粘貼完成之后即可形成多通道紙基微流控芯片。
將多通道紙基微流控芯片用于三氮同時檢測時,標準檢測液為包含亞硝酸鹽、硝酸鹽和NH4Cl的梯度混合液,其中梯度混合液中亞硝酸鹽、硝酸鹽和氨氮的濃度梯度分別與單通道紙基微流控芯片中的樣本梯度濃度液相同。在使用多通道紙基微流控芯片檢測梯度混合液時,取每種濃度的梯度混合液40 μL滴加在加樣區,室溫放置3 min后,使用CCD相機對亞硝酸鹽和硝酸鹽的檢測區進行拍照; 15 min后,對氨氮的檢測區進行拍照,顯色照片的處理方法同2.2.2節。
3?結果與討論
3.1?檢測原理
用于水中三氮檢測的紙基微流控芯片包含3個檢測區、3條流道和1個加樣區,3個檢測區分別用于硝酸鹽、亞硝酸鹽和氨氮的檢測。亞硝酸鹽的檢測是通過NO2與對氨基苯磺酸重氮化后,再與1,2萘乙基鹽酸鹽耦合,在檢測區形成紫紅色染料,通過檢測區顏色強度的變化判斷亞硝酸鹽的含量,此方法參照國標亞硝酸鹽檢測法[15]; 在使用微流控芯片檢測硝酸鹽時,首先用鋅粉將其還原成亞硝酸鹽,再用上述方法檢測; 氨氮檢測是在苯酚存在下,利用NH+4與HClO形成藍綠色絡合物進行顯色[14]。檢測區的顏色深度與目標物的濃度呈正相關,檢測區顏色越深,目標物濃度越高。通過Image J軟件分析檢測區域圖片的灰度值,與標準曲線進行比對,實現3種目標物的定量檢測。
3.2?亞硝酸鹽單通道檢測結果與反應條件優化
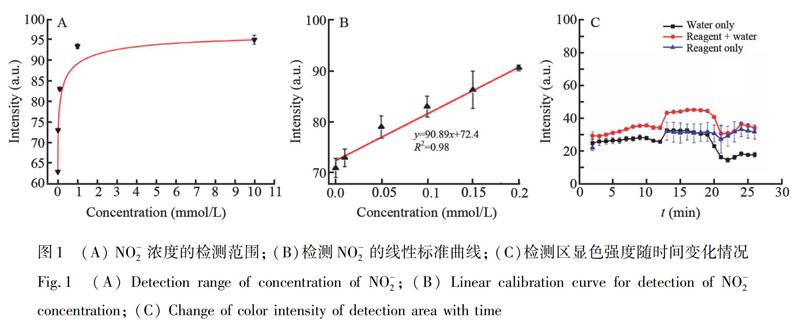
亞硝酸鹽濃度的檢測范圍和線性標準曲線如圖1A和1B所示,檢測范圍為0.001~10 mmol/L,在0.001~1 mmol/L之間呈良好的線性關系,線性回歸方程為y=90.89x+72.4 (R2=0.98),檢出限為0.001 mmol/L。與Zheng等[16]使用水溶性銅納米簇檢測亞硝酸鹽的方法相比,本方法避免了復雜的納米材料制備過程,僅通過化學試劑相互作用產生的顏色變化便可觀察顯色結果。
在亞硝酸鹽檢測中,顯色劑在濕潤條件下可能會與空氣中的某些物質發生氧化反應,進而影響檢測結果。對顯色劑開始產生氧化的時間進行判斷,進而推斷檢測時目標物的最佳反應時間。 以不含顯色劑的空白檢測區作為參照,分別在空白檢測區和含有顯色劑的檢測區滴加等體積的水,以20 s的時間間隔,使用CCD相機記錄檢測結果。檢測結果如圖1C所示,在0~3 min內,空白顯色區和含有顯色劑的檢測區灰度值相近,此時未發生氧化; 在3~6 min內,檢測區被完全浸透,與空白顯色區相比,含有顯色劑的檢測區灰度值較高,表明顯色劑開始氧化; 6 min后,樣本液體逐漸蒸發,含有顯色劑的顯色區灰度值明顯高于參照組。因此,檢測亞硝酸鹽時反應時間控制在3 min,此時顯色劑未發生氧化,顯色效果達到最優。
3.3?硝酸鹽單通道檢測結果與反應條件優化
硝酸鹽濃度的檢測范圍和線性標準曲線分別如圖2A和2B所示,檢測范圍為1~300 mmol/L,線性檢測范圍為1~210 mmol/L,線性方程為y=0.5377x + 69.04 (R2=0.99),檢出限為1 mmol/L。
在硝酸鹽檢測方案中,鋅粉對硝酸鹽的還原情況是影響檢測結果的主要因素。對紙基微流控芯片中活化后鋅粉的加入量進行了考察,分別在單通道紙基微流控芯片的流道上滴加1、2、3次鋅粉溶液,每次滴加的量為1 μL,芯片的顯色結果如圖2C所示,滴加兩次鋅粉時,顯色強度達到最佳; 繼續增加鋅粉的量后,可能會導致樣品損失,使達到檢測區的樣本量減少,影響顯色結果。本研究選擇鋅粉加入量為2 μL,每次滴加1 μL于流道上。
3.4?氨氮單通道檢測結果與反應條件優化
氨氮濃度的檢測范圍和線性標準曲線分別如圖3A和3B所示,檢測范圍為1~50 mg/L,在1~20 mg/L 之間呈良好的線性關系,線性標準方程 y=15.3x+ 68.72 (R2=0.96),檢出限為1 mg/L。在氨氮檢測中,催化劑硝普鈉的含量對顯色強度有直接影響。在其它試劑保持不變的情況下,考察了硝普鈉的含量為8、12、16、20和24 mg的影響,檢測結果如圖3C所示,當硝普鈉的含量為20 mg時,顯色強度達到最佳。
3.5?多通道紙基微流控芯片結構的優化
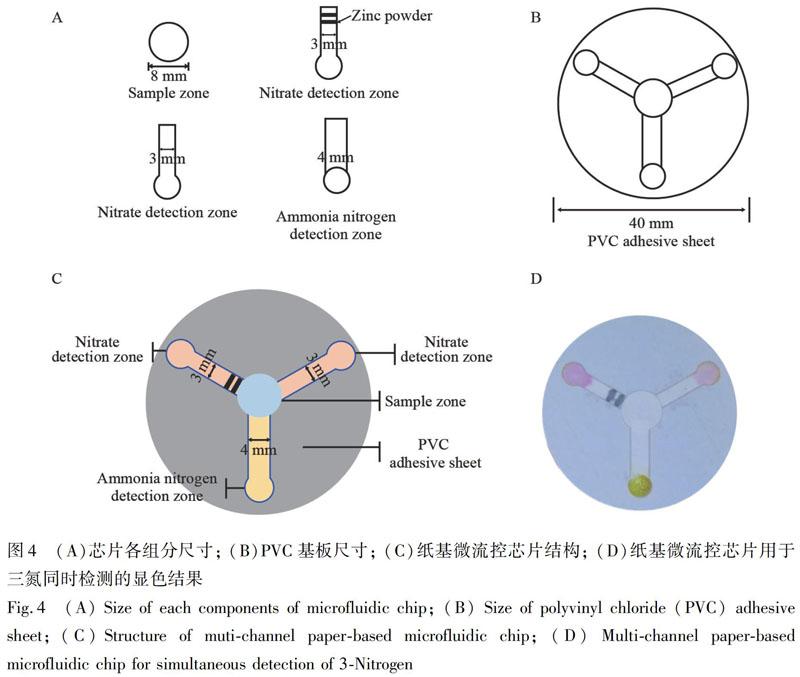
紙基微流控芯片可以通過合理的結構設計實現在同一檢測平臺上多種目標物的同時檢測。本研究在構建了檢測亞硝酸鹽、硝酸鹽及氨氮的單通道紙基芯片的基礎上,通過結構優化,將3種單通道紙基微流控芯片集成,制成用于同時檢測三氮化合物的多通道紙基微流控芯片,多通道紙基微流控芯片的初始流道寬度及檢測區面積和單通道紙基微流控芯片一致。但是,由于亞硝酸鹽和硝酸鹽的檢測體系所需樣本體積小于氨氮檢測所需的樣本體積,故對氨氮流道的尺寸進行調整,亞硝酸鹽和硝酸鹽流道寬度保持不變 (3 mm) 。在對氨氮流道進行尺寸調整時,以超純水為樣本,驗證不同的流道直徑可容納的樣本量。分別稱量加樣前后檢測區的重量,最終確定當氨氮流道的寬為4 mm時,檢測區可容納約210 mg超純水,滿足氨氮檢測所需的樣本量,紙基微流控芯片各組分的尺寸如圖4A所示,最終的多通道紙基微流控芯片結構如圖4C 所示。
3.6?實際水樣分析
使用制備的紙基微流控芯片對隨機選取的實際湖水樣品進行檢測,亞硝酸鹽、硝酸鹽和氨氮的檢出值分別為0.008 mmol/L、14.79 mmol/L和1.50 mg/L。實際樣本中三氮的加標回收實驗結果(表1)表明,三氮的加標回收率均在95.4%~114.0%之間。與Lin等[17]將分光光度法和流動注入分析結合的方式相比,本方法成本低廉,無需借助大型儀器便可對檢測結果進行讀取。
4?結 論
設計和制備了基于顯色反應的紙基微流控芯片,用于同時檢測水中三氮的含量,亞硝酸鹽、硝酸鹽和氨氮的檢出限分別為0.001 mmol/L、1 mmol/L和1 mg/L,實際樣本3種含氮化合物的加標回收率在95.4%~114.9%之間。相比于現有的三氮化合物檢測方法,本研究提出的紙基微流控芯片法有效簡化了操作步驟,降低了成本,操作簡單,無需借助大型儀器和專業的操作人員,有望用于資源匱乏的地區的水質監測。
References
1?Yu C Q,Huang X,Chen H,Godfray H C J,Wright J S,Hall J W,Gong P,Ni S Q,Qiao S C,Huang G R,Xiao Y C,Zhang J,Feng Z,Ju X T,Ciais P,Stenseth N C,Hessen D O,Sun Z L,Yu L,Cai W J,Fu H H,Huang X M,Zhang C,Liu H B,Taylor J. Nature,2019,567(7749): 516-520
2?Landrigan P J,Fuller R,Acosta N J R,Adeyi O,Arnold R,Basu N,Balde A B,Bertollini R,Bose-O′Reilly S,Boufford J I,Breysse P N,Chiles T,Mahidol C,Coll-Seck A M.,Cropper M L,Fobil J,Fuster V,Greenstone M,Haines A,Hanrahan D,Hunter D,Khare M,Krupnick A,Lanphear B,Lohani B,Martin K,Mathiasen K V,McTeer M A.,Murray C J L,Ndahimananjara J D,Perera F,Potocnik J,Preker A S,Ramesh J,Rockstrom J,Salinas C,Samson L D,Sandilya K,Sly P D,Smith K R,Steiner A,Stewart R B,Suk W A,van Schayck Onno C P,Yadama G N,Yumkella K,Zhong M. Lancet,2018,391(10119): 462-512
3?Zhu Z L,Guan X D,Zheng H T,Yang C,Xing Z,Hu S H. J. Anal. Atom. Spectrom.,2018,33(12): 2153-2159
4?Correa-Duarte M A,Perez N P,Guerrini L,Giannini V,Alvarez-Puebla R A.J. Phys. Chem. Lett.,2015,6(5): 868-874
5?Baciu A,Manea F,Pop A,Pode R,Schoonman L.Proc. Safety Environ. Protect.,2017,108: 18-25
6?Oh J W,Chung W J,Heo K,Jin H E,Lee B Y,Wang E,Zueger C,Wong W,Meyer J,Kim C,Lee S Y,Kim W G,Zemla M,Auer M,Hexemer A,Lee S W. Nat. Commun.,2014,5: 3043
7?Cho Y B,Jeong S H,Chun H,Kim Y S. Sens. Actuators B,2018,256: 167-175
8?Jin B R,Yang Y X,He R Y,Park Y I,Lee A,Bai D,Li F,Lu T J,Xu F,Lin M. Sens. Actuators B,2018,276: 48-56
9?You M L,Lin M,Gong Y,Wang S R,Li A,Ji L Y,Zhao H X,Ling K,Wen T,Huang Y,Gao D F,Ma Q,Wang T Z,Ma A Q,Li X L,Xu F. ACS Nano,2017,11(6): 6261-6270
10?Xia Y Y,Si J,Li Z Y. Biosens. Bioelectron.,2016,77: 774-789
11?Jayawardane B M,Wei S,McKelvie I D,Kolev S D. Anal. Chem.,2014,86(15): 7274-7279
12?GB 5749-2006,Standards for Drinking Water Quality. National Standards of the People′s Republic of China
生活飲用水衛生標準. 中華人民共和國國家標準. GB 5749-2006
13?Sun J,Zhang X J,Broderick M,Fein H. Sensors,2003,3(8): 276-284
14?Lau K T,Edwards S,Diamond D. Sens. Actuators B,2004,98(1): 12-17
15?GB/T 5009.33-1996,National Food Safety Standard Determination of Nitrite and Nitrate in Food. National Standards of the People′s Republic of China
食品中亞硝酸鹽與硝酸鹽的測定. 中華人民共和國國家標準. GB/T 5009.33—1996
16?Zheng X J,Liang R P,Li Z J,Zhang L,Qiu J D. Sens. Actuators B,2016,230: 314-319
17?Lin K N,Ma J,Yuan D X,Feng S C,Su H T,Huang Y M,Shanguan Q P. Talanta,2017,167: 166-171

