葛蘭心寧軟膠囊中絞股藍皂苷A大鼠體內藥代動力學研究
胡小虎,孫文軍,高昕,王夕靜
1.西安千禾藥業股份有限公司,陜西 西安 710075;2.西安新通藥物研究有限公司,陜西 西安 710077;3.西安交通大學 藥學院,陜西 西安 710061
葛蘭心寧軟膠囊為西安千禾藥業股份有限公司開發的由成分明確的葛根總黃酮、山楂提取物、絞股藍總皂苷組成的中藥復方制劑,具有活血化瘀、通絡止痛的功效,臨床用于預防和治療瘀血閉阻所致的冠心病、心絞痛[1]。其主要組成組分絞股藍總皂苷由絞股藍提取制成,主要活性成分為達瑪烷型皂苷類物質,含量較高,具有保護心腦血管、抗腫瘤、增強免疫等顯著作用[2],其中含量較大的皂苷為絞股藍皂苷A(結構式見圖1)。文獻[3]報道了用高效液相色譜串聯紫外檢測器(HPLC-UV)測定絞股藍中絞股藍皂苷A的含量、文獻[4]報道了用高效液相串聯蒸發光散射檢測器(HPLC-ELSD)測定絞股藍中絞股藍皂苷A的含量,但尚未有絞股藍皂苷A有關藥代動力學研究的文獻報道。本研究應用超高效液相色譜-質譜聯用分析方法(UPLC-MS)建立葛蘭心寧軟膠囊中絞股藍皂苷A的體內分析方法,進行絞股藍皂苷A的大鼠血漿藥代動力學研究,為葛蘭心寧軟膠囊藥效物質基礎研究提供方法學參考和實驗依據。
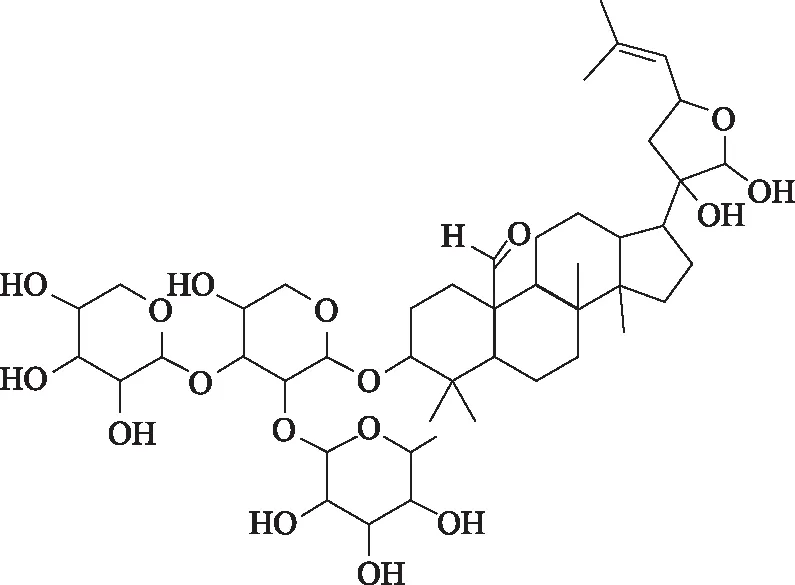
圖1 絞股藍皂苷A的結構式
1 材料
Waters UPLC H-Clas/Xevo TQD型超高效液相色譜串聯四級桿質譜聯用儀(QSM四元梯度泵、FTN自動進樣器、6通道在線脫氣機、數據處理系統MassLynx V4.1,美國Waters公司);德國Sartorius BS124S型電子天平(0.1 mg,最大稱量120 g,德國賽多利斯公司);德國Sartorius BT125D型萬分之一/十萬分之一雙量程電子天平[0.01 mg·(0.1 mg)-1,最大稱量41 g·(120 g)-1,德國賽多利斯公司];TD10001B型電子天平(0.1 g,最大稱量1000 g,余姚市金諾天平儀器有限公司);ULT2186-4-V -86 ℃立式超低溫冰箱(美國Thermo Revco公司);臺式高速冷凍離心機(TGL16M,長沙湘智離心機儀器有限公司);多通道微量移液器(M12-50,德國brand公司)。
葛蘭心寧軟膠囊(批號:20170603,西安千禾藥業股份有限公司);絞股藍皂苷A對照品(批號:DRK-1392-920117,純度:98.9%,成都德瑞可生物科技有限公司);內標丹參酮ⅡA對照品(批號:MUST-16111007,純度:99.71%,成都曼斯特生物科技有限公司);甲酸(LC/MS級,中國國藥控股有限公司);甲醇(LC/MS級,德國Merck 公司);乙腈(LC/MS級,德國Merck公司);純化水(實驗室自制)。
雄性SPF級SD種大鼠,體質量220~250 g[四川省中醫藥科學院實驗動物中心,生產許可證號:SCXK(川)2018-19]。動物接收后進行常規檢疫和適應性觀察,連續觀察7 d,每天1次。IVC獨立送風大鼠飼養系統,四川省實驗動物設施使用許可證號:SYXK(川)2018-008。飼養溫度:20~26 ℃,相對濕度:40%~70%,飼養密度1~5只/盒。
2 方法與結果
2.1 色譜與質譜方法
Waters UPLC H-Clas超高效液相色譜儀;Waters CORTECSTMUPLC C18色譜柱(50 mm×2.1 mm,1.6 μm);柱溫45 ℃;流動相:A(0.1%甲酸水溶液)-B(0.1%甲酸甲醇溶液),梯度洗脫(0~1 min,70%B;1~2.5 min,70%~95%B;2.5~4.5 min,95%~100%B;4.5~6.0 min,100%~70%B),流速0.2 mL·min-1;進樣體積5 μL。
質譜參數:Waters UPLC H-Clas/Xevo TQD型超高效液相色譜串聯三重四級桿質譜聯用儀,電噴霧離子源;正離子檢測;毛細管電壓:3.0 KV,離子源溫度:120 ℃,去溶劑溫度:350 ℃,去溶劑流速:600 L·h-1,錐孔電壓:30 V,噴霧氣與反吹氣N2,反吹氣流速:50 L·h-1,碰撞氣Ar,碰撞氣流速:0.16 mL·min-1,碰撞能量:15 V,掃描模式MRM;定量分析特征離子,絞股藍皂苷A:m/z899.35~814.47,內標丹參酮ⅡA:m/z295.1~206.03。液質系統為 MassLynx V4.1。
2.2 給藥方案與血漿樣品采集
2.2.1給藥方案 參照供試品用法用量,計算60 kg成人日用量為:0.58×2×3÷60≈0.058 g/kg/日。計算大鼠等效劑量:(dA×kB)÷kA=(0.058×0.71)÷0.11≈0.37 g·kg-1,式中,dA為A種動物的給藥計量;kA為A種動物等效劑量的折算系數;kB為B種動物等效劑量的折算系數。根據預實驗探索結果,調整給藥量為灌胃給予0.5 mL·kg-1。實驗前禁食不禁水12 h。給藥1次。
2.2.2血漿樣品采集 根據預試驗結果設置取血時間點設置如下:灌胃給藥前約0.5 h(零時間),灌胃給藥后0.25、0.5、0.75、1、2、3、4、6、8、12、24 h由眼眶靜脈叢取血約0.5 mL。置肝素化試管中,輕輕搖勻,4 ℃ 3000 r·min-1離心10 min分離血漿,-80 ℃保存待測。
2.3 血漿樣品的預處理
2.3.1空白血漿樣品的預處理 取大鼠空白血漿,精密量取50 μL,置1.0 mL塑料離心管中,加入200 μL甲醇,渦旋混勻2 min后,置于離心機中,4 ℃,25 000 r·min-1(離心半徑為5.35 cm)離心10 min,取上清液,進行超高效液相色譜串聯質譜(UPLC-MS) 分析。
2.3.2含藥血漿樣品 取大鼠血漿50 μL,精密量取,置1.5 mL 塑料離心管中,加入內標溶液丹參酮ⅡA(100 ng·mL-1,甲醇) 50 μL,渦混1 min,再加入甲醇150 μL,渦混2 min,4 ℃ 25 000 r·min-1離心10 min,取上清液進樣,UPLC-MS分析。
2.4 方法學考察
2.4.1專屬性考察 取大鼠空白血漿,分別精密量50 μL,6份,按照2.3.1項下方法操作,經UPLC-MS/MS分析,得空白樣品色譜圖。將一定濃度的絞股藍皂苷A對照品溶液和內標丹參酮ⅡA對照品溶液,37 ℃氮氣吹干后,加入空白血漿渦旋混勻,依法操作,得相應色譜圖。通過比較可以判斷大鼠血漿中內源性物質是否干擾待測物的測定。
2.4.2線性關系、檢測限與定量限 精密移取各系列絞股藍皂苷A對照品溶液各50 μL,37 ℃ 氮氣吹干后,加入50 μL大鼠空白血漿,渦旋混勻,得絞股藍皂苷A系列對照品溶液(10、20、50、100、200、400、500 ng·mL-1),其余按2.3.2項下方法操作。以絞股藍皂苷A血藥濃度為橫坐標(C),絞股藍皂苷A與內標物的色譜峰面積比值為縱坐標(Y),以加權系數1/C2進行線性回歸,得到標準曲線。
2.4.3準確度和精密度試驗 按2.4.2標準曲線和線性范圍項下方法分別配制高、中、低濃度(20、100、400 ng·mL-1)的質控樣品,同法配制與定量下限(LLOQ)質量濃度(10 ng·mL-1)相當的質控(QC)樣品,每個濃度平行分析5次,連續測定3 d,求得方法的日內和日間精密度和準確度。
準確度=(實測濃度/標示濃度)×100%
(1)
2.4.4提取回收率試驗 分別取空白血漿50 μL,配制20、100、400 ng·mL-13個質量濃度QC樣品,每個濃度平行配制6份,按2.4.2標準曲線和線性范圍項下操作方法處理,取5 μL進樣,UPLC-MS分析,得絞股藍皂苷A峰面積A1和內標峰面積A2。
另取空白血漿50 μL,置1.5 mL 塑料離心管中,加入甲醇200 μL,渦混2 min,4 ℃ 25 000 r·min-1離心10 min,得空白血清上清液。取沉淀蛋白后的空白血漿上清液,配制20、100、400 ng·mL-13個質量濃度QC樣品,再分別加入50 μL內標溶液,渦旋混合1 min,25 000 r·min-1(離心半徑為5.35 cm)離心10 min,取上清液5 μL進樣,UPLC-MS分析,得絞股藍皂苷A峰面積B1和內標峰面積B2。
絞股藍皂苷A的提取回收率=A1/B1×100%
(2)
內標的提取回收率=A2/B2×100%
(3)
2.4.5穩定性試驗 取空白血漿50 μL,配制20、100、400 ng·mL-13個質量濃度QC樣品,每個濃度配制6份溶液,進行穩定性考察。
考察條件:QC樣品在室溫下放置8 h;QC樣品在-80 ℃下凍存2個月;QC樣品在3個凍-融循環;按2.3.2項下方法處理后的3種質量濃度的QC樣品在自動進樣器(10 ℃)下放置12 h;儲備液在-20 ℃下放置30 d。計算絞股藍皂苷A在不同穩定性考察條件下的偏差,若偏差在±15%以下,則認為樣品穩定[5]。
2.5 基質效應
分別取6份空白血漿樣品(來源于6只大鼠)各50 μL,置1.5 mL 塑料離心管中,加入甲醇200 μL,渦混2 min,4 ℃ 25 000 r·min-1(離心半徑為5.35 cm)離心10 min,得空白血清上清液。取沉淀蛋白后的空白血漿上清液,配制20、100、400 ng·mL-13個質量濃度QC樣品,每個濃度平行配制6份,加入50 μL內標溶液,渦混1 min,4 ℃,25 000 r·min-1(離心半徑為5.35 cm)離心10 min,吸取上清液5 μL,進行UPLC-MS/MS分析,得到絞股藍皂苷A峰面積C1和內標峰面積C2。
取質量濃度為4、20、80 ng·mL-1的絞股藍皂苷A溶液和20 ng·mL-1的內標溶液,各取5 μL,進行UPLC-MS/MS分析,得到絞股藍皂苷A峰面積D1和內標的峰面積D2。
絞股藍皂苷A的基質效應= C1/D1×100%
(4)
內標的基質效應=C2/D2×100%
(5)
若結果在85. 0%~115.%,則認為沒有基質效應。
2.6 藥動學研究
實驗數據采用DAS 3. 0 進行統計分析,分析時用非房室模型進行。
3 結果
3.1 定量離子對的選擇
對絞股藍皂苷A和內標丹參酮ⅡA進行全掃描分析。正離子下,絞股藍皂苷A能夠產生m/z899.35[M+H]+,二級質譜主要碎片為m/z814.47。因此,選擇m/z899.35~814.47為絞股藍皂苷A的定量離子對。同樣選擇m/z295.1~206.03作為丹參酮ⅡA的定量離子對。
3.2 血漿樣品處理方法
比較了幾種常規的血漿樣品處理方法,其中固相萃取法,可以除掉大部分干擾物質,但價格較為昂貴;沉淀蛋白法,操作簡單,重復性好,成本最低。所以,從經濟角度考慮,選擇了沉淀蛋白法作為本研究中的血漿樣品的處理方法[6]。
3.3 分析方法學驗證
3.3.1系統適用性與專屬性試驗 在本研究優化后的色譜條件下,空白血漿色譜圖、空白血漿加標準品色譜圖和給藥后血漿色譜圖分別見圖2。結果表明,血漿中內源性雜質不干擾絞股藍皂苷A和內標的測定。

注:A.空白血漿;B.含絞股藍皂苷A標準物質的空白血漿;C.給藥1 h后血漿樣品中的絞股藍皂苷A;D.空白血漿;E.含有內標丹參素ⅡA標準物質的空白血漿;F.給藥1 h后血漿樣品中的內標丹參素ⅡA。圖2 絞股藍皂苷A和內標丹參素ⅡA的血漿樣品典型色譜圖
3.3.2標準曲線與最低定量限 以絞股藍皂苷A血藥濃度為橫坐標,絞股藍皂苷A與內標物的色譜峰面積比值為縱坐標(Y),以加權系數1/C2進行線性回歸,得到標準曲線Y=0.001 6X+0.003 2 (r=0.998 4)。結果表明,血漿中絞股藍皂苷A在10~500 ng·mL-1線性關系良好。方法最低定量限(LLOQ)為10 ng·mL-1(S/N>10),表明該方法靈敏度較高,可用于絞股藍皂苷A的定量分析。
3.3.3準確度和精密度 準確度與精密度結果見表1,結果表明,準確度為 97.0%~98.5%,日內精密度RSD<7%,日間精密度RSD<4%。

表1 大鼠血漿中絞股藍皂苷A UPLC-MS/MS測定的準確度和精密度(n=5)
3.3.4基質效應與提取回收率 提取回收率結果見表2,結果表明,3個濃度提取回收率為84.7%~86.4%,符合生物樣本的分析要求,且RSD<4%。基質效應結果表明,內源性物質不干擾絞股藍皂苷A的測定,且RSD<5%。
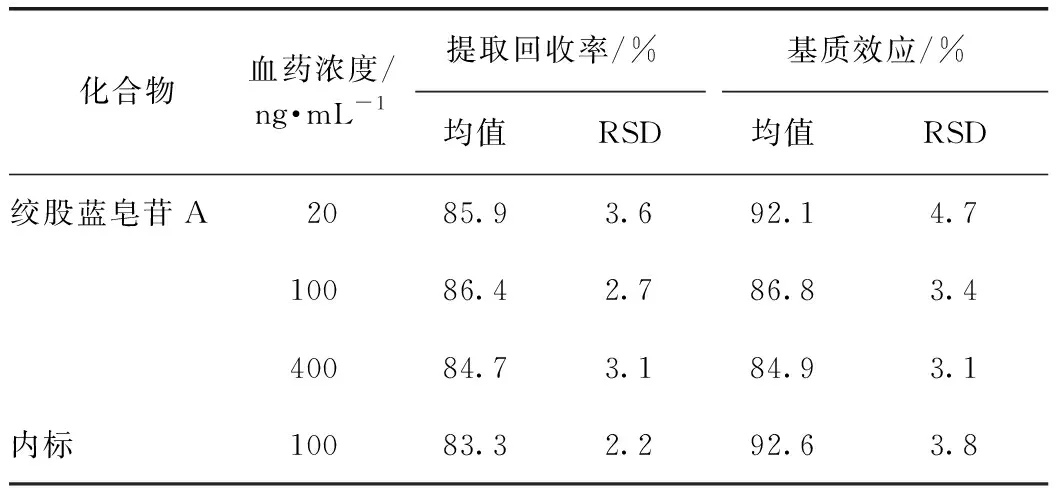
表2 絞股藍皂苷A和內標在大鼠血漿中提取回收率和基質效應考察(n=6)
3.3.5樣本穩定性 穩定性試驗結果表明,絞股藍皂苷A在血漿中-80 ℃下凍存2個月、-20 ℃下放置30 d、室溫下放置8 h、在自動進樣器(10 ℃)下放置12 h、經過3個凍-融循環后基本穩定,不同穩定性考察條件下的偏差均在±15%以下,穩定性良好,結果見表3。
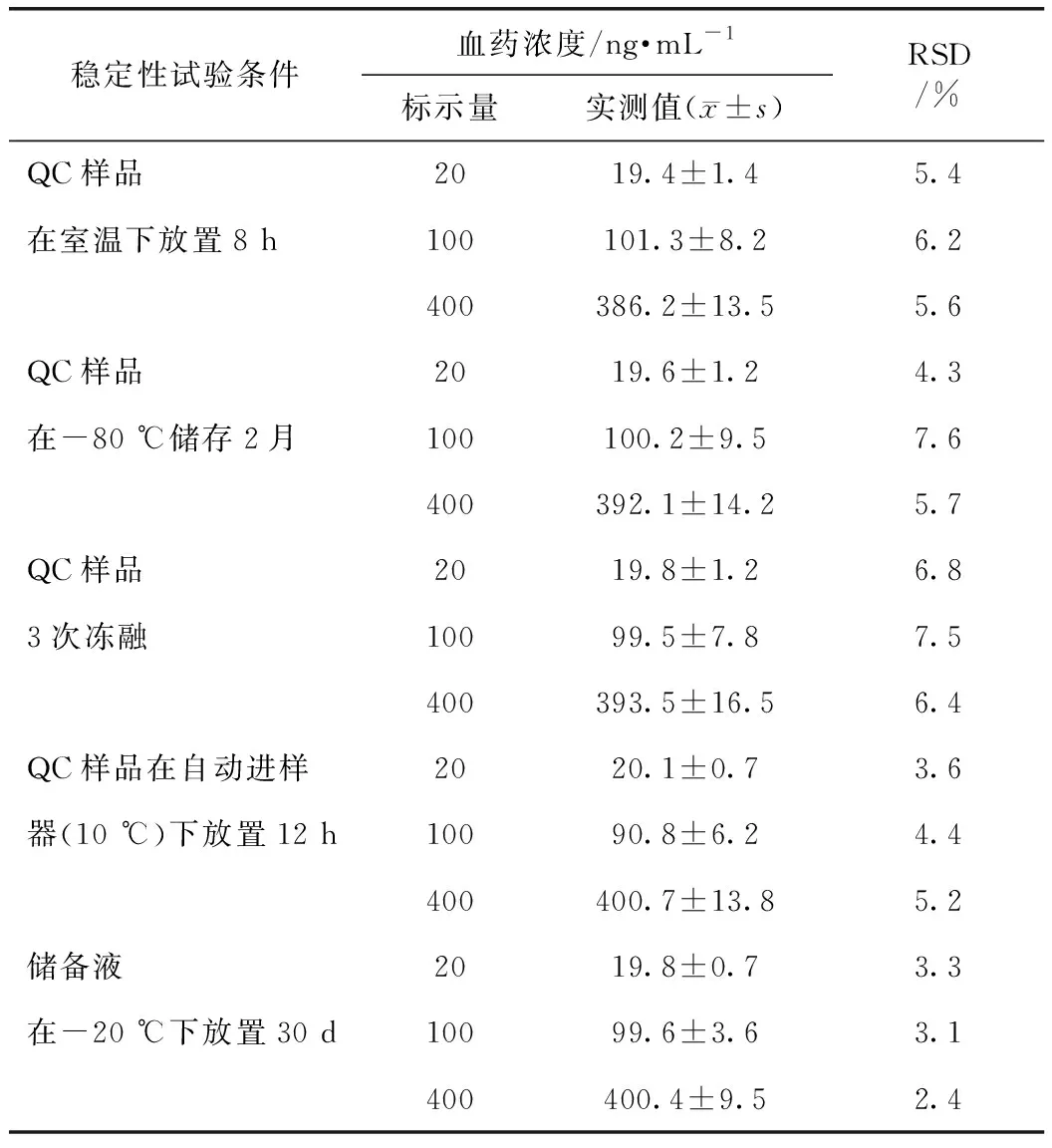
表3 絞股藍皂苷A在大鼠血漿中不同條件下的穩定性考察(n=6)
結果表明,本研究所建立的大鼠血漿樣品分析方法符合藥動學研究的相關要求,可以用于絞股藍皂苷A的大鼠體內藥代動力學研究。
3.4 藥動學研究
大鼠口服給予葛蘭心寧軟膠囊后,絞股藍皂苷A的體內血藥濃度-時間曲線見圖3。
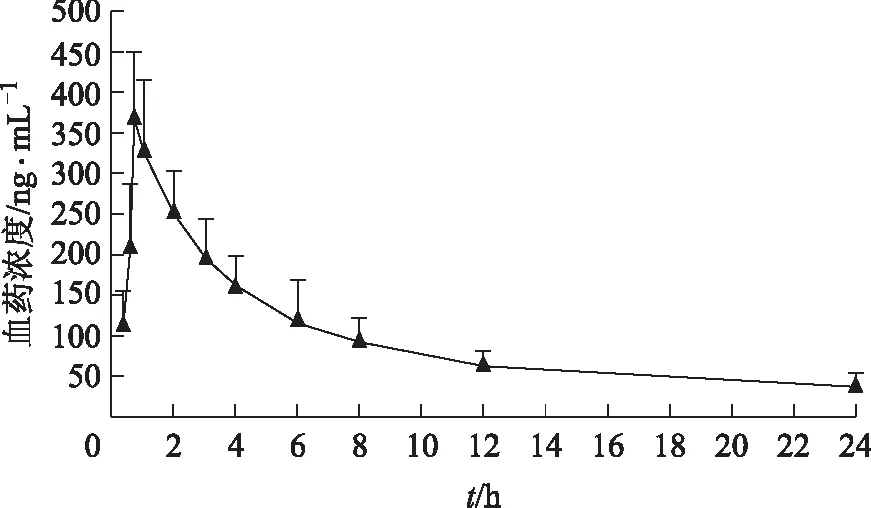
圖3 大鼠口服給予葛蘭心寧軟膠囊后絞股藍皂苷A的藥時曲線動物數=12)
葛蘭心寧軟膠囊口服后其主要藥效成分絞股藍皂苷A能夠迅速吸收進入血液中,給藥后15 min在血中可以檢測到絞股藍皂苷A,并于0.75 h迅速達到最大血藥濃度,消除相對較快,半衰期為(6.247±2.039)h。非房室模型分析所得藥動學參數見表4。

表4 大鼠口服給予葛蘭心寧軟膠囊后絞股藍皂苷A的藥動學參數
4 結論
本研究建立了大鼠灌胃葛蘭心寧軟膠囊內容物后,血漿中絞股藍皂苷A的 LC-MS/MS 測定方法,并采用非房室模型計算分析了其藥動學參數。該方法簡單、快捷、靈敏度高、精密度及線性關系良好,可以用于生物樣本中絞股藍皂苷A的藥代動力學研究。藥動學參數Cmax反映了藥物在血漿中的最大濃度,絞股藍皂苷A的Cmax為(377.6±75.3)μg·L-1,0.75 h迅速達到最大血藥濃度,t112為(6.247±2.039)h,CL為(0.249 2±0.050 02)L·h-1·kg-1,清除非常快。絞股藍皂苷 A 是絞股藍中含量較高且有效的單體成分[3],其結構屬于達瑪烷型四環三萜皂苷。Zhang等[7]報道了大鼠口服絞股藍總皂苷后,2個達瑪烷型四環三萜皂苷類成分gypenoside LⅥ和gypenoside ⅩLⅥ的藥代動力參數,半衰期與本研究的結果相近,但是Tmax為4 h,可能與糖基的種類、數量、連接位置不同有關。

