用回收無水硫酸銅制備硫酸銅晶體的實驗探究
翟志勇
摘要: 組織學生通過小組合作學習,帶著問題進行實驗探究,以學生實驗后回收的無水硫酸銅為原料,采用重結晶方法制備硫酸銅晶體,使其達到能夠滿足實驗室正常使用的要求。學生通過該實踐活動,經歷了自主、合作、探究等多種方式的學習實踐,取得了預期的成效。
關鍵詞: 無水硫酸銅; 重結晶法; 硫酸銅晶體
文章編號: 10056629(2020)06007503? 中圖分類號: G633.8? 文獻標識碼: B
1 問題由來
結晶水合物中結晶水含量的測定是普通高中化學教材(滬科版)[1]中的定量實驗之一。根據化學課程標準[2]和教學基本要求[3]對此實驗學習水平的要求,屬于設計(C)層次。在學生分組實驗后,回收的無水硫酸銅一直沒有得到有效的處理,累積質量已達到2500克。如何將其重新制成帶有五個結晶水的硫酸銅晶體再次利用?按照綠色化學理念,在實驗教學或實踐活動中,盡量多地體現“4R”原則,“Reduce——減量使用,Recycle——循環使用,Reuse——重新使用”都是其中要義。為此,我們專門組建綠色化學課題小組,以一個真實問題情景[4]為抓手,利用學生課余時間和學校對學生開放實驗室的契機,以小組合作學習的方式開展實驗探究活動[5]。
2 實踐過程
2.1 實驗用品
試管(25×180mm)、滴定管25mL、電子天平、稱量紙、無水硫酸銅(AR)、無水硫酸銅(回收)、蒸餾水、燒杯(25mL, 1000mL)、電爐(2000w)、石棉網、濾紙(Φ=8cm)、玻璃棒、DIS實驗系統(數據采集器、電腦、溫度探頭、DIS軟件)、不銹鋼藥匙、鑷子、研缽(Φ=6cm)
2.2 實驗原理
從上述反應的化學方程式可知: 160g無水硫酸銅與90g水完全反應,可以得到250g硫酸銅晶體。
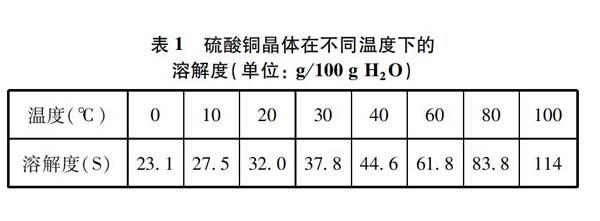
據此,我們設計了實驗室制取硫酸銅晶體的兩種方式: (1)直接將無水硫酸銅與水按照上述質量比進行混合,制取硫酸銅晶體。(2)根據硫酸銅晶體在不同溫度下溶解度不同(見表1)[6],利用重結晶方法把無水硫酸銅先溶解制成熱飽和溶液,讓其自然冷卻、結晶。制取硫酸銅晶體。
2.3 實驗探究
首先,通過百度學術搜索引擎,搜索關鍵詞“實驗室利用回收無水硫酸銅”“制備硫酸銅晶體”,獲得3960條信息。經過辨析,沒有發現與我們研究相關的有價值信息。其次,再通過專業網站,如“知網”“中國期刊網”“萬方數據資源系統”等查找上述關鍵詞。經甄別后發現: 王明華[7]偏重于得到較大的硫酸銅晶體,運用正交設計控制實驗條件進行研究。鄒洪炎,李秀林[8]在制取晶核及在晶體繼續增長過程中選擇比室溫高出5~10℃進行制作。盧宗右[9]通過使用棉線纏繞的方法,改變晶核的多少與分布,同時控制硫酸銅飽和溶液的溫度制取“心形”“燕子形”硫酸銅晶體。本課題組與之相比較,主要目的是將實驗室回收的無水硫酸銅重新轉化成可重新使用的硫酸銅晶體,并不需要制成比較大的具有一定幾何形狀的晶體。
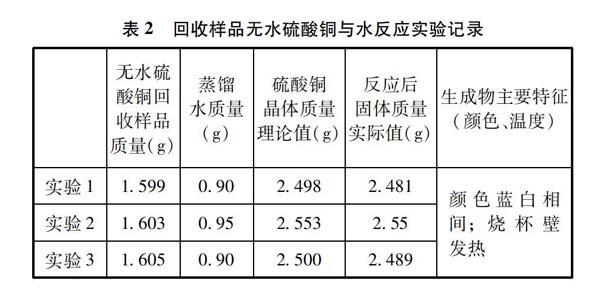
實驗1 稱量大約1.600g無水硫酸銅回收樣品于小燒杯中,并使用滴定管向其中滴加0.90mL蒸餾水。平行實驗做3次。實驗記錄如表2所示。
三次實驗相對誤差都比較小。說明實驗數據真實可靠。
實驗中發現,燒杯壁用手觸摸感覺比較熱。由此可知此反應是放熱反應。由于反應放熱,帶走一部分水分,因此所得到的硫酸銅晶體的質量都比其理論值要小,并且樣品與水反應得到的硫酸銅晶體顏色藍白相間,沒有硫酸銅晶體(分析純)那么藍。
放熱究竟對于二者混合有多大影響?下面借用DIS實驗的溫度探頭加以定量研究。
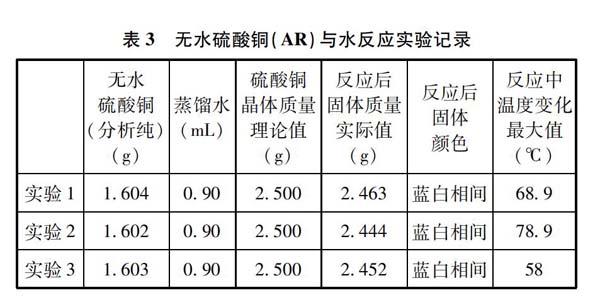
實驗2 稱量大約1.600g無水硫酸銅(AR)于大試管中,并使用滴定管向其中滴加0.90mL(g)蒸餾水。進行三次平行實驗。實驗記錄如表3所示。
實驗3 取無水硫酸銅回收樣品大約1.600g,重復實驗2的操作步驟(操作步驟、實驗記錄略)。
三次平行實驗反應過程中最高溫度分別為44.7℃、 58.3℃、 45.1℃。與表3無水硫酸銅(AR)所列溫度變化最大值比較,都顯得略低一些。實驗2、實驗3所得到硫酸銅晶體顏色相差不大。
綜合以上實驗1、實驗2和實驗3的情況分析,得出如下初步結論:
結論1: 無水硫酸銅(AR)及樣品(回收)與水反應都放出熱量,導致生成的硫酸銅沉淀的顏色沒有出現我們所應該看到的純藍色晶體。
結論2: 從質量守恒角度來看,無水硫酸銅與水反應后的生成物質量的減少,說明在反應中有少量水被蒸發,導致生成的硫酸銅顏色不是純藍色的晶體,而是藍白相間的固體。
結論3: 直接使用無水硫酸銅與水混合制取硫酸銅晶體的方法,理論上可行,但在具體實踐中很難得到純凈的硫酸銅晶體。
既然直接使用無水硫酸銅與水混合無法制取硫酸銅晶體(特別是顏色要匹配)。那么能否利用重結晶方法,制取硫酸銅晶體呢?
實驗4 (1)取適量的無水硫酸銅樣品(回收)于1000mL燒杯中,加入適量蒸餾水,放置于電爐上,進行加熱溶解;小心地不斷攪拌,加熱至100℃,制成飽和溶液;然后停止加熱,取下靜置,放置24小時,讓其自然冷卻。(2)出現晶體之后,將上層溶液轉移至另一個大燒杯中,再重復操作步驟(1)。(3)將所得硫酸銅晶體用藥匙或鑷子刮下,平鋪在濾紙上,上面覆蓋一張濾紙,輕輕地將硫酸銅晶體表面用濾紙吸干(濾紙用過后,晾干后還可以反復使用)。(4)將吸干后的硫酸銅晶體放置研缽中輕輕研碎(如芝麻大小),放置于干燥器中24h后,裝瓶即可。(5)剩余的硫酸銅飽和溶液另裝瓶備用。
經過上述實驗5個主要步驟,得到了我們預期的效果: 所制備的硫酸銅晶體顏色與其分析純的顏色基本一致。
3 結束語
指導學生利用課余時間,把普通中學實驗室都會遇到的一個看似簡單的真實問題以及解決問題的主動權交給學生,給予學生思考、創造和表現成功的時間和機會。促使學生帶著問題查閱文獻、設計實驗方案、開展實驗探究。通過小組合作、實驗探究、討論交流等多樣化方式解決問題[10]。在這樣的問題解決過程中學生的化學學科核心素養得到培養和提升,生態文明的意識得到增強[11]。盡管實驗過程看似簡單,但其中蘊含著豐富的學科教育內涵。通過這次自主、合作、探究等形式的教學活動,有效地促進了學生學習方式的轉變,獲得了預期效果。
(參與課題研究成員有徐晟智、黃子揚、徐靂申、陸黃懿、蔡祎宸、解欣悅等,在此一并表示感謝)
參考文獻:
[1] 姚子鵬主編. 化學?高中二年級第一學期(試用本)[M]. 上海: 上海科學技術出版社, 2007: 52.
[2] 上海市教育委員會. 上海市中學化學課程標準(試行稿)[S]. 上海: 上海教育出版社, 2004: 61.
[3] 上海市教育委員會教學研究室編.上海市高中化學學科教學基本要求(試驗本)[M]. 上海: 華東師范大學出版社2017: 175.
[4][10][11] 中華人民共和國教育部制定. 普通高中化學課程標準(2017年版)[S]. 北京: 人民教育出版社, 2018: 73~86.
[5] http://www.moe.gov.cn/srcsite/A06/s3321/201911/t20191128_409958.html. 教育部關于加強和改進中小學實驗教學的意見.
[6] 顧翼東主編. 化學詞典[M]. 上海: 辭書出版社, 2003: 616.
[7] 王明華. 硫酸銅晶體的制備[J]. 化學教學, 2003, (11): 5.
[8] 鄒洪炎, 李秀林. 硫酸銅晶體制作探索[J]. 化學教育(中英文), 1986, (6): 35~36.
[9] 盧宗右. 硫酸銅結晶的趣味實驗設計[J]. 化學教學, 2019, (5): 73~75.

