藥物流產術后宮內絨毛組織中CD34、VEGF、Ⅷ-RAg變化及臨床意義
趙琳 肖瑩 李文娟 張維丹 白楓
(遼寧省人民醫院婦科,遼寧 沈陽 110000)
藥物流產后的異常子宮出血,往往與患者子宮內膜血管以及蛋白表達水平有關,積極進行藥物流產后患者子宮內膜變化有利于預防藥物流產后異常的子宮出血以及大出血等[1-3]。白細胞分化抗原簇34(CD34)是血管內皮細胞標志物,在血管的新生、重鑄以及成熟過程中具有重要作用[4]。血管內皮生長因子(VEGF)是一種血管內皮細胞多功能因子,可增加血管通透性,促進血管內皮細胞的增殖、分裂、增生,誘導血管生成。人凝血因子Ⅷ相關抗原(Ⅷ-RAg)是廣泛存在于內皮細胞中的一種糖蛋白,是新生血管內皮細胞特異性標志物,反應血管內皮細胞黏附狀態,參與血管形成過程[5]。本文主要探討宮內絨毛組織中CD34、VEGF、Ⅷ-RAg的不同表達與藥物流產術后異常子宮出血的關系。
1 材料與方法
1.1研究對象 選取本院2016年4月至2019年1月本院就診行米非司酮藥物流產的早孕婦女80例作為藥物流產組,另選擇同期采用手術流產的方式終止妊娠的早孕婦女30例作為對照組,兩組均收集孕囊排出后或手術完成后的宮內絨毛組織。藥物流產組年齡18~34歲,平均(26.93±4.30)歲;停經天數34~48 d,平均(42.80±5.61)d;孕囊直徑0.7~2.4 cm,平均(1.43±0.32)cm;孕次1~4次,平均(1.83±0.45)次;產次0~3次,平均(0.94±0.14)次;子宮位置:前傾前屈位34例,水平位25例,后傾后屈位21例。對照組年齡19~35歲,平均(27.25±4.98)歲;停經天數34~49 d,平均(42.79±5.56)d;孕囊直徑0.8~2.4 cm,平均(1.45±0.39)cm;孕次1~4次,平均(1.89±0.36)次;產次0~4次,平均(0.98±0.12)次;子宮位置:前傾前屈位12例,水平位10例,后傾后屈位8例。納入對象的月經周期均規則,在28~33 d之間;停經天數≤49 d;通過血β-hCG、尿HCG以及B超檢查,經臨床證實已妊娠;流產前無陰道出血與難免流產癥狀。已排除血、尿、白帶檢測異常;1年內放置過宮內節育器;近3個月內服用過避孕藥或其他激素藥物;合并凝血功能障礙;合并全身性疾病。兩組患者一般資料比較差異無統計學意義(P>0.05)。
1.2儀器與試劑 鼠抗人CD34單克隆抗體、鼠抗人VEGF單克隆抗體、鼠抗人Ⅷ-R Ag單克隆抗體均來自美國Santz Cruz公司。二氨基聯苯胺(DAB)、鏈霉菌抗生物素蛋白—過氧化物酶連結(SP)試劑盒來自北京中杉金橋生物技術有限公司。
1.3檢測方法 所有標本進行切片(4 μm),于60℃溫度下烘烤處理20 min,二甲苯脫蠟,梯度酒精連續脫水,采用PBS清洗3次,并使用去離子水沖洗,3%H2O2室溫條件下10 min阻斷處理,使用PBS清洗3次,進行抗原熱修復,再次以PBS清洗3次。將標本浸泡于10%的BSA中,室溫下孵育5 min,封閉非特異性位點,滴加一抗,4℃下孵育過夜,使用PBS清洗3次。滴加SP,37℃下孵育30 min,使用PBS清洗3,DAB顯色10 min,使用PBS清洗3次,蘇木素溶液復染,鹽酸分化,脫水處理10 min,封片,鏡下觀察。
1.4染色結果判斷 由2名病理科醫生對標本進行觀察。染色強度以平均光密度(OD)表示,OD=各點光密度累積值/有效目標分布區域的面積。切片拍照采用日本Olympus BX-53光鏡,放大倍率為×400,每張切片選擇5個不連續視野拍照,條件參照圖片分析軟件要求,5個視野的平均值即為切片光密度結果。
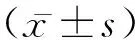
2 結 果
2.1宮內絨毛組織中CD34、VEGF、Ⅷ-RAg的表達 藥物流產組CD34、VEGF蛋白表達水平高于對照組,Ⅷ-RAg蛋白表達水平低于對照組(t=4.646、5.890、6.698,P均<0.05)。見表1。
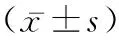
表1 宮內絨毛組織中CD34、VEGF、Ⅷ-RAg的表達
2.2CD34、VEGF、Ⅷ-RAg蛋白表達相關性分析 CD34與VEGF蛋白表達水平呈現正相關,與Ⅷ-RAg蛋白表達呈現負相關(r=0.578,-0.468,P<0.05);VEGF蛋白表達水平與Ⅷ-RAg呈現負相關(r=-0.505,P<0.05)。
2.3單因素分析 藥物成功組與藥物出血組婚姻狀況比較(P>0.05);藥物成功組患者年齡、孕囊直徑小于藥物出血組,孕次、產次少于藥物出血組(P<0.05);兩組慢性盆腔炎、哺乳期早孕、瘢痕子宮、子宮位置狀態比較(P<0.05);藥物成功組CD34、VEGF蛋白表達水平低于藥物出血組,Ⅷ-R Ag蛋白表達水平高于藥物出血組(P<0.05)。見表2。
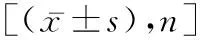
表2 藥物成功組與藥物出血組一般資料分析比較
2.2Logistic回歸分析 Logisitic回歸分析顯示,年齡、慢性盆腔炎、哺乳期早孕、瘢痕子宮、子宮位置、孕次、產次、孕囊直徑、CD34蛋白表達、VEGF蛋白表達、Ⅷ-RAg蛋白表達是藥物流產效果的影響因素。見表3。
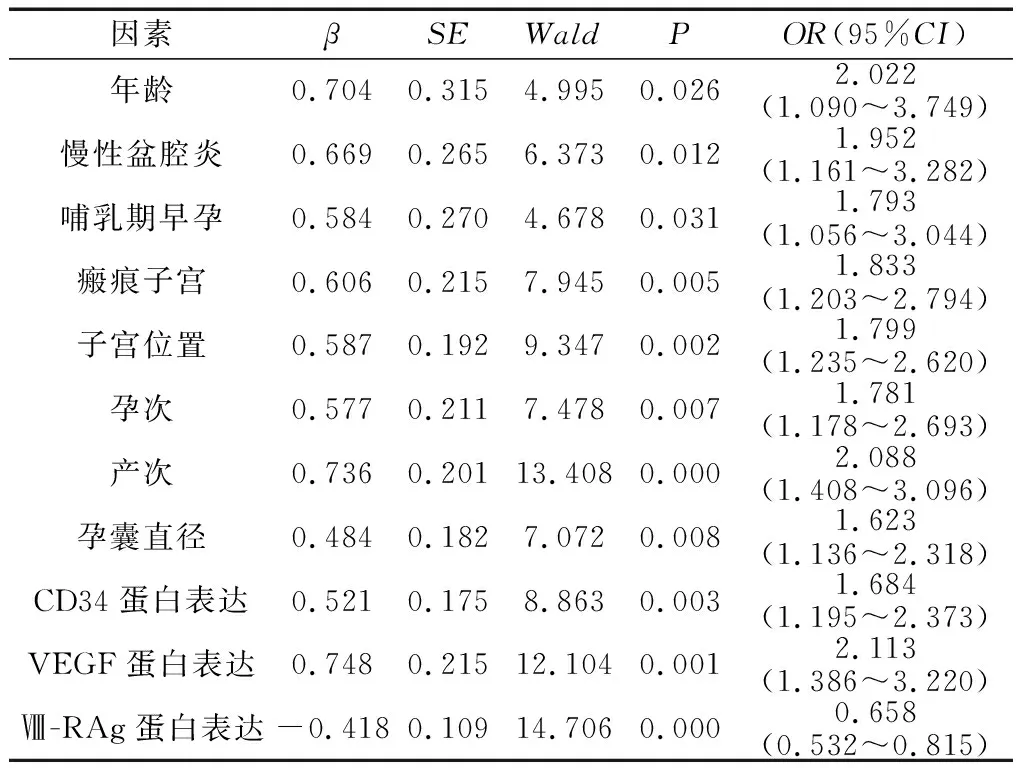
表3 藥物流產術后出血影響Logistic回歸分析
3 討 論
米非司酮作為一種抗孕激素的藥物,其靶結合位點為孕激素受體,米非司酮抗早孕機制為使高濃度孕激素蛻膜變性、壞死,導致絨毛滋養細胞的變性,進一步造成胚胎死亡,終止妊娠。然而臨床應用過程中發現藥物流產由于陰道出血時間較長,易導致一系列并發癥例如感染引起的不孕等,存在一定的弊端。
VEGF是一種同源二聚體糖蛋白物質,由兩條單鏈以二硫鍵鏈接而成,其作為血管內皮細胞中特異性肝素結合生長細胞因子,與體內血管誘導新生有關[6-7]。CD34是一種高特異性血管內皮細胞標記物,可通過特異性抗體與內皮細胞結合,直接反映體內微血管狀態[8]。本研究中藥物流產組CD34、VEGF蛋白表達水平均高于人工流產患組。研究[9-10]表明,VEGF的mRNA由剪切方式衍生出了VEGF121、145、165、185、206等蛋白亞型,其中VEGF121、145、165是可溶性蛋白,可直接作用于血管內皮細胞,促進血管內皮細胞增殖,增加血管通透性。VEGF表達水平的提高,可進一步造成子宮血管異常增殖,增加子宮異常出血風險。CD34具黏附作用,CD34的存在使得正常內皮細胞具有較強的黏著力,可承受血流壓力,藥物流產后CD34明顯減少,內皮細胞黏著力降低,使得血管容易斷裂,導致出血。本研究進一步分析發現CD34蛋白表達、VEGF蛋白表達是藥物流產效果的影響因素。
Ⅷ因子由內皮細胞產生,以Ⅷ-RAg以及和ⅧC兩種形式存在。Ⅷ-RAg廣泛存在于內皮細胞表面,是一種糖蛋白,為新生血管內皮特異性標記物,通常于小的毛細血管或尚未形成管腔的分支中表達,參與血管形成過程,同時也是反映血管內皮細胞粘附狀態的標志物之一。VEGF通過上調內皮細胞Ⅷ因子的表達,影響血管的生成或衰退;Ⅷ-RAg的減少可導致內膜微血管的形成減少,導致結構不良,出現不規則出血[11-12]。本實驗通過免疫組織化染色方法對Ⅷ-RAg進行標記,結果顯示藥物流產組Ⅷ-RAg蛋白表達水平低于對照組,提示藥物流產可導致內膜血管形成不良。本實驗結果顯示Ⅷ-RAg蛋白表達降低是導致藥物流產術后出血的危險因素。米非司酮通過調節VEGF的表達,影響內膜的增殖和血管的生成,改變局部微環境,引起局部Ⅷ-RAg明顯減少,血管內皮細胞的粘著力降低,導致微血管障礙,造成術后出血。另外,本研究Logisitic回歸分析顯示年齡、慢性盆腔炎、哺乳期早孕、瘢痕子宮、子宮位置、孕次、產次、孕囊直徑也是藥物流產效果的影響因素。提示在使用藥物流產時,臨床醫生應嚴格掌握適應證與禁忌證,對高危早孕婦女及時采取應對措施,保障治療的安全與有效。
綜上所述,藥物流產術后宮內絨毛組織中CD34、VEGF蛋白表達增加,Ⅷ-RAg表達降低,且CD34蛋白表達、VEGF蛋白表達、Ⅷ-RAg蛋白表達是藥物流產效果的影響因素。

