基于網絡藥理學的左金丸治療胃癌作用機制研究
黃鉦凱 梁明坤 吳發勝 陸飛國 陳廣文 梁健


〔摘要〕 目的 基于網絡藥理學方法探討左金丸治療胃癌的作用機制。方法 利用TCMSP數據庫獲得左金丸所含中藥的化學成分及對應作用靶點基因,檢索GeneCards和OMIM數據庫獲得疾病胃癌相關靶點基因,然后取兩者的交集,得到左金丸作用于胃癌的預測靶基因;利用Cytoscape 3.7.1 軟件構建左金丸化合物-作用靶點-疾病三者相互關系網絡,采用STRING數據庫對左金丸作用于胃癌的預測靶基因進行蛋白互作網絡分析,利用Cytoscape3.7.1 軟件的插件cytohubba篩選出關鍵靶基因,并利用ONCOMINE數據庫分析關鍵靶基因在胃癌中的表達情況;利用在線工具DAVID進行GO功能富集分析并利用Cytoscape3.7.1軟件的ClueGO插件進行KEGG通路富集分析。結果 共篩選出左金丸作用于胃癌的預測靶基因68個,關鍵靶基因15個,這些關鍵基因在ONCOMINE數據庫的胃癌樣本和正常樣本中的表達存在顯著性差異。GO功能富集分析顯示,左金丸作用于胃癌的預測靶基因主要涉及對有機物質的反應、細胞凋亡的負調控、細胞程序性死亡的負調控等生物過程;KEGG通路富集分析主要涉及癌癥通路、p53信號通路、VEGF信號通路等。結論 本研究初步揭示了左金丸治療胃癌的主要作用靶點及多靶點、多維調控、協同作用、整體調節的作用機制,可為后續進一步深入研究其作用機制提供參考。
〔關鍵詞〕 左金丸;胃癌;網絡藥理學;信號通路
〔中圖分類號〕R285.5;R96;R735.2 ? ? ? 〔文獻標志碼〕A ? ? ? 〔文章編號〕doi:10.3969/j.issn.1674-070X.2020.06.014
〔Abstract〕 Objective To study the mechanism of Zuojin Pills in the treatment of gastric cancer based on network pharmacology. Methods Chemical constituents and corresponding action target genes of Chinese materia medica in Zuojin Pills were obtained from TCMSP database, while GeneCards and OMIM database was retrieved for the target genes of gastric cancer. Then the intersection of the 2 groups of genes were taken to get the predicted target gene of Zuojin Pills acting on gastric cancer. Cytohubba, the plug-in of Cytoscape3.7.1 software was used to screen out key target genes. And the ONCOMINE database was used to analyze the expression of key target genes in gastric cancer. Gene ontology (GO) enrichment analysis was conducted by DAVID online tool and kyoto encyclopedia of genes and genomes (KEGG) pathway analysis was carried out using Cytoscape3.7.1 software. Results A total of 68 target genes and 15 key genes were screened for Zuojin Pills in the treatment of gastric cancer. There were significant differences in the expression of these key genes in gastric cancer samples and normal samples in ONCOMINE database. GO functional enrichment analysis showed that Zuojin Pills acting the predicted target gens of gastric cancer involved in a series of biological process, such as response to organic substance, negative regulation of apoptosis, negative regulation of programmed cell death, etc. KEGG pathway enrichment analysis mainly involved pathways in cancer, p53 signaling pathway, VEGF signaling pathway, etc. Conclusion This study preliminarily revealed the main targets of Zuojin Pills in the treatment of gastric cancer, and the action mechanism of multi-target, multi-dimensional regulation, synergistic effect and overall regulation, which can provide beneficial thinking for further deeper study on its action mechanism in the furture.
〔Keywords〕 ?Zuojin Pills; gastric cancer; network pharmacology; signaling pathway
胃癌(gastric cancer)是起源于胃上皮的腫瘤。胃癌在世界上最常見惡性腫瘤中排名第五,腫瘤相關死亡中排名第三,5年生存率僅為29%[1-3]。近年來雖然胃癌的總體發病率正在下降,但其在所有惡性腫瘤中,發病率仍居第二位,僅次于肺癌[4-5]。胃癌化療和放療效果欠佳[6],手術仍是其治療的重要手段,但遺憾的是大多數患者發現已是晚期,預后較差[7]。中醫藥治療胃癌有自己的特色與優勢,中醫藥在協同增效、降低西藥毒性、提高患者生存質量等方面發揮重要的作用,越來越受到人們的重視[8-9]。左金丸是經典方劑,由黃連和吳茱萸組成,近年來不少研究表明左金丸有較好的抗胃癌作用[10-12]。
網絡藥理學綜合了系統生物學、生物信息學、藥理學等多個學科的技術和知識,可構建藥物的“成分-靶標-通路-疾病”網絡,從整體水平、分子層面及多靶點、多通路深入探索藥物與疾病的關系,是研究藥物治療機制的一種新的有效手段[13-14],將該技術與方法引入中醫藥研究,從中藥研究、復雜疾病治療等生命科學的海量數據中,挖掘、發現、闡釋其中所包含生物學意義[15],可彌補傳統研究模式“一病一靶一藥”的不足,有助于從整體水平、分子層面全面深入闡明中藥多成分、多途徑、多靶點的綜合作用,從而為中醫藥研究提供新的思路。鑒于此,本研究借鑒系統生物學技術,采用網絡藥理學技術與方法,探索分析左金丸治療胃癌的潛在作用靶點和可能的分子機制,以期為后續研究及臨床應用提供理論依據。
1 材料與方法
1.1 ?左金丸的化學成分及作用靶點篩選
將左金丸所含中藥黃連和吳茱萸以完整拼音的形式輸入網絡在線數據庫TCMSP(http://lsp.nwu.edu.cn/tcmsp.php)進行檢索,根據口服生物利用度(oral bioavailability,OB)≥30%、類藥性(druglikeness,DL)≥0.18的標準,篩選出左歸丸所含中藥化合物,并通過查閱相關文獻與數據庫逐一核對驗證化合物的結構等基本信息,確保化合物分子的準確無誤;然后在TCMSP數據庫檢索上述篩選出的左歸丸化合物對應的相關作用靶點,并將其轉換為官方基因名。
1.2 ?疾病胃癌靶點篩選
通過檢索 Genecards數據庫(https://www.genecards.org/)和OMIM數據庫(https://www.omim.org/search/advanced/geneMap)篩選疾病胃癌相關靶點基因,建立胃癌靶點數據集。
1.3 ?網絡的構建及分析
將篩選出的左金丸的作用靶點與獲取的胃癌的疾病靶點,利用網絡在線工具Venny2.1.0(http://bioinfogp.cnb.csic.es/tools/venny/index.html)繪制韋恩圖,進行Venn分析,得到交集的共同靶點基因,即為左金丸作用于胃癌的預測靶基因。利用Cytoscape3.7.1軟件構建左金丸化合物-作用靶點-胃癌三者相互關系網絡。采用在線工具STRING(http://string-db.org)構建左金丸作用于胃癌的靶點蛋白相互作用(protein protein interaction, PPI)網絡。將蛋白種類參數設置為“人類”,最低相互作用閾值設為中等(>0.7),其他參數采用默認設置,獲得蛋白相互作用網絡。并將該蛋白相互作用網絡導入Cytoscape 3.7.1的軟件中,利用該軟件的插件cytohubba,根據網絡拓撲結構篩選關鍵靶基因,并利用ONCOMINE數據庫分析關鍵靶基因在胃癌中的表達情況。
1.4 ?基因本體(gene ontology,GO)功能富集分析
使用網絡在線工具DAVID(https://david.ncifcrf.Gov)的“functional annotation”模塊進行GO功能富集分析。將獲得的左金丸作用于胃癌的預測靶基因導入在線的DAVID數據庫,選擇物種參數為“homo sapiens”,選擇標識符參數為“official gene symbol”,選擇列表類型參數為“gene list”,其余參數為默認值,然后提交獲取GO功能富集結果。
1.5 ?京都基因和基因組百科全書(kyoto encyclopedia of genes and genomes, KEGG)通路富集分析
利用Cytoscape 3.7.1軟件的插件ClueGO對左金丸作用于胃癌的預測靶基因進行KEGG通路富集分析,設置參數為P<0.05,獲得左金丸治療胃癌的顯著富集的信號通路。
2 結果
2.1 ?左金丸化學成分及作用靶點篩選
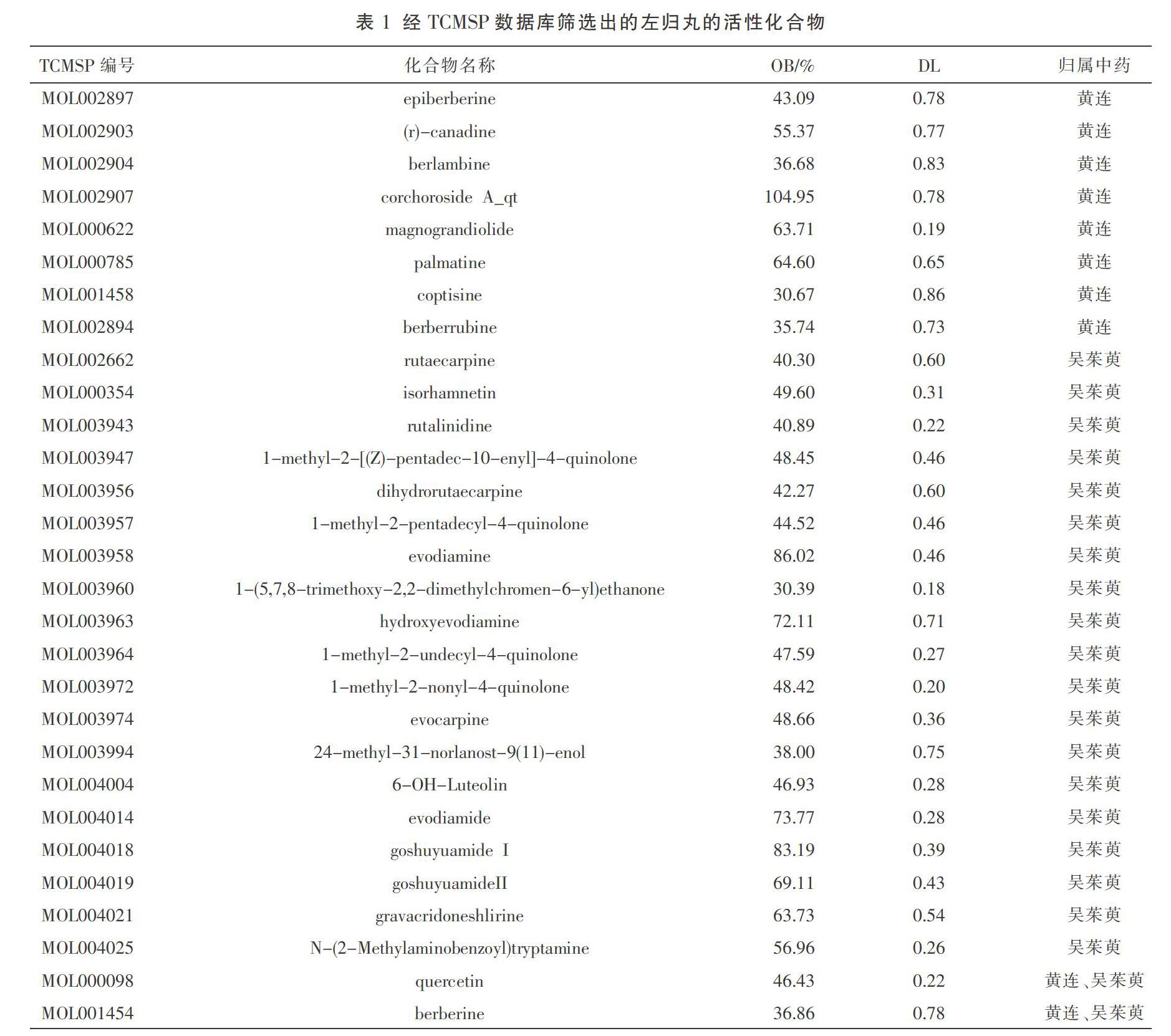
檢索TCMSP數據庫,初步獲得左金丸所含中藥黃連的化合物14個,作用靶點223個;吳茱萸的化合物30個,作用靶點449個;匯總并去重后,最終獲得左金丸的化合物共29個,其中黃連獨有的化合物8個,吳茱萸獨有的化合物19個,黃連與吳茱萸共同含有的化合物2個,見表1。去除重復項和非人種屬靶點,最終獲得左金丸的作用靶點共96個,其中黃連32個,吳茱萸64個,黃連與吳茱萸的共同作用靶點25個;然后運用Uniprot數據庫和NCBI數據庫將上述篩選的作用靶點轉換校正為官方基因名。
2.2 ?疾病胃癌靶點的篩選
檢索GeneCards數據庫,并以relevance score≥5的標準篩選出胃癌的靶點基因共2 110個;檢索OMIM數據庫得到胃癌的靶點基因共240個。將兩個數據庫的胃癌的靶點基因合并去重后,最終獲得胃癌靶點基因共2 260個。
2.3 ?網絡的構建及分析
將左金丸靶點基因與胃癌靶點基因數據導入在線軟件Venny 2.1.0繪制韋恩圖。通過韋恩圖(見圖1)分析發現,左金丸靶點與胃癌靶點交集靶點基因共68個,左金丸作用于胃癌靶基因映射率為3%,提示左金丸存在確切防治胃癌的作用靶點,對胃癌具有一定特異性的防治作用。利用Cytoscape 3.7.1軟件構建左金丸的化合物-作用靶點-疾病(胃癌)三者相互關系網絡,見圖2。該網絡圖生動明了地展示了左金丸的各成分、各靶點之間的相互聯系及多成分、多靶點相互作用的復雜網絡關系,充分體現了左金丸治療胃癌多途徑、多環節、多靶標、協同作用、整體調節的作用特點。
2.4 ?靶點蛋白相互作用網絡(PPI網絡)構建及關鍵靶點篩選
本研究使用在線工具STRING構建蛋白相互作用網絡(PPI網絡),見圖3。在此基礎上,利用Cytoscape 3.7.1的軟件的cytohubba插件,通過Degree、EPC、BottleNeck等12種網絡結構和節點間加權重聯系的計算分析算法,根據得分篩選出15個關鍵靶基因:MYC、CASP9、CASP3、EGFR、CCND1、VEGFA、CASP8、ESR1、FOS、ERBB2、AR、IL6、CCNB1、RB1、PGR,見圖4。提示這些基因在該網絡中發揮了關鍵作用,可能是左金丸治療胃癌的關鍵靶點。同時,利用ONCOMINE數據庫獲得上述關鍵靶基因在正常樣本和胃癌樣本中的表達情況(見圖5)。從圖5中可看出,15個關鍵靶基因在正常樣本和胃癌樣本中的表達存在顯著性差異(P<0.05),表明這些關鍵靶基因與胃癌的發生發展存在一定聯系。
2.5 ?GO功能富集分析
GO功能富集分析涵蓋生物學3個方面的內容:細胞組分(cellular component)、分子功能(molecular function)、生物過程(biological process)。本研究采用網絡在線工具DAVID對獲得的左金丸作用于胃癌的預測靶基因進行GO功能富集分析,結果共獲得679個功能富集,其中生物過程575個,細胞組分46個,分子功能58個,然后再依據P<0.05的基準,選取GO富集的前15位,進行可視化展示。GO功能富集分析提示,左金丸作用于胃癌的靶基因的生物過程主要涉及對有機物質的反應(response to organic substance)、細胞凋亡的負調控(negative regulation of apoptosis)、細胞程序性死亡的負調控(negative regulation of programmed cell death)等;細胞組分主要涉及微粒體(microsome)、細胞溶質(cytosol)、細胞內膜系統(endomembrane system)等;分子功能主要涉及配體依賴的核受體活性(ligand-dependent nuclear receptor activity)、類固醇結合(steroid binding)、轉錄因子活性(transcription factor activity)等,見圖6-8。
2.6 ?KEGG通路富集分析
采用Cytoscape 3.7.1軟件的ClueGO插件對左歸丸作用于胃癌的預測靶基因進行KEGG通路富集并進行可視化處理,設置參數P<0.05,共獲得61個通路富集,按照P值排序,排除明顯無關通路后,排名靠前的主要涉及癌癥通路(pathways in cancer)、p53信號通路(p53 signaling pathway)、VEGF信號通路(VEGF signaling pathway)等,表明左金丸治療胃癌的作用可能與上述通路有關。見圖9-10。
3 討論
左金丸出自著名醫家朱丹溪之《丹溪心法·火方》,方中黃連六兩、吳茱萸一兩,常用于胃部疾病[16]。現代研究顯示左金丸可抑制胃癌細胞增殖,且抑制作用呈濃度-時間依賴關系[17-18]。左金丸的主要活性成分吳茱萸堿和鹽酸小檗堿等可誘導胃癌細胞凋亡[19-21],吳茱萸堿和小檗堿可以通過阻滯胃癌細胞周期、抑制血管形成等發揮抗胃癌效應[22-24]。以上相關研究均表明,左金丸具有較好的抗胃癌作用,但與其相關的分子機制仍待研究。
本研究采用網絡藥理學方法,探討左金丸治療胃癌的分子機制,結果顯示:左金丸所含化學成分的作用靶點基因有96個,檢索相關數據庫獲得胃癌靶點基因共2 260個,左金丸靶點與胃癌靶點交集靶點基因共68個。同時,我們發現,左金丸每味中藥存在多個化學活性成分,每個中藥化學成分可作用于多個靶點,同一靶點可參與不同的信號通路及生物學過程,各個化學成分之間存在著密切的網絡藥理聯系,各靶標之間也存在相互作用關系。充分體現了左金丸多靶點、多途徑、多效應、協同作用、整體調節的作用特點。通過對68個交集靶基因進一步篩選,獲得了關鍵靶基因共15個:MYC、CASP9、CASP3、EGFR、CCND1、VEGFA、CASP8、ESR1、FOS、ERBB2、AR、IL6、CCNB1、RB1、PGR。其中MYC基因是較早發現的一組癌基因,包括C-myc,N-myc,L-myc。研究表明C-myc在胃癌的生長、遷移、凋亡方面發揮著重要的作用[25-27]。C-myc基因與DDX6基因有協同作用,在胃癌細胞中起癌基因的作用,促進胃癌的發展[28]。C-myc啟動子與ISL1結合可激活胃癌細胞中C-myc的表達,從而促進胃癌細胞增殖[29]。有多項研究表明Caspase-9與胃癌的發生發展密切相關[30-32]。此外,研究證實Caspase-3、Caspase-9的異常表達參與胃癌的發生、發展,兩者起正協同作用[33]。Caspase-9是細胞線粒體依賴的凋亡途徑中重要起始因子,Caspase-9的表達降低,使該凋亡途徑受到抑制,細胞凋亡異常,從而導致胃癌的發生[34]。
此外,本研究的KEGG通路富集分析結果顯示,左金丸作用于胃癌的靶點主要涉及癌癥通路、p53信號通路、VEGF信號通路等。p53是公認的腫瘤抑制基因,在細胞周期調控、DNA損傷修復、細胞分化和凋亡中發揮重要作用[35]。有研究表明miR-18a可通過靶向結合IRF2抑制p53信號通路,促進胃癌細胞的增殖、轉移和侵襲[36];此外,另一項研究提示miR-30可能作為一種致癌miRNA通過調節p53途徑調控線粒體凋亡[37];可見p53信號通路在胃癌中扮演重要角色,這與本研究通路富集結果提示左金丸主要通過干預p53信號通路等發揮抗癌作用是一致的,同時上述這些既往研究也在一定程度上證明了本研究結果的可靠性。
本研究從網絡藥理學角度,初步揭示左金丸治療胃癌的主要作用靶點及多靶點、多維調控、協同作用的分子機制,為后續進一步深入研究其作用機制奠定了基礎。但是,本研究主要基于網絡藥理學和生物信息學數據庫資料,因而存在一定的局限性,后續將在此基礎上,進行相關實驗驗證,以進一步闡釋左金丸抗胃癌的作用機制。
參考文獻
[1] 林果為,王吉耀,葛均波.實用內科學[M].15版.北京:人民衛生出版社,2017:1519.
[2] MACHLOWSKA J, MACIEJEWSKI R, SITARZ R. The pattern of signatures in gastric cancer prognosis[J]. International Journal of Molecular Sciences, 2018, 19(6): 1658-1664.
[3] AHMAD S A, XIA B T, BAILEY C E, et al. An update on gastric cancer[J]. Current Problems in Surgery, 2016, 53: 449-490.
[4] CHEN W, SUN K, ZHENG R, et al. Cancer incidence and mortality in China, 2014[J]. Chinese Journal of Cancer Research, 2018,30(1):1-12.
[5] ZHENG R, ZENG H, ZHANG S, et al. Estimates of cancer incidence and mortality in China, 2013[J]. Chinese Journal of Cancer Research, 2017, 36(1): 66.
[6] OZDEN S, OZGEN Z, OZYURT H, et al. Survival in gastric cancer in relation to postoperative adjuvant therapy and determinants[J]. World Journal of Clinical Cases, 2015, 3(1): 42-51.
[7] NAKAMURA T, OLNUMA T, YAMAGISHI H, et al. Evaluation of a novel high-resolution magnifying video endoscope that is capable of photodynamic diagnosis and therapy for gastric cancer[J]. Photodiagnosis and Photodynamic Therapy, 2014, 20: 135-142.
[8] 劉沈林.中醫藥治療胃癌臨床述評[J].江蘇中醫藥,2019,51(4):1-5.
[9] 田劭丹,陳信義.中醫藥治療惡性腫瘤特色與優勢[J].現代中醫臨床,2019,26(2):8-17.
[10] 孫夢瑤,王丹丹,吳秋雪,等.左金丸對胃癌耐藥細胞SGC-7901/DDP增殖和糖酵解的抑制作用[J].上海中醫藥大學學報,2019,33(1):71-75.
[11] PENG Q X, CAI H B, PENG J L, et al. Extract of Zuojin Pill induces apoptosis of SGC-7901 cells via mitochondria-dependent pathway[J]. Chinese Journal of Integrative Medicine, 2015, 21(11): 837-845.
[12] 張彥博,李 ?琦,劉艷娜,等.左金丸通過Wnt/β-catenin信號通路對幽門螺桿菌感染的人胃癌細胞轉移的影響[J].上海中醫藥大學學報,2015,29(2):44-47.
[13] ZUO J, WANG X, LIU Y, et al. Integrating network pharmacology and metabolomics study on anti-rheumatic mechanisms and antagonistic effects against methotrexate-Induced toxicity of Qing-Luo-Yin[J]. Frontiers in Pharmacology, 2018, 9: 1472-1487.
[14] YANG M, CHEN J, XU L, et al. A network pharmacology approach to uncover the molecular mechanisms of herbal formula Ban-Xia-Xie-Xin-Tang[J]. Evidence-based Complementary and Alternative Medicine, 2018, 2018: 4050714.
[15] 王程成,封 ?亮,劉 ?丹,等.結合生物信息學的中藥組分結構研究思路[J].中國中藥雜志,2015,40(22):4514-4519.
[16] 葉乃菁,劉 ?宣,李 ?琦.左金丸及其活性成分抗胃癌的實驗研究進展[J].中華中醫藥雜志,2014,29(4):1162-1164.
[17] 彭求賢,余惠旻,胡勝全,等.左金丸誘導人胃癌細胞SGC-7901凋亡的研究[J].江蘇中醫藥,2009,41(4):70-71.
[18] 湯慶豐,劉 ?宣,葛 ?艷,等.左金丸醇提物抑制幽門螺旋桿菌感染人胃癌細胞增殖及誘導凋亡的實驗研究[J].重慶醫學,2012,41(15):1462-1464.
[19] ZHU L H, BI W, LIU X D, et al. Induction of apoptosis by evodiamine involves both activation of mitotic arrest and mitotic slippage[J]. Oncology Reports, 2011, 26(6): 1447-1455.
[20] HUANG H, ZHANG Y, LIU X, et al. Acid sphingomyelinase contributes to evodiamine-induced apoptosis in human gastric cancer SGC-7901 cells[J]. DNA and Cell Biology, 2011, 30(6):407-412.
[21] 周紅祖,徐麗霞,余惠旻,等.左金方、黃連、吳茱萸誘導人胃癌細胞SGC-7901凋亡的作用比較[J].藥物分析雜志,2015,31(2):1160-1165.
[22] LIN J P, YANG J S, LEE J H, et al. Berberine induces cell cycle arrest and apoptosis in human gastric carcinoma SNU-5 cell line[J]. World Journal of Gastroenterology, 2006, 12(1): 21-28.
[23] RASUL A, YU B, ZHONG L, et al. Cytotoxic effect of evodiamine in SGC-7901 human gastric adenocarcinoma cells via simultaneous induction of apoptosis and autophagy[J]. Oncology Reports, 2012, 27(5): 1481-1487.
[24] LIN S, TSAI S C, LEE C C, et al. Berberine inhibits HIF-1alpha expression via enhanced proteolysis[J]. Molecular Pharmacology, 2004, 66(3): 612-619.
[25] BA M, LONG H, YAN Z, et al. BRD4 promotes gastric cancer progression through the transcriptional and epigenetic regulation of c-MYC[J]. Journal of Cellular Biochemistry, 2018, 119(1): 973-982.
[26] 馮海一,張友波,李柱虎.C-myc基因及蛋白在木脂素對人胃癌MGC-803細胞抗增殖過程中的作用[J].時珍國醫國藥,2015,26(2):381-383.
[27] YANG D D, CHEN Z H, YU K, et al. METTL3 promotes the progression of gastric cancer via targeting the MYC pathway[J].frontiers in Oncology, 2020, 10: 115-123.
[28] TANIGUCHI K, IWATSUKI A, SUGITO N, et al. Oncogene RNA helicase DDX6 promotes the process of C-myc expression in gastric cancer cells[J]. Molecular Carcinogenesis, 2018, 57(5):579-589.
[29] SHI Q, WANG W, JIA Z, et al. ISL1, a novel regulator of CCNB1, CCNB2 and C-myc gene, promotes gastric cancer cell proliferation and tumor growth[J]. Oncotarget, 2016, 7(24): 36489-36500.
[30] 楊 ?靜,程 ?玉,王明娟,等.Caspase-3、Caspase-9在胃癌組織中的研究進展[J].承德醫學院學報,2016,33(6):506-509.
[31] 文亞淵,劉寶華,付 ?濤.基因Survivin、Caspase-9在胃癌組織中的表達及其與胃癌發生的關系[J].中國腫瘤臨床,2005,32(17):969-972.
[32] PARK I C, PARK M J, HWANG C S, et al. Mitomycin C induces apoptosis in a caspase-dependent and Fas/CD95-independent manner in human gastric adenocarcinoma cells[J]. Cancer Letters, 2000, 158(2): 125-132.
[33] 楊 ?靜.凋亡相關基因Caspase-3、Caspase-9和c-IAP1在胃腺癌組織中的表達及意義[D].承德:承德醫學院,2017.
[34] 潘 ?科,盧書明,于勁達,等.胃癌及癌前病變細胞凋亡與caspase-9、Bax的關系[J].現代腫瘤醫學,2010,18(2):317-319.
[35] 張 ?健,王 ?冬,于景翠.胃癌中miRNA功能相關的信號通路[J].中國腫瘤生物治療雜志,2017,24(11):1331-1335.
[36] CHEN Y J, WU H, ZHU J M, et al. MicroRNA-18a modulates P53 expression by targeting IRF2 in gastric cancer patients[J]. Journal of Gastroenterology and Hepatology, 2015,31(1): 155-163.
[37] WANG J, JIAO Y, CUI L, et al. MiR-30 functions as an oncomiR in gastric cancer cells through regulation of P53-mediated mitochondrial apoptotic pathway[J]. Bioscience Biotechnology and Biochemistry, 2016, 81(1): 119-126.

