HPLC法同時測定珠芽景天藥材中8種黃酮苷類成分的含量
吳瑩瑩 雷艷 姚成芬 馬雪 黃勇 李勇軍 林昌虎
中圖分類號 R917 文獻標志碼 A 文章編號 1001-0408(2020)12-1436-04
DOI 10.6039/j.issn.1001-0408.2020.12.06
摘 要 目的:建立同時測定珠芽景天藥材中8種黃酮苷類成分含量的方法。方法:采用高效液相色譜法測定珠芽景天藥材中山柰酚-3-O-β-D-吡喃葡萄糖-(1→2)-α-L-吡喃葡萄糖-7-O-α-L-吡喃鼠李糖苷(KGGR)、山柰酚-3-O-β-D-吡喃葡萄糖-7-O-α-L-吡喃鼠李糖苷(KGR)、槲皮素-3-O-α-L-鼠李糖-7-O-α-L-鼠李糖苷(QRR)、BulbiferumosideⅡ、山柰酚-3-O-(6-香豆酰基)-β-D-葡萄糖-(1→2)-β-D-葡萄糖-7-O-α-L-鼠李糖苷(KcGGR)、山柰酚-3-O-(2-β-D-葡萄糖)-α-L-鼠李糖-7-O-α-L-鼠李糖苷(KGRR)、山柰酚-3-O-α-L-鼠李糖苷-7-O-α-L-鼠李糖苷(KRR)、山柰酚-3-O-(6″-乙酰基-β-D-葡萄糖)-7-O-α-L-鼠李糖苷(KaGR)的含量。色譜柱為Waters CORTECS C18,流動相為乙腈-0.1%磷酸水溶液(梯度洗脫),流速為0.8 mL/min,檢測波長為254 nm,柱溫為35 ℃,進樣量為5 μL。結果:上述8種成分均達到基線分離,檢測進樣量的線性范圍分別為0.013~0.052、0.005~0.018、0.008~0.031、0.010~0.042、0.009~0.038、0.008~0.030、0.009~0.037、0.032~0.130 μg(r均不低于0.999 0);檢測限分別為0.08、0.14、0.11、0.21、0.42、0.35、0.23、0.28 μg/mL,定量限分別為0.25、0.47、0.38、0.69、1.40、1.17、0.77、0.93 μg/mL;精密度、重復性、穩定性(24 h)試驗的RSD均小于3%(n為6或7);平均加樣回收率為99.67%~104.20%(RSD為0.17%~1.59%,n=6)。13批樣品中,上述8種成分的平均含量分別為0.893 8、0.312 6、0.490 8、0.964 9、0.751 2、0.502 2、0.606 2、1.915 7 mg/g(n=3)。結論:該方法簡便、準確、重復性好,可用于同時測定珠芽景天藥材中8種黃酮苷類成分的含量。
關鍵詞 珠芽景天;高效液相色譜法;黃酮苷類成分;含量測定
Simultaneous Determination of 8 Flavonoid Glycosides in Sedum bulbiferum by HPLC
WU Yingying1,2,LEI Yan1,2,YAO Chengfen1,2,MA Xue1,HUANG Yong3,LI Yongjun1,LIN Changhu1(1. Engineering Research Center for the Development and Application of Ethnic Medicine and TCM/State Key Laboratory of Functions and Applications of Medicinal Plants, Guizhou Medical University, Guiyang 550004, China; 2. School of Pharmacy, Guizhou Medical University, Guiyang 550004, China; 3. Guizhou Provincial Key Laboratory of Pharmaceutics, Guizhou Medical University, Guiyang 550004, China)
ABSTRACT ? OBJECTIVE: To establish a method for simultaneous determination of 8 flavonoid glycosides in Sedum bulbiferum. METHODS: HPLC method was adopted to determine the contents of kaempferol-3-O-β-D-glucopyranoside-(1→2)-α-L-glucopy- ranoside-7-O-α-L-glucopyranoside (KGGR), kaempferol-3-O-β-D-glucopyranosyl-7-O-α-L-rhamnopyranoside (KGR), quercetin-3- O-α-L-rhamnose-7-O-α-L-rhamnoside (QRR), BulbiferumosideⅡ, kaempferol-3-O-(6-coumarinyl)-β-D-glucose-(1→2)-β-D-glu- cose-7-O-α-L-rhamnoside (KcGGR), kaempferol-3-O-(2-β-D-glucose)-α-L-rhamnose-7-O-α-L-rhamnoside (KGRR), kaempferol-3- O-α-L-rhamnoside-7-O-α-L-rhamnoside (KRR), kaempferol-3-O-(6″-acetyl-β-D-glucose)-7-O-α-L-rhamnoside (KaGR) in S. bulbi- ferum. The determination was performed on Waters CORTECS C18 column with mobile consisted of acetonitrile -0.1% phosphoric acid water solution (gradient elution) at the flow rate of 0.8 mL/min. The detection wavelength was set at 254 nm, and column temperature was 35 ℃. The sample size was 5 μL. RESULTS: The linear range of 8 constituents were 0.013-0.052, 0.005-0.018, 0.008-0.031, 0.010-0.042, 0.009-0.038, 0.008-0.030, 0.009-0.037, 0.032-0.130 μg, respectively (all r were not less than 0.999 0). The limits of detection were 0.08, 0.14, 0.11, 0.21, 0.42, 0.35, 0.23, 0.28 μg/mL,respectively. The limits of quantification were 0.25, 0.47, 0.38, 0.69, 1.40, 1.17, 0.77, 0.93 μg/mL, respectively. RSDs of precision, reproducibility and stability tests (24 h) were all lower than 3% (n=6 or n=7). The average recoveries were 99.67%-104.20% (RSDs=0.17%-1.59%, n=6). Average contents of above 8 constituents in 13 batches of samples were 0.893 8, 0.312 6, 0.490 8, 0.964 9, 0.751 2, 0.502 2, 0.606 2, 1.915 7 mg/g(n=3). CONCLUSIONS: The method is simple, acourate and reproducible, and can be used for simultaneous determination of 8 flavonoid glycosides in ? ? ? ?S. bulbiferum.
KEYWORDS Sedum bulbiferum; HPLC; Flavonoid glyco- sides; Content determination
珠芽景天為景天科植物珠芽景天(Sedum bulbiferum Makino.)的干燥全草,又名小箭草、珠芽半支,廣泛分布于我國南部地區,野生資源豐富,是我國民間常用的植物藥,可用于治療寒熱瘧疾、食積腹痛、熱毒癰腫等癥[1-3]。化學成分研究顯示,珠芽景天主要含有生物堿類、多糖類、三萜類、黃酮類、礦質元素等化學成分[4-9]。本課題組前期研究中發現,黃酮類化合物為珠芽景天的主要成分,并分離得到以山柰酚、槲皮素為母核的苷類化合物,包括山柰酚-3-O-β-D-吡喃葡萄糖-(1→2)-α-L-吡喃葡萄糖-7-O-α-L-吡喃鼠李糖苷(KGGR)、山柰酚-3-O-β-D-吡喃葡萄糖-7-O-α-L-吡喃鼠李糖苷(KGR)、槲皮素-3-O-α-L-鼠李糖-7-O-α-L-鼠李糖苷(QRR)、BulbiferumosideⅡ、山柰酚-3-O-(6-香豆酰基)-β-D-葡萄糖-(1→2)-β-D-葡萄糖-7-O-α-L-鼠李糖苷(KcGGR)、山柰酚-3-O-(2-β-D-葡萄糖)-α-L-鼠李糖-7-O-α-L-鼠李糖苷(KGRR)、山柰酚-3-O-α-L-鼠李糖苷-7-O-α-L-鼠李糖苷(KRR)、山柰酚-3-O-(6″-乙酰基-β-D-葡萄糖)-7-O-α-L-鼠李糖苷(KaGR)等。已有藥理活性研究表明,珠芽景天的黃酮類成分對人肝癌細胞株HepG2、人食管癌細胞株EC109、人結腸癌細胞株SW480的體外增殖有抑制作用[10-11]。
中藥成分復雜多樣且質量不易控制,這在一定程度上制約了中藥的研究與開發。目前,有關珠芽景天質量控制的研究報道較少,僅見黃酮苷元槲皮素和山柰素的定量研究[10-11],然而僅通過單一化學成分的含量測定難以全面評估珠芽景天的質量。近年來,多指標含量測定已廣泛應用于中藥材的質量控制,如白花蛇舌草、大黃、三葉青等[12-14]。因此,本研究擬建立同時測定珠芽景天藥材中上述8種主要黃酮苷類成分含量的高效液相色譜法(HPLC),旨在為該藥材的質量控制研究提供參考。
1 材料
1.1 儀器
UltiMate 3000型HPLC儀,包括系統控制器、輸液泵、脫氣組件、低壓梯度組件、自動進樣器、柱溫箱、溫控樣品室、二極管陣列檢測器、Chromeleon 7.0色譜數據工作站(美國Thermo Fisher Scientific公司);Allegra 64R型低溫高速離心機(美國Beckman Coulter公司);WP-UP-Ⅳ-20型超純水機(四川沃特爾科技發展有限公司);EL204型電子天平[梅特勒-托利多儀器(上海)有限公司]。
1.2 藥品與試劑
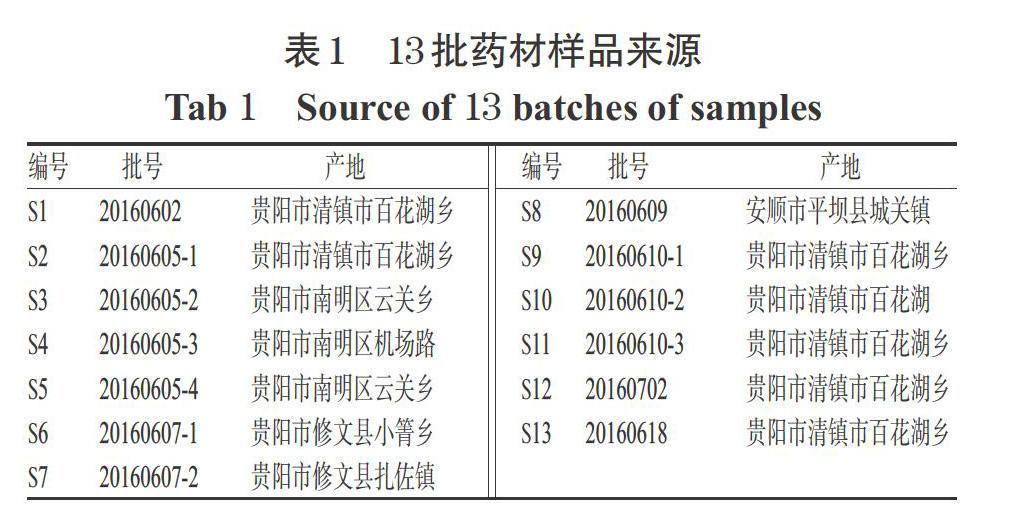
珠芽景天藥材采自貴州省各地,經貴州中醫藥大學藥學院孫慶文教授鑒定為景天科景天屬植物珠芽景天(S. bulbiferum Makino.)的干燥全草,13批藥材樣品來源見表1。KGGR、KGR、QRR、BulbiferumosideⅡ、KcGGR、KGRR、KRR、KaGR對照品均為本實驗室自制,經HPLC面積歸一法檢測純度均大于98.0%;乙腈、甲醇均為色譜純,其余試劑均為分析純,水為超純水。
2 方法與結果
2.1 色譜條件
色譜柱:Waters CORTECS C18(150 mm×4.6 mm,2.7 μm);流動相:乙腈(A)- 0.1%磷酸水溶液(B);梯度洗脫(0~5 min,5%A→12%A;5~15 min,12%A→13%A;15~30 min,13%A;30~45 min,13%A→14%A;45~60 min,14%A→15%A);流速:0.8 mL/min;柱溫:35 ℃;檢測波長:254 nm;進樣量:5 μL。
2.2 溶液的制備
2.2.1 混合對照品溶液的制備 取KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR對照品適量,精密稱定,分別用甲醇溶解并定容至10 mL量瓶中,得單一對照品貯備液。精密吸取上述單一對照品貯備液各適量,置于同一10 mL量瓶中,用甲醇溶解并稀釋至刻度,制成每1 mL含KGGR 13.0 μg、KGR 4.6 μg、QRR 7.7 μg、Bulbiferumoside Ⅱ 10.4 μg、KcGGR 9.4 μg、KGRR 7.5 μg、KRR 9.3 μg、KaGR 32.4 μg的混合對照品溶液,保存于4 ℃冰箱中,備用。
2.2.2 供試品溶液的制備 取珠芽景天藥材適量,粉碎后,過40目篩。精密稱取上述粉末1 g,加入50%乙醇20 mL,稱定質量后,水浴加熱回流1 h,冷卻至室溫,再次稱定質量,用50%乙醇補足減失質量,搖勻,以12 000 r/min離心10 min,取上清液,即得供試品溶液。
2.3 方法學考察
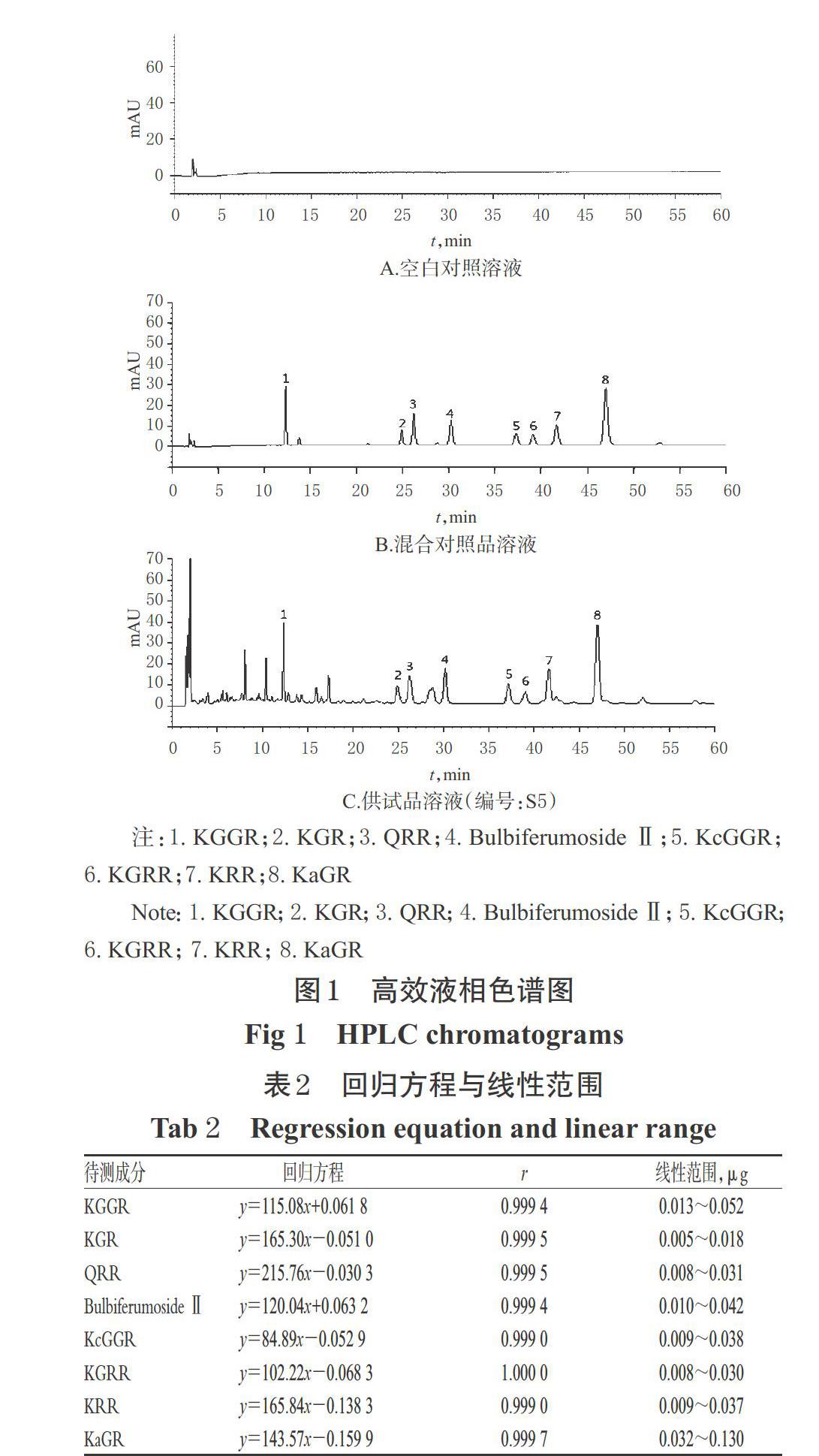
2.3.1 專屬性考察 精密吸取空白對照溶液(甲醇溶液)和“2.2”項下供試品溶液(編號:S5)、混合對照品溶液適量,空白對照溶液和供試品溶液按“2.1”項下色譜條件進樣測定,混合對照溶液用甲醇稀釋5倍后進樣測定,記錄色譜圖,詳見圖1。結果,在該色譜條件下,KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR的分離度均良好,且色譜峰峰形對稱,理論板數按QRR峰計均不低于17 000。
2.3.2 標準曲線繪制 精密吸取“2.2.1”項下混合對照品溶液1.0 mL,置于5 mL量瓶中,加甲醇溶解稀釋至刻度,制成KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR質量濃度分別為2.60、0.92、1.54、2.08、1.88、1.50、1.86、6.48 μg/mL的混合溶液,分別精密吸取5、8、10、12、15、18、20 μL,按“2.1”項下色譜條件進樣測定,記錄峰面積。以待測成分進樣量(x,μg)為橫坐標、峰面積(y)為縱坐標進行線性回歸,結果見表2。
2.3.3 檢測限與定量限考察 取“2.2.1”項下混合對照品溶液適量,以甲醇倍比稀釋,按“2.1”項下色譜條件進樣測定,以信噪比10 ∶ 1、3 ∶ 1分別確定其定量限、檢測限。結果,KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR的檢測限分別為0.08、0.14、0.11、0.21、0.42、0.35、0.23、0.28 μg/mL,定量限分別為0.25、0.47、0.38、0.69、1.40、1.17、0.77、0.93 μg/mL。
2.3.4 精密度試驗 取同一批珠芽景天(編號:S5)供試品溶液,按“2.1”項下色譜條件連續進樣測定6次,記錄峰面積。結果,KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR峰面積的RSD分別為0.48%、0.96%、0.86%、0.86%、0.39%、0.77%、0.82%、0.83%(n=6),表明方法精密度良好。
2.3.5 重復性試驗 取同一批珠芽景天藥材(編號:S5)粉末,按“2.2.2”項下方法平行制備供試品溶液6份,再按“2.1”項下色譜條件進樣測定,記錄峰面積,按標準曲線法計算各待測成分的含量。結果,KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR含量的RSD分別為1.00%、0.47%、2.15%、1.66%、2.53%、2.72%、2.71%、1.17%(n=6),表明方法重復性良好。
2.3.6 穩定性試驗 取同一批珠芽景天藥材(編號:S5)粉末,按“2.2.2”項下方法制備供試品溶液,分別于室溫下放置0、1、2、4、8、12、24 h時按“2.1”項下色譜條件進樣測定,記錄峰面積。結果,KGGR、KGR、QRR、Bulbiferumoside Ⅱ、KcGGR、KGRR、KRR和KaGR峰面積的RSD分別為1.39%、1.29%、1.99%、1.90%、1.80%、1.97%、1.10%、0.84%(n=7),表明供試品溶液在室溫下放置24 h內穩定性良好。
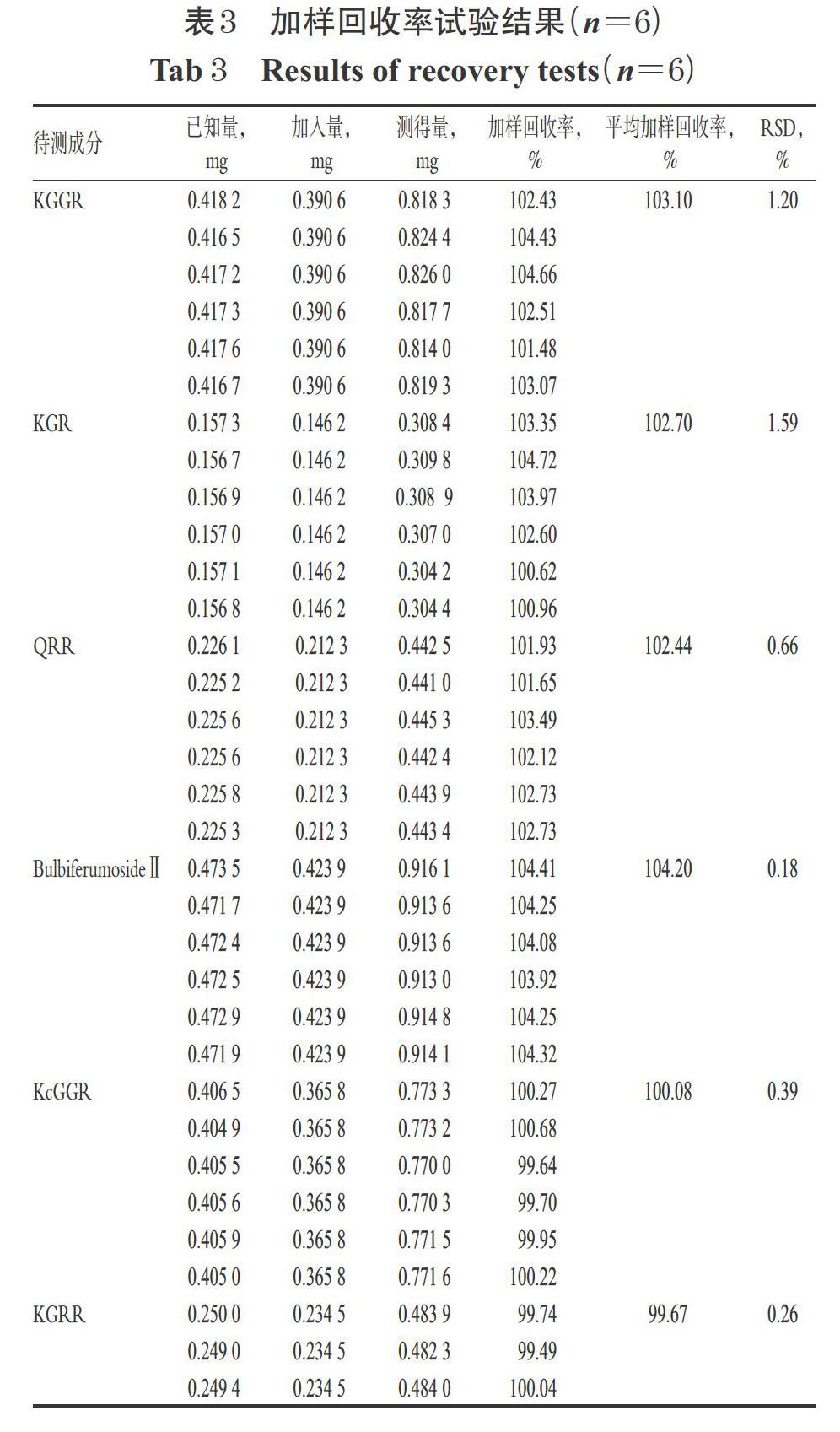
2.3.7 加樣回收率試驗 取已知含量的珠芽景天藥材(編號:S5)粉末,共6份,每份約0.5 g,精密稱定,分別按各成分在藥材中的含量等量加入相應單一對照品貯備液,按“2.2.2”項下方法制備供試品溶液,再按“2.1”項下色譜條件進樣測定,記錄峰面積并計算加樣回收率,結果見表3。
2.4 樣品含量測定
稱取13批珠芽景天藥材粉末各1 g,精密稱定,按“2.2.2”項下方法制備供試品溶液,再按“2.1”項下色譜條件進樣測定,記錄峰面積,按標準曲線法計算8種黃酮苷類成分的含量。每批平行操作3次,結果見表4。
由表4結果可見,所測13批珠芽景天藥材中8種黃酮苷類成分含量差異不大,其中平均含量最高的是KaGR(1.915 7 mg/g),平均含量最低的是KGR(0.312 6 mg/g)。
3 討論
3.1 供試品溶液制備方法選擇
本課題組前期分別考察了提取方法(超聲、回流)、提取溶劑[水、不同體積分數(100%、75%、50%、25%)的甲醇和乙醇]、提取時間(0.5、1、2、4 h)對珠芽景天提取率的影響。結果發現,以50%乙醇回流1 h的提取率較高,且提取時間適宜,故最終選擇此方法作為供試品溶液的制備方法。
3.2 色譜條件選擇
本課題組前期分別對色譜柱(ACE Excel 5 C18-AR、ACE Excel 5 C18、Waters CORTECS C18)、流動相(乙腈-0.1%磷酸水溶液、乙腈-0.1%甲酸水溶液、甲醇-0.1%磷酸水溶液、甲醇-0.1%甲酸水溶液)、流速(0.8、1.0、1.2 mL/min)進行了考察。結果發現,當色譜柱為Waters CORTECS C18、流動相為乙腈-0.1%磷酸水溶液(梯度洗脫)時,珠芽景天中8種黃酮苷類成分的色譜峰峰形、分離度均較好,且基線平穩,故最終選用此色譜條件。本課題組在全波長掃描時發現,珠芽景天中這8種黃酮苷類成分均在254 nm波長處有較理想的色譜響應,且與其他雜質峰分離度也較好,故選擇254 nm波長作為檢測波長。
綜上所述,本研究所建方法操作簡便,準確度、精密度高,重復性、穩定性好,可用于同時測定珠芽景天藥材中8種黃酮苷類成分的含量,可為其質量控制及進一步開發利用提供方法支持。
參考文獻
[ 1 ] 《貴州植物志》編輯委員會.貴州植物志:第2卷[M].貴陽:貴州人民出版社,1986:198.
[ 2 ] 《全國中草藥匯編》編寫組.全國中草藥匯編:下冊[M].北京:人民衛生出版社,2000:481.
[ 3 ] 萬定榮.垂盆草及其同屬(景天屬)藥用種的民族醫療應用[J].時珍國醫國藥,2007,18(8):1853-1855.
[ 4 ] KIM JH,THART H,STEVENS JF. Alkaloids of some Asian Sedum species[J]. Phytochemistry,1996,41(5):1319-1324.
[ 5 ] 《湖南植物志》編輯委員會.湖南藥物志:第5卷[M].長沙:湖南科學技術出版社,2004:3392-3393.
[ 6 ] 江蘇新醫學院.中藥大辭典:上冊[M].上海:上海科學技術出版社,1986:260.
[ 7 ] WARASHINA T,MIYASE T. Flavonoid glycosides from Sedum bulbiferum[J]. Chem Pharm Bull:Tokyo,2017,65(12):1199-1204.
[ 8 ] 姚成芬,汪洋,蔣禮,等.珠芽景天的化學成分研究[J].中藥材,2018,41(6):1369-1371.
[ 9 ] 楊耿,鞏吉力,鄭艷,等.珠芽景天的礦質元素分析[J].基層中藥雜志,2000,14(3):8-9.
[10] 胡婧.珠芽景天的鑒定、黃酮類成分含量測定及抗腫瘤活性研究[D].武漢:中南民族大學,2012.
[11] 胡婧,王璐瑤,萬定榮,等.珠芽景天抗腫瘤活性研究及槲皮素和山柰素的含量測定[J].中國實驗方劑學雜志,2013,19(24):139-142.
[12] 段和祥,劉緒平,陳希,等. HPLC法同時測定白花蛇舌草中6種有機酸類成分的含量[J].中藥材,2019,42(8):1842-1845.
[13] 陸文瑾,竇志華,曹瑞,等. HPLC法同時測定大黃藥材中8個非蒽醌類成分的含量[J].中國藥房,2019,30(14):1975-1980.
[14] 李彩鳳,胡欣,金鵬飛,等. HPLC法同時測定三葉青塊根中6個黃酮類成分的含量[J].中國藥房,2019,30(13):1755-1758.
(收稿日期:2020-01-17 修回日期:2020-04-06)
(編輯:鄒麗娟)

