澳大利亞藥品特別準入計劃對完善我國同情用藥制度的啟示
任磊 張麗楊 韓丹 柴逸峰 張黎 舒麗芯
中圖分類號 R95 文獻標志碼 A 文章編號 1001-0408(2020)12-1409-05
DOI 10.6039/j.issn.1001-0408.2020.12.01
摘 要 目的:為完善我國同情用藥制度體系提供國外經驗借鑒。方法:對澳大利亞藥品特別準入計劃(SAS)的申請人、藥品范圍、申請途徑、處理流程、主體職責、費用支付等具體內容進行介紹和分析,并對我國同情用藥相關制度的完善提出建議。結果與結論:澳大利亞醫療用品管理局(TGA)根據病情的嚴重程度以及藥品安全性將SAS分為3類通道,對于病情十分緊急的患者可通過SAS-A類通道,對于安全性相對較高的藥品可通過SAS-C類通道,通知TGA后即可直接使用未批準藥品;其他情況需通過SAS-B類通道以“申請-審評”的形式向TGA提出申請,經審評通過后方可實現同情用藥。澳大利亞SAS制度體系對醫師、政府監管機構、贊助商的相關職責均作了詳細規定,形成了相對完善的制度體系。建議我國建立多種同情用藥申請通道,構建多層次同情用藥評估體系,并與現有制度有機銜接,以構建完善的同情用藥體系,提高藥品的可及性,使藥物研發成果能夠更加及時地惠及臨床。
關鍵詞 澳大利亞;特別準入計劃;同情用藥制度
Enlightenment of Australias Drug Special Access Scheme to the Improvement of Chinas Sympathetic Drug Use System
REN Lei1,ZHANG Liyang2,HAN Dan1,CHAI Yifeng3,ZHANG Li4,SHU Lixin5(1. Demonstration Center of Military Medical Supply, School of Pharmacy, Naval Medical University, Shanghai 200433, China; 2. Chinese Pharmaceutical Association,Beijing 100050,China; 3. Dept. of Pharmaceutical Analysis, School of Pharmacy, Naval Medical University, Shanghai 200433, China; 4. Dept. of Pharmacy, Changhai Hospital, Navy Medical University,Shanghai 200433, China;5. Dept. of Military Medical Supply Administration, School of Pharmacy, Naval Medical University, Shanghai 200433, China)
ABSTRACT ? OBJECTIVE: To provide foreign experience for the improvement of sympathetic drug use system in China. METHODS: Australias Special Access Scheme (SAS) was introduced and analyzed in respects of applicant, drug scope, application method, processing flow, main responsibilities, drug payment and other specific content. The suggestion were put forward for the improvement of sympathetic drug use system in China. RESULTS & CONCLUSIONS: Therapeutic Goods Administration (TGA) divided SAS into 3 channels according to disease severity and drug safety, the patients with very urgent medical conditions could use drugs directly through SAS-A channel, and unapproved drugs with relatively high safety can also be used directly through SAS-C channel after informing TGA; in other conditions, drugs can be used through SAS-B channel by the form of “application-evaluation” after approved by TGA. At the same time, Australia has made detailed regulations on the responsibilities of doctors, government regulators and sponsor in the system, forming a relatively perfect system. In order to improve compassionate use system, improve the feasibility of drugs, make drug research and development results more timely benefit clinical, its suggested that we should establish multiple application channels, construct the multi-level drug evaluation system and connect with the existing system well.
KEYWORDS ? Australia; Special Access Scheme; Sympathetic drug use system
同情用藥制度是指參照特殊的制度安排,允許已窮盡現有醫療救治手段的危重患者使用尚未批準上市的藥物,該制度對于挽救特定患者的生命具有重要意義[1]。同情用藥在不同國家或地區具有不同名稱或形式,例如美國稱為“擴展使用”、英國稱為“早期獲取藥物計劃”、法國稱為“臨時使用授權”等[2],而我國則以“拓展性臨床試驗”的形式實現同情用藥。因新藥上市審批時間相對較長,藥物研發成果無法及時惠及臨床,2017年10月8日,我國發布《關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見》,明確提到要“支持拓展性臨床試驗”;2017年12月20日,國家食品藥品監督管理總局公布《拓展性同情使用臨床試驗用藥物管理辦法(征求意見稿)》(以下簡稱“《管理辦法(征求意見稿)》”);2019年12月1日實施的新版《藥品管理法》第二十三條在法律層面確立了我國同情用藥制度,并對其適用條件和程序作了概括性規定[3]。我國同情用藥制度建立不久,在制度的具體內容、配套措施等方面尚未作出詳細規定,可操作性有限,且尚無同情用藥的具體實踐;而澳大利亞已具有相對成熟的同情用藥制度體系,每年有超過6萬份同情用藥申請。鑒于此,本文對澳大利亞同情用藥制度體系進行介紹和分析,以期對我國同情用藥制度的完善提供經驗借鑒。
1 澳大利亞未批準藥品使用通道概述
擬在澳大利亞上市藥品的持有人必須向澳大利亞藥品注冊管理機構即醫療用品管理局(Therapeutic Goods Administration,TGA)提出注冊或登記申請(TGA根據藥品成分及使用情況將藥品分為注冊類藥品與登記類藥品),并將藥品列入澳大利亞醫療用品登記/注冊表(Australian register of therapeutic goods,ARTG)[4]。截至2019年10月,ARTG中共有藥品90 988種[5]。而未包含在ARTG中的治療藥品稱為“未批準藥品”。
在澳大利亞,患者可以通過4種通道使用未批準藥品,即“處方者授權計劃(Authorized prescriber scheme,APS)”通道、“特別準入計劃(Special access scheme,SAS)”通道[6]、臨床試驗通道和“個人用藥進口”通道[7]。其中,APS是指經澳大利亞人類研究倫理委員會批準或其他途徑認可的特定執業醫師可以自行決定對患有特定疾病的一類患者使用未批準藥品中被TGA認定該藥品在國內外某特定情形下有既定預期用途的使用歷史、且在3年內沒有發生與該藥品相關的重大安全問題的治療藥品;SAS則允許執業醫師或其他醫務人員對單個患者使用未批準藥品。一般來講,APS的藥品范圍僅局限于未批準藥品中有相關使用歷史的藥品,且僅授權給具有一定資質的執業醫師,并適用于多個患者;而SAS則適用于所有未批準藥品,并且除執業醫師外,其他醫務人員也可能具有相關處方資質,但僅適用于單個患者。此外,二者在用藥權限上也存在區別,通過APS通道使用未批準藥品時不必通知TGA或向TGA提出申請,而SAS則需要。由于我國目前并沒有公布未批準但被認為有使用歷史的治療藥品目錄,且醫師在同情用藥中的自主權也相對不高,故澳大利亞APS制度在短期內尚不適于我國國情。鑒于此,本文重點對澳大利亞的SAS制度進行介紹。臨床試驗通道是指患者參與該藥品的注冊臨床試驗獲得藥品治療;“個人用藥進口”通道是指個人為了讓本人或直系親屬使用某藥品而從國外帶回本國或向海外供貨商購買該藥品,以上兩種通道均不屬于同情用藥的研究范疇,故本文不作討論。
2 澳大利亞SAS制度
根據澳大利亞《治療用品法令》第19(7A)條規定,為了保障患者生命健康,在特定情況下可允許對單個患者使用未批準藥品,即SAS。SAS包括SAS-A類通知、SAS-B類申請和SAS-C類通知等3類。據TGA統計,2019年7-12月共收到A類通知23 859份, B類申請27 714份, C類通知8 654份[8]。
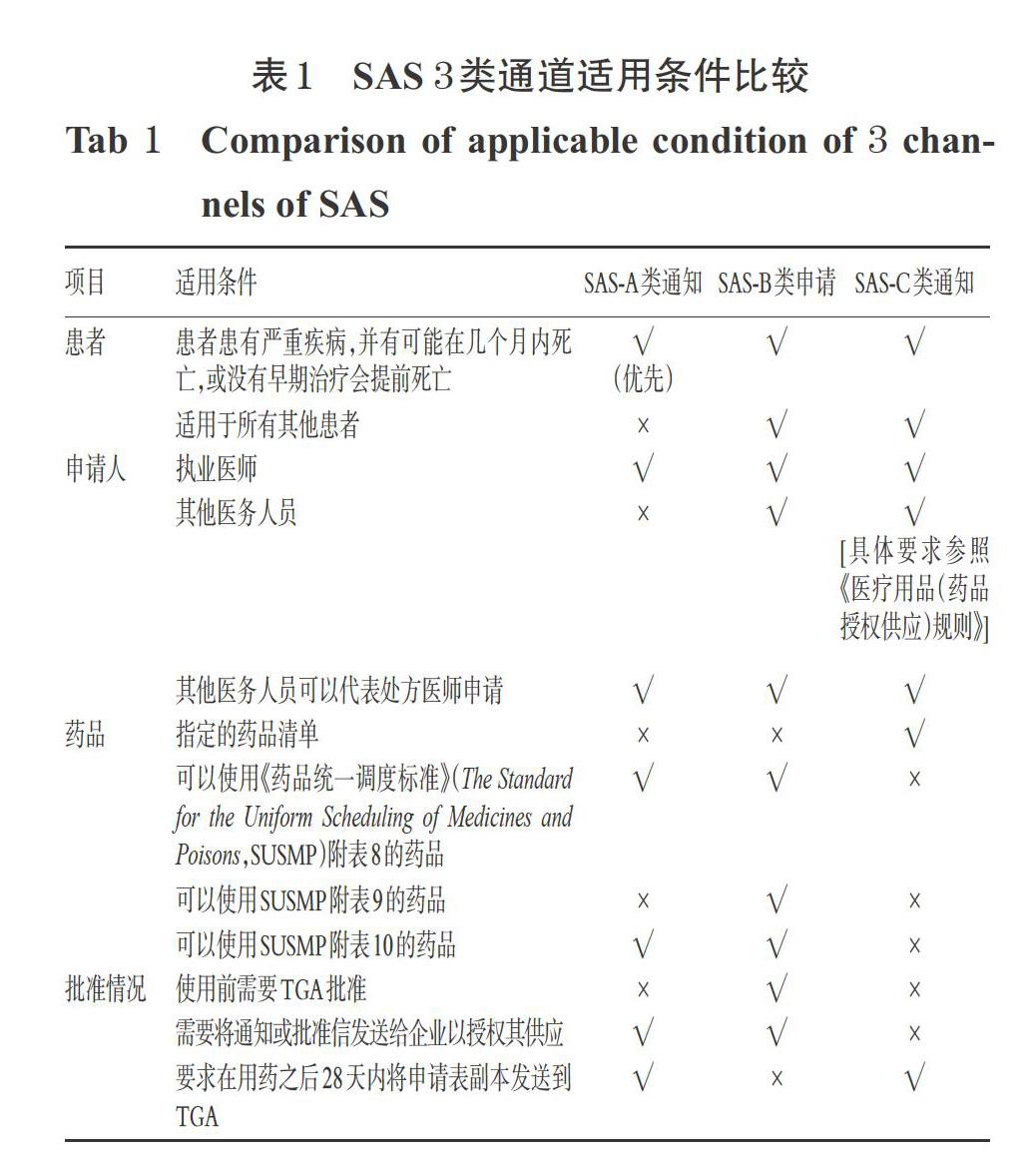
SAS的3類通道具有不同的適用條件:當患者患有可能會在幾個月內死亡或沒有早期治療會提前死亡的嚴重疾病,申請人可按通知的形式,在向TGA提交資料后對患者使用符合要求的藥品,此為SAS-A類通知;對于有使用歷史的未批準藥品,申請人也可按通知的形式,在向TGA提交資料后對患者使用,此為SAS-C類通知;如果患者不符合SAS-A類通知要求,同時又不適用SAS-C類通知通道,醫務人員可向TGA提出申請,經TGA批準之后使用未批準藥品對患者進行治療,此為SAS-B類申請。值得一提的是,SAS-C類通知的藥品清單與APS制度使用的藥品清單一致,該清單由TGA根據澳大利亞《醫療用品(藥品授權供應)規則》[Therapeutic Goods(Authorised Supply of Medicines)Rules]確定。SAS 3類通道適用條件比較詳見表1(表中,“√”表示適用,“×”表示不適用)。
2.1 SAS 3類通道的申請人
SAS-A類通道的申請人為具有處方權的執業醫師,也可以是代表執業醫師的其他醫務人員。其他醫務人員包括土著居民和托雷斯海峽島民醫師(Aboriginal and Torres Strait Islander health practitioner,ATSIHP)、牙醫、放射科技師、護士、助產士、職業治療師、驗光師、藥劑師、足科醫師、心理醫師等[9]。SAS-B類和SAS-C類通道的申請人除具有處方權的執業醫師和代表處方醫師的其他醫務人員外,還可以由其他醫務人員直接申請。之所以存在這樣的區別,主要考慮A類通道患者通常患有十分嚴重的疾病,其用藥應更為慎重,因此對于申請人的要求也更為嚴格。
2.2 SAS 3類通道適用的藥品范圍
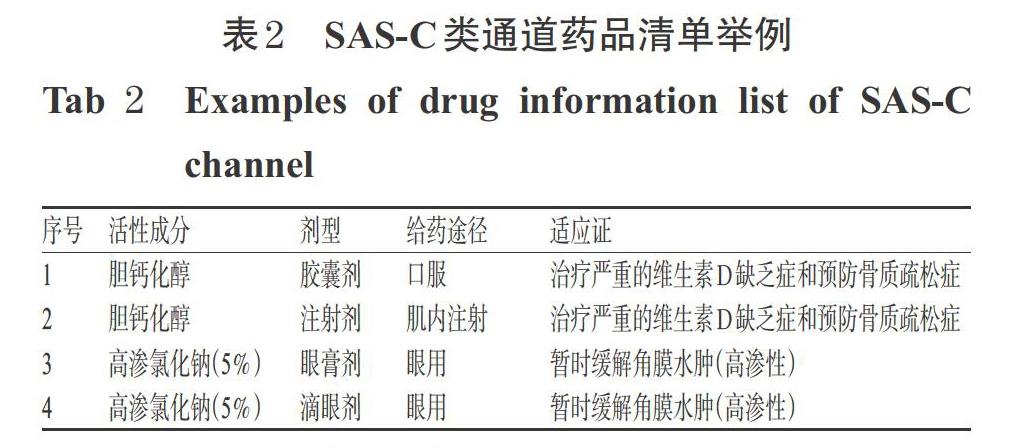
SAS允許申請人對患者使用的未批準藥品包括還在試驗或研究中的藥品、已經由其他人進行臨床試驗的藥品、在海外銷售但未在澳大利亞銷售的藥品[7]、因商業或其他原因從澳大利亞市場撤出的藥品[9]。同時,SAS還給出了負面清單,例如,澳大利亞衛生部發布的SUSMP附表8收錄了受澳大利亞政府管控的藥品(例如安非他明、丁丙諾啡等),附表9為違禁藥品(例如醋托啡、麥角二乙胺等),附表10為毒性藥品(例如苦杏仁苷等)。經SAS-A類通道對患者使用的藥品不得含有附表9中列舉的成分;經SAS-C類通道對特定患者使用的藥品清單為澳大利亞政府接受《藥品和醫療器械監管專家審查》建議并具有使用歷史的未批準藥品,該藥品清單以法律文件的形式刊載于衛生部發布的《醫療用品(藥品授權供應)規則》中(現行版本于2019年9月發布,共計78個品規[10]),且規定了藥品的活性成分(濃度)、劑型、給藥途徑、適應證等,詳見表2。
2.3 SAS 3類通道的申請途徑
如果需要進行SAS用藥,申請人可從TGA官方網站下載相應表格(3類通道的表格不同),并進行填寫。為減少申請處理的時間,TGA于2018年7月30日發布了“SAS線上系統”,申請人可以在線提交SAS申請或通知。該申請系統可用于查詢申請狀態(針對SAS-B類申請)、搜索歷史申請或通知、患者詳細信息、藥品信息、處方信息、提交日期、申請或通知狀態(批準、拒絕、撤回、完成)等,也可以下載相關的證明文件副本,警示即將到期或已經過期的申請或通知等。雖然TGA仍接受紙質SAS表格的申請或通知,但該線上申請系統已成為目前申請人提交申請或通知的首選。
2.4 SAS 3類通道的材料清單
申請人除按照SAS 3類通道的不同要求提交相應表格外,為確保通知或申請符合要求,還可能會被TGA要求提供其他資料,包括:患者的情況(只有A類通道需要)、藥品供應、藥品處理、對藥品供應的監管措施、藥品供應的結果等。TGA要求申請人提供材料的行為受到相關法律的授權和保護,如果申請人沒有遵守相關規定則會受到相應的處罰[9]。
2.5 SAS 3類通道的處理流程
由于SAS 3類通道適用的患者以及藥品的屬性不同,故其處理流程也不同。SAS-A類和SAS-C類是以通知的形式,SAS-B類則需要向TGA提交申請并經過審批才能使用。
2.5.1 SAS-A類通知
處方醫師須評估患者的情況,并判斷其是否符合SAS-A類通道的病情標準,在獲得患者或其監護人知情同意的基礎上,依據相關規范開具處方。若符合要求,申請人需要填寫并提交SAS-A類表格,同時將通知交給藥品生產企業以便為患者提供藥品。該表格具有一定的法律效力,可以授權生產企業供應藥品。由于SAS-A類通道患者通常病情較為嚴重,通知后無需TGA審批即可使用,但申請人應在患者用藥之后的28天內將申請表的副本交給TGA,否則視為犯罪并處罰款。
2.5.2 SAS-B類申請
該類藥品在使用之前需要提請TGA進行評估,其評估標準依據患者的不同需求而有所區別。
(1)患者:SAS-B類申請應具有充分的臨床用藥依據,并需提供患者的一般資料(例如姓名首字母、出生日期和性別等)和診斷資料等。其中,診斷資料包括患者病情嚴重程度的概要、診療詳情、預期的臨床獲益與潛在的使用風險評估、使用未批準藥品的理由[需要權衡藥品的療效、安全性(藥品安全性與藥品海內外注冊批準信息緊密關聯,如果該藥品在監管體系相似的國家已經獲批則認為其安全性相對較高)以及患者病情的嚴重程度,以確保治療方案的風險-收益平衡]。
(2)藥品:申請表應說明藥品的相關信息[商品名(如已知)、生產商或供應商名稱、有效成分、濃度、劑型、給藥途徑、給藥劑量、給藥頻次、療程和(或)治療所需用量],并包括對該藥品的質量、有效性和安全性的評價。對于藥品的評估證據可根據其安全性和有效性的證據級別進一步分類,評估證據來源于已發表的隨機對照試驗、非隨機試驗、個案報道、專家及學會的共識等。
(3)申請人:申請人的專業資質和經驗豐富程度也是TGA審評考慮的重要因素。如果全科醫師或處方醫師缺少特定情況下的用藥經驗,可以由合適的專家出具支持信或類似文件,支持該患者在一定病情下使用該藥品。此外,如果申請資料不完備,TGA可以拒絕申請,同時說明拒絕的理由,在被通知后的90天內申請人可向TGA提出重新審評的請求。此外,如果需要為某患者就相同的藥品和適應證進行SAS重復申請,還需要提供之前的監測結果。
2.5.3 SAS-C類通知
該類通道適用的藥品清單上注明了可獲授權使用的醫務人員種類,且獲得授權的醫務人員需獲得患者或其監護人的知情同意,并按適當規則使用該藥品。申請人需要填寫SAS-C類通知表格并提交給TGA,該類通知雖不需要TGA事先批準,但其申請表的副本必須在用藥后的28天內送交TGA,否則視為犯罪并處罰款。
2.6 SAS 3類通道的相關主體職責
2.6.1 處方醫師的職責
處方醫師在SAS制度中具有重要作用,可銜接患者、TGA和贊助商,替患者提交SAS申請以獲得未批準藥品的使用資格。處方醫師在其中承擔的重要職責包括:①確認患者的病情,例如評判是否符合SAS某類患者的要求;②確定使用未批準的藥品是治療當前患者疾病的最適當方案,并符合相關要求;③確保在治療前已獲得患者或其監護人知情同意;④遵守相關的規范和法律要求;⑤監測該藥品的使用,在發現任何不良反應后的15天內應向TGA和藥品生產企業報告,報告方式首選TGA網站在線報告。同時,醫師應明確告知患者,該藥品在澳大利亞未被批準、治療后的獲益情況以及任何已知的風險和副作用、可能會出現的未知風險和副作用、其他使用上市藥品治療的方案等。此外,若該藥品無法在澳大利亞獲得,而需從海外采購該藥品,申請人需要檢查該進口藥品是否受到海關規定的管制,比如是否為管控或違禁藥品(例如麻醉劑、安非他明、精神藥物)、是否屬于運動員禁用藥品(如合成代謝類固醇、促紅細胞生成素、生長激素等)或抗生素等[7]。
2.6.2 TGA的職責
TGA負責對SAS流程進行管理,對通過SAS 3條通道的藥品使用情況進行監測;對申請人提交的SAS-B類申請進行評估,并有責任在評估過程中的任何時段鼓勵申請人使用經過充分評估的ARTG藥品,并對相關資料進行必要的檢索(如果申請人提供了較為全面的相關資料,將有助于縮短處理時間),收集申請人可能不知道的信息(例如,藥品在海外的狀態、TGA內部審評信息等)等。
2.6.3 藥品贊助商的職責
無論SAS申請是否被批準,或者TGA是否收到SAS通知,藥品贊助商都沒有義務提供未批準的藥品[8]。一旦藥品贊助商同意向申請人提供藥品,就要根據澳大利亞《治療用品法令》第47B條的規定,每6個月向TGA提供1次藥品的相關報告,詳細說明該藥品的供應情況(包括供應次數及數量);如果預期藥品可能會長期供應,則可考慮進行藥品注冊申請[11]。同時,還要對藥品不良反應進行監測,向TGA報告所有之前未知的嚴重的不良反應以幫助TGA評估該藥品的安全性。對于致命或危及生命的不良反應,應在初次知悉后的1周內向TGA報告,并繼續跟進8天以提供更完整的報告;對于其他情況需在發生的15天內向TGA報告。
2.7 SAS 3類通道的藥品費用支付
在藥品費用支付方面,澳大利亞政府通過藥品福利計劃(Pharmaceutical benefits scheme,PBS)補貼大部分社區和私立醫院以及公立醫院的非住院患者的藥品費用,已涵蓋了大部分疾病的治療藥品[12]。但對于通過SAS 3類通道使用的非批準藥品,澳大利亞不會通過PBS進行補貼。在某些情況下,藥品贊助商可自行決定是否以同情用藥的形式按較低或不收費的方式向患者提供藥品。
3 澳大利亞SAS制度對我國的啟示
3.1 設立多通道申請同情用藥,提高藥品的可及性
澳大利亞SAS制度對病情十分嚴重的患者,可以不經政府批準由具有一定資質的執業醫師直接對其提供含非批準藥品的相關治療,保障了患者的用藥權和生命權。SAS-A類通道和SAS-C類通道只需向TGA提交通知即可對患者用藥,而病情相對不重的患者則可借助SAS-B類通道即“申請-審評”的模式保障其用藥安全。澳大利亞通過設立多種同情用藥申請通道使醫務人員擁有較大的自主性。《管理辦法(征求意見稿)》指出,我國同情用藥是以生產企業提出申請的“申請-審評”模式為主,通道單一,醫師也沒有自主處方“拓展性用藥”的權力。建議我國在今后同情用藥制度體系的完善過程中,可以適當增加申請通道,進一步提高藥品的可及性,保障患者的用藥權和生命權。
3.2 構建多層次同情用藥評估體系,保障患者的生命健康
澳大利亞SAS制度明確規定了醫師、政府監管機構、生產企業等主體的具體責任,包括藥品不良反應監測與報告、患者知情同意等,并注重權衡藥品的療效、安全性以及患者病情的嚴重程度間的關系,形成了相對完善的藥品評估體系。而我國《管理辦法(征求意見稿)》第三、四條等條款對適用于同情用藥的患者、藥品、臨床療效等僅作出了原則性規定,缺乏具體規范,可操作性不強。建議我國盡快建立同情用藥制度多層次評估體系,例如,對患者的評估,應對其年齡、疾病種類、疾病嚴重程度、患者或其監護人的知情同意等細節作出具體規定;對藥品的評估,比如藥品的安全性、有效性等,應充分利用國內外臨床指南、共識和已經進行的臨床試驗數據;對藥品同情使用的評估,同情用藥期間應不斷收集治療效果或不良反應等信息,對藥品的同情使用進行再評價,以確保同情用藥能否繼續進行。通過構建完備的多層次同情用藥評估體系,保障患者的生命健康。
3.3 與現有制度有機銜接,促進醫藥產業的健康發展
澳大利亞SAS制度對于藥品的不良反應監測作了較為詳細的規定。隨著新版《藥品管理法》對藥物警戒制度的確立,我國同情用藥制度與藥物警戒制度如何有效銜接值得相關部門關注。除此之外,《管理辦法(征求意見稿)》第十七條提到拓展性臨床試驗與注冊臨床試驗的相互關系,如何實現同情用藥制度與我國藥品臨床試驗管理、藥品注冊審評審批制度的銜接,以及與藥品上市后采購、費用支付管理等相關制度銜接,關系到醫藥企業的研發積極性,且完善的同情用藥制度體系可在一定程度上助力醫藥企業的創新,促進醫藥產業的健康發展。
4 結語
澳大利亞根據患者病情的嚴重程度以及藥品安全性將SAS分為3類通道進行管理,對于病情十分緊急的患者,通過SAS-A類通道通知TGA后可直接使用;對于安全性相對較高的藥品,通過SAS-C類通道通知TGA后也可直接使用;其他情況則需通過SAS-B類通道以“申請-審評”的形式向TGA提出申請,經審評通過后方可實現同情用藥。該制度極大提高了藥品的可及性,保障了患者的生命健康。我國新版《藥品管理法》實施時間不長,在同情用藥制度初步確立的背景下,本研究對澳大利亞SAS制度的具體內容進行了介紹和分析,以期為完善我國同情用藥制度體系提供參考,使藥物研發成果能夠更加及時地惠及臨床。
參考文獻
[ 1 ] 徐景和.加快建立體現人文關懷的同情給藥制度[N].中國醫藥報,2017-06-05(004).
[ 2 ] 袁妮.制度先行探新途[N].中國醫藥報,2020-03-09(003).
[ 3 ] 李艷蓉,崔一民,王海學,等.美國突發公共衛生事件醫療對策對我國藥品審評審批和監管的啟示[J].中國臨床藥理學雜志,2020,36(7):907-911.
[ 4 ] 朱越,蔣蓉,邵蓉.澳大利亞藥品注冊與醫保準入并行程序研究[J].中國衛生經濟,2018,37(11):89-92.
[ 5 ] Australia Government Department of Health. Australian register of therapeutic goods[EB/OL].(2019-10-29)[2020-
03-02]. https://www.tga.gov.au/australian-register-therape-
uticgoods.
[ 6 ] JAN B,ANDRZEJ G. Compassionate use of unauthorized drugs:legal regulations and ethical challenges[J]. Eur J Intern Med,2019. DOI:10.1016/j.ejim.2019.04.008.
[ 7 ] Donovan P. Access to unregistered drugs in Australia[J]. Aust Prescr,2017,40(5):194-196.
[ 8 ] Australia Government Department of Health. Therapeutic goods administration half yearly performance snapshot 1 July to 31 December 2019 [EB/OL].(2020-05-05)[2020-
03-01]. https://www.tga.gov.au/sites/default/files/halfye- arly-performance-snapshot-july-december-2019.docx.
[ 9 ] Australia Government Department of Health. Special access scheme:guidance for health practitioners and sponsors[EB/OL].(2018-01-05)[2020-03-01]. https://www.tga.gov.au/book-page/information-health-practitioners#resp.
[10] Australia Government. Therapeuticgoods(authorised supply of medicines)rules 2019[EB/OL].(2019-09-13)[2020-
03-01]. https://www.legislation.gov.au/Details/F2019L01-
194.
[11] Australia Government Department of Health. Special access scheme guidance for health practitioners and sponsors[EB/OL].(2017-09)[2020-03-01]. https://www.tga.gov.au/sites/default/files/special-access-scheme-guidance- for-health-practitioners-and-sponsors.pdf.
[12] 趙緋麗,吳晶,吳久鴻.澳大利亞藥物福利計劃可持續措施:基于2015年新一輪改革方案[J].中國醫療保險,2016(4):67-70.
(收稿日期:2020-03-23 修回日期:2020-05-13)
(編輯:孫 冰)

