納米氧化鋅改性復合樹脂即刻抗菌性能及其機制的研究
梁蓓蕾 逯宜 李蘊聰 劉瑞瑞
復合樹脂由于色澤美觀、操作簡便等優點而廣泛應用于口腔臨床各種牙體缺損修復和美容修復之中[1],但因其自身理化性質制約及聚合收縮引起的結構缺陷,容易在細菌及其產物的作用下發生降解,導致修復體出現邊緣滲漏、繼發齲乃至脫落失敗[2]。許多學者曾嘗試在復合樹脂中添加抗菌劑對其改性來解決這一問題[3-4]。
納米氧化鋅(nano-ZnO)作為一種新型多功能無機納米材料,具有優良的抗菌性能,同時兼具納米晶粒的優點,其抗菌性能較普通氧化鋅更加出色,已經成為無機抗菌劑研究的熱點之一[5-6]。本實驗將nano-ZnO作為無機填料的一部分加入復合樹脂中,通過對其即刻抗菌性能的測定及及其抗菌機制的初步探索,研究nano-ZnO抗菌改性復合樹脂的可能性,為進一步研究探索具有抗菌性能的樹脂提供實驗依據。
1 材料與方法
1.1 實驗材料與儀器
1.1.1 實驗材料 雙酚A 雙甲基丙烯酸縮水甘油酯/雙甲基丙烯酸二縮三乙二醇酯(Bis-GMA/TEGDMA)混合物、硅烷化處理的無機填料、光引發劑樟腦醌(CQ)、胺促進劑(DMAEMA)(Esstech公司,美國);納米氧化鋅(17 nm,北京博宇高科新材料技術有限公司);變形鏈球菌(UA159,第四軍醫大學口腔醫院檢驗科);腦心浸液培養基、腦心浸液瓊脂(北京陸橋技術有限責任公司);鋅(Zn)測定試劑盒(南京建成生物工程研究所);24 孔細胞培養板、96 孔細胞培養板(Corning公司,美國)。
1.1.2 實驗儀器 電子天平(Denver公司,美國);可見光固化燈(Spectram,Dentsply公司,美國);酶標儀(BMG公司,德國);超純水儀(Millipore公司,美國);高壓蒸汽滅菌鍋(上海博訊公司);無菌操作臺(蘇州凈化設備廠);電熱恒溫培養箱(上海躍進醫療器械廠);MGC厭氧培養罐及厭氧產氣袋(三菱公司,日本);漩渦混合器(Vortex QL-901,江蘇海門市其林貝爾儀器制造有限公司);微量加樣器(Eppendorf公司,德國)。
1.2 樣本的制備與分組
1.2.1 實驗分組 實驗所用復合樹脂均在實驗室條件下進行配制。實驗組復合樹脂所含填料由nano-ZnO與硅烷化處理的無機填料兩部分組成,其添加總量均恒定為70%,依照填料中nano-ZnO所占比例不同設置3 個實驗組(nano-ZnO添加量依次為1%、5%、10%),空白對照組填料中不含nano-ZnO。
1.2.2 復合樹脂的制備 稱取混合樹脂體系(Bis-GMA/TEGDMA)(BGT),避光條件下加入光引發體系(CQ和DMAEMA添加量均為1%),均勻混合后按照實驗分組加入相應質量分數的填料(表1),攪拌均勻后避光保存備用。

表1 復合樹脂各組分組成比例Tab 1 The proportion of modified composite resin
1.2.3 樣本的制備 制作內徑 10 mm、厚度2 mm的金屬模具,按照實驗分組分別使用各組對應樹脂制備試件,每組6 個,充分光固化后脫模,37 ℃條件下浸泡于無菌三蒸水中24 h備用,實驗前使用無菌水反復沖洗并用70%乙醇溶液消毒擦拭試件表面,無菌水再次沖洗后干燥備用。
1.3 實驗方法
1.3.1 抗菌性能測定 取一定量復蘇后的變形鏈球菌,加入腦心浸液培養基中37 ℃厭氧培養18~20 h(N2:85%,CO2:5%,H2:10%)。將已消毒備用的試件分別放入每孔加有入1.8 ml腦心浸液培養基和0.2 ml菌液的24 孔細胞培養板中,37 ℃厭氧培養24 h后將試件取出,放置于加有10 ml腦心浸液培養基的試管中,劇烈震蕩1 min,充分洗脫試件表面黏附的細菌。洗脫液倍比稀釋后,接種于腦心浸液瓊脂平板上,厭氧培養24~48 h,以平板上菌落數為30-300的平板為準進行菌落計數,按照下述公式計算抗菌率。
r(%)=[(b-c)/b]×100%
r:抗細菌率(%);b:空白對照試件組的平均菌落數(CFU/片);c:nano-ZnO改性光固化復合樹脂試件組的平均菌落數(CFU/片)。
1.3.2 鋅離子釋放量的測定 為測定各組光固化復合樹脂的鋅離子釋放量,將各組樣本浸泡于裝有4 ml無菌三蒸水的試管中,37 ℃保存,于24 h時取浸析液,依照鋅(Zn)測定試劑盒(南京建成生物工程研究所)說明,取10 μl待測樣本依次與160 μl試劑一、40 μl試劑二進行混合,并在37 ℃條件下進行孵育。使用560 nm波長分別于2 次混合后測定其吸光度值A1,A2,按照下述公式計算鋅離子濃度,再按照溶液體積計算相應時期的鋅離子釋放量。
鋅離子濃度(mol/L)=C標準×ΔA測定/ΔA標準
ΔA=A2-A1
其中,C標準和A標準均為試劑盒中所含鋅離子標準液測定結果。
為去除無菌三蒸水中可能含有的離子物質所造成的誤差,實驗計算所得鋅離子釋放量需減去相同劑量無菌三蒸水樣品所得結果的均值才能作為實際鋅離子釋放量。
1.4 統計學分析
使用SPSS 19.0軟件進行統計學分析,通過單因素方差分析(one-way ANOVA)比及LSD-t檢驗(Fisher's least significant test)多重比較分析各組之間的差異,P<0.05時差異有統計學意義。
2 結 果
2.1 改性復合樹脂的即刻抗菌率
不同nano-ZnO添加量改性復合樹脂的即刻抗菌率如表2所示。各組復合樹脂樣品培養所得變形鏈球菌菌落生長情況如圖1所示。
由于1%ZnO組抗菌率數值過低,為評估其是否具有抗菌作用,使用兩獨立樣本t檢驗比較其與空白組間菌落個數的差異,結果顯示1%ZnO組與空白組間菌落計數的差異無統計學意義(t=0.408,P=0.692),可以認為nano-ZnO的添加量為1%時,復合樹脂未被賦予額外的抗菌性能。

表2 各組nano-ZnO改性復合樹脂的即刻抗菌率Tab 2 The immediate antibacterial rate of nano-ZnO modified composite resin
注:不同右上標數字序號表示:不同nano-ZnO添加量改性復合樹脂組間即刻抗菌率之間的差異有統計學意義(P<0.05)
2.2 改性復合樹脂鋅離子釋放量
各組nano-ZnO添加量改性復合樹脂浸析液所得鋅離子釋放量如圖2所示。不同nano-ZnO添加量改性復合樹脂浸析液中鋅離子釋放量的差異有統計學意義(P<0.05)。
3 討 論
在口腔醫學領域,已有許多國內外學者關注到nano-ZnO的優點并對其應用進行深入探索。研究[5-7]證實nano-ZnO抗菌劑對口腔常見致病菌有較強的抑制殺滅作用,作為根管封閉劑,取得了較普通ZnO封閉劑更明顯的根尖封閉療效;曹香林等[8]研究了以nano-ZnO作為填料組分的熱凝樹脂基托的抗菌性能及機械性能,結果顯示在一定的添加劑量內,樹脂基托對變形鏈球菌的抗菌作用隨nano-ZnO含量的提高而逐漸增強;Toledano等[9-11]發現用含nano-ZnO的粘接劑處理脫礦牙本質表面能提高其與樹脂的即刻粘接強度,降低混合層膠原的降解,并具有促進齲損組織再礦化的潛力;Tavassoli Hojati等[12]嘗試將nano-ZnO添加在流動樹脂當中,并證明nano-ZnO可以使流動樹脂具備一定的抗菌性能,并且能夠提高流動樹脂的粘接強度及部分機械性能。如上所述,nano-ZnO已在口腔醫學領域獲得廣泛的應用,本試驗結果也表明,加入nano-ZnO確實能夠使復合樹脂具有抑制變形鏈球菌生長的能力,且這一抑制能力隨著nano-ZnO含量的增加而逐漸提高。
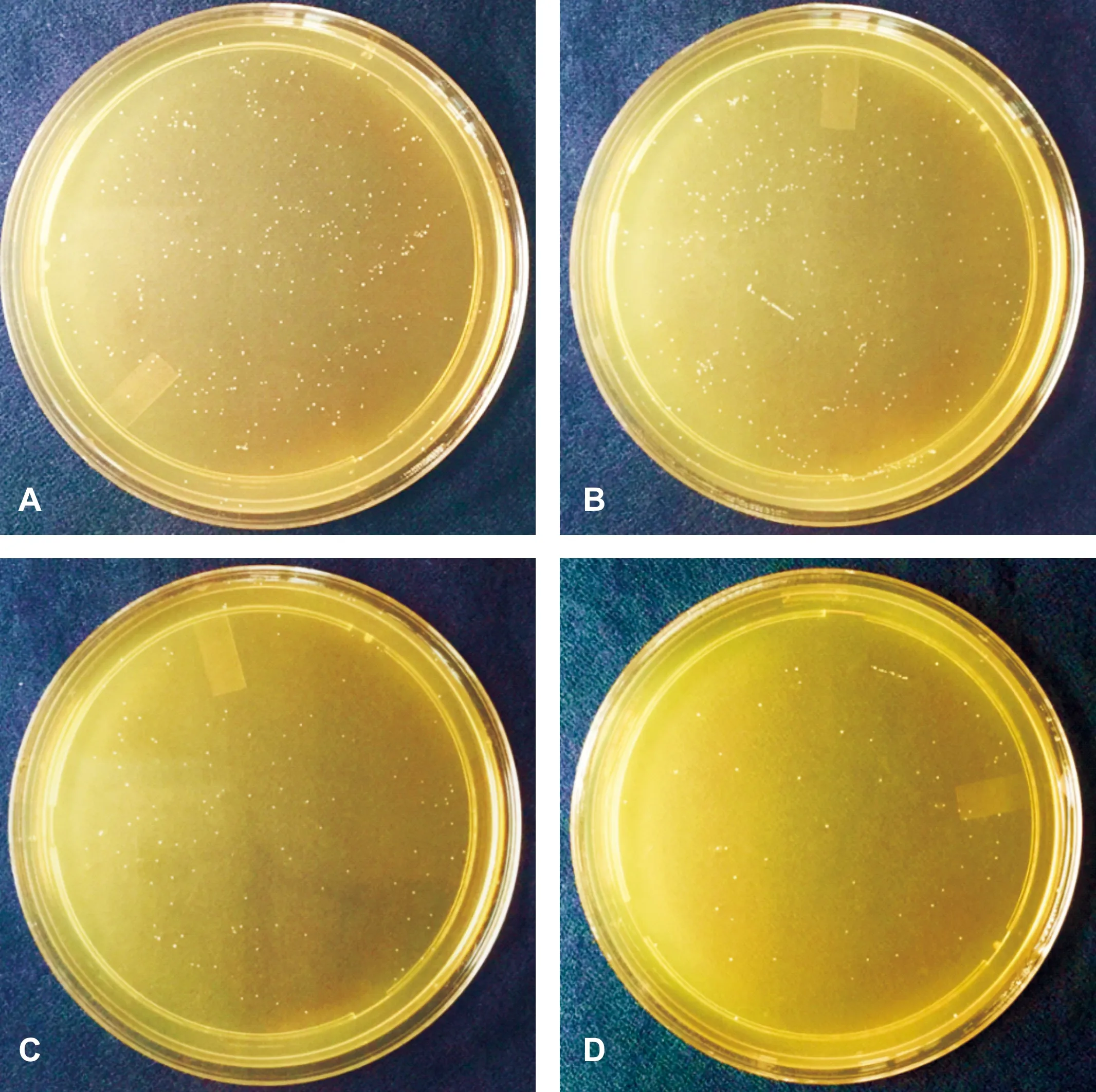
A:對照組;B:1% ZnO;C:5% ZnO;D:10% ZnO圖1 各組復合樹脂即刻抗菌性能測定的變形鏈球菌菌落生長情況A:Control;B:1% ZnO;C:5% ZnO;D:10% ZnOFig 1 The growth of Streptococcus mutans colonies in the groups

圖2 各組nano-ZnO改性復合樹脂浸析液鋅離子釋放量(10-2 μmol)Fig 2 The amount of zinc ions(10-2 μmol) released from the nano-ZnO modified composite resin of each group
目前nano-ZnO的抗菌機制雖然尚不明確,但有許多學者認為nano-ZnO能夠緩慢的釋放出Zn2+,可以依靠異種電荷間的相互吸引結合到細菌表面,破壞細胞膜的生物性能,抑制細菌的生長和繁殖;同時,過剩的Zn2+也穿過細胞膜進入細胞內部,與細菌體內的蛋白質,DNA等發生反應,妨礙細菌的正常功能活動及代謝從而達到抗菌的目的。當前細菌被殺滅之后,Zn2+又會從細菌中游離出來,與其他細菌發生接觸,再次通過以上機制發揮抗菌作用[13-15]。本試驗表明,在水溶液體系中,含有nano-ZnO作為填料組分的復合樹脂均可以檢測到鋅離子的釋放,同即刻抗菌率所得結果相同,其釋放量也隨nano-ZnO添加量的增加而增加,這從側面表明Zn2+的釋放是nano-ZnO重要的抗菌機制之一。
在實際臨床操作中,窩洞預備常無法將病損中的細菌完全去除干凈,微滲漏建立的通道也使口腔內的微生物能夠自由進出,然而復合樹脂相較于其他牙科材料更容易黏附和聚集細菌。通過本實驗結果表明使用nano-ZnO改性復合樹脂,可以賦予其抗菌活性,對牙體-充填體界面及充填體表面的細菌發揮抑制作用,降低繼發齲產生的可能性,為臨床新型抗菌牙科材料的研發提供了必要的實驗依據,但其長效性及更深層次的抗菌機制的探討還需進一步的研究及努力。

