抗結腸炎藥美沙拉嗪的合成研究進展
鞏冰倩 張文雯 楊利蘋 葉愛英 翁智兵
(常州工程職業技術學院 化工與制藥工程學院,江蘇 常州 213164)
美沙拉嗪,又名馬沙拉嗪,化學名5-氨基-2-羥基苯甲酸(5-ASA),是治療潰瘍性結腸炎的藥物。隨著人們生活方式的不斷變化,潰瘍性結腸炎的發病率不斷上升[1]。與其它同類藥物相比,美沙拉嗪具有結腸定位釋放,低毒性,低不良反應和耐受性強等特點。一經面市,就成為抗結腸炎的臨床首選藥物[2]。近年有研究表明[3],美沙拉嗪在治療由視黃醛循環障礙引起的視網膜疾病方面具有極好的應用前景。因此,研究該藥的化學制備方法具有重要的現實意義。
美沙拉嗪最初由瑞典Pharmacia AB開發,英國Tillots Labs于1985年6月上市[4]。國內目前批準的美沙拉嗪原料藥生產廠家不多。本文就美沙拉嗪原料藥合成研究進展進行綜述,以期為該原料藥的合成研究提供參考。
1 水楊酸硝化還原法
水楊酸硝化還原法是以水楊酸(1)為原料,經硝化反應合成5-硝基水楊酸(2),再還原得5-氨基水楊酸(3)。

該法在20世紀20年代就已有報道[5],是一種較早用于制備5-氨基水楊酸的方法。硝化反應以不同濃度的硝酸[5-6]或硝酸與硫酸[7]或硝酸與冰醋酸[8-11]的混合液作為硝化劑。由于硝基苯分子中羥基及羧基的定位作用,硝化反應在生成化合物2的同時,還生成了大量的3-硝基水楊酸,致使中間體分離麻煩,產物收率不高,僅30~40%[5-8]。王勤等[12]提出了水楊酸在固體酸催化下,被硝酸選擇性硝化,合成化合物3,可提高硝化反應的選擇性,該法催化劑不明確,且未見后續報道。
化合物2經還原反應得到3的選擇性還原過程,是獲得目標化合物的最終步驟。文獻主要報道了金屬還原和催化氫化兩種方法。
金屬還原劑主要是鐵粉[4-9,11]和鋅粉[5,13]兩種,都是金屬與給質子劑結合,選擇性還原芳環上的硝基。雖然鐵粉較鋅粉的成本有所降低,二者在反應時均需在鹽酸存在下進行,造成嚴重的污染和設備腐蝕,收率不高,多在60~70%間。
Gabriele Breviglieri等[14]人嘗試用金屬鎳作催化劑,在回流下加入水合肼,將2還原成3,收率可達89%。此工藝為硝基化合物的轉移氫化法還原,肼為供氫體,反應設備和操作較簡便,只需將硝基化合物與過量的水合肼溶于醇中,然后加入鎳、鈀等氫化催化劑,在較溫和的條件下即可完成反應。分子中的羧基不受影響。但肼有較強毒性,與空氣接觸或高溫情況下有爆炸分解的安全隱患。
催化氫化是化合物2在鉑[15-16]或鈀[10,16]或鎳[12,14]等金屬催化劑下,在一定的壓力和溫度下,以氫氣為還原劑,通過催化劑和反應條件選擇性還原芳環上的硝基,使其得到化合物3。反應收率在90%以上,通常,使用活性鎳時,氫氣壓力和溫度要求較高,而鈀和鉑可在較溫和的條件下進行。與金屬還原相比,收率明顯提高。但反應過程需使用貴金屬作催化劑,且在高壓條件下進行,反應成本高,操作麻煩。
以1為原料經硝化-還原制備化合物3的合成方法,工藝雖成熟,但硝化反應不僅反應選擇性差,反應收率低,而且放熱性強,存在著安全生產隱患。還原反應污染嚴重,生產成本較高,不符合目前的工業化生產要求。
2 苯偶氮水楊酸還原法
苯偶氮水楊酸還原法是目前工業上制備美沙拉嗪的主流方法。此法[17-19]多以苯胺(4)為原料,經重氮化合成氯化重氮苯(5)或直接以5為原料[20],再與水楊酸在低溫下偶合得苯偶氮水楊酸(6),進一步還原合成化合物3。反應路線如下。
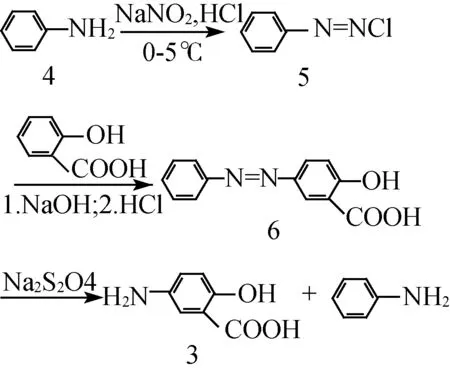
通過氮-氮鍵的還原獲得伯胺的方法較多,主要有連二亞硫酸鈉化學還原法和催化氫化還原法。
連二亞硫酸鈉是常用的還原劑,還原能力強,但在水溶液中迅速分解,產生大量有害氣體。實際操作中,連二亞硫酸鈉通常在堿性條件下加入6中,還原得到3。反應總收率60~70%[17-21]。
廖如佴[22]提出了在亞硫酸鈉和2-羥基-5-甲基-3-硝基吡啶混合液中,將偶氮苯水楊酸和氯化鉬升溫回流反應,加入二甲苯溶液,后處理得化合物,單步反應收率可達91%。
催化氫化還原一種是以雷尼鎳為催化劑[23-24],苯偶氮水楊酸溶液直接加氫,在一定氫壓下反應,化合物3的總收率在50~60%左右。另一種是戴國華等[25]人采用的以水合肼、Raney Ni催化轉移氫化還原,收率70%。
苯偶氮水楊酸還原法在原料及產物中均有苯胺存在,毒性較大,不僅不符合綠色化學的生產要求,也嚴重影響了原料藥的質量要求。
為避免苯胺,相繼出現了以取代苯胺代替苯胺為原料使用[25-26],其中,以G.桑切斯-卡努[27]提出的方法為佳,文中以對氨基苯磺酸取代苯胺,由重氮化反應制得對磺基重氮苯鹽,再與水楊酸偶合得5-(對-磺苯基偶氮)-水楊酸,并將其通過低溫特殊電極,直接電化學還原制備對氨基苯酚類化合物,避免了連二亞硫酸鈉的使用,收率大于80%。反應路線如下。
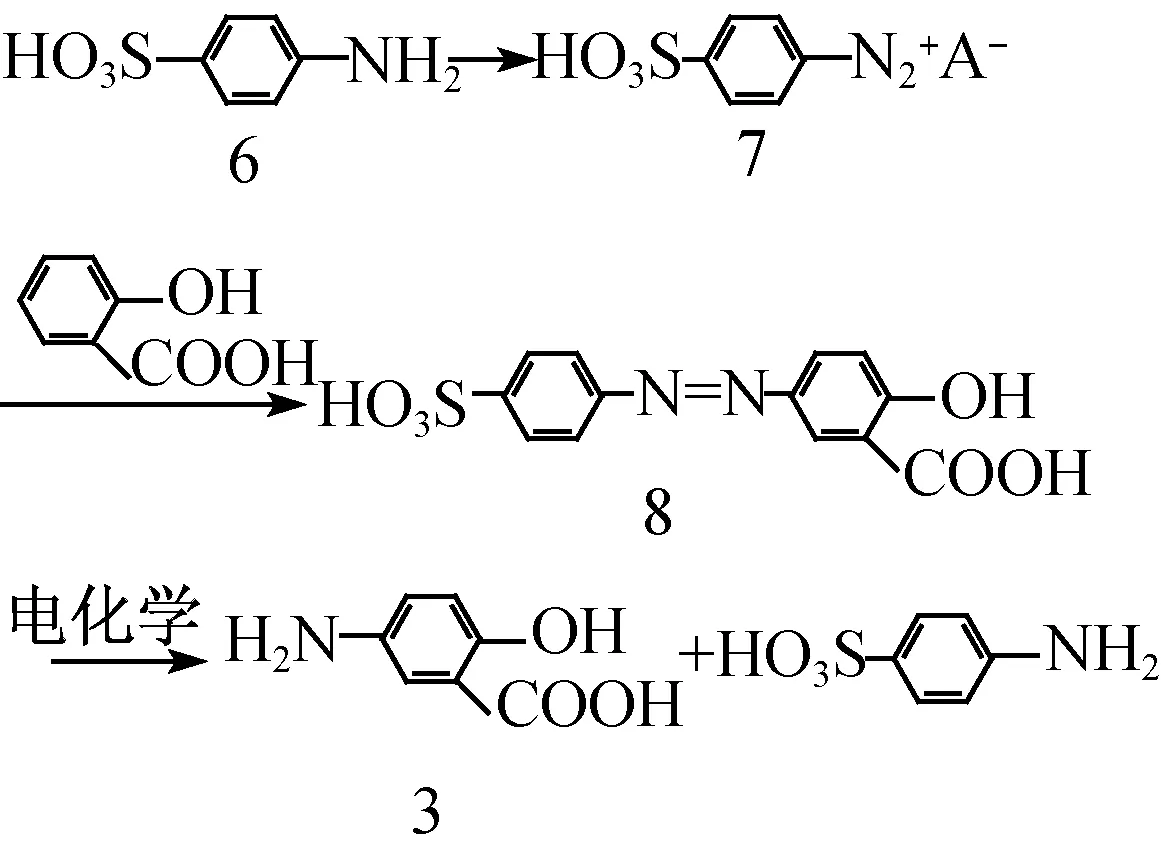
苯偶氮水楊酸還原法克服了水楊酸硝基還原法中水楊酸硝化的多位選擇性問題,使產品總收率得到提高。但反應步驟多,過程中需多次進行酸堿中和,操作繁復。重氮化合物不穩定,遇光易分解,干燥的重氮鹽會分解放出氮氣而爆炸,存在安全隱患。
3 Kolbe-Schmitt法
Kolbe-Schmitt反應是在干燥的酚鈉或類似物上與親電試劑二氧化碳發生甲酰化反應,最終在芳環上形成羧基。文獻[28-31]根據Kolbe-Schmitt反應,以對氨基苯酚為原料,在催化劑作用下,于高溫高壓氣固反應得化合物3,收率80~90%。反應路線如下。
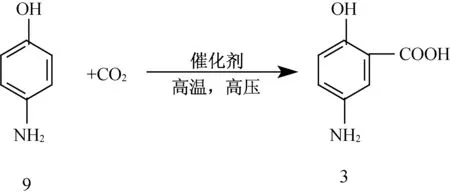
Hailiang Lü等[33]人使用超臨界CO2氣體,在高溫高壓下與酚鈉反應制備5-氨基水楊酸,收率大于90%。
該法工藝路線簡單,收率高。但反應為氣固相反應,局部易過熱,氨基苯酚在高溫高壓下易被氧化和聚合,且毒性大。對此,李光興等[32]人參考印度專利[29],對原料9進行了改進。以對乙酰氨基苯酚(10)和堿性氫氧化物或其碳酸鹽為原料,在固體催化劑存在下,經二氧化碳氣相催化羧化制備5-氨基水楊酸鹽(11),再酸化得產物。收率最高達92%。

劉志剛等[34]人以對氨基苯酚鈉為原料,加入離子液體氯化1-丁基-3-甲基咪唑,通入二氧化碳氣體,在高溫高壓下將氣固羧合反應改為氣液羧合反應,得5-氨基水楊酸鈉的反應混合物后,用鹽酸酸化,收率81%。
Kolbe-Schmitt法工藝路線短,反應收率高。反應對水敏感,即使是微量的水也會顯著降低產品的量,無水操作要求高。且需高溫高壓,反應條件苛刻,操作不便。原料毒性大,不符合環保及藥品生產要求。同時,由于苯環上-OH、-NH2(或-NHCOCH3)的定位效應,反應中仍會有一定量的異構體存在,給后處理帶來麻煩。
4 鹵代芳烴水解還原法
鄭玉梅等[35]人以鄰氯苯甲酸(12)為起始原料,硝化反應生成5-硝基鄰氯苯甲酸(13),也有報道[36-37]直接以13為起始原料,根據鹵代烴的水解原理,在堿性條件下水解得到2,經鋅粉/鹽酸還原得到最終產物。總收率28.7%。反應路線如下。
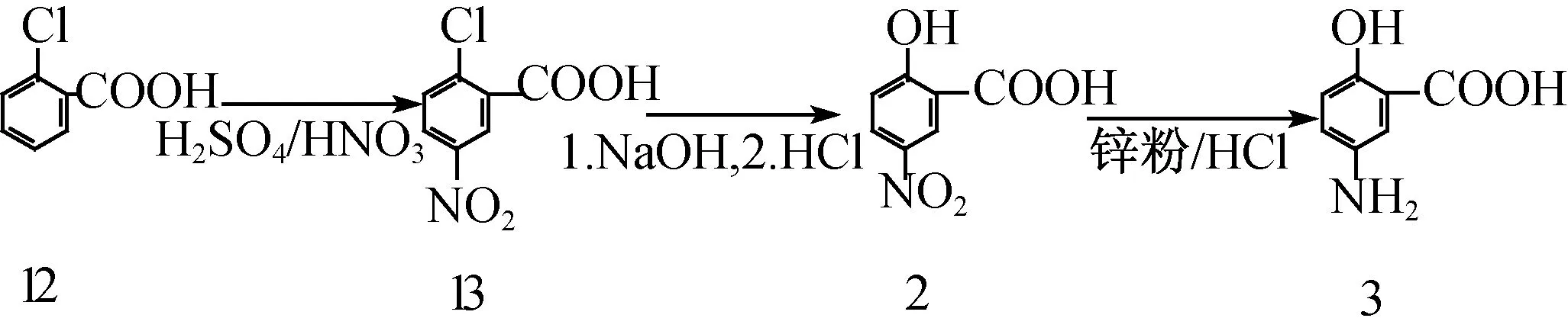
李運山等[38]人在此基礎上對反應條件做了改進,12得13后,以銅粉催化、吡啶助催化13生成2,在鋅- 甲酸肼復合體系作用下還原得目標化合物。報道總收率約88%。
鹵代芳烴水解還原法中,苯環上吸電子基尤其是對位硝基的存在,使5-硝基鄰氯苯甲酸的水解反應較易進行,且反應選擇性較好。但鹵代芳烴為環境有害物質,后期還原反應中同樣有成本高或污染嚴重等問題存在。
綜上所述,美沙拉嗪的合成仍存在較多壁壘和挑戰,諸如如何降低原料成本,如何確保反應過程綠色環保,如何確定原料、輔料安全無毒,如何提高產率等。隨著原料藥合成研究的不斷深入,開發無毒、生物相容、生物可降解的美沙拉嗪原料藥仍是今后研究重點,以滿足工業生產中“優質、高產、低耗、環保”的要求。
致謝:江蘇亞邦強生藥業有限公司橫向課題“抗結腸炎藥物美沙拉嗪原料藥合成工藝研究”經費支持。

