泮托拉唑鈉腸溶片的處方工藝研究
劉登(山東理工職業學院化工學院,山東 濟寧 272067)
0 引言
泮托拉唑鈉腸溶片為質子泵抑制劑類抗酸藥,生物利用度高于同類拉唑類抗酸藥如奧美拉唑和蘭索拉唑。FDA 網站橙皮書[1]列出的參考列表樣品商品名為PROTONIX,生產廠家Weyth pharmaceuticals。FDA 推薦的釋放度方法為USP 藥典方法。橙皮書藥物制劑專利為美國專利5997903,從專利和參考列表樣品說明書中可以得到相關的處方工藝信息,結合腸溶制劑的輔料應用經驗,可能的處方組成如表1 所示,生產工藝為濕法制粒工藝。
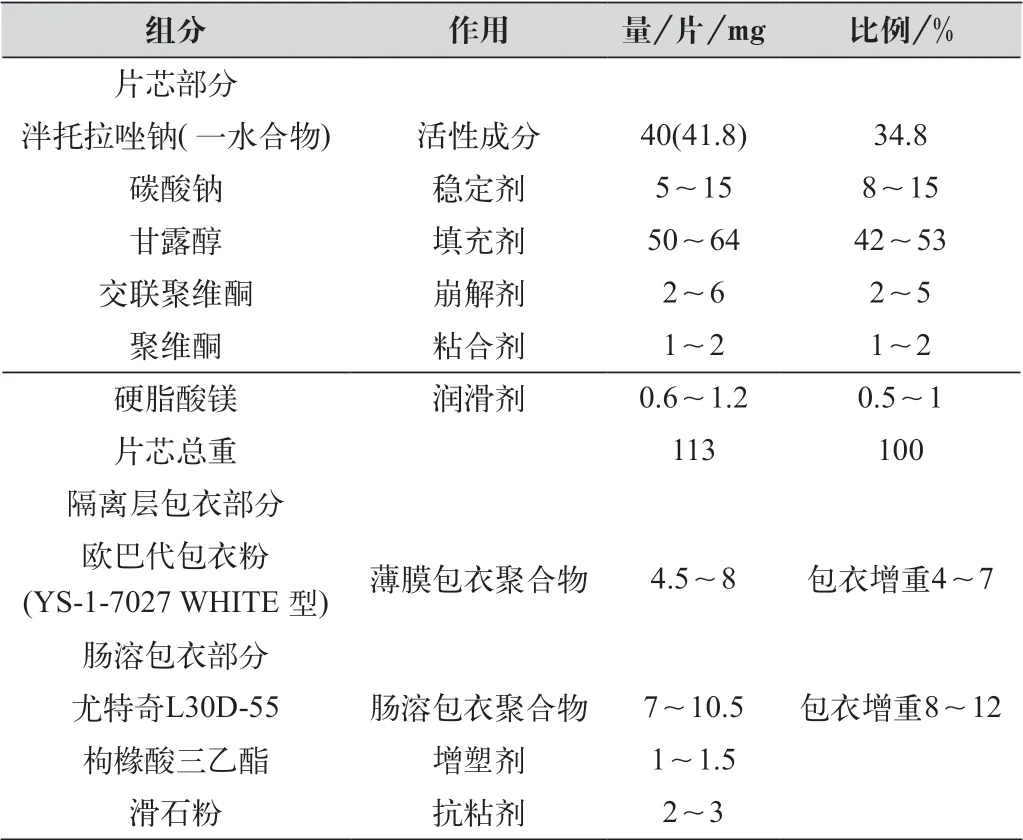
表1 泮托拉唑鈉腸溶片的處方組成
ICH 指導原則Q8 藥物開發[2]中提到關鍵質量屬性的概念,關鍵質量屬性(CQA)指產品的物理、化學、生物學、或微生物學性質或特征,應在適當的限度、范圍或分布之內,以確保預期的產品質量。風險評估是質量風險管理[3](見ICH Q9)中一個重要的以科學為依據的過程,有助于確定哪些工藝參數對產品的CQA 有影響,在實際生產中,泮托拉唑腸溶片產品質量的主要風險為產品片芯變色的外觀問題和釋放度下降。外觀主要是原料降解變色造成,碳酸鈉在處方組成中的作用為建立堿性環境,是主要的抑制原料降解的因素,需要在處方工藝研究中重點試驗碳酸鈉的比例,交聯聚維酮屬于崩解劑,交聯聚維酮在處方中的比例可影響崩解時間,并最終影響釋放度,需要在處方工藝研究中重點進行試驗,最終獲得性質穩定的制備工藝。
1 主要材料與設備
泮托拉唑鈉(武漢大華偉業醫藥化工有限公司,批號:08050112),流化床制粒包衣機(LBL-30 重慶科旭制藥機械設備制造有限公司)濕法混合制粒機(HLSG50E 中國航空工業集團公司北京航空制造工程研究所),高效包衣機(BG-10D 中國航空工業集團公司北京航空制造工程研究所),Dlogan UDT-812自動溶出儀,Agilent1290 高效液相色譜。
2 方法與結果
泮托拉唑鈉腸溶片處方開發研究中使用的設備和固定的工藝參數如表2 所示。

表2 試驗中使用的設備和固定的工藝參數
2.1 碳酸鈉在處方中的比例的試驗
各處方具體參數見表3。
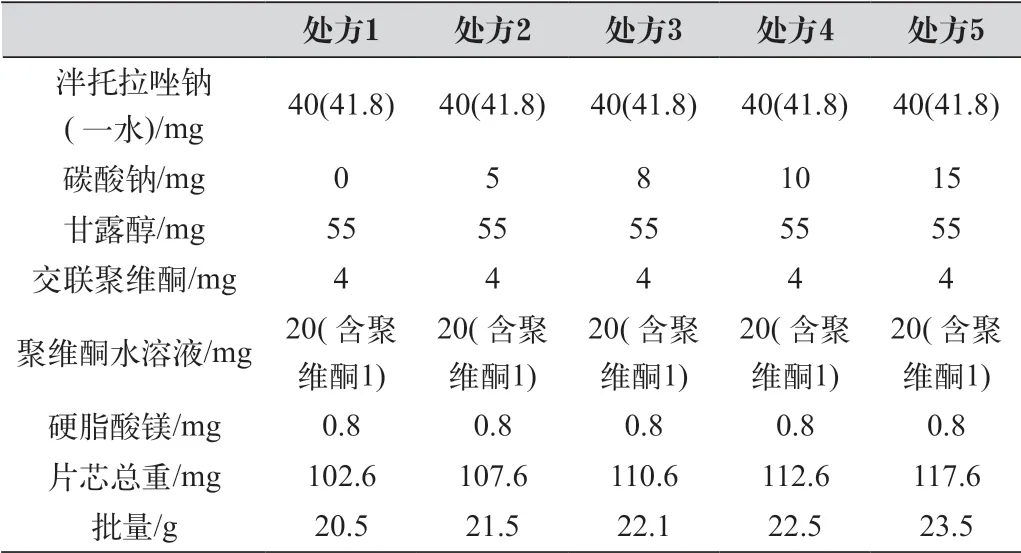
表3 碳酸鈉在處方中的比例
工藝參數見表2。取半成品顆粒于60℃,90%濕度條件下,敞口放置,每天觀察顆粒外觀。根據usp40 泮托拉唑鈉腸溶片各論[4]檢測有關物質。具體數據如表4 所示。
實驗結果表明碳酸鈉的量偏低時主成分容易降解變色,偏高時則容易吸潮,碳酸鈉與主成分的比例在20%~25%為最佳范圍,最終處方采用碳酸鈉與主成分比例為22.5%為最佳處方。
2.2 交聯聚維酮在處方中的比例的試驗
交聯聚維酮在處方中的比例如表5 所示。

表4 半成品隨時間的變化
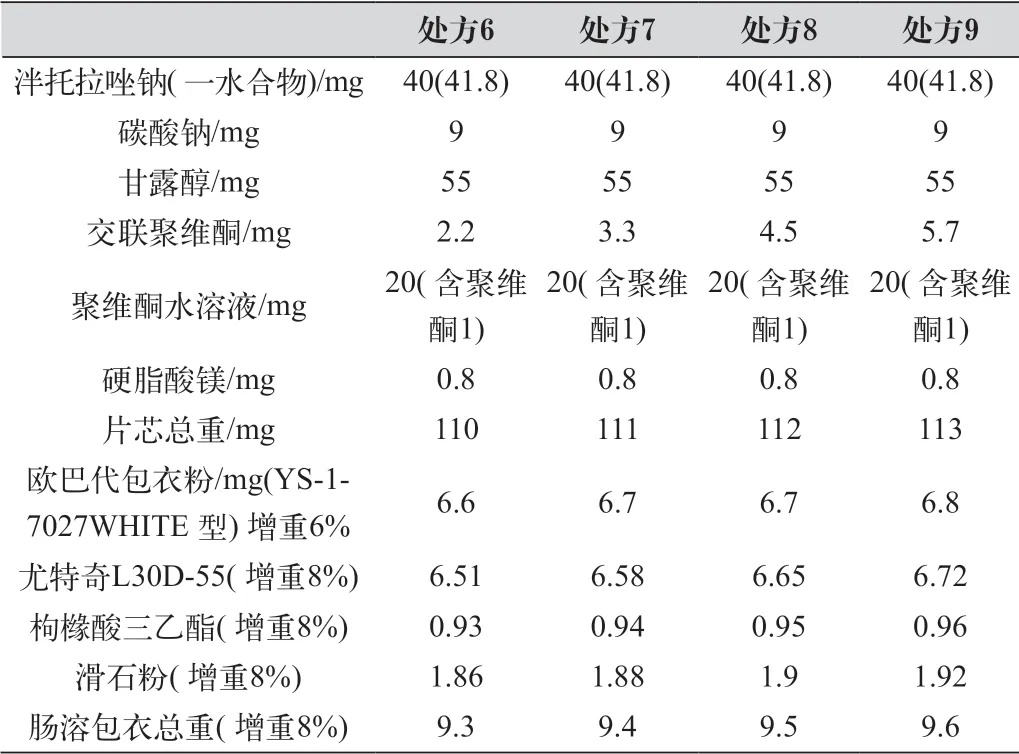
表5 交聯聚維酮在處方中的比例
工藝參數見表2。根據USP40 泮托拉唑鈉腸溶片各論項下釋放度方法檢測成品片劑釋放度。記錄片劑崩解時間,具體數據見表6 所示。
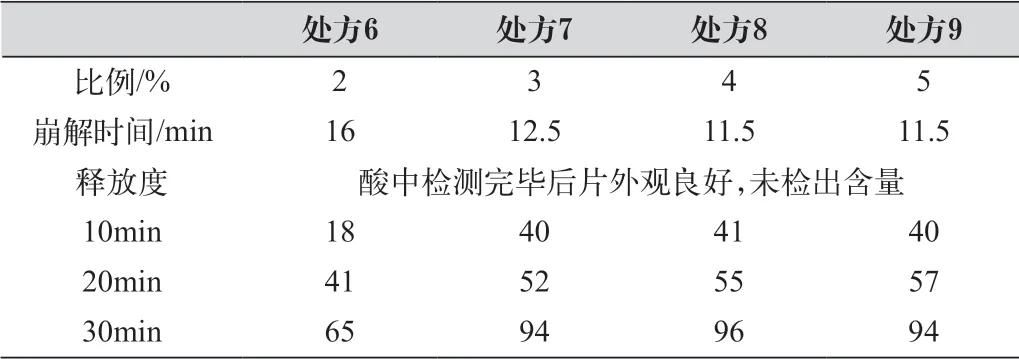
表6 片劑崩解時間
實驗結果表明交聯聚維酮在片芯中的比例在3%~5%時都可以符合釋放度的要求,最終處方采用交聯聚維酮在片芯中的比例為4%為最佳處方。
3 結語
藥品研發的目的在于設計一個高質量的產品,以及能持續生產出符合預期質量水平的產品的生產工藝,產品的質量無法通過檢驗賦予,而是通過設計賦予的,本論文的特點在于依據風險評估的原理科學的進行處方工藝研究,并最終確定了一系列工藝參數,但是目前進行的試驗仍然只是初始的試驗階段,隨著留樣考察的進行和小試到中試的放大還會對以上的工藝參數進行進一步優化。

