表面活性劑CTAB對二氧化硅表面間膠體作用力的影響
張 燕,丁明山,任嗣利
(1.蘭州交通大學交通運輸學院,蘭州 730070;2.中國石化勝利油田分公司石油工程技術研究院;3.江西理工大學冶金與化學工程學院)
由于風化油砂礦表面為親油性,在油砂水基分離過程中瀝青難以從沙粒表面脫附,導致瀝青的提取效率較低。為解決這一問題,有必要在礦漿中注入適宜的表面活性劑,改變油砂表面的潤濕性,實現潤濕性由親油向親水的方向反轉。近年來國內外研究用于潤濕反轉的陽離子表面活性劑主要是十六烷基三甲基溴化銨(CTAB)[1],研究表明,利用陽離子表面活性劑改變二氧化硅表面的潤濕性可以獲得較高的瀝青油剝離效率。Bi Zhichu等[2]發現當CTAB在潔凈的二氧化硅表面形成單層吸附時,水的潤濕角增大,固體表面變為中性潤濕,隨著活性劑濃度的繼續升高,形成雙層吸附后,固體表面變為弱水濕。CTAB在固體表面的吸附比較復雜,在親水性基底上的吸附量及吸附形態會隨著其結構和濃度的改變而不同[3]。低濃度條件下,通過靜電吸附使二氧化硅表面電荷被中和形成單層吸附;高濃度時,表面活性劑烷基鏈間的疏水吸引力形成雙層吸附,從而導致二氧化硅表面的電性反轉而帶正電荷。CTAB在二氧化硅表面的吸附除了與濃度有關,還會受到電解質的影響。Atkin等[4]考察了溴化鉀(KBr)作為電解質對不同濃度CTAB在二氧化硅表面吸附過程的影響,100 s左右CTAB開始在硅片上吸附,隨著時間的推移,硅片上的CTAB會被KBr替代,這種替代行為會導致二氧化硅表面的潤濕性變化。Velegol等[5]研究發現當CTAB的濃度與臨界膠束濃度(CMC)的比值從0.9增加到1.0時,無論溶液中是否有KBr,CTAB在二氧化硅表面上的吸附形態都會由短棒狀變為長條的蠕蟲狀。Wanless等[6]研究也證實KBr的加入使CTAB的吸附形態由雙層吸附轉變為圓柱狀。雖然已有采用原子力顯微鏡(AFM)形貌掃描[7-9]和吸附動力學[10-11]等方法對陽離子表面活性劑這種復雜界面行為進行研究的報道,但研究結果仍存在一定的局限。將AFM膠體探針技術作為研究膠體間微觀力學行為的測試手段,能揭示陽離子表面活性劑在二氧化硅表面的界面行為,進而為提高瀝青回收率提供可靠的研究方法。
本研究在陽離子表面活性劑CTAB溶液中,利用AFM原位檢測二氧化硅表面間的膠體作用力,通過膠體作用力的變化來判斷CTAB在二氧化硅表面的吸附行為。在相應的溶液環境中測試二氧化硅表面的Zeta電位,以驗證二氧化硅表面間的長程作用力。結合AFM提供的作用力及二氧化硅表面的Zeta電位來研究CTAB的濃度及電解質的存在對二氧化硅表面潤濕性的影響。
1 實 驗
1.1 原 料
CTAB,CMC約為0.9 mmol/L,購于Alfa公司;KCl,色譜純,購于Alfa公司;HCl和H2O2(質量分數為30%)均為分析純,購于上海三友試劑廠;NaOH和乙醇均為分析純,購于西隴化工股份有限公司;H2SO4,質量分數為98%,購于白銀良友化學試劑有限公司;水為超純水,其電阻率為18.25 MΩ·cm;二氧化硅,粒徑約為8 μm,購于美國Duke Scientific公司,用于制備膠體探針;二氧化硅微粒,粒徑約為3 μm,購于上海CNPC粉體材料公司,用于測試Zeta電位;環氧樹脂膠,型號為DP-190,購于3M公司。
1.2 探針和親水性基底的制備
利用AFM(型號為Multimode 8,由Bruker公司生產)測試砂粒間的相互作用力。首先將二氧化硅黏附到V形針尖懸臂梁末端制備膠體探針,放置24 h以上。采用高倍顯微鏡(50倍)觀察二氧化硅和膠體探針的形貌(見圖1)。每次用AFM測試相互作用力前采用等離子濺射儀清洗針尖10 min,去除探針上可能存在的污染物,使探針表面為親水性。膠體探針的彈性常數采用Thermal Tune法進行校準。

圖1 采用高倍顯微鏡觀察的二氧化硅和膠體探針的形貌
為了獲得完全親水的基底,將面積為12 mm×12 mm(長×寬)的硅片置于90 ℃的Piranha溶液[98%(w)H2SO4和30%(w)H2O2的體積比為7∶3]中清洗30 min。然后用超純水和乙醇沖洗,在超聲波清洗儀中處理30 min,最后用超純水沖洗,超純氮氣吹干,獲得完全親水的基底。
1.3 二氧化硅表面間膠體作用力的測試
二氧化硅表面間作用力測試的具體操作過程[12-14]是:在O型密封圈內測試探針與二氧化硅表面間的相互作用,測試時注入溶液浸沒膠體探針與二氧化硅表面,注入溶液時速度緩慢,防止氣泡進入小室。穩定時間分別為10,30,60 min,測試過程施加的最大壓力值為10 mNm。當馬達帶動基底向上靠近二氧化硅探針時獲得二氧化硅表面間的長程作用力,探針與二氧化硅接觸后立刻離開,此時得到二氧化硅表面間的黏著力。為了保證力曲線的可重復性,每組樣品測試至少3個基底表面,每個基底表面測試10個點。由于長程作用力的重復性比較高,所以在作圖時僅選取一條曲線代表長程作用力。在分析黏著力時,由于探針從基底表面脫離時需要克服的黏著力變化較大,因此在統計時每組樣品統計數量為100組。為了減小探針尺寸大小對長程作用力和黏著力的影響,對測試結果均除以探針小球半徑。所有的測試均在室溫(25 ℃)下進行。
1.4 二氧化硅微粒表面Zeta電位的測試
采用高分辨Zeta電位分析儀(型號是Zeta PALS,由Brookhaven布魯克海文生產)測量二氧化硅微粒表面的Zeta電位。稱取二氧化硅微粒(粒徑約為3 μm)配制成質量濃度為0.1 gmL的二氧化硅懸濁液。所有測試溶液pH調節為5.5左右。每組樣品測試5次,每次測試循環5輪,然后計算測試結果的平均值及相應的標準偏差。所有樣品的Zeta電位測量均在室溫(25 ℃)下進行。
2 結果與討論
2.1 CTAB濃度的影響
兩個表面間的膠體作用力如果只包含范德華力和靜電作用力,那么可以與經典的DLVO理論值擬合[15],如果兩個表面間的范德華力比較微弱,而靜電作用力和疏水吸引力占主導,那么兩表面間的作用力就應與擴展的DLVO(E-DLVO)理論值相擬合[16]。靜電作用力與表面電荷有關,可以由物質表面的Zeta電位反映出來,而疏水作用力往往與表面潤濕性有關。
2.1.1 CTAB濃度對二氧化硅表面間作用力的影響不同濃度的CTAB溶液中,隨著穩定時間的變化,二氧化硅表面間的長程作用力變化見圖2,二氧化硅表面間的黏著力的變化見表1。由圖2和表1可以看出:在不含電解質的溶液中,當CTAB的濃度由0.03 mmol/L增加為0.05 mmol/L時,長程作用力為吸引力,由3.6 mN/m增加為6 mN/m,而黏著力由4.1 mN/m增加為7.8 mN/m;當CTAB的濃度由0.07 mmol/L增加為0.10 mmol/L時,長程作用力雖然仍為吸引力,但隨著濃度的增加長程作用力和黏著力逐漸減小;當溶液中CTAB的濃度增大為1.0 mmol/L和10 mmol/L時,長程作用力轉變為排斥力,黏著力為0。隨著穩定時間的延長,在同一濃度的CTAB溶液中,長程作用力和黏著力幾乎沒有改變。CTAB在二氧化硅表面的吸附量只隨著濃度的增加而增加,吸附形態由低濃度的單層吸附逐漸轉變為高濃度的雙層吸附[17]。
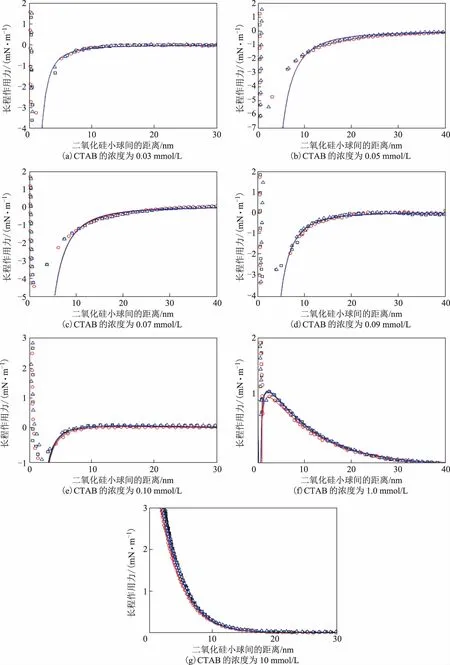
圖2 CTAB溶液中二氧化硅表面間的長程作用力隨穩定時間的變化(實線為E-DLVO理論值曲線)□—10 min; ○—30 min; △—60 min。 圖4同

表1 CTAB溶液中二氧化硅表面間的黏著力隨穩定時間的變化 mN/m
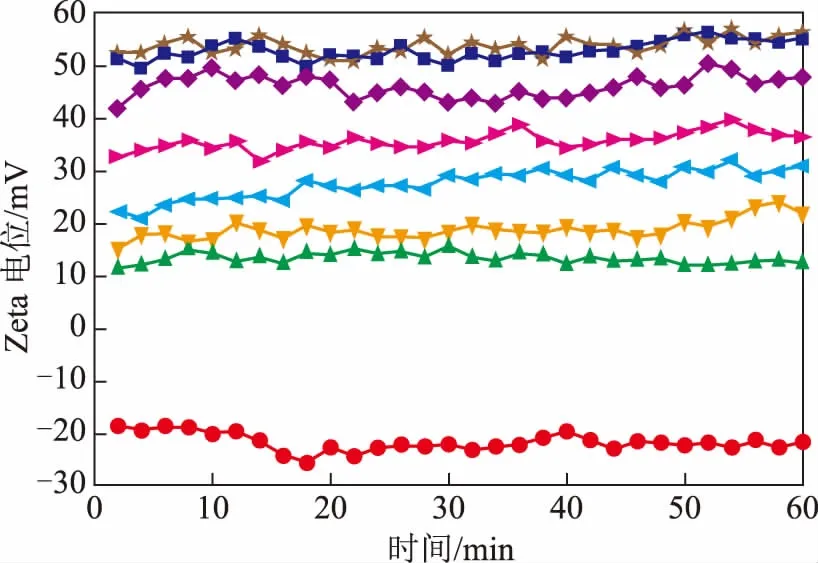
圖3 CTAB的濃度對二氧化硅微粒表面Zeta電位的影響CTAB濃度,mmol/L: ●—0.01; ▲—0.03 ; ◆—0.10; ■—1.0; ★—10
2.1.2 CTAB濃度對二氧化硅表面Zeta電位的影響CTAB濃度對二氧化硅微粒表面Zeta電位的影響見圖3。由圖3可以看出:二氧化硅表面Zeta電位隨著CTAB濃度的升高逐漸增大,甚至反轉為正值;當CTAB濃度為0.01 mmol/L時,二氧化硅表面的Zeta電位約為-20 mV;當CTAB濃度增加為0.03 mmol/L時,二氧化硅表面的Zeta電位開始轉變為正值,并且隨著CTAB濃度增加,Zeta電位繼續增大;當CTAB的濃度增加至1.0 mmol/L時,二氧化硅表面的Zeta電位為52 mV左右,長程作用力轉變為排斥力,黏著力為0,此時CTAB在二氧化硅表面形成完整而致密的雙層排布,故靜電作用力占主導。繼續增大CTAB的濃度為10 mmol/L時,二氧化硅表面的Zeta電位增幅不大,為55 mV左右。可見,CTAB的濃度高于CMC時就能使二氧化硅表面的水潤性發生徹底反轉。
2.1.3 CTAB濃度對二氧化硅表面疏水作用力常數的影響CTAB濃度對二氧化硅表面疏水作用力常數的影響見表2。由表2可以看出:在同一濃度的CTAB溶液中隨著系統穩定時間的延長疏水作用力常數不變,說明在某一濃度下,CTAB在二氧化硅表面的吸附有一個飽和度,這個結果與Atkin[17]的研究結果相吻合。隨著CTAB濃度的增加二氧化硅表面間的長程吸引力和黏著力均先增大再減小,相應的疏水作用力常數也先增大再減小,當CTAB濃度由0.01 mmol/L增大為0.05 mmol/L時,疏水作用力常數由6×10-21J增加到1×10-18J,二氧化硅基片表面疏水性增強。CTAB的濃度由0.07 mmol/L增加到0.1 mmol/L時,二氧化硅表面間的長程吸引力和黏著力均減小,相應的疏水作用力常數由8.5×10-19J減小為6×10-20J,二氧化硅基片表面疏水性減弱。當CTAB濃度增加到1.0 mmol/L和10 mmol/L時,疏水作用力常數均為3×10-21J,二氧化硅表面間只存在靜電作用力和范德華力,說明二氧化硅表面徹底轉變為親水性。
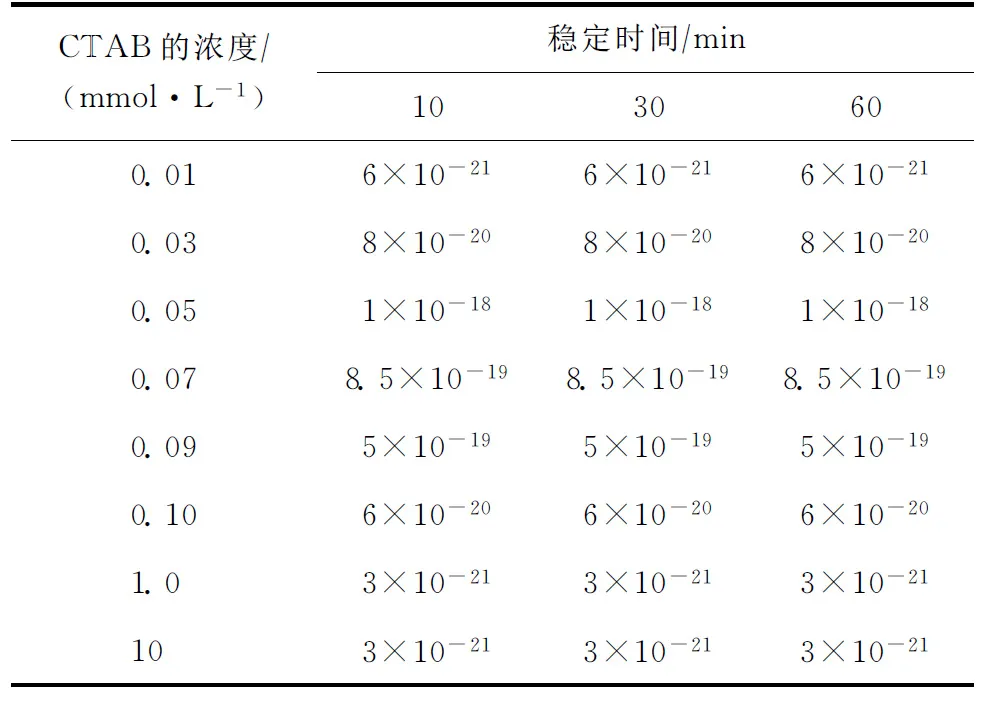
表2 CTAB的濃度對二氧化硅表面疏水作用力常數的影響 J
2.2 電解質的影響
2.2.1 電解質對二氧化硅表面間作用力的影響向不同濃度的CTAB溶液中分別加入KCl,使其濃度為10 mmol/L,隨著穩定時間的變化,二氧化硅表面間膠體作用力的變化曲線見圖4,二氧化硅表面間的黏著力變化見表3。由圖4(a)和表3可以看出:當CTAB濃度為0.03 mmol/L時,穩定時間為10 min,長程排斥力非常微弱,在距離為3 nm處為弱吸引力,黏著力為2.5 mN/m;當穩定時間從30 min延長至60 min時,長程排斥力逐漸增大,相應的黏著力由2.2 mN/m減小為1.6 mN/m。
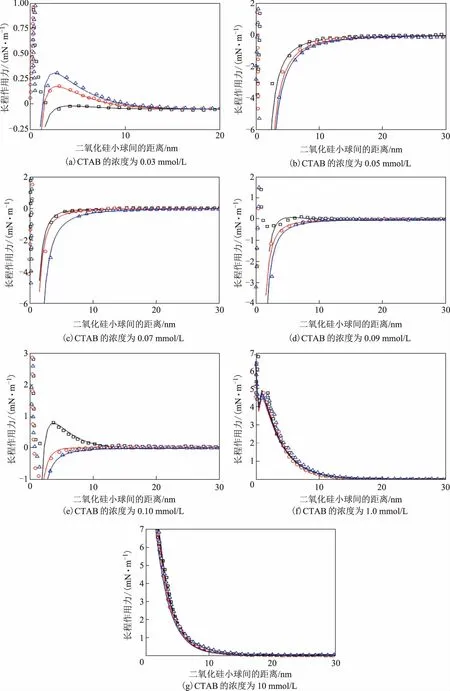
圖4 在CTAB溶液中加入KCl后二氧化硅表面間的作用力隨穩定時間的變化
此時CTAB在二氧化硅表面的吸附是單層吸附,并且吸附量隨著穩定時間的延長逐漸減小。
由圖4(b)~(e)可以看出:當CTAB的濃度低于CMC時,隨著濃度的增加,CTAB在二氧化硅表面的吸附量增加,但是加入電解質KCl會導致二氧化硅表面間的膠體作用力隨著穩定時間的延長而發生改變。這是由于KCl的加入導致CTAB在二氧化硅表面發生不同程度的解吸附。以上試驗結果與文獻所報道的結果相似[17],即在低濃度的CTAB溶液中加入濃度為10 mmol/L的電解質,觀察到二氧化硅表面基底上的CTAB吸附量很快減少最后完全消失。
由圖4(f)~(g)可以看出:當CTAB的濃度增大為1.0 mmol/L時,長程作用力為強排斥力,黏著力為0,且在整個測試過程中所獲得的作用力幾乎無差異,此時CTAB在二氧化硅表面的形成致密的雙層吸附。當CTAB溶液的濃度增加為10 mmol/L,實驗結果與濃度為1.0 mmol/L時差別較小。可見只要CTAB的濃度大于CMC時,在二氧化硅表面形成致密的雙層吸附或者膠束,就不會因電解質的存在而被取代。
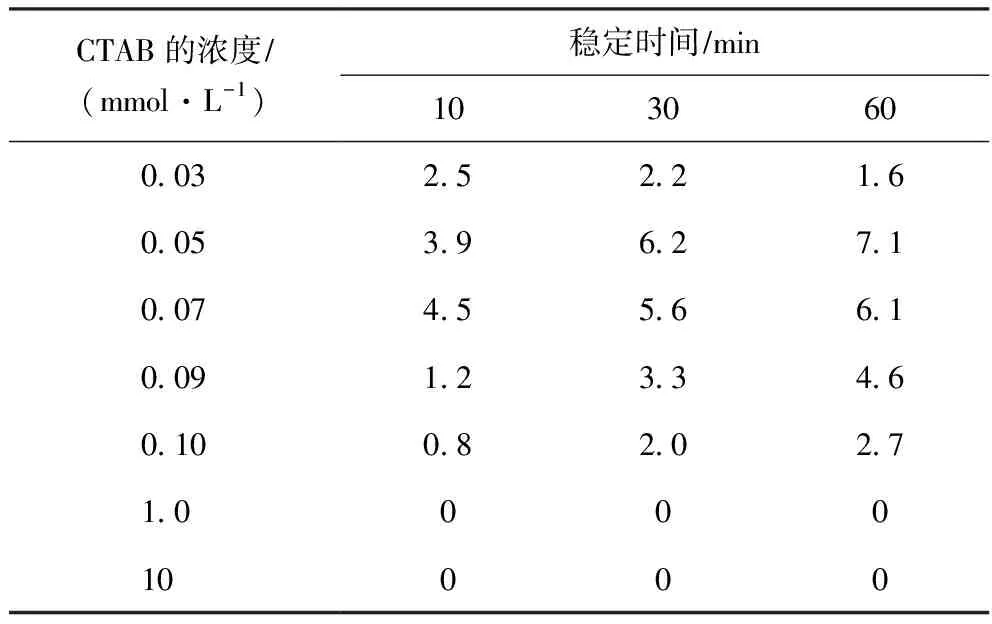
表3 在CTAB溶液中加入KCl后二氧化硅表面間的黏著力隨穩定時間的變化 mN/m
2.2.2 電解質對二氧化硅表面Zeta電位的影響向不同濃度的CTAB溶液中加入濃度為10 mmol/L的電解質KCl溶液,二氧化硅表面的Zeta電位隨著時間的變化曲線見圖5。由圖5可以看出:在濃度為0.01 mmol/L的CTAB溶液中加入10 mmol/L KCl時,隨著穩定時間的延長二氧化硅表面的Zeta電位升高(電負性減小),穩定時間分別為10,30,60 min時,Zeta電位依次為-37,-32,-25 mV;當CTAB的濃度從0.03 mmol/L增加到0.10 mmol/L時,二氧化硅表面的Zeta電位持續升高;同一濃度的CTAB溶液中,二氧化硅表面的Zeta電位隨著穩定時間的推移電負性逐漸增強;當CTAB濃度進一步增加為1.0 mmol/L和10 mmol/L時,在系統穩定時間內Zeta電位一直穩定在70 mV左右。可見,在濃度低于1.0 mmol/L的CTAB溶液中加入濃度為10 mmol/L的KCl溶液,隨著穩定時間的延長,二氧化硅表面的Zeta電位變化幅度較大,這種變化是由于電解質的解吸附作用影響了CTAB在二氧化硅表面的吸附所造成的。
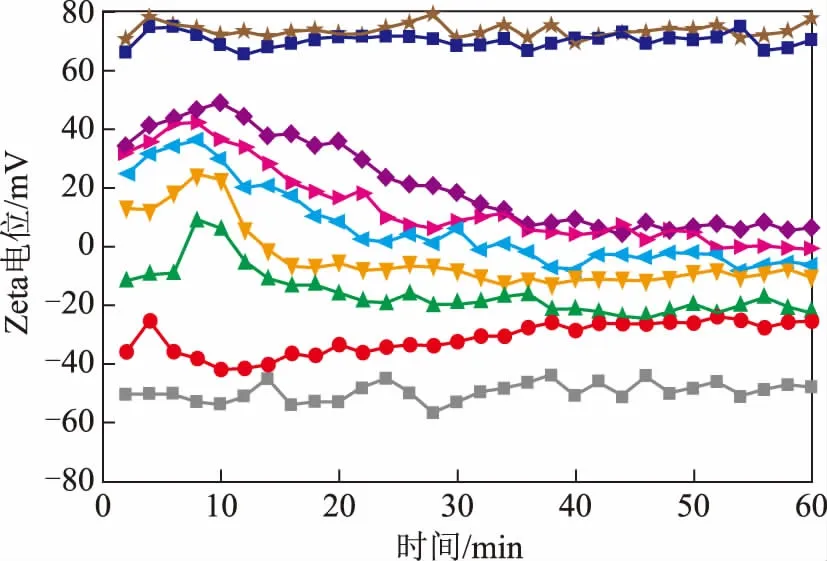
圖5 向不同濃度的CTAB溶液中加入電解質對二氧化硅微粒表面Zeta電位的影響CTAB濃度,mmol/L: ■—0; ●—0.01; ▲—0.03; ◆—0.1; ■—1.0; ★—10
2.2.3 電解質對二氧化硅表面疏水作用力常數的影響CTAB溶液中加入電解質后,隨著穩定時間的延長會影響二氧化硅表面間的膠體作用力,這可以通過疏水作用力常數來證實。電解質對疏水作用力常數的影響見表4。由表4可以看出:CTAB濃度為0.03 mmol/L的溶液中加入濃度為10 mmol/L的KCl溶液時,系統穩定時間為10 min,疏水作用力常數為9×10-21,當穩定時間延長為60 min,疏水作用力常數減小為5×10-21,說明二氧化硅表面的疏水性隨著穩定時間的延長而減弱;在濃度較低時,CTAB在二氧化硅表面呈單層吸附狀態,由于KCl將吸附在二氧化硅表面的CTAB取代[15],導致吸附的CTAB總量減少;當CTAB的濃度由0.05 mmol/L增加到0.10 mmol/L時,二氧化硅表面間長程作用力為吸引力,表明CTAB在二氧化硅表面形成雙層吸附,疏水吸引力常數隨著穩定時間的延長而增大;當CTAB的濃度增大為1.0 mmol/L時,疏水作用力常數為3×10-21J,表明二氧化硅表面的潤濕性轉變為親水性,CTAB在二氧化硅表面形成致密的雙層吸附;當CTAB的濃度增加為10 mmol/L時,疏水作用力常數仍然穩定為3×10-21J。可見,只要CTAB的濃度大于CMC,在二氧化硅表面形成致密的雙層吸附或者膠束,就不會因電解質的存在而被取代。

表4 電解質對二氧化硅表面疏水作用力常數的影響 J
2.3 電解質與CTAB協同作用的討論
CTAB在二氧化硅表面的吸附及被電解質取代的過程示意見圖6。在不含電解質的低濃度溶液中,CTAB在帶負電荷的二氧化硅表面通過靜電作用實現單層吸附即親水基朝向二氧化硅表面而疏水基團朝向水溶液,這使得二氧化硅基片表面疏水性增強。CTAB的濃度進一步增加,由于CTAB尾基鏈-鏈間的疏水吸引力,形成頭基朝向水溶液的雙層吸附,二氧化硅表面潤濕性再次向親水性方向轉變。雙層吸附的形成過程是:首先陽離子表面活性劑分子通過靜電吸引力在二氧化硅表面形成單層吸附,然后通過疏水性尾基間的疏水吸引力形成第二層吸附。這樣的雙層吸附不僅增強了二氧化硅表面的正電性,而且減小了二氧化硅表面的疏水性。
當向低濃度的CTAB溶液中加入KCl時,CTAB在二氧化硅表面呈單層吸附狀態,二氧化硅表面的疏水性隨著穩定時間的延長而減弱。這是由于吸附在二氧化硅表面的CTAB被KCl取代,減少了吸附在二氧化硅表面的CTAB總量。隨著CTAB濃度的進一步增加,疏水作用力常數隨著穩定時間的延長而增大,表明二氧化硅表面的疏水性逐漸增強。原因是隨著CTAB溶液濃度的增大,在二氧化硅表面形成雙層吸附,但是由于電解質的解吸附作用,隨著穩定時間的延長,KCl將第二層CTAB取代導致吸附形態變成單層吸附[如圖6(b)所示],從而增強了二氧化硅表面的疏水性。可見,當CTAB的濃度低于CMC時,隨著濃度的增加,CTAB在二氧化硅表面的吸附量增加,由于電解質KCl的加入導致CTAB在二氧化硅表面發生不同程度的解吸附,使得二氧化硅表面間的膠體作用力隨著穩定時間的延長而發生改變。當CTAB濃度大于CMC時,在系統穩定時間內Zeta電位一直穩定在70 mV左右,二氧化硅表面間的長程作用力為排斥力,黏著力為0,疏水作用力常數也非常穩定,表明在CTAB濃度高于CMC的溶液中,隨著穩定時間的延長,二氧化硅表面的電化學性質穩定,并不會被電解質取代。
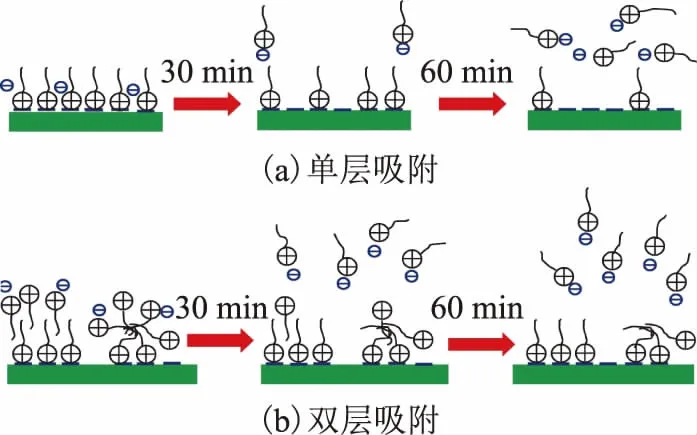
圖6 CTAB在二氧化硅表面的吸附及被電解質取代的過程示意 —CL-; —CTAB
3 結 論
(1) CTAB的濃度、電解質、吸附穩定時間均會影響二氧化硅表面間的膠體作用力和二氧化硅表面的潤濕性。隨著CTBA濃度的增加,無論溶液中是否加入電解質KCl溶液,CTAB在二氧化硅表面的吸附量也會不斷增加,長程作用力由吸引力轉變為排斥力,相應的黏著力先增大后減小最終為0,這表明CTAB在二氧化硅表面的吸附由單層吸附轉變為致密的雙層吸附,二氧化硅表面的潤濕性由親水性變為疏水性最后又轉變為親水性。
(2) 當CTAB溶液中含有濃度為10 mmol/L 的KCl時,CTAB濃度較低時,隨著穩定時間的延長,長程作用力由弱吸引力逐漸轉變為排斥力,相應的黏著力減小;CTAB濃度較高時,隨著穩定時間的延長,長程吸引力逐漸增強,相應的黏著力也增加。當CTAB濃度增大到1.0 mmol/L和10 mmol/L時,在整個測試過程中,長程作用力為排斥力,黏著力為0。電解質的加入及測試系統穩定時間的延長所獲得的二氧化硅表面間膠體作用力的變化能反應出CTAB在二氧化硅表面吸附形態改變的情況,從而反映出二氧化硅表面潤濕性的變化。
(3) 二氧化硅表面的長程作用力和黏著力測試結果均可由二氧化硅表面的Zeta電位來驗證。CTAB在二氧化硅表面的吸附對其表面間的膠體作用力和表面電荷有重大的影響,從而導致表面潤濕性的改變,并且所獲得的二氧化硅表面間的長程作用力與包含疏水作用力的E-DLVO理論值能很好地擬合。試驗結果不僅能為CTAB在二氧化硅表面的吸附或者解吸附所改變的表面潤濕性提供理論論證,而且能為提高油砂中瀝青油的收率提供理論依據。因此為了提高瀝青的回收效率,在油砂水基分離過程中需要考慮CTAB的濃度、電解質、吸附穩定時間等因素的影響。

