不同眼內灌注液對PDR患者玻璃體切割術后晶狀體混濁程度的影響
張曉培,姚 進
0引言
增殖性糖尿病視網膜病變(proliferative diabetic retinopathy, PDR)是糖尿病(DM)重要的眼部并發癥,玻璃體切割手術是目前治療PDR的主要方法。硅油填充眼PDR患者術后白內障發展迅速,二次取油手術時為獲得更清晰的手術視野,部分需聯合白內障手術。研究顯示,PDR患者微血管病變嚴重,基礎抵抗力差,聯合手術操作多時間長,可加重術后繼發高眼壓、眼前節炎癥反應及虹膜新生血管等并發癥的發生[1-2]。眼內灌注液是應用于玻璃體切割手術的重要物質,術中灌注液長時間與眼組織直接接觸,其化學成分、滲透壓、離子緩沖容量、pH值等均可影響術后眼組織的結構和功能[3-4]。以往研究多集中于灌注液對術后角膜內皮[5]、視網膜神經細胞及視網膜血管[6]等的影響,而關于其影響玻璃體切割術后并發性白內障進展的報道卻甚少。本研究選擇臨床常用眼內灌注液BSS及國產世可灌注液進行研究,旨在探討不同灌注液對玻璃體切割術后PDR患者晶狀體混濁程度的影響,為內眼手術灌注液的選擇提供新的思路。
表1 兩組患者基線資料的比較

組別男/女(例)年齡(x±s,歲)DR病程(x±s,a)DM病程(x±s,a)HbA1c(x±s,%)BSS灌注液組11/1254.2±7.11.7±0.810.4±4.25.34±0.36世可灌注液組10/1555.8±5.72.1±1.29.3±5.85.46±0.32 t/χ20.298-0.873-1.237-1.693-0.797P0.5850.3870.2220.0970.430
1對象和方法
1.1對象選取2018-03/2019-02于我院行玻璃體切割手術的PDR患者48例48眼,其中男21例,女27例,平均年齡55.0±6.4歲。隨機分為BSS灌注液組(23例23眼)和世可灌注液組(25例25眼),術中分別采用BSS灌注液和世可灌注液。兩組患者患者年齡、性別、糖尿病病程、糖尿病視網膜病變(DR)病程及糖化血紅蛋白(HbA1c)水平比較,差異無統計學意義(均P>0.05),提示兩組患者行玻璃體切割手術前基線水平一致,具有可比性,見表1。本研究經醫院倫理委員會批準,所有患者均簽署受試者知情同意書。
1.1.1納入標準(1)經內分泌科確診為2型糖尿病,病程5a以上,確診為PDR,診斷符合中華醫學會《我國糖尿病視網膜病變臨床診療指南》(2014年)相關標準[7];(2)存在不同程度玻璃體積血,符合玻璃體切割手術適應證;(3)首次行玻璃體切割手術,術中未見明顯出血或出血后充分電凝止血。
1.1.2排除標準(1)既往有眼部手術史、創傷史者;(2)合并青光眼、葡萄膜炎及視網膜脫離等眼部病史者;(3)合并任何影響手術及術后恢復的全身性疾病者;(4)血糖、血壓等控制不理想者;(5)玻璃體切割術中聯合白內障手術者,術中發現合并牽拉性視網膜脫離者;(6)術后經檢查發現合并明顯黃斑囊樣水腫者;(7)術后3mo隨訪中發現合并繼發性高眼壓、葡萄膜炎及新生血管性青光眼等并發癥者;(8)術后檢查病歷資料不完善、檢查配合欠佳及依從性差者。
1.2方法
1.2.1手術方法所以患者玻璃體切割手術均由同一名具有豐富玻璃體視網膜手術經驗的醫師完成。采用23G標準三通道閉合式玻璃體切割術,術中動作盡可能輕柔,避免觸及晶狀體,盡可能切除全部玻璃體,清除全部纖維血管膜,充分電凝止血,同時完成視網膜激光光凝及硅油填充,其中術中激光光凝采用相同能量、曝光時間及光斑直徑,全視網膜激光光凝光斑點數均在600~650灶。手術持續時長約1~1.5h。術后常規局部使用抗生素滴眼液、糖皮質激素滴眼液、托吡卡胺滴眼液及玻璃酸鈉滴眼液。囑患者術后定期隨訪。
1.2.2隨訪觀察隨訪至術后3mo,觀察視力、眼壓及晶狀體混濁程度、密度和厚度情況,并記錄術后并發癥發生情況。
1.2.2.1視力視力檢測包括裸眼視力和最佳矯正視力(BCVA),采用標準對數視力表檢查,結果轉換為最小分辨角對數(LogMAR)視力進行統計分析。
1.2.2.2眼壓使用非接觸眼壓計(NCT)測量眼壓,囑患者下顎固定于下支架上,前額緊貼上支架,使眼睛與NCT噴嘴位于同一高度,睜大眼睛注視檢測噴嘴內的紅色亮點。當眼壓計焦距與角膜映光點重疊且清晰時,NCT 即自動噴氣,顯示屏即顯示被測眼眼壓,連測3次,取平均值。
1.2.2.3晶狀體混濁程度通過眼前節彩色照相檢查觀察晶狀體混濁程度,并進行分級評分。患者經充分散瞳后,于暗室采用0.2mm裂隙光寬度,45°照射,聚焦晶狀體核中央,裂隙燈光長度完全覆蓋瞳孔邊緣,采集晶狀體核(NC)照片;于暗室采用3.0~4.0mm裂隙光寬度,3°~5°照射,分別聚焦于瞳孔水平及后囊膜水平,采集晶狀體皮質(C)及后囊膜(P)照片[8]。
晶狀體LOCSⅢ分級評分標準:根據LOCSⅢ分級系統的標準圖片,將每相鄰2張標準圖片之間再細分成10等份,判斷晶狀體混濁程度在兩級之間的位置。LOCSⅢ分級分值范圍:晶狀體核(NC)顏色為1.0~6.9,皮質(C)混濁為1.0~5.9,后囊膜(P)混濁為1.0~5.9。由2位主治醫師分別在獨立檢查室的裂隙燈下判斷晶狀體混濁程度,并進行分級評分,取平均值。
1.2.2.4晶狀體密度和厚度采用Petacam眼前節分析儀測量晶狀體密度及厚度。囑患者切勿眨眼或轉動眼球,注視藍色光帶中央的固視目標,采用Enhanced dynamic模式掃描,掃描軸向為90°~270°,掃描時間為0.3s。檢查結束記錄晶狀體密度及厚度值。所有檢查均由同一位經驗豐富的醫師完成,重復測量3次,取平均值。
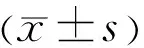
2結果
術前,兩組患者視力(裸眼視力和BCVA)、眼壓比較,差異無統計學意義(均P>0.05);術后3mo,兩組患者視力均較術前顯著改善(P<0.05),眼壓均無明顯變化(P>0.05),但兩組之間視力和眼壓比較,差異無統計學意義(t=0.83、0.645、-1.389,均P>0.05)。術前,兩組患者晶狀體LOCSIII分級NC、C和P評分值及晶狀體密度和厚度值比較,差異均無統計學意義(P>0.05)。術后3mo,兩組患者晶狀體LOCSIII分級NC、P評分值及晶狀體密度顯著高于術前(P<0.05),而C評分值與術前均無顯著差異(P>0.05);此外,BSS灌注液組患者晶狀體厚度顯著高于術前(P<0.05),而世可灌注液組與術前無顯著差異(P>0.05)。術后3mo,世可灌注液組患者晶狀體LOCSIII分級NC、P評分值均顯著低于BSS灌注液組(t=5.4、7.559,均P<0.05),但兩組患者C評分值差異無統計學意義(t=-0.113,P>0.05);世可灌注液組患者晶狀體密度和厚度值均顯著低于BSS灌注液組,差異具有統計學意義(t=7.432、3.360,均P<0.05)。兩組患者手術前后眼前節彩色照相檢查結果見圖1。

圖1 手術前后兩組患者眼前節彩色照相檢查結果 A:BSS灌注液組患者術前檢查;B:圖A同患者術后3mo檢查;C:世可灌注液組患者術前檢查;D:圖C同患者術后3mo檢查。
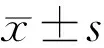

觀察指標BSS灌注液組術前術后3motP世可灌注液組術前術后3motP裸眼視力1.2±0.20.8±0.37.888<0.0011.1±0.20.7±0.28.365<0.001BCVA1.2±0.20.5±0.312.566<0.0011.1±0.20.4±0.314.210<0.001眼壓(mmHg)14.6±4.414.96±3.94-0.7860.44815.2±3.916.40±3.25-1.9670.064LOCSIII分級評分(分) 晶狀體核(NC)2.39±0.573.30±0.52-5.152<0.0012.36±0.512.73±0.41-4.044<0.001 皮質(C)2.40±0.482.45±0.45-0.5960.5572.40±0.442.46±0.39-1.2740.216 后囊膜(P)1.06±0.172.64±0.67-9.483<0.0011.08±0.201.53±0.28-7.467<0.001晶狀體密度(%)26.13±3.1131.26±2.62-6.366<0.00125.52±3.4227.12±0.93-2.4030.024晶狀體厚度(mm) 3.44±0.243.66±0.19-3.9340.0013.38±0.253.49±0.16-1.8080.083
3討論
PDR患者組織細胞長期處于高糖環境中,其視網膜局部氧化應激產物大量激活,炎癥因子表達增加,組織能量代謝障礙,導致眼組織氧化應激與氧化損傷加重,是玻璃體切割術后并發性白內障迅速發展的高危人群[9]。并發性白內障是玻璃體切割術后最常見的并發癥之一,患者年齡、術中手術器械是否接觸晶狀體、術中眼內灌注液的使用及術后眼內填充物等均可導致并發性白內障的發生[10]。其發生的機制主要包括以下三方面:(1)氧分壓改變[11-12]:正常眼球內角膜、前房和視網膜氧分壓相對較高,而玻璃體和晶狀體則相對較低。晶狀體維持透明性主要依賴于其所處的相對低氧環境。玻璃體一經切除,晶狀體暴露于高氧環境下,其蛋白基因不同位點發生突變,進而造成蛋白聚合、不溶性增加,發生晶狀體的核性混濁。(2)光損傷[13]:手術顯微鏡及光導纖維術中長時間直射晶狀體,可打破其自由基動態平衡,引發氧化應激反應,損害晶狀體上皮細胞及線粒體膜功能,最終導致晶狀體內不溶性蛋白增加,晶狀體透明性下降。(3)晶狀體營養代謝障礙[14]:玻璃體切割術后,玻璃體腔內結構和組份改變,晶狀體氧攝入及代謝產物清除等無法正常進行,其營養代謝障礙,誘發其透明性下降。因此,通過術中、術后采取相關保護措施,延緩PDR患者玻璃體切割術后并發性白內障的發展,降低聯合白內障手術率,將給PDR患者帶來福音。
隨著玻璃體切割手術的廣泛應用,眼內灌注液的研究也趨向深入。目前臨床使用較多的為BSS灌注液,而近年來國產世可灌注液亦逐漸進入人們的視野。本研究結果顯示,世可灌注液相較于BSS灌注液,可在一定程度上抑制PDR患者玻璃體切割術后并發性白內障的發生發展,但目前尚缺乏世可灌注液減緩玻璃體切割術后并發性白內障發生的具體機制的研究。世可灌注液配方成份顯示,相較于常用的BSS灌注液,其中添加了碳酸氫鈉及葡萄糖兩種主要物質分別作為眼內能量代謝來源和組織緩沖劑,使其組織成分更接近生理房水和玻璃體狀態,大大減少了術中或術后由于眼內環境改變所造成的眼內組織的損傷。正常機體細胞生長所需的pH值約為7.2~7.4,若細胞處于低pH值的酸性環境,氧自由基大量生產,誘導細胞發生凋亡[15]。Winkler等[15]認為眼內灌注液中的碳酸氫根離子可使睫狀體上皮靜止電位的極性反轉,房水側由負電位變成正電位,其后房水中濃度遠高于血漿,構成了眼內的主要緩沖系統,在一定程度上可對抗由其他添加物引起的pH值的改變,有利于保護眼內組織。世可灌注液中增添碳酸氫鈉或可通過上述原理保護眼內組織的結構及功能。
此外,所有細胞正常功能的維持均來源于葡萄糖代謝所產生的能量。據報道,機體細胞在缺乏葡萄糖的情況下,氧自由基大量生產,細胞凋亡增加[15]。玻璃體切割術后,晶狀體上皮細胞氧化磷酸化作用減弱,三磷酸腺苷(ATP)產生減少,繼而晶狀體中離子及氨基酸轉運受阻,白內障發展加速。而世可灌注液中另一種區別于BSS灌注液的有效成分即為葡萄糖。葡萄糖可作為晶狀體的主要能量來源,其在組織液中有助于維持晶狀體的透明性。研究表明,眼內灌注液中添加葡萄糖可保持糖尿病大鼠晶狀體的透明性[13]。Christiansen等[16]使用不同灌注液灌注離體猿晶狀體,發現格林液中若加入5%葡萄糖可使晶狀體的透明性增加20%,加入碳酸氫鈉可繼續增加40%,如同時加入二者則晶狀體透明率可達70%。我們推測這或與葡萄糖作為能量來源,可改善玻璃體切割術后晶狀體的營養代謝狀況有關。
本研究納入樣本量較少,后期研究中需進一步擴大樣本量,以佐證世可灌注液抑制玻璃體切割術后并發性白內障發展的作用。此外,本研究隨訪時間較短,仍需更長時間的追蹤以明確玻璃體切割術后兩組患者間白內障的發展情況。總之,世可灌注液作為國產自主研發產品,其價格便宜,是一種前景良好的眼內灌注液,可供臨床工作者選擇。

