電磁效應對心肌細胞搏動行為的影響
蘆珺

【摘?要】本文以竇房結心肌細胞模型為研究對象,在離子通道上引入磁控憶阻器模型,構建細胞內(nèi)電荷和磁通量之間的非線性關系,以此表征細胞內(nèi)外離子交換誘發(fā)的電磁感應效應,研究電磁效應對細胞動力學行為的影響,通過對 Zhang 等人構建的完整兔子心臟模型進行改進,討論電磁輻射作用對心肌細胞體系動力學行為的影響。有助于分析和預測在復雜電磁環(huán)境下,外部刺激對其動力學行為的影響和調(diào)控,為揭示心律失常、心臟離子通道疾病的內(nèi)在規(guī)律提供新的研究思路。
【關鍵詞】竇房結,電磁輻射,刺激,憶阻突觸
眾所周知,心臟的自律性來源于心臟內(nèi)特殊的自律細胞—竇房結細胞. 心臟的節(jié)律活動受到竇房結的控制,早在80年,人們就首次建立了兔子竇房結細胞的數(shù)學模型來描述心肌細胞的膜電活動[1],后來Noble等人進行了修正[2].近年來,曼徹斯特大學的張恒貴領導的生物物理中心,在實驗的基礎上考慮了迷走神經(jīng)對心臟活動的影響,在從心臟系統(tǒng)亞細胞級到整個器官級等多維結構生物建模與計算方面的研究取得了較大的進展,建立了許多哺乳動物竇房結細胞的實驗模型[3,4]. 從以上結果可以看出,人們從實驗和理論角度,利用不同的模型從對心臟中竇房結細胞的動力學過程進行了研究,但是,到目前為止,人們在研究細胞模型時,較多的是考察通道電流和外界電刺激引起的膜電位的產(chǎn)生及波動情況,較少涉及細胞內(nèi)部電磁感應作用以及外部電磁輻射的調(diào)控作用[6],為了進一步研究生物網(wǎng)絡中存在的電磁場作用,人們將新型電子元件憶阻器引入到生物系統(tǒng)中,圍繞憶阻器與細胞模型構建新的生物模型。在本文中,為考察電磁輻射對心肌細胞起搏行為的影響,我們基于Luo-Rudy(LR)模型,并在張恒貴等人構建的兔子竇房結-心肌完整的動作電位模型的基礎上[4],借助于三次磁控憶阻器模型,將電磁輻射的作用引入到心肌竇房結細胞體系中,構建了電磁輻射下竇房結-心肌動作電位模型耦合體系,并利用此體系研究了電磁輻射對竇房結起搏行為的影響及調(diào)控作用。
1?模型描述與方法
隨著實驗技術的不斷進步,Zhang等人在2000年建立較為完整的兔子竇房結-心房二維組織結構模型,能較好地描述竇房結組織細胞的起搏行為[4]。單個細胞動力學行為滿足如下:
其中,V代表膜電壓,Cm是膜電容。參照以往文獻[6,7]的方法,我們引入一個新增變量磁通量來考察電磁輻射的作用。根據(jù)法拉第電磁感應定律可知,利用等效感應電流i 來近似表征感應電動勢的作用,結合憶阻器的定義,附加在細胞膜離子通道上的感應電流i可表示為:
考慮電磁感應對細胞的作用后,我們將上述模型方程(1a)改進為兩變量方程:
其中,表示穿過細胞膜的磁通,是三次磁控憶阻器的電導[6],用來描述磁通量和膜電位之間的作用,滿足,,為相對應的參數(shù)[23]。參數(shù),和分別表示磁通和膜電位的相互作用且與介質(zhì)相關的參數(shù)。細胞離子通道上電荷定向移動而產(chǎn)生電磁感應現(xiàn)象,從而調(diào)制其搏動節(jié)律并影響動作電位。分別將中心竇房結SANC、邊緣竇房結SANP到心房Atrium等細胞按生理結構順序依次排列,記錄其放電規(guī)律。
2?結果與討論
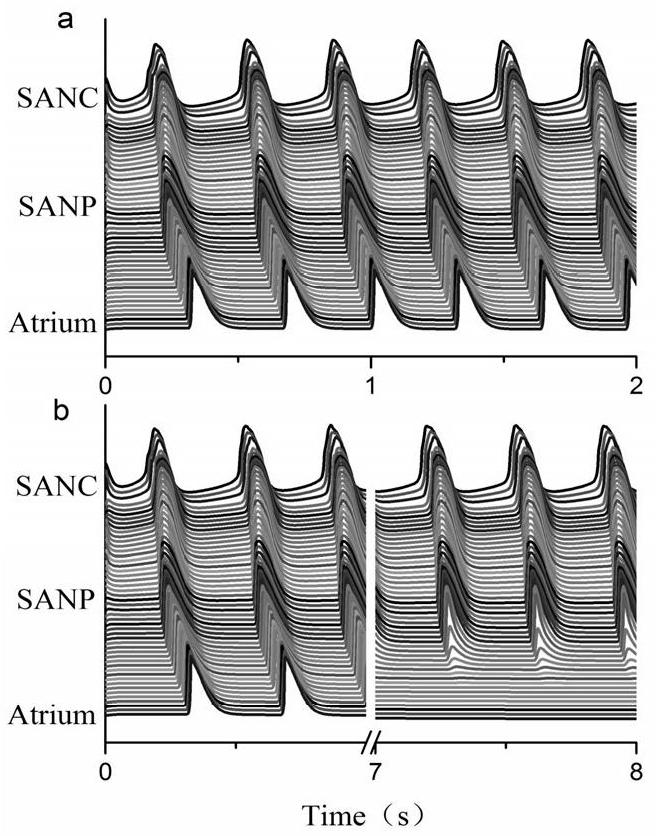
取=0.01,=0.01,=0.8,取電磁感應參數(shù)的值為0.005和0.0095。從圖a模擬結果可以看出,動作電位先從中心竇房結處產(chǎn)生然后傳播至邊緣竇房結以及心房區(qū)域,該振動過程可以持續(xù)進行,記錄細胞起搏周期CL=377ms,與正常值相符,這表明在適當?shù)膬?nèi)部電磁輻射下,竇房心肌細胞能夠維持正常的起搏過程。當增大電磁感應參數(shù)=0.0095時,圖b可以看到,竇房結仍可產(chǎn)生起搏過程并持續(xù)向外傳遞,不過,這種電信號的傳遞無法持續(xù),一段時間后出現(xiàn)時間上的死振。
3?結?論
綜上所述,在兔子二維竇房結-心房結構模型基礎上,引入三次磁控憶阻器對原模型中細胞方程加以改造,從而將電磁輻射的作用效果疊加到細胞體系中。模擬結果發(fā)現(xiàn),電磁作用對竇房結體系的起搏周期有一定的影響,正常心肌細胞中存在在一定范圍的電感效應。而當通道上離子流動過快從而導致過大的電磁感應效應時,體系內(nèi)出現(xiàn)了死振的現(xiàn)象,這表明細胞離子通道上離子的定向移動導致的感應電流會引起一定程度的竇性過速和房顫等癥狀,嚴重時甚至會導致心臟停跳,這將有助于進一步了解電磁輻射的生物效應的作用機理,以及對心臟竇房結體系的動力學行為進行實驗研究和臨床診斷提供一定的理論依據(jù)。
參考文獻:
[1]Clancy CE,Rudy Y. Linking a genetic defect to its cellular phenotype in a cardiac arrhythmia. Nature,1999,400:566-569.
[2]Hodgkin AL,Huxley AF. A quantitative description of membrane current and its application to conduction and excitation in nerve. J Physiol,1952,117:500-544.
[3]Zhang HG,Holden AV,Noble D,Boyett MR,Analysis of the Chronotropic Effect of Acetylcholine on Sinoatrial Node Cells. J of Cardiovascular Electrophysiology,2002,13:H465-474.
[4]Zhang HG,Holden AV,Kodama I,Honjo H,et al,Mathematical models of action potentials in the periphery and center of the rabbit sinoatrial node.Am J Physiol Heart Circ Physiol 2000,279:H397-421.
[5]J.Ma,Y.Wang,C.Wang,et al,Mode selection in electrical activities of myocardial cell exposed to electromagnetic radiation. Chaos,Solitons & Fractals,2017,99:219–225.
基金項目:
皖南醫(yī)學院中青年科研基金(WK201923)。
(作者單位:皖南醫(yī)學院公共基礎學院)

