酸性染料易染氨綸的染色動力學
韓 虎, 李偉婷, 魏會芳, 王小艷, 孫 昌, 許長海
(1. 煙臺泰和新材料股份有限公司, 山東 煙臺 264006;2. 生態紡織教育部重點實驗室(江南大學), 江蘇 無錫 214122)
氨綸的化學組成為聚氨基甲酸酯,是一種嵌段共聚體,分子中包含柔性鏈段和剛性鏈段,具有優良的彈性和良好的回彈性能。由各種形態的氨綸紗(如裸紗、包纏紗、合捻紗、包芯紗等)織成的彈力面料具有良好的服用性、舒適性和功能性,在國內外市場極受歡迎[1]。然而,對于氨綸含量較高的紡織面料,尤其是氨綸以“裸絲”織造的面料,必須解決氨綸染色的問題,否則紡織面料在拉伸狀態下會產生氨綸“露白”現象,影響紡織品的外觀質量[2]。
氨綸通常以分散染料染色為主[3-5],其玻璃化轉變溫度低(聚酯型為25~45 ℃,聚醚型為50~70 ℃),分子鏈段在低溫下即可運動,使染料分子進入纖維內部而上染,但由于分散染料在低溫下溶解性差,上染速率低,染色效果不理想;而使用分散染料在高溫下染色則會對氨綸的結構性能造成影響[6]。有研究報道以中性和弱酸性染料對氨綸進行染色[7-8],但氨綸染色性能對染料的結構和類別依賴性大,因此使用較少。通過向氨綸中物理添加助劑或者對氨綸進行化學改性,賦予氨綸可染基團或“染座”,可達到氨綸纖維易染的效果[9]。或者向聚氨酯溶液中加入混合胺擴鏈劑的方法制備酸性染料易染氨綸,在酸性染色條件下,酸性染料易染氨綸帶正電荷,因此,可使用酸性染料進行染色[10]。本文擬使用結構簡單的酸性橙II對酸性染料易染氨綸染色,通過分析染色動力學過程,對其酸性染料染色性能進行評價。
1 實驗部分
1.1 實驗材料
普通氨綸(T-315 267型)、酸性染料易染氨綸(T-315 267R型),煙臺泰和新材料股份有限公司。
1.2 實驗藥品
酸性橙Ⅱ(即C.I.酸性橙7,純度>97%),上海梯希愛化成工業發展有限公司;檸檬酸、檸檬酸三鈉、醋酸、醋酸鈉、碳酸鈉、磷酸氫二鈉、磷酸二氫鈉,均為分析純,國藥集團化學試劑有限公司;去油劑TF109-H(工業級),浙江傳化集團有限公司。
1.3 實驗設備
UC 152D型磁力攪拌器(英國STUART公司);AHIBA IR型染色小樣機(美國Datacolor 公司);UV-260型紫外-可見分光光度計(日本島津公司)。
1.4 氨綸前處理
將一定量的氨綸按浴比為1∶50投入到含有 2 g/L 去油劑TF-109H和2 g/L碳酸鈉的前處理液中,在90 ℃條件下處理30 min,然后對其進行充分水洗,在室溫下晾干待用。
1.5 氨綸染色及上染量測試
分別使用pH值為3的檸檬酸鈉緩沖溶液(濃度為0.05 mol/L)、pH值為5的醋酸鈉緩沖溶液(濃度為0.05 mol/L)和pH值為7的磷酸鈉緩沖溶液(0.05 mol/L)配制質量濃度為0.2 g/L的酸性橙II染液,將2 g 氨綸纖維按浴比為1∶100投入染液,分別在染色小樣機于50和70 ℃下染色。當染色進行一定時間后,取適量染液,以pH值為4.0的醋酸鈉緩沖溶液(濃度為0.05 mol/L)按倍數稀釋,采用紫外-可見分光光度計測量染液吸光度。使用pH值為4的醋酸鈉緩沖溶液(濃度為0.05 mol/L)精確配制不同濃度的酸性橙II標準溶液,繪制染料在最大吸收波長(485 nm)處的標準工作曲線。通過標準工作曲線計算染液濃度(CS,mg/g),進而計算酸性橙II對氨綸纖維的上染量(CF,mg/g),計算公式為
CF=(0.2-CS)×100
(1)
2 結果與討論
2.1 上染過程分析
由于酸性染料易染氨綸是通過向聚氨酯溶液中加入混合胺擴鏈劑的方法制備得到,因此,分子鏈段中含有可質子化的氨基。在酸性染色條件下,酸性染料易染氨綸纖維因氨基質子化而帶正電荷,形成了陽離子“染座”。酸性橙II是含有1個磺酸基的強酸性染料,在染液中可發生電離而形成染料陰離子,因此,酸性染料易染氨綸在適當染色條件下可通過靜電吸附作用使酸性橙II上染。本文利用上染速率曲線來描述酸性橙II在酸性染料易染氨綸纖維上的動態上染過程。
2.1.1 酸性染料易染氨綸與普通氨綸對比
圖1示出在pH值為3、溫度為70 ℃條件下,酸性橙Ⅱ對酸性染料易染氨綸和普通氨綸染色時的上染速率曲線。染色初期,酸性橙II在酸性染料易染氨綸纖維上的上染量快速增加,隨著染色時間的延長,上染速率逐漸降低,當染色時間達到60 min時,染色過程基本達到平衡;普通氨綸纖維的初始上染速率和上染量均明顯低于酸性染料易染氨綸纖維,而且染色時間延長至120 min時仍未達到平衡狀態。造成二者之間明顯差別的原因是酸性橙II在上染普通氨綸纖維時主要通過分子間作用力與纖維結合,而上染酸性染料易染氨綸纖維時除分子間作用力外,主要通過靜電引力與纖維相結合。
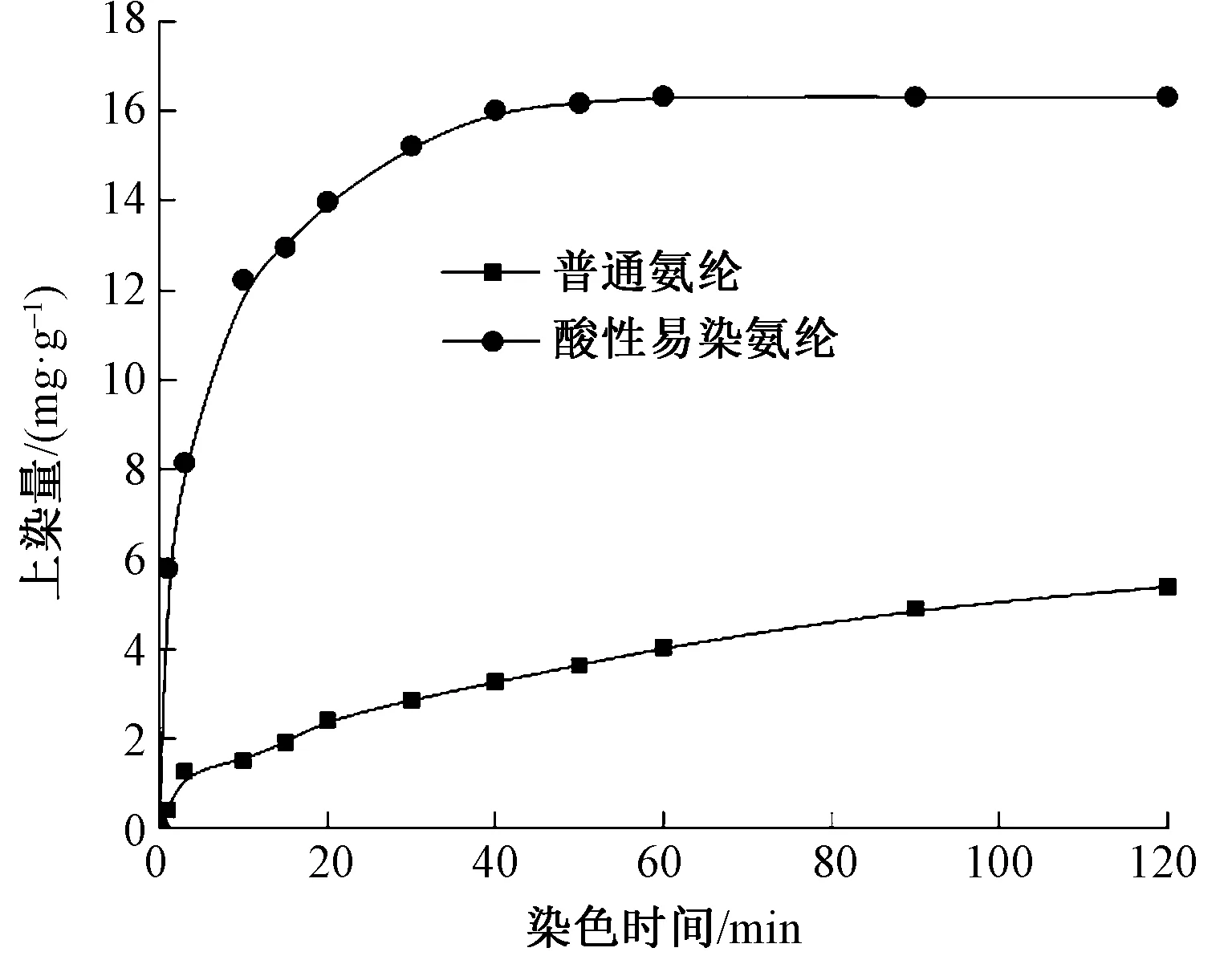
圖1 酸性染料易染氨綸和普通氨綸的上染速率對比Fig.1 Dyeing rate comparison of dyeable spandex fiber and common spandex fiber
2.1.2 pH值效應
由于酸性染料易染氨綸是通過分子鏈段中的氨基質子化實現易染,因此,染液pH值是影響染色性能的一個重要因素。圖2示出酸性橙Ⅱ在溫度為70 ℃、pH值分別為3、5和7條件下對酸性染料易染氨綸的染色速率曲線。可知,pH值越低,越有利于酸性染料易染氨綸上染。這主要是因為在低pH值條件下酸性染料易染氨綸更易發生質子化,能夠產生足夠多的正電荷,有利于酸性橙Ⅱ陰離子對氨綸快速上染且上染量高;但隨著pH值增加至中性,酸性染料易染氨綸的質子化程度越來越低,產生的正電荷越來越少甚至消失,因此,逐漸喪失了對酸性橙II陰離子的靜電吸附作用,初始上染速率和上染量均顯著降低。
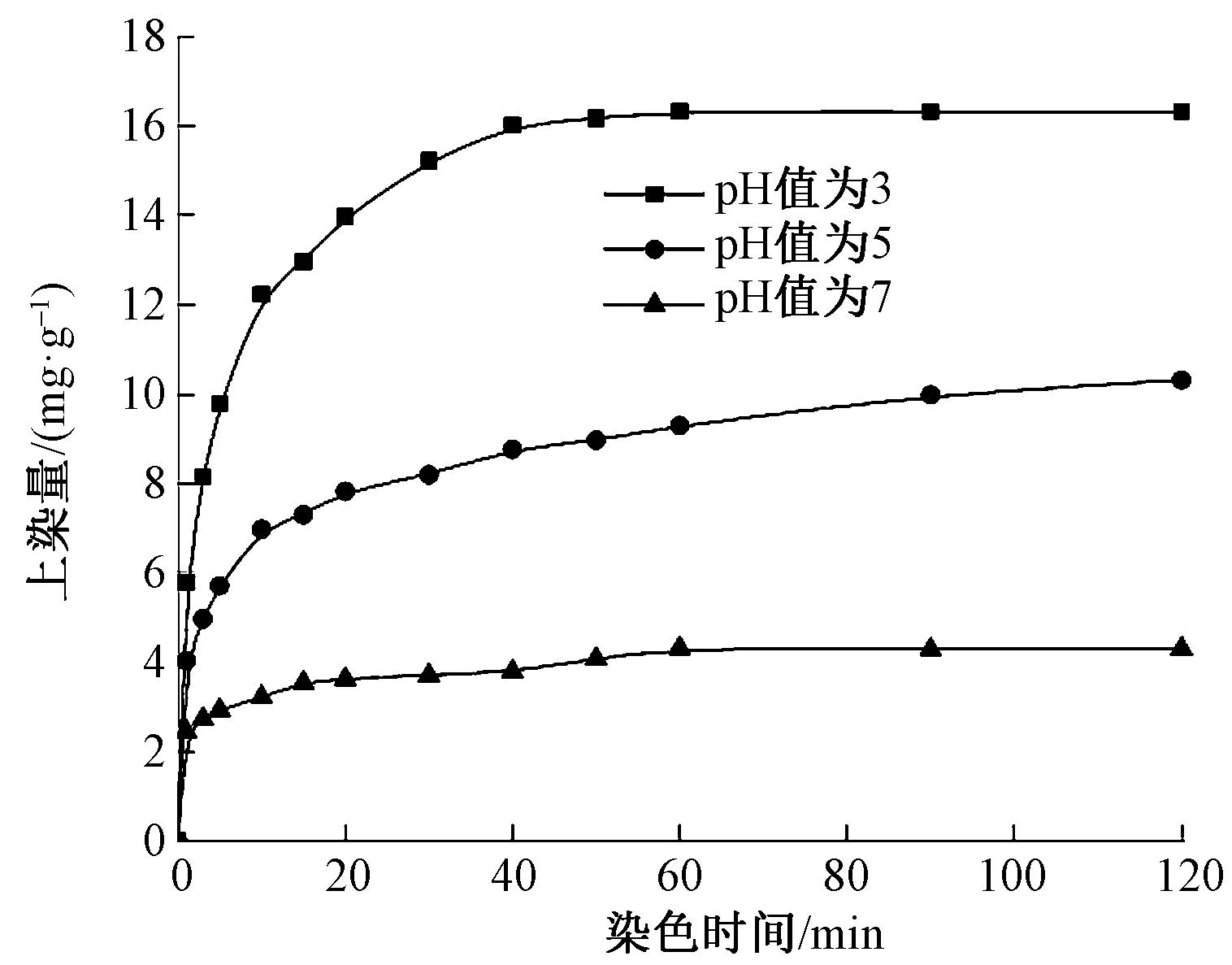
圖2 pH值對酸性染料易染氨綸染色速率的影響Fig.2 Effect of pH value on dyeing rate of dyeable spandex fiber with acid dye
2.1.3 溫度效應
圖3示出酸性橙II在pH值為3、溫度分別為50和70 ℃條件下對酸性染料易染氨綸的染色速率曲線。
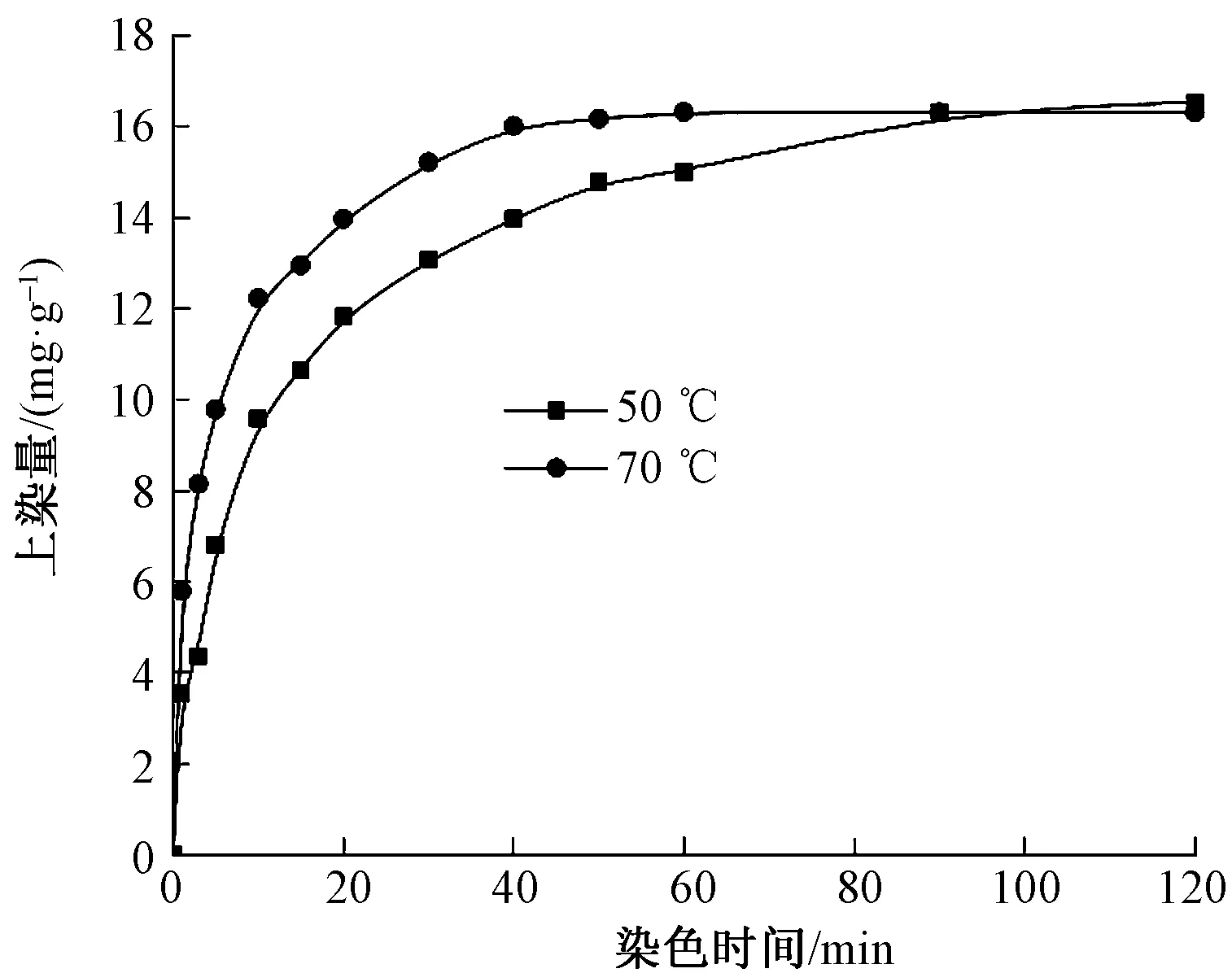
圖3 溫度對酸性染料易染氨綸染色速率的影響Fig.3 Effect of temperature on dyeing rate of dyeable spandex fiber with acid dye
由圖3可知:酸性橙II在50 ℃時對酸性染料易染氨綸上染較慢,即使延長染色時間至120 min,仍未達到染色平衡;當升高溫度至70 ℃時,酸性橙Ⅱ對酸性染料易染氨綸初始上染速率有了明顯提高,繼續染色60 min即可達到染色平衡,因此,適當提高染色溫度可將酸性染料易染氨綸的染色時間縮短至60 min以內。
2.2 染色動力學模型擬合
為準確描述酸性染料易染氨綸的染色動力學,將酸性橙II對酸性染料易染氨綸的上染速率曲線分別與準一級動力學模型(式(2))和準二級動力學模型(式(3))進行擬合。
ln(Ce-Ct)=lnCe-k1t
(2)
(3)
式中:k1為準一級動力學速率常數,g/min;k2為準二級動力學常數,g/(mg·min);Ce為染料在纖維上的平衡上染量,mg/g;Ct為染色時間t時染料在纖維上的上染量,mg/g。
以酸性橙II在pH值為3、溫度為70 ℃條件對酸性染料易染氨綸纖維的染色為例,將上染速率曲線分別與準一級動力學模型和準二級動力學模型進行線性擬合,所得直線如圖4所示。
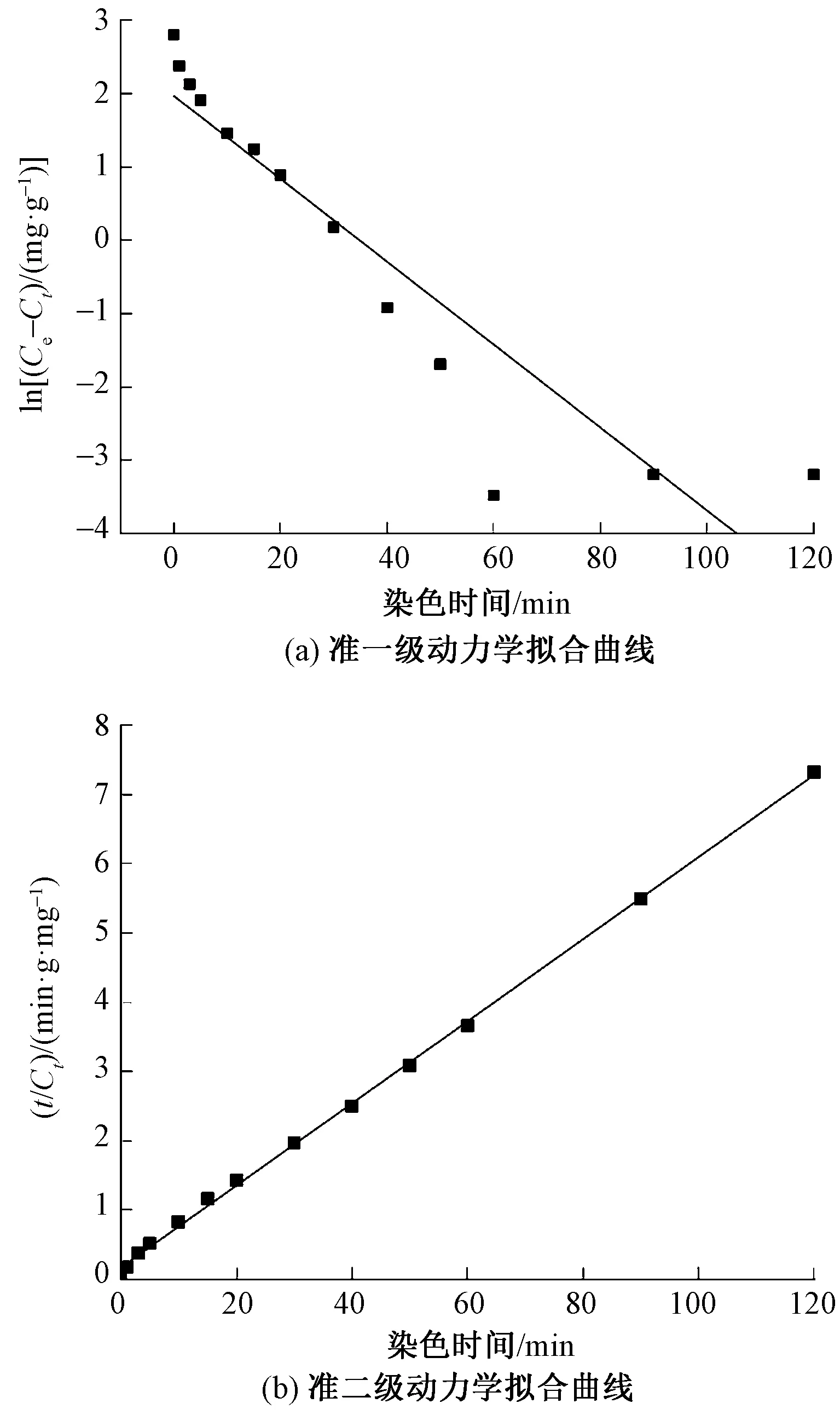
圖4 酸性橙II對酸性染料易染氨綸染色的動力學模型擬合Fig.4 Fitting of dyeing rate curve of Acid Orange Ⅱ on dyeable spandex fiber with kinetic models. (a) Pseudo-first-order model; (b) Pseudo-second-order model
酸性橙II對酸性染料易染氨綸的上染速率曲線與準一級動力學模型的擬合系數只有0.876 8,而與準二級動力學模型的擬合系數高達0.999 4,因此,采用準二級動力學模型對酸性染料易染氨綸的染色速率曲線進行擬合,動力學參數如表1所示。可知,不同pH值、溫度條件下擬合系數均高于0.99,這說明采用準二級動力學模型對酸性染料易染氨綸染色速率曲線的擬合結果是可靠的。由酸性橙II對酸性染料易染氨綸的染色符合準二級動力學模型可以確認,酸性橙II在纖維上發生了定位吸附作用,歸因于二者之間的靜電吸附作用[11]。
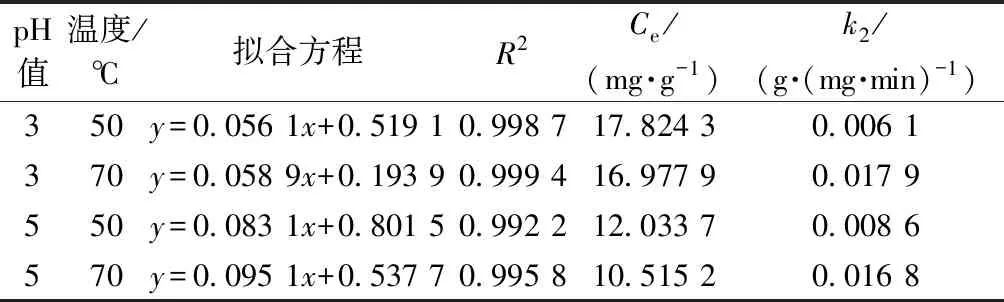
表1 酸性橙II對酸性染料易染氨綸染色的準二級動力學參數Tab. 1 Pseudo-second-order kinetic parameters of Acid Orange II on dyeable spandex fiber
由表1可知,酸性染料易染氨綸在pH值為3時的平衡吸附量明顯高于pH值為5時的平衡吸附量,而溫度對平衡吸附量的影響要小得多。這主要是因為酸性染料易染氨綸在pH值為3時的質子化程度更高,使纖維帶有更多正電荷,有利于更多染料陰離子的上染。由動力學速率常數可知,pH值對上染速率的影響不大,但升高溫度可顯著提高上染速率,這主要是因為在較高溫度下染料分子熱運動加快,使得分子的擴散和吸附加快,同時纖維膨脹,微隙增加,染料分子更易擴散進入纖維內部,從而使上染速率增加。
3 結 論
1)酸性染料易染氨綸在使用酸性橙II進行染色時,初始染色速率和上染量明顯優于普通氨綸。
2)酸性橙II在酸性染料易染氨綸上的染色動力學更符合準二級動力學模型,靜電吸附作用是驅動染色過程的主要作用力。
3)酸性橙II在酸性染料易染氨綸上的平衡上染量與染色pH值密切相關,pH值越低,平衡上染量越高。
4)酸性橙II對酸性染料易染氨綸的上染速率主要受溫度影響,溫度越高,上染越快。
FZXB

