鼻咽癌調強放射治療中自動計劃與人工計劃的劑量學差異
周露,張書旭(通信作者),彭瑩瑩,王琳婧,李慧君
廣州醫科大學附屬腫瘤醫院放療中心 (廣東廣州 510095)
放射治療是目前治療惡性腫瘤患者的重要手段之一。目前,60%~70%的腫瘤患者在病程不同時期,因不同的目的需要放射治療。現代化精準調強放射治療(intensity modulated radiation therapy,IMRT)具有副作用小、治療效果好、綜合成本低等優勢,與其他治療方式配合可以取得較好的療效。此外,放射治療存在不確定性,如不同醫師間靶區勾畫的差異性及不同機構間和機構內部放射治療計劃設計的差異性[1-2]。放射治療計劃的劑量分布取決于物理師所定義的劑量目標,為了在保證靶區劑量的前提下盡可能地減小正常組織的受照劑量,物理師需要不斷對給出的劑量目標進行調整優化,此過程需要耗費大量的人力與時間,而且很難確保達到最優方案[3]。因此,放射治療計劃優化過程的自動化,能在減少優化時間的同時提高計劃質量,降低人為因素導致的計劃質量差異。此外,還可以將自動計劃所生成的劑量分布作為手動計劃的起點,在此基礎上根據醫師的具體要求進行優化與調整[4-5]。由Pinnacle推出的自動計劃(auto planning,AP)技術的核心是治療計劃系統(treatment planning system,TPS)模仿有經驗的物理師來做計劃,生成劑量成形結構(dose shaping structure,DSS)來使得劑量成型,勾畫出冷點(cold spot,CS)和熱點(hot spot,HS)來使得劑量均勻。
世界衛生組織調查報道,全球有80%的鼻咽癌患者在中國。鼻咽癌的發病率以中國南方較高,也被稱為“廣東瘤”。目前,調強放射治療已經廣泛應用于鼻咽癌的放射治療中,該技術能夠保證給予靶區規定的照射劑量,同時最大限度降低正常組織的受照劑量。由于頭頸部解剖結構比較復雜,需要保護的正常組織也較多,因此鼻咽癌調強放射治療的人工優化過程比較費時,AP的提出可以很好地解決這個問題。本研究選取24例鼻咽癌患者,分別采用人工調強放射治療計劃和AP進行劑量學評估,探討鼻咽癌AP的可行性。現報道如下。
1 資料與方法
1.1 一般資料
選取2018年5月至2019年3月本院收治的24例病理確診為鼻咽癌,無遠處轉移的患者。其中男12例,女12例;年齡30~76歲,中位年齡46歲。患者均無放射治療禁忌證,鼻咽及上頸部均行調強放射治療照射。
1.2 體位固定及CT掃描
患者在平板床上采取仰臥位,行熱塑面罩固定,采用美國GE公司的Lightspeed 16排螺旋CT進行計算機斷層成像,層厚3 mm,層間距3 mm,矩陣512×512,掃描范圍從頭頂至鎖骨下緣下3 cm。
1.3 靶區及危及器官勾畫
由放射治療醫師根據ICRU第50、62號報告原則及RTOGO225治療規范勾畫靶區和危及器官,CTVnx為影像學及臨床檢查可見的原發腫瘤區和咽后轉移淋巴結,GTVnd為頸部轉移淋巴結,CTV1為鼻咽腫瘤極易侵犯的結構和高危淋巴引流區,CTV2為頸部預防照射區。正常組織勾畫包括腮腺、脊髓、腦干、視交叉、視神經、眼球、晶狀體、垂體、下頜骨、顳頜關節和口腔。
1.4 調強計劃設計
采用Pinnacle3 9.10計劃系統,對所有患者分別進行調強放射治療人工計劃和AP設計。調強放射治療計劃的射線能量為6 MV X線,處方劑量GTVnx為70 Gy,GTVnd為66 Gy,CTV1為60 Gy,CTV2為56 Gy。5次/周,共32次。射野角度分別為0°、40°、80°、120°、160°、200°、240°、280°、320°。人工計劃靶區和危及器官的劑量體積限值以及對應的權重根據臨床經驗設置,AP初始優化時危及器官的劑量體積限值與人工計劃相同。調強放射治療人工計劃設計:危及器官劑量限制條件為腦干≤54 Gy,脊髓≤45 Gy,50%腮腺體積劑量≤30 Gy,晶狀體≤8 Gy等。
1.5 計劃評估
(1)靶區:靶區D2為2%的靶區體積所接受的照射劑量,D98為98%的靶區體積所接受的照射劑量,D50為50%的靶區體積所接受的照射劑量,Dmean為靶區的平均受照劑量;V95%定義為靶區中劑量達到95%處方劑量的百分體積,V107%定義為靶區中劑量達到107%處方劑量的百分體積。(2)危及器官:脊髓所受的最大劑量Dmax、平均劑量Dmean以及所受劑量大于35 Gy的體積V35;腦干所受的最大劑量Dmax和平均劑量Dmean;左右晶狀體所受的最大劑量Dmax和平均劑量Dmean。
1.6 統計學處理
2 結果
2.1 靶區劑量參數
D2%(%)、D50%(%)、D98%(%)、Dmean(%)分別為D2、D50、D98、Dmean相對于處方劑量的百分比。AP和人工計劃相比,靶區的D2、D98、V107%、V95%差異均無統計學意義(P>0.05)。AP中靶區的D50、Dmean大于人工計劃,差異均有統計學意義(P<0.05)。見表1。
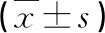
表1 24例患者的靶區劑量參數
2.2 危及器官劑量
人工計劃中脊髓的Dmax,腦干的Dmax、Dmean,以及左右晶狀體的Dmax均大于AP,差異均有統計學意義(P<0.05)。見表2。
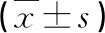
表2 24例患者的危及器官劑量參數
2.3 計劃耗時
本研究的病例中,AP平均耗時30 min;人工計劃受到靶區與危及器官位置關系以及物理師經驗等因素的影響,最短耗時約60 min,最長耗時130 min左右,平均耗時100 min。
3 討論
AP和人工計劃均可以滿足臨床對于靶區劑量的要求,此外,AP在危及器官保護方面的優勢更加明顯[6-7]。利用Pinnacle的自動計劃模塊可以得到高質量的鼻咽癌調強放射治療計劃。在人工設計調強放射治療計劃時,如果只對靶區和危及器官進行劑量限制,而對其他沒有關注的正常組織區域不設定劑量要求,所得到的治療計劃很可能出現靶區外劑量熱點,劑量分布適合度不好,脊髓或腦干等危及器官有劑量“套圈”的現象。而AP采用DSS,在最優化問題中給定相應的劑量要求。例如,將靶區外擴一定距離(1~3 mm),給定外擴區域的最大劑量為靶區的處方劑量或最低劑量來提高靶區劑量的適形度。對于凹形靶區的凹陷區,給定凹陷區的最大劑量容許值為靶區的處方劑量或最低劑量,同時根據凹陷區內危及器官的臨床劑量處方要求給定一個劑量體積約束條件來消除劑量“套圈”現象。當腫瘤亞臨床CTV外擴PTV侵犯到重要器官時,可將PTV侵犯到重要器官部分及PTV外的該重要器官部分分別設定最大劑量或最低劑量,可以使正常組織的高劑量區減小,從而滿足醫師臨床要求。
鼻咽部解剖結構復雜,存在骨骼、軟組織、氣腔等,組織密度差異大,而且靶區周圍的危及器官比較多,造成調強放射治療計劃的設計存在一定的難度,而且比較耗時。此外,由于治療過程中腫瘤退縮、患者體重減輕、照射范圍形態變化等因素會導致靶區和危及器官的體積和位置發生明顯的變化,若繼續采用初始放射治療計劃,可能導致靶區漏照或使危及器官卷入射野內,加重放射治療副反應[8]。臨床上我們采用自適應放射治療(adaptive radiotherapy,ART)技術來解決上述問題,這就需要快速、多次地設計和修改放射治療計劃,AP計劃可以很好地滿足ART技術的要求。此外,在人工調強放射治療計劃中,需要物理師手動設置靶區以及危及器官的劑量限值,物理師的經驗直接影響了計劃的質量,因此,采用鼻咽癌AP計劃能夠減少計劃設計中人為因素的影響,更加科學、合理地設置目標參數。

