玉米醇溶蛋白菊粉糖基化改性成膜工藝及其性能研究
陳又銘 張慧君,2 郭 浩 沙迪昕 王一正
(1.齊齊哈爾大學食品與生物工程學院,黑龍江 齊齊哈爾 161006;2.黑龍江省果蔬雜糧飲品工程技術研究中心,黑龍江 齊齊哈爾 161006)
隨著現代科技的飛速發展,由于塑料制品的不可降解性導致的環境污染,已直接威脅到人們的健康及生活。
近年來,美國、歐盟、日本等發達國家十分重視可降解材料產業,特別是原料來自可再生資源或產業廢棄的可降解材料的發展[1]。作為一種生物可降解材料,玉米醇溶蛋白(zein)膜憑借良好的成膜性逐漸凸顯出來,玉米醇溶蛋白是玉米深加工的一種副產物,不需加入任何添加劑即可制成薄膜,該膜防潮、隔氧、抗紫外線、保香、不透油、防靜電等特性較好,在食品、醫藥、包裝等行業具有廣闊的應用前景[2]。
玉米醇溶蛋白膜的膜質較脆,機械性能較差。蛋白質改性是提高膜機械性能的一種常見方法,改性方法有物理改性、化學改性、酶法改性和基因工程改性。傳統方法通常選擇加入增塑劑的酰化改性,如張雪娜等[3]在玉米醇溶蛋白中添加增塑劑后制成薄膜,考察了其對荷蘭瓜的保鮮效果,結果表明玉米醇溶蛋白膜可有效減少果蔬的水分散失。崔和平等[4]研究了不同甘油含量對玉米醇溶蛋白膜儲藏穩定性的影響,結果表明甘油含量為0.3 g/g的蛋白膜機械性能的穩定性較好。但此種改性方法通常會有化學試劑殘留,同時酰化改性改變了蛋白質的結構,有研究[5]表明此種改變會使蛋白質的生物效價降低。而糖基化改性僅通過加熱使糖與蛋白質發生反應,改性產物的性能較好,并且具有一定的安全性。糖基化改性又分為干熱法和濕熱法,干熱法是蛋白質與多糖基于固相體系發生的反應,反應時間長,但操作簡單;而濕熱法雖具有反應時間短、速度快等優點,但機械性能遠低于干熱法[6]。
菊粉(inulin)是由果糖分子通過β(2-1)鍵連接,末端含有一個葡萄糖分子的高分子碳水化合物,平均分子量5 500 Da[7],是一種多聚果糖。菊粉作為天然功能性食品的配料,具有膳食纖維和益生元雙重功效,促進礦物質吸收、維生素合成和預防癌癥等作用[8]。目前,采用糖基化改性玉米醇溶蛋白,制備成膜的研究較少,本研究擬采用菊粉對玉米醇溶蛋白進行干法糖基化改性,并將改性產物制成薄膜,通過對水蒸氣透過率、透光率、阻油性、阻氧性等性能的測定,為干法改性的玉米醇溶蛋白膜的后期應用提供理論依據。
1 材料與方法
1.1 材料與儀器
1.1.1 材料與試劑
玉米醇溶蛋白:蛋白含量90%,自制;
菊粉:聚合度(DP)>10,純度>95%,佐源生物工程科技有限公司;
α-淀粉酶:7×104U/mL,寧夏夏盛實業集團有限公司;
鄰苯二甲醛:化學純,天津市光復精細化工研究所;
十二烷基硫酸鈉:電泳級,天津市耀華化學試劑公司;
β-巰基乙醇:分析純,天津市北聯精細化學品開發公司;
硼砂:分析純,天津市東麗區天大化學試劑廠;
硫代硫酸鈉:分析純,天津市博迪化工有限公司;
三氯甲烷:分析純,天津市富宇精細化工有限公司。
1.1.2 儀器與設備
質構儀:QTS-25型,美國博樂飛公司;
紫外可見分光光度計:L5型,上海儀電分析儀器有限公司;
超聲波信號發生器:WSL-1000D型,南京順流儀器有限公司;
真空冷凍干燥機:LYOQUEST-85型,西班牙泰士達公司;
超低溫冰箱:Thermo702型,賽默飛世爾科技有限公司;
數顯膜測厚儀:GBCY01型,浙江盛泰芯電子科技有限公司;
隔水式恒溫培養箱:PXY-DHS-5008S型,北京市光明醫療器械廠。
1.2 方法
1.2.1 原料預處理 取適量玉米黃粉(CGM),經酶法除淀粉、丙酮脫色后,用70%乙醇溶液浸提后得到上清液,用冰水浸提,冷凍干燥后得玉米醇溶蛋白樣品。
1.2.2 糖基化改性 稱取玉米醇溶蛋白,用70%乙醇溶液溶解,配制成一定濃度的玉米醇溶蛋白乙醇溶液,按比例加入一定質量菊粉,混勻,調節體系pH,超聲,凍干,打磨成粉,置于60 ℃、相對濕度為79%的干燥器內反應一定時間,得玉米醇溶蛋白—菊粉糖基化改性產物。
1.2.3 改性成膜工藝優化
(1)物料比(蛋白/糖):在反應溶液pH 6、反應時間36 h條件下,考察物料比[5∶1,7.5∶1,10∶1,12.5∶1,15∶1 (g/g)]對玉米醇溶蛋白改性成膜的影響。
(2)pH:在物料比(蛋白/糖)10∶1 (g/g)、反應時間36 h條件下,考察反應溶液pH值(pH 4,6,8,10)對玉米醇溶蛋白改性成膜的影響。
(3)反應時間:在物料比(蛋白/糖)10∶1 (g/g)、pH 6的條件下,考察糖基化反應時間(24,36,48,60,72 h)對玉米醇溶蛋白改性成膜的影響。
(4)正交試驗優化設計:在單因素基礎上以物料比(蛋白/糖)、pH、反應時間為試驗因素,以膜的抗拉強度為指標,探索最佳工藝條件。
1.2.4 膜的制備 稱取糖基化改性產物,用70%乙醇溶解配成8%樣品溶液,溶膠后倒入模具于70 ℃烘干成膜。將膜置于30 ℃、相對濕度43%的干燥器內平衡48 h,進行測定。
1.2.5 接枝度的測定 采用鄰苯二甲醛OPA法[9]。
(1)試劑①:0.080 0 g OPA,2 mL甲醇,6 mL水混合均勻。
(2)試劑②:10 mL SDS,0.1 mol/L硼砂100 mL,0.4 mLβ-巰基乙醇,加少量蒸餾水混合后,定容至200 mL。
(3)測定時,量取0.3 mL試劑①,3.7 mL試劑②和200 μL 樣品,35 ℃水浴下反應2 min,以200 μL乙醇為空白對照,在340 nm波長處測其吸光值。采取同樣的方法,用賴氨酸代替樣品作標準曲線,依據賴氨酸的曲線圖計算得出樣品中游離氨基的含量C。按式(1)計算接枝度。
(1)
式中:
DG——接枝度,%;
C0——未改性前溶液中游離氨基含量,mol/L;
C1——改性后溶液中游離氨基含量,mol/L。
1.2.6 膜機械性能抗拉強度和斷裂伸長率的測定 將玉米醇溶蛋白膜及改性膜裁成矩形條狀(40 mm×10 mm),隨機取10個點用數顯測厚儀準確測量其膜厚度,取平均值。質構儀夾距20 mm,拉伸速度5.0 mm/s,每種膜測3次取平均值,按式(2)計算抗拉強度。
(2)
式中:
TS——抗拉強度,MPa;
F——最大拉力,N;
L——膜樣品厚度,mm;
W——膜樣品寬度,mm。
1.2.7 水蒸氣透過系數的測定 采用杯式法測定膜的水蒸氣透過系數,根據GB 1037—1988,并略作修改:將無水氯化鈣(CaCl2)粉碎為粒度2 mm粉末,于200 ℃干燥箱中干燥 2 h,待冷卻后加入到試管中,使加入的CaCl2量至試管口5 mm 處為止。選擇均勻、無孔洞、無皺褶的膜將裝有CaCl2的試管封口再用石蠟將其密封,并將試管稱重。將稱重后的試管放入底部為去離子水的干燥器中(保持相對濕度 100%),將干燥器放入25 ℃隔水式恒溫培養箱(純水在25 ℃時飽和水蒸氣壓為3.167 1 kPa),使膜內外兩側保持一定的蒸氣壓差。每隔24 h取出試管,將其稱重,按式(3)計算水蒸氣透過系數。
(3)
式中:
WVP——水蒸氣透過系數,g·mm/(m2·d·kPa);
ΔP——水蒸氣壓差,kPa;
T——膜厚,mm;
ΔW——水增加量,g;
t——時間,h;
S——膜的面積,m2。
1.2.8 透明度的測定 根據文獻[10],修改如下:將平衡后的膜裁剪成條狀(12 mm×40 mm),將裁剪好的薄膜緊貼于比色皿(玻璃)外側,以空比色皿(玻璃)作對照,在460 nm波長下測定其透光率,以透光率的大小間接表示透明度。
1.2.9 阻氧性的測定 根據油脂過氧化值的大小,來評價膜的阻氧性。在250 mL容器中加入20.0 g新鮮花生油,用平衡后的膜覆蓋瓶口并用石蠟密封,將碘量瓶存放在60 ℃培養箱中陳化12 d,根據GB 5009.227—2016方法,測定花生油的過氧化值。過氧化值按式(4)計算。
(4)
式中:
POV——樣品中過氧化值,g/100 g;
V1——樣品消耗硫代硫酸鈉標準溶液的體積,mL;
V2——空白試劑消耗硫酸鈉標準溶液的體積,mL;
C——硫代硫酸鈉標準溶液的濃度,mol/L;
m——待滴定樣品的量,g。
1.2.10 阻油性的測定 根據透油系數的大小,來評價膜的阻油性。取一只潔凈干燥的試管,加入1.00 mL 新鮮花生油,挑選完整均勻的膜將試管口封住并用高熔點石蠟密封,將試管倒置于已稱重的濾紙上。將試管連同倒置試管的濾紙放置在相對濕度為50%的恒濕箱中,每隔3 d稱重1次,稱量得出濾紙質量的變化,稱量至濾紙質量不變為止。按式(5)計算透油系數。
(5)
式中:
P0——透油系數,g·mm/(cm2·d);
ΔW——濾紙質量前后變化,g;
FT——膜厚度,mm;
S——膜面積,m2;
T——放置時間,d。
1.3 數據處理
試驗均平行3次,圖像處理采用Excel軟件,數據統計分析采用SPSS 19.0 軟件,并進行Duncan多重比較。
2 結果與分析
2.1 改性成膜工藝優化
2.1.1 物料比(蛋白/糖)對玉米醇溶蛋白改性成膜的影響 由圖1可知,隨著物料比的增加,玉米醇溶蛋白—菊粉產物的接枝度增大,抗拉強度也逐漸增強。當物料比為10∶1 (g/g)時,接枝度和抗拉強度均達到最高。說明玉米醇溶蛋白和菊粉分子接觸碰撞幾率逐漸增加,反應機會增多,接枝度增加,使得改性后的分子結構發生改變[11],增加其抗拉強度。繼續增加物料比,接枝度和抗拉強度都下降,可能是接枝部位的作用點被多余的物料包埋,無法進行有效的糖基化反應[12]。綜合考慮選取最合適的物料比為10∶1 (g/g)。
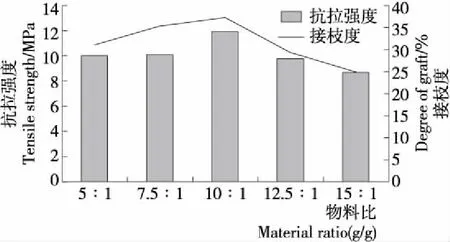
圖1 物料比對膜抗拉強度和接枝度的影響Figure 1 Effect of different material ratio on tensile strength of film and degree of graft
2.1.2 pH對玉米醇溶蛋白改性成膜的影響 由圖2可知,干法糖基化反應的最適pH值環境處于弱酸環境。當pH由5提高到6時,其接枝度達到最高,此時,糖基化反應迅速,糖與蛋白的接枝反應程度大大增加。隨著pH值的繼續增加,玉米醇溶蛋白—菊粉產物的接枝度開始下降,接枝反應達到平衡狀態,說明改性產物在堿性條件下,會使蛋白質發生水解,結構發生改變,不利于糖基化反應的進行[13]。而抗拉強度呈先升高后降低的趨勢,當體系處于pH 6~7時,其抗拉強度達到最大值,此時膜的韌性最佳,繼續增加體系的pH值,會對糖基化反應不利,使膜的抗拉強度下降50%左右。因此選擇pH 6的反應溶液作為改性體系。
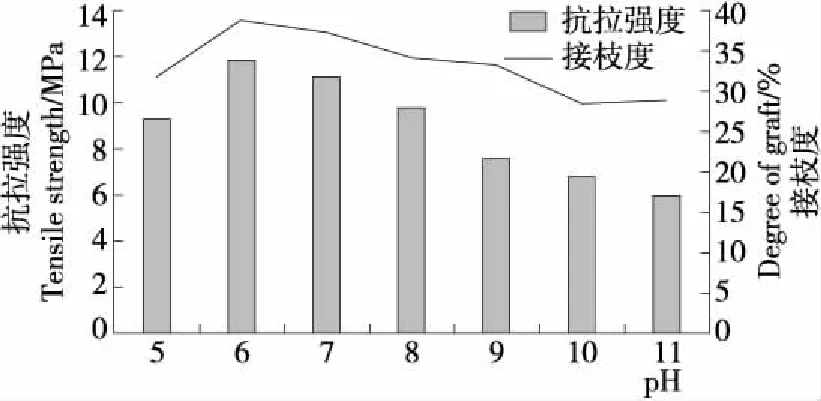
圖2 糖基化反應溶液pH對膜抗拉強度和接枝度的影響Figure 2 Effect of different pH on tensile strength of film and degree of graft
2.1.3 反應時間對玉米醇溶蛋白改性成膜的影響 由圖3 可知,隨著糖基化反應時間的增加,改性產物的抗拉強度和接枝度均呈先增后減的趨勢,反應開始后,不斷加熱使蛋白質結構部分展開,多糖與蛋白質受熱逐步接合,接枝度逐漸提高。當糖基化反應時間達到36 h時,接枝度達到最大值,膜的抗拉強度效果較好,如果再繼續延長反應時間,會破壞蛋白質分子的一些賴氨酸,還會造成蛋白質分子伸展,使分子間的相互作用力增強,造成蛋白質凝聚和沉淀,而不利于接枝反應[14]。綜合考慮,選擇糖基化反應時間為36 h,此時的成膜效果和接枝度都相對較高。
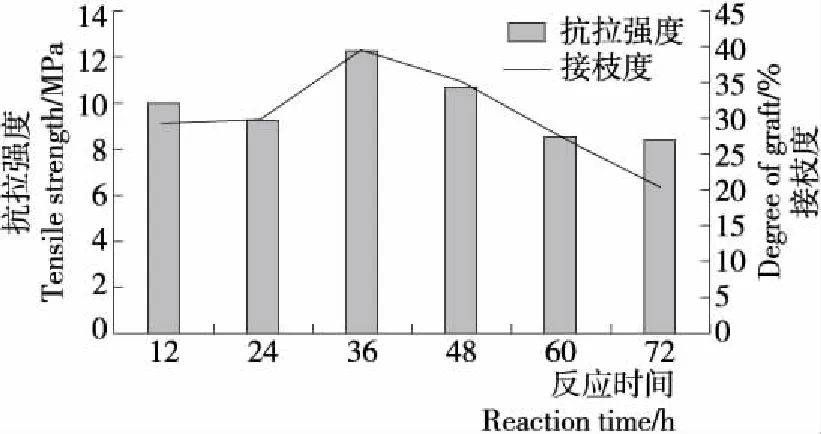
圖3 糖基化反應時間對膜抗拉強度和接枝度的影響Figure 3 Effect of different reaction time on tensile strength of film and degree of graft
2.1.4 正交試驗設計 在單因素試驗基礎上,以物料比、pH、反應時間3個因素,采用正交試驗進一步優化糖基化改性玉米醇溶蛋白成膜的工藝條件。正交試驗因素水平表和結果分析如表1、2所示。
由表2可知,各因素對菊粉改性玉米醇溶蛋白的影響程度依次是pH>物料比>加熱時間,最佳成膜條件為物料比10∶1 (g/g),反應溶液pH 6,反應時間48 h,在此條件下制得玉米醇溶蛋白—菊粉共價交聯膜的抗拉強度為10.12 MPa,接枝率為37.5%。

表1 正交試驗因素水平表Table 1 Hactor levels table of orthogonal ezperiment
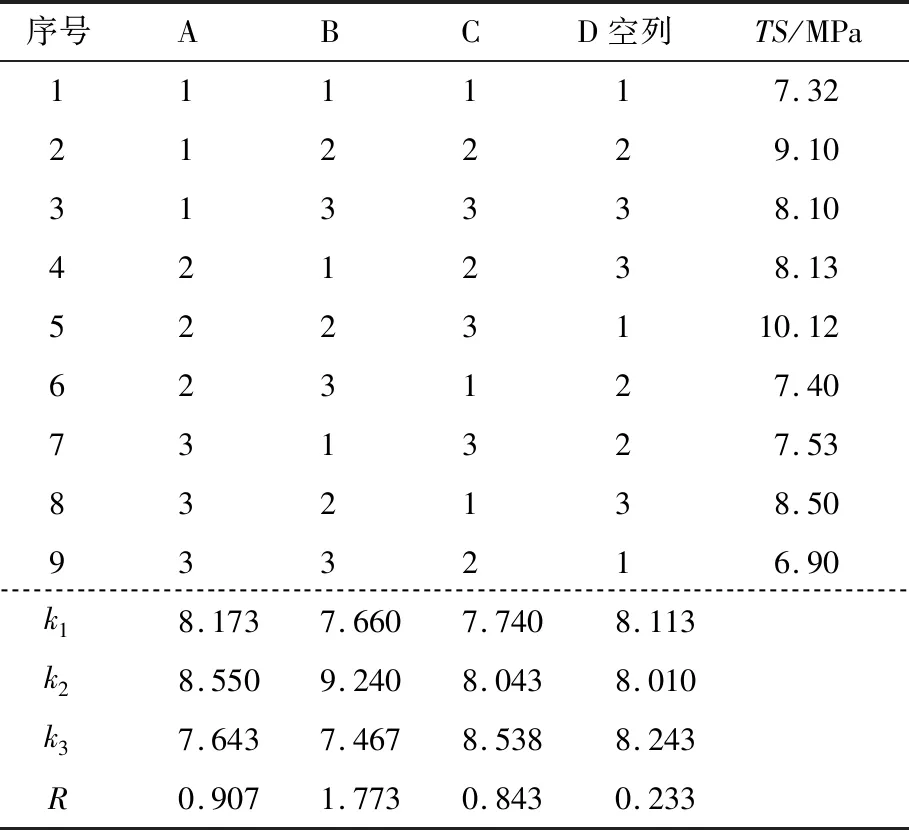
表2 正交試驗設計結果分析Table 2 The result analysis of orthogonal experiment
2.2 膜性能分析
水蒸氣透過率是考察膜的透氣性與膜擴散性的一個重要指標[15]。由表3可知,純玉米醇溶蛋白膜的水蒸氣透過率優于改性后的膜,表明經菊粉糖基化改性能夠有效改善原玉米醇溶蛋白膜的阻水性。可能是在糖基化反應的過程中形成的接枝產物中引入了一定量的多聚果糖,將玉米醇溶蛋白中所含的親水氨基酸包裹,使膜的結構更加密實,有效地阻止其與水蒸汽接觸[16],該結果與孫琳琳等[17]對脫脂豆粕膜水蒸氣透過系數的測定數值相比有顯著提高。另一方面,由于親水性的糖分子會吸引水分子從而產生具有黏性且不會脫落的復合物,進一步阻隔水蒸氣的進入,使水蒸氣覆蓋在膜的表面,降低了水蒸氣透過率。
膜的透明度與原料自身顏色、膜液濃度和添加助劑的種類及含量有關[18]。本研究結果表明,經菊粉改性后制備的膜較純玉米醇溶蛋白膜透明度提高了2倍多,與文獻[19]結果一致,但透明度相對較低。另本研究后期主要應用于制備膠囊殼方面,膠囊在使用過程中為了防止內容物活性的降低,通常會添加遮光劑等,雖透光率較明膠膠囊略低,但仍符合使用規范。根據表3可以看出,改性后的玉米醇溶蛋白—菊粉膜的過氧化值與透油系數較改性前均有提高,說明糖基化改性可有效改善蛋白膜的分子結構,使其內部結構更加緊密,阻礙氧分子或油脂分子的擴散,從而提高玉米醇溶蛋白膜的阻油性與阻氧性。
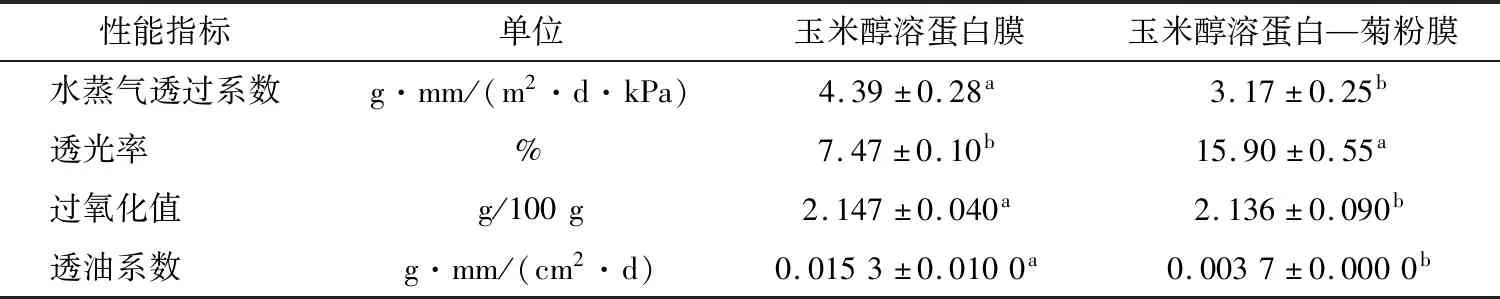
表3 膜性能檢測結果?Table 3 The testing result of film performance
? 同行字母不同表示差異顯著(P<0.05)。
3 結論
本研究以玉米濕法生產淀粉的副產物——玉米醇溶蛋白為原料,探討菊粉糖基化改性的成膜工藝,并在最優條件下對膜的基本性質進行測定。結果表明,改性蛋白膜的各項性能均優于純玉米醇溶蛋白膜,尤其是解決了玉米醇溶蛋白膜質較脆的弊端,這一優良的性能可使其替代明膠制備的膠囊殼。
本研究采用的還原糖——菊粉,相比其他多糖雖功能性優異,但價格較高,后期研究中會篩選一些成本更低的多糖作為糖基化改性的羰基供體;此外,由于玉米醇溶蛋白膜在酸性條件下不溶,而溶于弱堿性或中性的溶液中,適宜制備腸溶膠囊殼,故后續將研究腸溶膠囊殼的制備及腸溶性的考察。

