膽囊膽固醇結石發生機制的研究進展
劉 超,薛東波
(哈爾濱醫科大學附屬第一醫院微創膽道外科,哈爾濱 150001)
膽石癥為臨床常見疾病,包括膽囊結石、膽總管結石、肝內膽管結石[1]。據統計,目前在全球大約有10%的成年人患有膽石癥,中年婦女的發病率甚至高達15%[2]。隨著經濟的發展及膳食結構的改變,中國人脂肪的攝入量大量增加,中國也成為膽石癥大國。在西方國家及我國沿海城市,因膽石癥手術的患者已超過闌尾炎,成為普外科第一急癥。
膽囊結石按所含成分可分為膽固醇結石和膽色素結石。隨著蛋白、脂肪的攝入增加,膽囊膽固醇結石患者占比逐年上升[3],目前超過80%的膽石癥患者為膽囊膽固醇結石。膽囊膽固醇結石雖屬良性疾病,但在治療方面仍存在很多問題,如藥物溶石、體外超聲波碎石耗時費力,停止治療后易復發;保膽取石術同樣存在復發問題,手術切除膽囊也不能解決肝內外膽管結石再生的問題[4]。目前膽固醇結石的病因及發病機制尚不明確,有必要對膽囊結石的成因進行深入研究。膽固醇結石的形成是一個極其復雜的過程,其形成機制大體包括膽汁中膽固醇超飽和(熱力學失衡)、成核因子致微泡穩態失衡(動力學失衡)和膽汁纖溶系統紊亂3方面因素[5]。現就膽囊膽固醇結石發生機制的研究進展進行綜述。
1 膽固醇超飽和與熱力學失衡
膽汁是一種含類脂的水溶液,類脂成分主要包括膽固醇、膽汁酸鹽及磷脂3種[6]。正常膽囊膽汁含有大約67%的膽汁酸鹽、22%的磷脂及4%的膽固醇。脂溶性的膽固醇在膽汁中通過膽汁酸和磷脂,以微膠粒和微泡形式保持溶解狀態[7]。微膠粒直徑為5~6 μm,微泡直徑為50~100 μm。膽固醇-磷脂-膽鹽聚合的微膠粒與膽固醇-磷脂的復合微泡存在動態平衡關系,可以互相轉換。膽固醇、膽汁酸鹽及磷脂三者比例失衡是導致結石形成的主要因素之一。膽汁酸鹽和磷脂溶解膽固醇的能力是有一定限度的,成石性膽汁包括膽固醇飽和(或)過飽和膽汁,其形成原因為肝臟分泌的膽固醇過多或產生的膽汁酸和磷脂過少。在成石性膽汁中,膽固醇含量可高達8%~10%[7]。
1.1 膽囊運動障礙 正常膽囊的收縮運動可以促進膽囊膽汁排放,任何原因引起的膽囊運動功能障礙都會導致膽囊內的膽汁過度濃縮,從而導致膽囊結石。研究發現胃切除術是胃癌以及胃十二指腸潰瘍的主要治療手段,胃切除術后除常見的術后并發癥外,術后發生膽囊結石也是并發癥之一,影響患者的生活質量甚至需要二次手術治療[8]。解剖生理學證實迷走神經肝膽支能夠促進膽囊運動與收縮,同時降低Oddi括約肌張力,促進膽汁排放[9]。研究發現在胃切除術中損傷迷走神經的分支肝膽支后,術后發生膽囊結石的概率增加[10]。Yi等[11]在動物實驗研究中發現,保留支配膽囊的迷走神經動物較沒有保留該神經的動物能更有效預防胃切除術后膽囊結石的形成。因此,保留迷走神經肝膽支對促進膽囊收縮、減輕膽汁淤積與膽固醇濃縮起重要作用。
1.2 膽固醇代謝紊亂 肝臟功能代謝紊亂在膽囊結石形成的過程中起重要作用。在機體內對膽固醇的合成、分解、吸收轉運進行有效調控可以使體內膽固醇達到平衡。大致調節過程如下:①人體內的膽固醇絕大部分是通過自身合成的,其合成的主要場所是肝臟。該途徑的具體步驟:首先乙酰輔酶A在乙酰硫解酶和3-羥基-3-甲基戊二酰輔酶A合成酶的催化下生成3-羥基-3-甲基戊二酰輔酶A,然后在酶的作用下還原成甲羥戊酸。該酶是3-羥基-3-甲基戊二酸單酰輔酶A還原酶,是一種重要的限速酶。甲羥戊酸經過一系列復雜的反應合成鯊烯,鯊烯催化成羊毛甾醇,最后轉化成膽固醇。他汀類藥物降低血中膽固醇是通過降低膽固醇合成的限速酶活性實現的[12]。②提高肝臟膽固醇分解代謝的限速酶膽固醇7α-羥化酶(cholesterol 7α-hydroxylase,CYP7A1)活性可降低體內膽固醇濃度。膽酸是膽固醇的分解產物,體內主要以牛磺膽酸鹽和甘氨膽酸鹽的形式存在,并參與肝腸循環[13]。③抑制小腸膽固醇吸收、促進膽固醇外排可降低膽固醇。小腸對膽固醇吸收轉運主要由核受體肝臟X受體調控,激活的肝臟X受體能夠促進膽固醇吸收、流出、轉運和分泌相關基因的表達。目前,降低膽固醇的治療靶點[14]及作用機制是通過降低3-羥基-3-甲基戊二酸單酰輔酶A還原酶的活性來減少膽固醇的合成,抑制尼曼-匹克C1型類似蛋白1的轉運功能來減少膽固醇的吸收,提高CYP7A1的活性使膽固醇快速向膽汁酸轉化[12]。
1.3 膽固醇反向轉運 膽固醇反向轉運是體內清除膽固醇的唯一機制,對維持體內膽固醇穩態具有積極意義[15]。膽固醇反向轉運的過程是一個極其復雜的過程,大體機制是先形成高密度脂蛋白顆粒,再由ATP結合盒轉運體G1將膽固醇轉運至高密度脂蛋白顆粒,從而清除體內的膽固醇。高密度脂蛋白顆粒是由兩種物質在細胞外結合形成的,這兩種物質是載脂蛋白A1和ATP結合盒轉運體A1[16]。目前研究已經證實miR-33可以通過調節ATP結合盒轉運體A1達到清除膽固醇的目的,miR-33同時能夠抑制CYP7A1、ATP結合盒亞家族B成員11(ATP binding cassette subfamily B member 11,ABCB11)、腺苷三磷酸酶磷脂運輸8 b1基因調控膽固醇反向轉運過程影響膽酸的合成[17]。ATP結合盒轉運體位于毛細膽管膜區域。ABCB11轉運體、ABCB4轉運體和ATP結合盒亞家族G成員(ATP binding cassette subfamily G member,ABCG)5/8異二聚體轉運體分別負責膽鹽、磷脂和膽固醇的分泌。研究發現膽固醇結石患者的ABCG5/ABCG8基因表達增加[18]。在動物模型中,敲除ABCB11、ABCB4基因可影響膽汁脂質的分泌,并導致膽固醇過飽和膽汁的形成[19]。
1.4 代謝紊亂綜合征 患有代謝紊亂綜合征的患者由于對胰島素的抵抗,體內膽固醇的平衡會受到影響,一方面由于代謝的紊亂,膽固醇在體內的自身生成會相應增加,另一方面膽汁酸的生成過程受到抑制導致膽汁酸相應減少。此消彼長的情況下,溶解于膽汁中的膽固醇會極大增加[20]。膽鹽、膽固醇、磷脂等構成膽汁的主要成分失去正常的成分占比,儲存在膽囊內膽汁中的過多膽固醇會附著在膽囊黏膜表面,形成膽囊息肉和膽囊結石。脂肪肝和脂肪肝并發膽石癥患者體內瘦素水平普遍高于正常人,瘦素與胰島素的關系密切,彼此之間通過體內與其相關的雙向反饋內分泌軸相互影響使內分泌軸保持平衡,兩者任何一方或雙方在體內的含量升高或發生抵抗時,該內分泌軸就會失去現有的平衡,導致惡性循環[21]。瘦素可以改變膽汁中的成分占比[22]。腰圍增加、三酰甘油升高、高密度脂蛋白降低被證實是膽囊結石發生的危險因素[22]。
2 微泡穩態失衡與動力學失衡
在毛細膽管中,膽固醇與親水的磷脂形成穩定的單層微泡。其能穩定地承載膽固醇,另一種穩定的載體是微膠粒,微膠粒是由單層微泡結合膽汁酸生成。當膽汁中膽固醇的濃度升高超出兩者的承載能力時,單層微泡轉變成不穩定的復合微泡。復合微泡易破裂釋放出疏水的膽固醇,最終聚集形成結晶與結石。膽鹽調節單層微泡與微膠粒之間的動態平衡。微泡相的膽固醇易于結晶析出,形成膽固醇性結石,而微膠粒相的膽固醇相對較穩定,能夠大大降低膽汁的成石性,但是微膠粒溶解膽固醇的能力遠小于微泡,這就增加了膽固醇結石形成的風險。研究發現膽鹽能夠促使微泡相膽固醇向微膠粒相轉移,因此加大膽鹽濃度能夠有效降低膽固醇性結石的形成[23]。同時“微泡”也是膽固醇結晶析出及沉淀發生的場所,而微膠粒中的膽固醇并不直接聚合形成膽固醇結晶。許多過飽和膽汁樣本中不出現膽固醇結晶的原因可能是它們含有豐富的微泡。但當微泡相膽固醇過飽和(即膽固醇∶卵磷脂摩爾比>1)時,微泡極不穩定而易凝聚,利于膽固醇結晶析出。試驗發現部分正常人膽囊膽汁中的膽固醇也是過飽和的,其中未檢測出膽固醇結晶[23]。以上研究表明膽汁中的膽固醇處于飽和狀態不是形成膽固醇結石的唯一條件,必然還有其他促成核因子的參與。研究發現,膽汁中存在著促/抑成核因子動力學系統[23]。公認的促成核蛋白[24]包括刀豆凝集素A結合蛋白(磷脂酶C、免疫球蛋白、α-1酸性糖蛋白、氨肽酶N等)和非刀豆凝集素A結合蛋白(黏液性糖蛋白、某些鈣結合蛋白等);抑成核蛋白[25]則包括載脂蛋白A1和A2、磷脂酶A2、膽汁分泌性IgA、骨橋蛋白[26]等。研究發現[23],促成核蛋白和抑成核蛋白起到促/抑成核作用的機制是通過其自身的疏水性和親水性對微泡和微膠粒的穩定性形成影響,同時干擾微泡和微膠粒對膽固醇的溶解。在膽汁類脂熱力學體系失衡的基礎上,促/抑成核因子動力學失衡在膽石形成過程中發揮關鍵作用。
3 凝血纖溶功能紊亂在膽固醇結石形成中的作用
1969年,Okamo對人類膽囊中的膽汁進行研究證實了膽汁中纖溶酶激活物-膽激酶的存在[27]。近年來相繼又有學者對人類膽囊中的膽汁進行研究,證實了凝血-抗凝系統[28]和纖溶因子的存在。葉生愛等[29]在膽囊膽固醇結石中發現大量纖維蛋白骨架,所有膽固醇結晶都鑲嵌在其網眼中。唐兆賀等[30]研究發現成石膽汁中含有大量的組織因子和纖維蛋白,進一步研究發現組織因子外源凝血激活途徑的啟動者是凝血酶原的激活者,兩者共同作用導致纖維蛋白的大量生成。同時,還在上述膽汁中發現纖溶酶原激活物抑制物1和2的含量增高,其抑制了纖溶酶的激活,使纖溶活性并未相應增強,膽汁處于一種高凝、低抗凝和相對低纖溶狀態,最終導致交聯纖維蛋白的大量累積并參與膽石的形成與生長。凝血過程中,凝血因子的激活需要由活化的血小板膜提供磷脂表面。在有血小板參與的情況下凝血激活的速度比沒有血小板參與的情況下升高約2萬倍[28]。進一步研究在血小板膜表面發現了磷脂酰絲氨酸,并證實其是血小板能夠加快凝血激活速度的主因[28]。
對磷脂酰絲氨酸進行研究發現,其主要存在于細胞膜的內表面,細胞膜的外表面幾乎不存在,磷脂酰絲氨酸的本質是一種磷脂[28]。在血小板活化的過程中,磷脂酰絲氨酸翻轉血小板膜的外表面,從而為凝血因子通過負電荷附著在血小板膜的外表面提供了附著位點,活化的血小板起到了催化加速凝血激活的作用。在凝血過程的“瀑布”式激活反應鏈的啟動、維持和終止階段都需要細胞膜表面磷脂酰絲氨酸的參與,見圖1。研究發現,成石膽汁的凝血激活過程并無血小板的參與,而微泡含有大量磷脂成分,可能參與凝血通路的激活[27]。
4 磷脂微泡與凝血激活
膽固醇結晶主要在微泡中產生,微泡中膽固醇的含量較高。同時研究發現纖維蛋白原存在于微泡的“泡”相蛋白中,細胞、血小板的泡膜成分也與微泡一致,磷脂酰絲氨酸等成分都存在其中[31-32]。故推測可能是微泡提供了凝血激活過程所需的磷脂表面。葉生愛等[27]的研究也初步證實了這一猜測,他們用提取的膽汁微泡提供凝血活性表面進行活化部分凝血活酶時間檢測,結果發現無論在膽石患者組還是非膽石患者組中都能形成凝膠塊,而在無微泡的對照組中則無凝血發生。凝血激活過程在膽石形成過程中發揮多大作用以及微泡在膽石形成過程中發揮哪些作用還有待深入研究。
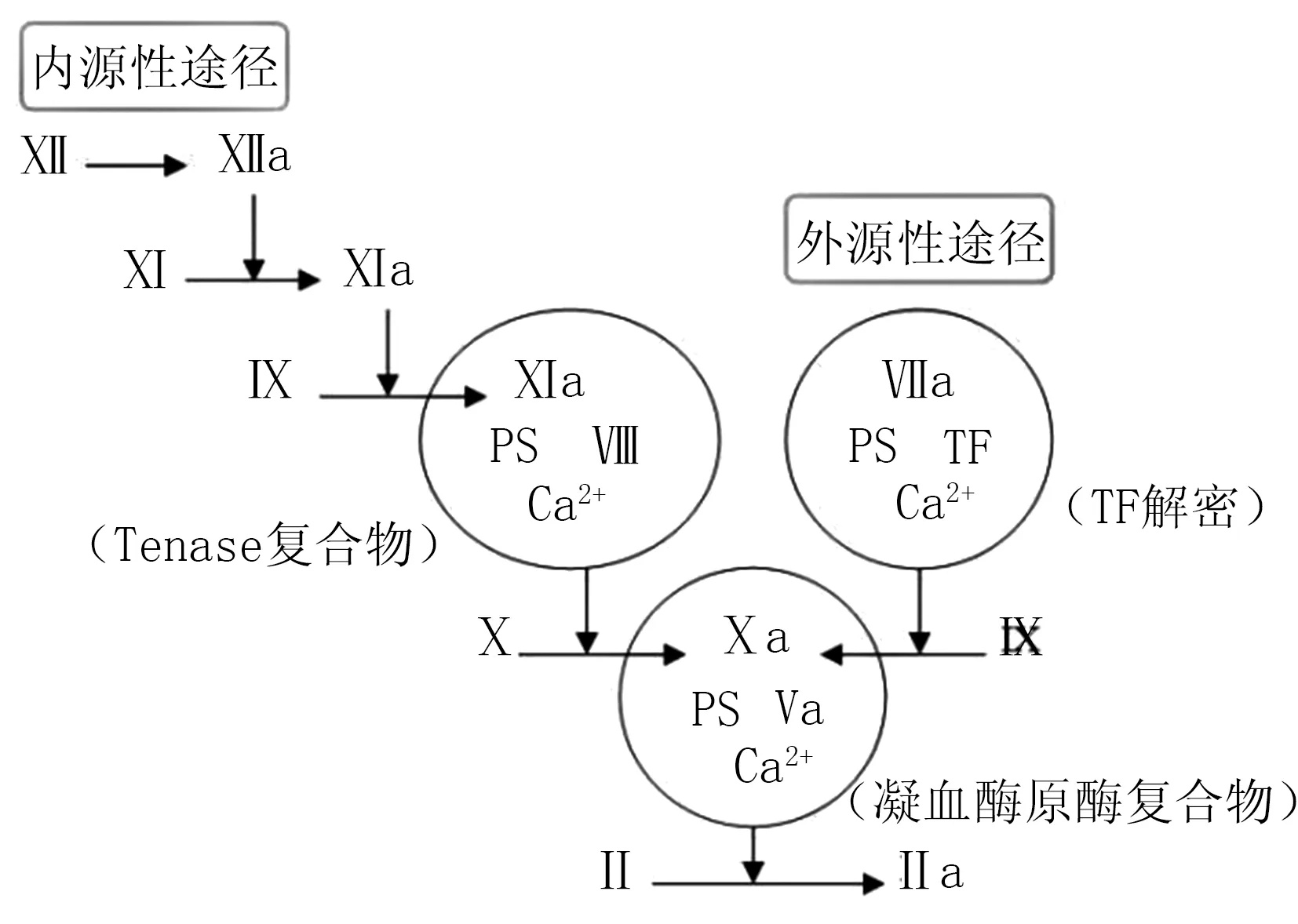
PS:磷脂酰絲氨酸;TF:組織因子;Tenase complex:內源性途徑因子X酶復合物
圖1 PS在凝血通路中的作用示意圖
5 膽固醇結石相關蛋白
膽固醇結石的形成是一個極其復雜的過程,通過對膽固醇結石成因的研究,人們發現相關蛋白對膽固醇結石的形成起重要作用[33]。如膽甾醇酯轉運蛋白是血漿脂蛋白之間脂質交換和逆向膽固醇轉運的重要因素。通過調節膽甾醇酯轉運蛋白可以有效影響膽固醇的逆向轉運[33]。ATP結合盒轉運蛋白是表達于細胞膜和部分細胞器的一種重要的膽固醇流出調節蛋白,其主要功能是將細胞內的膽固醇轉運至細胞外與高密度脂蛋白結合,從而降低細胞內的膽固醇負荷,調節血漿脂質代謝[34]。7α-羥化酶是膽汁酸合成的限速酶,7α-羥化酶的基因多態性與血脂水平又存在一定的關聯[35]。載脂蛋白[36]是構成血漿脂蛋白的重要組分,賦予脂類以可溶的形式,并在血漿脂蛋白代謝中起重要作用:①促進脂類運輸;②調節酶活性;③引導血漿脂蛋白與細胞表面受體結合。載脂蛋白是功能上極其活躍的一組血漿蛋白質。
目前發現了許多與膽固醇結石形成相關的蛋白。但是相關研究只是注重個別蛋白對于膽固醇結石的形成有哪些影響,并未從總體上研究與膽固醇結石形成的相關蛋白,同時對于這些相關蛋白之間是否有一定的關聯性也沒有進行深入研究。為全面展示與膽固醇結石形成有關蛋白的研究進展,利用文獻挖掘技術對Pubmed文獻數據庫進行了查詢,最終得到14個與膽固醇結石發病相關的已知肝臟蛋白。進一步利用GO(Gene ontology)數據庫將具有相同GO功能注釋的蛋白通過注釋術語連接起來構建網絡(圖2),發現這些蛋白絕大多數與脂類代謝相關。
國內外運用組學技術[37]研究膽石癥成因的報道還較少見。對易患結石小鼠和不易患結石小鼠的肝組織進行比較的轉錄組學研究發現,差異表達的基因主要集中于脂類代謝、氧化應激、免疫炎癥反應、凋亡等功能通路[31,38-39]。Zhou等[41]將1例膽固醇結石患者的膽汁分別利用二維電泳技術/質譜技術、二維電泳-液相色譜-串聯質譜技術兩種蛋白組學技術進行研究分析,結果分別有48和218種蛋白質被鑒定出來。張殿彩等[41]采用二維電泳技術/質譜技術比較蛋白組學技術研究膽固醇結石患者膽囊的膽汁微泡相與微膠粒相的蛋白質表達譜的差異,結果成功鑒定出差異表達蛋白質8個,6個蛋白在微泡相中表達上調,2個下調。膽固醇結石發生機制的研究將會成為新熱點,對預防和治療發揮指導作用。
6 結 語
膽囊結石的患者日益增多,目前膽囊結石的病因及機制尚不十分清楚,闡明疾病的發生機制對預防和治療疾病意義重大。已經發現膽囊結石的形成與膽汁膽固醇超飽和、微泡穩態失衡,膽汁中凝血纖溶功能紊亂相關。通過降低膽汁中膽固醇濃度,維持促/抑成核因子的動力學穩態可以有效較少膽固醇結石的發生。目前僅闡述了凝血激活過程和微泡在膽石形成過程中起到的部分作用,深入研究兩者的作用對闡明膽石癥的病因及機制具有重要意義,同時有助于預防膽固醇結石的發生。
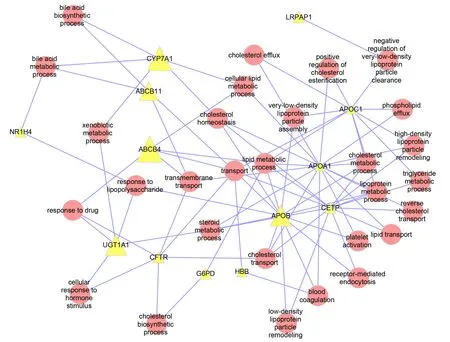
圖2 與膽囊膽固醇結石相關的蛋白及GO注釋可視化關系
ANK1:錨蛋白1;NR1H4:核受體亞科1 H組的成員4;CYP7A1:膽固醇7α-羥化酶;ABCB11:ATP結合盒亞科11 B成員;ABCB4:ATP結合盒亞科4B成員;UGT1A1:UDP葡萄糖醛酸轉移家庭成員1 A1;GFTR:囊性纖維化跨膜電導調節蛋白;G6PD:葡萄糖-6-磷酸脫氫酶;HBB:血紅蛋白β亞基;APOB:載脂蛋白B;APOA1:載脂蛋白A1;APOC1:載脂蛋白C1;CETP:膽甾醇酯轉運蛋白;LRPAP1:低密度脂蛋白受體相關蛋白1;signal transduction:信號轉導;bile acid metabolic process:膽汁酸代謝過程;bile acid biosynthetic process:膽汁酸生物合成過程;xenobiotic metabolic process:異生素代謝過程;response to drug:對藥物的反應;response to lipopolysaccharide:對脂多糖的反應;transmembrane transport:跨膜轉運;transport:運輸;cellular response to hormone stimulus:細胞對激素刺激的反應;cholesterol biosynthetic process:膽固醇生物合成過程;cholesterol homeostasis:膽固醇體內平衡;steroid metabolic process:類固醇代謝過程;lipid metabolic process:脂質代謝過程;cellular lipid metabolic process:細胞脂質代謝過程;cholesterol transport:膽固醇運輸;cholesterol efflux:膽固醇流出;very low density lipoprotein particle assembly:極低密度脂蛋白顆粒組裝;low density lipoprotein particle remodeling:低密度脂蛋白顆粒重塑;positive regulation of cholesterol esterification:膽固醇酯化的正調節;negative regulation of very low density lipoprotein particle clearance:非常密度脂蛋白顆粒清除的負調節;phospholipid efflux:磷脂外排;high density lipoprotein particle remodeling:高密度脂蛋白顆粒重塑;cholesterol metabolic process:膽固醇代謝過程;lipoprotein metabolic process:脂蛋白代謝過程;triglyceride metabolic process:三酰甘酯代謝過程;reverse cholesterol transport:逆轉膽固醇轉運;lipid transport:脂質運輸;platelet activation:血小板活化;receptor mediated endocytosis:受體介導的內吞作用;blood coagulation:血液凝固;黃三角:檢索到的與膽囊膽固醇結石發病相關的蛋白,黃三角越大表示該蛋白與膽囊膽固醇結石發生的關聯程度越高;紅圓圈:與膽囊膽固醇結石發病及上述蛋白均相關的GO功能注釋(主要涉及生物學過程和分子功能);黃三角與紅圓圈之間的連線表示該蛋白參與該功能或生物學過程

