達英-35聯合二甲雙胍治療青春期多囊卵巢綜合征療效Meta分析
林珊珊 蔣鳳艷 滕紅艷
[摘要]目的系統評價達英-35聯合二甲雙胍治療青春期多囊卵巢綜合征療效性,為青春期多囊卵巢綜合征的治療提供循證醫學證據。方法通過計算機全面檢索PubMed、CochraneLibrary、EMBASE、CMB、CNKI、VIP數據庫中關于達英-35聯合二甲雙胍治療青春期多囊卵巢綜合征的隨機對照試驗(RCTs)。根據Cochrane系統評價的方法,對文獻進行篩選、數據提取和對納入研究進行偏倚風險評價。應用RevMan5.3軟件對數據進行統計分析。結果納入6個RCT,共379名患者。通過Meta分析,達英-35聯合二甲雙胍與達英-35單獨治療療效比較,結果顯示,聯合用藥治療效果好。(1)臨床指標:體重指數(BMI)、F-G評分均顯著降低(P<0.01);(2)激素代謝指標:血睪酮(T)降低(P<0.05)、黃體生成素/卵泡刺激素(LH/FSH)顯著降低(P<0.01);(3)糖代謝指標:空腹血糖(FPG)、空腹胰島素(FINS)均降低(P<0.05),胰島素抵抗指數(HOMA-IR)顯著降低(P<0.01)。結論達英-35聯合二甲雙胍在青春期PCOS患者減輕體重,改善多毛癥狀,降低血清雄激素水平及LH/FSH比值,改善胰島素抵抗等方面優于達英-35單獨治療。
[關鍵詞]多囊卵巢綜合征;青春期;達英-35;二甲雙胍;Meta分析
[中圖分類號]R711.75
[文獻標識碼]A
[文章編號]2095-0616(2019)02-25-06
多囊卵巢綜合征(polycysticovarysyndrome,PCOS)是婦科常見的生殖內分泌疾病,其患病率為1.8%~15%[1-2]。青春期PCOS是PCOS的一種特殊類型,多表現為月經稀發或閉經、多毛、痤瘡、肥胖、胰島素抵抗[3]。若不及早發現,積極治療,不僅會使青春期PCOS女孩產生自卑心理,并且上述癥狀可能持續至成年,可能導致不孕、2型糖尿病、子宮內膜癌等風險增加。青春期PCOS的最佳一線治療仍存在爭議,激素類避孕藥(達英-35)是治療青春期PCOS患者月經紊亂、多毛、痤瘡的首選藥物,二甲雙胍是近年來用于治療PCOS合并胰島素抵抗的首選用藥。本文首次對達英-35聯合二甲雙胍治療青春期PCOS療效進行系統評價。
1 資料與方法
1.1 資料來源
文獻檢索時間從2007年1月1日~2018年6月1日。研究對象為11~19歲的青春期PCOS女性,符合2003年鹿特丹診斷標準[4]及其他相關標準:包括高雄表現、初潮后月經稀發持續至少2年或閉經、并應包括超聲下卵巢體積增大(>10cm3)。同時應排除其他導致雄激素水平升高的病因(包括先天性腎上腺皮質增生、Cushing綜合征、分泌雄激素的腫瘤等),其他引起排卵障礙的疾病(如高催乳素血癥、卵巢早衰或下丘腦-垂體性閉經,以及甲狀腺功能異常)。研究類型為隨機對照研究,觀察組為達英-35聯合二甲雙胍,對照組為達英-35。納入指標:(1)臨床指標:體重指數(BMI),多毛評分(F-G評分);(2)激素指標:睪酮(T),黃體生成素/卵泡刺激素(LH/FSH),黃體生成素(LH),卵泡刺激素(FSH);(3)糖代謝指標:空腹血糖(FPG),空腹胰島素(FINS),胰島素抵抗指數(HOMA-IR)。
1.2 檢索策略
計算機系統檢索PubMed、CochraneLibrary、EMBASE、CMB、CNKI、VIP數據庫中關于達英-35聯合二甲雙胍治療青春期PCOS的隨機對照試驗(randomized controlled trials,RCTs)。采用主題詞和自由詞聯合檢索。英文檢索詞為:“polycysticovarysyndrome、PCOS、polycysticovariansyndrome、Metformin、Diane-35、adolescent”。中文檢索詞為:
“多囊卵巢綜合征、二甲雙胍、達英-35、青春期”。
1.3 文獻篩選、數據提取、質量評價文獻篩選
文獻篩選由2名研究者獨立完成。首先通過閱讀文獻標題及摘要初篩,排除不符合納入標準的文獻。再閱讀可能符合標準的文獻全文,根據納入及排除標準確定最終是否納入。同時交叉核對篩選結果,若出現分歧,則請第3名研究者裁定。兩位研究者獨立的從納入文獻中提取數據。當出現差異時,由兩位研究者討論決定。針對每項研究都對一下信息進行提取:第一作者、發表年份、年齡、樣本量、干預措施、納入指標、干預時間。依據Cochrane風險偏倚評估工具對納入的每個隨機對照試驗進行偏倚風險程度的評價,依據偏倚風險評估標準,對每個條目做出“低風險(Lowrisk)”、“未知風險(Unclearrisk)”、“高風險(Highrisk)”的判定,繪制偏倚風險圖及偏倚風險總結圖。
1.4 統計學分析
采用RevMan5.3軟件對納入研究數據進行統計學分析。連續性變量采用均數差(meandifference,MD)、標準化均數差(std.meandifference,SMD)以及95%可信區間(confidenceinterval,CI)表示。采用I2值判斷納入研究間的異質性,當I2<50%時,表明研究間異質性小,使用固定效應模型;當I2≥50%時,表明研究間存在高度異質性,采用隨機效應模型。P<0.05表示差異有統計學意義。
2 結果
2.1 文獻檢索及篩選結果
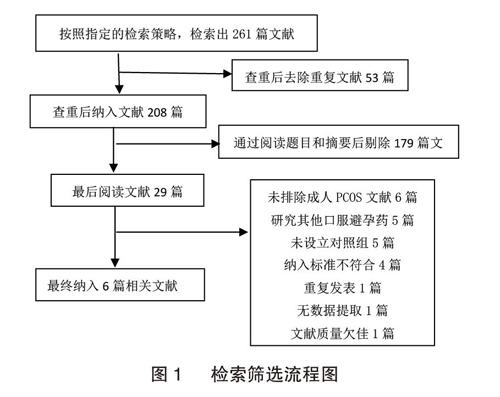
有261篇可能相關的文章被系統的檢索出來,經過篩選最終有6篇文獻符合標準[5-10],檢索過程見圖1。
2.2 納入研究基本特征
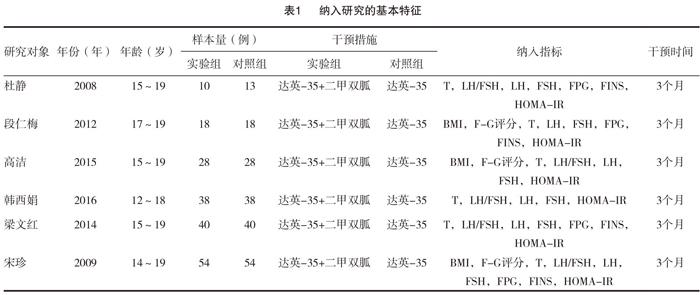
所納入的6項研究均為隨機對照試驗(RCTs),共包括379例青春期PCOS女性。6項研究中實驗組與對照組患者的年齡、臨床癥狀等基線情況基本一致,納入研究的基本特征詳見表1。
2.3 納入研究質量評價納入研究質量評價
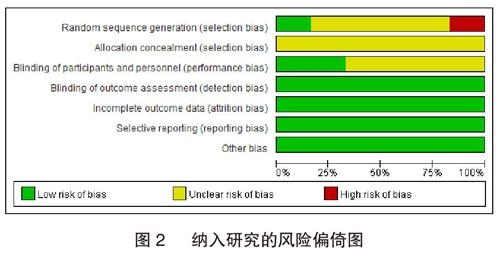
依據Cochrane風險偏倚評估工具對納入的每個隨機對照試驗進行偏倚風險程度的評價,繪制偏倚風險圖及偏倚風險總結圖,見圖2~3。
2.4 統計分析結果
達英-35聯合二甲雙胍與達英-35單藥治療比較的總的Meta分析結果詳見表2。
2.4.1 體重指數有3項研究報道了患者的BMI[6-7,10]。各研究中有統計學異質性(I2=52%,P=0.13),采用隨機效應模型,兩組之間的BMI差異有統計學意義(P=0.002),結果表明:達英-35聯合二甲雙胍組降低體重指數優于達英-35組。
2.4.2F-G評分有3項研究報道了患者的F-G評分[6-7,10]。各研究中無統計學異質性(I2=25%,P=0.27),采用固定效應模型,兩組之間的F-G評分差異有統計學意義(P<0.00001),結果表明:達英-35聯合二甲雙胍組減輕多毛癥狀優于達英-35組。
2.4.3睪酮有6項研究報道了患者的T[5-10]。各研究中有統計學異質性(I2=96%,P<0.00001),采用隨機效應模型,兩組之間的T差異有統計學意義
(P=0.03),結果表明:達英-35聯合二甲雙胍組降低血清睪酮優于達英-35組。
有4項研究報
2.4.4黃體生成素/卵泡刺激素有4項研究報道了患者的LH/FSH[5,7,9,10]。各研究中無統計學異質性(I2=0,P=0.60),采用固定效應模型,兩組之間的LH/FSH差異有統計學意義(P<0.00001),結果表明:達英-35聯合二甲雙胍組降低LH/FSH比值優于達英-35組。
2.4.5 黃體生成素有5項研究報道了患者的LH[5-7,9,10]。各研究中有統計學異質性(I2=75%,P=0.003),采用隨機效應模型,兩組之間的LH差異無統計學意義(P=0.21),結果表明:兩組在降低LH上無差異。
2.4.6 卵泡刺激素有5項研究報道了患者的FSH[5-7,9,10]。各研究中有統計學異質性(I2=71%,P=0.008),采用隨機效應模型,兩組之間的FSH差異無統計學意義(P=0.37),結果表明:兩組在降低FSH上無差異。
2.4.7 空腹血糖有4項研究報道了患者的FPG[5-6,9,10]。各研究中有統計學異質性(I2=69%,P=0.02),采用隨機效應模型,兩組之間的FPG差異有統計學意義(P=0.03),結果表明:達英-35聯合二甲雙胍組降低空腹血糖優于達英-35組。
2.4.8 空腹胰島素有4項研究報道了患者的FINS[5-6,9,10]。各研究中有統計學異質性(I2=90%,P<0.00001),采用隨機效應模型,兩組之間的FINS差異有統計學意義(P=0.02),結果表明:達英-35聯合二甲雙胍組降低空腹胰島素優于達英-35組。
2.4.9 胰島素抵抗指數有6項研究報道了患
者的HOMA-IR[5-10]。各研究中有統計學異質性(I2=96%,P<0.00001),采用隨機效應模型,兩組之間的HOMA-IR差異有統計學意義(P<0.00001),結果表明:達英-35聯合二甲雙胍組改善胰島素抵抗優于達英-35組。
3 討論
青春期是一種以生殖激素和月經模式變化為特征的時期,因下丘腦-垂體-性腺軸發育不成熟,對雌激素正反饋作用缺陷,正常青春期女性可出現月經不規則和不排卵或稀發排卵,若月經初潮后月經稀發持續2年或繼發性閉經,排除器質性卵巢功能障礙,則考慮青春期PCOS所致[11]。因青春期腎上腺初現,腎上腺及卵巢分泌雄激素增加,可出現痤瘡和輕度多毛表現,屬正常生理現象。若腎上腺初現亢進[12],出現中重度炎性痤瘡、中重度多毛,F-G評分大于8分或睪酮水平持續升高超過50ng/dL被視為高雄激素,排除其他引起高雄激素的原因,則考慮青春期PCOS所致。正常青春期少女行經腹超聲下可發現卵巢多囊性改變,但一般小于10個,此為青春期少女正常生理現象,隨著性腺軸發育成熟,出現排卵后卵巢中卵泡會逐漸減少,卵巢體積趨于穩定。若持續觀察,卵巢卵泡數目不減反增,每側卵巢小卵泡數大于12個,或體積增大超過10cm,卵巢間質回聲增強,卵巢皮質增厚等[13],則考慮青春期PCOS卵巢多囊改變。因青春期PCOS的癥狀和體征與正常青春期的生理特征相重疊,常常被人們忽略,故在診斷上比較困難。故PCOS最可靠的診斷標準是同時存在PCOS的三個癥狀和體征:高雄激素血癥、初潮后持續2年月經不規則,多囊卵巢形態所顯示卵巢體積增加(>10cm3)。此外,胰島素是青春期生長發育所必需的激素之一,胰島素可協同生長激素促進青春期女性的生長發育,故青春期胰島素分泌增加屬正常生理現象,在青春后期胰島素逐漸將至青春前期水平,若胰島素水平持續不降低,且出現明顯胰島素抵抗,糖耐量異常,腹型肥胖,黑棘皮癥[14],則考慮青春期PCOS所致。高雄激素血癥和胰島素抵抗、高胰島素血癥在青春期PCOS發病機制上起到關鍵作用,二者之間存在惡性循環關系。
我們對達英-35聯合二甲雙胍治療青春期PCOS進行研究,發現有6項研究符合納入和排除標準,共379名患者。總的Meta分析結果見表2,我們納入的每項研究所包含的樣本量均較小,23~108例。其中有3項研究納入了體重指數,與達英-35單藥治療比較,達英-35聯合二甲雙胍使體重指數下降了1.31。目前現有的證據不足以證明口服避孕藥與體重增加之間的因果關系[15]。一項關于口服避孕藥與二甲雙胍治療青春期PCOS的Meta分析[16]表示,與口服避孕藥相比較,二甲雙胍使體重指數降低4.02。二甲雙胍通過其厭食癥性質和通過直接抑制脂肪生成而導致的脂肪組織擴張降低體重指數效果確切[17]。故若青春期PCOS合并肥胖,聯合用藥對于降低體重指數效果更好。有6項研究納入了睪酮,3項研究納入了F-G評分,與達英-35單藥治療比較,達英-35聯合二甲雙胍使睪酮下降1.46,使F-G評分下降1.54。許多研究已經證實,達英-35通過與雙氫睪酮競爭受體,抑制5-α還原酶活性,刺激肝臟合成性激素結合球蛋白增多而降低雄激素水平療效確切[18-19]。二甲雙胍通過在受體后水平增強胰島素敏感性,降低青春期PCOS胰島素抵抗,從而打破高雄激素和胰島素抵抗之間的惡性循環[20],協同達英-35降低雄激素水平,從而改善青春期PCOS多毛、痤瘡等高雄激素的癥狀和體征。故若單獨使用達英-35降低雄激素不明顯時,應考慮是否存在胰島素抵抗,可聯合使用二甲雙胍。有4項研究納入了LH/FSH,有5項研究分別納入了LH、FSH,與達英-35單藥治療比較,達英-35聯合二甲雙胍使LH/FSH比值僅降低0.16,兩組間LH、FSH無明顯差異。從此結果可看出,二甲雙胍無明顯抑制性腺軸分泌LH的作用,聯合用藥較單藥組輕微降低LH/FSH比值,追其原因,可能與二甲雙胍改善胰島素抵抗,從而降低雄激素水平,負反饋減少性腺軸分泌LH有關。青春期PCOS女孩LH脈沖釋放頻率增加和幅度變大,導致LH分泌增加,LH/FSH大于2[21]。達英-35通過抑制性腺軸LH分泌,FSH分泌相對增加,而使LH/FSH比值降低。故若針對只存在LH/FSH比值升高,而無雄激素水平升高的疑似青春期PCOS患者,達英-35單藥治療和聯合用藥效果相差不大。有4項研究分別納入FPG,FINS,6項研究納入HOMA-IR,與達英-35單藥治療比較,達英-35聯合二甲雙胍使FPG降低0.30,FINS降低1.13,HOMA-IR降低0.92。二甲雙胍是一種胰島素增敏劑,抑制腸道葡萄糖的吸收,肝糖原異生和輸出,增加組織對葡萄糖的攝取利用,提高胰島素敏感性。不降低正常血糖,僅降低高血糖[22]。本Meta分析納入的青春期PCOS女孩的血糖均在正常水平,故無論達英-35單藥治療或聯合用藥均不會明顯降低PCOS患者的血糖水平,但達英-35聯合二甲雙胍可明顯降低血清胰島素水平,改善胰島素抵抗。青春期PCOS常常合并胰島素抵抗和高胰島素血癥,研究表明達英-35并不能改善PCOS患者胰島素抵抗。故對合并胰島素抵抗的青春期PCOS應聯合達英-35和二甲雙胍治療,不僅能顯著降低血清雄激素水平,還可明顯降低胰島素水平,改善胰島素抵抗。
本Meta分析局限性在于納入的均為中文文章,目前無針對達英-35聯合二甲雙胍治療青春期PCOS的外文文獻。所納入文章均無采用盲法,質量偏低。對脂代謝的研究僅一篇文章提及,未能納入研究。所納入文章研究時限均為3個月,缺乏長期隨訪。對藥物不良僅稍微提及,并未進行統計分析。
綜上所述,達英-35聯合二甲雙胍在青春期PCOS患者減輕體重,改善多毛癥狀,降低血清雄激素水平及LH/FSH比值,改善胰島素抵抗等方面優于達英-35單獨治療。由于納入研究數量較少,研究質量不統一,本結論尚需要更多高質量臨床隨機對照研究予以證實。
[參考文獻]
[1] Li R,Zhang Q,Yang D,et al.Prevalence of polycysticovary syndrome in women in China:a large
community-based study [J].Hum Reprod,2013,28 (9):2562-2569.
[2] Christensen SB,Black MH,Smith N,et al.Prevalence of polycystic ovary syndrome in adolescents [J].Fertil Steril,2013,100(2):470-477.
[3] Ibanez L,Oberfield SE,Witchel S,et al.An International Consortium Update:Pathophysiology,Diagnosis,and Treatment of Polycystic Ovarian Syndrome in Adolescence [J]. Horm Res Paediatr,2017,88(6):371-395.
[4] Rotterdam EA-SPCWG.Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome [J]. Fertil Steril,2004,81(1): 19-25.
[5]杜靜,梁曉燕.二甲雙胍聯合復方醋酸環丙孕酮治療青春期PCOS療效分析[J].國際婦產科學雜志,2008(1):69-71.
[6]段仁梅,吳亞菊,沈麗萍.復方醋酸環丙孕酮聯合二甲雙胍治療青春期多囊卵巢綜合征臨床觀察[J].中國當代醫藥,2012,19(34):68-69,71.
[7]高潔.炔雌醇環丙孕酮聯合二甲雙胍治療青春期多囊卵巢綜合征療效觀察[J].實用預防醫學,2015,22(4):492-494.
[8]韓西娟.達英-35聯合二甲雙胍對青春期多囊卵巢綜合征卵巢功能的影響[J].中國婦幼保健,2016,31(3):569-571.
[9]梁文紅.二甲雙胍治療青春期多囊卵巢綜合征患者的效果分析[J].中國醫藥科學,2014,4(6):88-90.
[10]宋珍,鄧曉惠.二甲雙胍聯合達英-35治療青春期多囊卵巢綜合征療效觀察[J].中國醫療前沿,2009,4(9):69-70.
[11] Apter D.Endocrine and metabolic abnormalities inadolescents with a PCOS-like condition:consequences for adult reproduction [J]. Trends Endocrinol Metab,1998,9(2):58-61.
[12] Oberfield SE,Sopher AB,Gerken AT.Approach to the girl with early onset of pubic hair [J].J Clin Endocrinol Metab,2011,96(6):1610-1622.
[13] Webber LJ,Stubbs S,Stark J,et al.Formation and early development of follicles in the polycystic ovary[J].Lancet,2003,362(9389):1017-1021.
[14] Moran A,Jacobs DR Jr,Steinberger J,et al.Insulin resistance during puberty:results from clamp studies in 357 children [J].Diabetes,1999,48(10):2039-2044.
[15] Gallo MF,Lopez LM,Grimes DA,et al.Combinationcontraceptives:effects on weight [J].Cochrane DatabaseSyst Rev,2014(1):CD003987.
[16] Al Khalifah RA,Florez ID,Dennis B,et al.Metforminor Oral Contraceptives for Adolescents With Polycystic Ovarian Syndrome:A Meta-analysis[J].Pediatrics,2016,137(5):e20154089.
[17] Alexandre KB,Smit AM,Gray IP,et al.Metformin inhibits intracellular lipid accumulation in the murine pre-adipocyte cell line,3T3-L1 [J].Diabetes Obes Metab,2008,10(8):688-690.
[18] Elter K,Imir G,Durmusoglu F.Clinical,endocrine and metabolic effects of metformin added to ethinylestradiol- cyproterone acetate in non-obese women with polycysticovarian syndrome:a randomized controlled study[J].HumReprod,2002,17(7):1729-1737.
[19] Feng W,Jia YY,Zhang DY,et al.Management of polycysticovarian syndrome with Diane-35 or Diane-35 plusmetformin[J].Gynecol Endocrinol,2016,32(2):147-150.
[20] Pauli JM,Raja-Khan N,Wu X,et al.Current perspectives of insulin resistance and polycystic ovary syndrome[J].Diabet Med,2011,28(12):1445-1454.
[21] Thompson IR,Kaiser UB.GnRH pulse frequency-dependent differential regulation of LH and FSH gene expression [J].MolCell Endocrinol,2014,385(1-2):28-35.
[22]郭勇,肖青,劉妍,etal.達英-35與二甲雙胍治療多囊卵巢綜合征療效Meta分析[J].中國實用婦科與產科雜志,2010,26(11):845-848.

