培美曲塞聯合順鉑與標準TP方案用于肺腺癌患者術后化療的近期療效比較
張旭宇 李潤浦 王艷麗 李冬杰
肺癌為全球癌癥死亡事件主要原因,其組織學類型包括小細胞肺癌以及非小細胞肺癌(non small lung cancer,NSCLC),腺癌是NSCLC最常見類型,約40%肺癌患者為腺癌[1-2]。當前,臨床常采取手術治療、化療與放療方式治療肺腺癌,其中首選療法為根治性外科手術。術后肺腺癌具有較高復發率,行輔助化療,則能減小復發風險。多西紫杉醇聯合鉑類屬于當前NSCLC術后標準化療手段。培美曲塞是現代新型多靶點有效抗腫瘤藥物,相較于標準方案,其治療優勢尚未明確[3-4]。本文以76例行肺癌根治術的肺腺癌患者作為研究對象,觀察培美曲塞聯合順鉑和標準TP方案對肺腺癌患者術后化療的近期療效及不良反應,為肺腺癌患者術后輔助化療提供參考。
1 資料與方法
1.1 一般資料
將2012年3月至2014年4月我院收治的76例行肺癌根治術的肺腺癌病例納入研究,采取抽簽法將其隨機分為2組,各38例。A組男性21例,女性17例,患者年齡38~68歲,中位年齡(58.17±5.94)歲;病理分化程度:低/低中分化13例,中/中高分化12例,高分化13例;N分期:N018例,N19例,N211例;術后病理分期:ⅠB期12例,Ⅱ期20例,ⅡA期6例。B組男性23例,女性15例,患者年齡37~69歲,中位年齡(57.86±5.82)歲;病理分化程度:低/低中分化15例,中/中高分化9例,高分化14例;N分期:N020例,N16例,N212例;術后病理分期:ⅠB期14例,Ⅱ期17例,ⅡA期7例。2組性別構成、平均年齡、病理分化程度、N分期及術后病理分期等一般資料水平比較,差異無統計學意義(P>0.05)。
1.2 納入標準
①臨床檢查聯合影像學診斷結果為肺腺癌,且接受肺癌根治術治療;②術后病理分期屬ⅠB、Ⅱ或者ⅡA期;③術后3~4周給予輔助化療;④化療開始前體力評分(eastern cooperative oncology group,ECOG)低于2分;⑤無化療禁忌;⑥簽署研究知情同意書;⑦獲得倫理委員會認可。
1.3 排除標準
①存在其他惡性腫瘤史;②伴隨急性感染、心肺肝腎相關疾病,無法耐受化療;③過敏體質;④發生遠處轉移;⑤行其他抗腫瘤治療。
1.4 方法
2組患者化療前1周直到化療結束后3周內均服用葉酸,400 μg/d,同時注射維生素B12,1 000 μg/次,每9周1次,且給藥前1 d、當天與給藥后1 d,需服用地塞米松,9 mg/d。A組實施培美曲塞聯合順鉑方案:化療第1天以靜脈滴注方式給予培美曲塞,每天500 mg/m2,并于第1~3天以靜脈滴注方式給予順鉑,每天25 mg/m2。B組實施TP方案:以靜脈滴注方式給予多西紫杉醇,于第1天予以75 mg/m2,第1~3天,每天以靜脈滴注方式給予順鉑75 mg/m2。2組方案1周期為21天,共治療4周期。整個化療周期結束后,患者需定期接受復查,予以3年隨訪,記錄生存情況。
1.5 觀察指標
觀察2組4周期后臨床療效、3年無病生存率與中位無病生存期(DFS)、3年總生存率與中位總生存期(OS)。記錄2組化療不良反應:包括白細胞減少、中性粒細胞減少、血小板減少、貧血、惡心嘔吐、腎毒性、疲乏、脫發、谷丙轉氨酶(ALT)升高、谷草轉氨酶(AST)升高、皮疹等。依據1981年WHO制定的抗癌藥物不良反應分度將其分為0~Ⅳ度[5]。療效評估參照世界衛生組織(world health organization,WHO)實體瘤療效標準[6]分為:完全緩解(complete response,CR)、部分緩解(partial response,PR)、穩定(stable disease,SD)、進展(progressive disease,PD),總有效率=(CR+PR)/總例數×100%。
1.6 統計學分析
2 結果
2.1 2組近期療效比較
化療4周期后,A組總有效率34.21%,與B組31.58%比較,無統計學差異(P>0.05)。見表1。
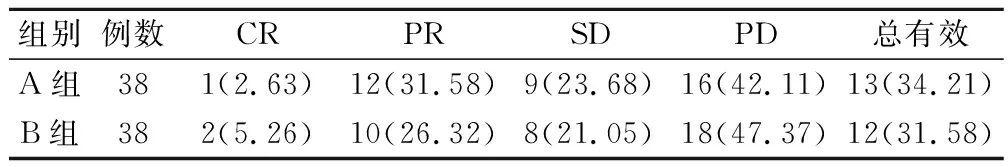
表1 2組近期療效比較(例,%)
2.2 2組3年內生存情況比較
A組無病生存率(60.53%)、中位DFS (25.13個月)、總生存率(78.95%)、中位OS(34.75個月)與B組無病生存率(55.26%)、中位DFS (24.96個月)、總生存率(81.58%)、中位OS(35.18個月)比較,無顯著差異(P>0.05)。見表2、圖1與圖2。
2.3 2組化療不良反應比較
A組Ⅲ~Ⅳ級白細胞減少率(5.26%)、Ⅲ~Ⅳ級中性粒細胞減少率(2.63%)及Ⅲ~Ⅳ級脫發率(7.89%)均明顯低于B組(26.32%)、(15.79%)、(28.95%)(P<0.05);其他不良反應發生情況比較無顯著差異(P>0.05)。見表3。

表2 2組3年內生存情況比較(例,%)
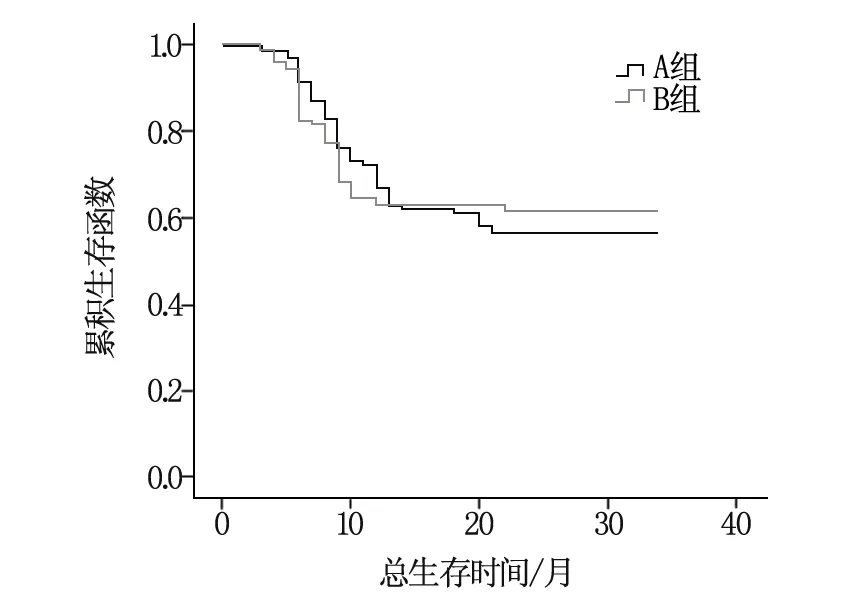
圖1 2組DFS生存曲線
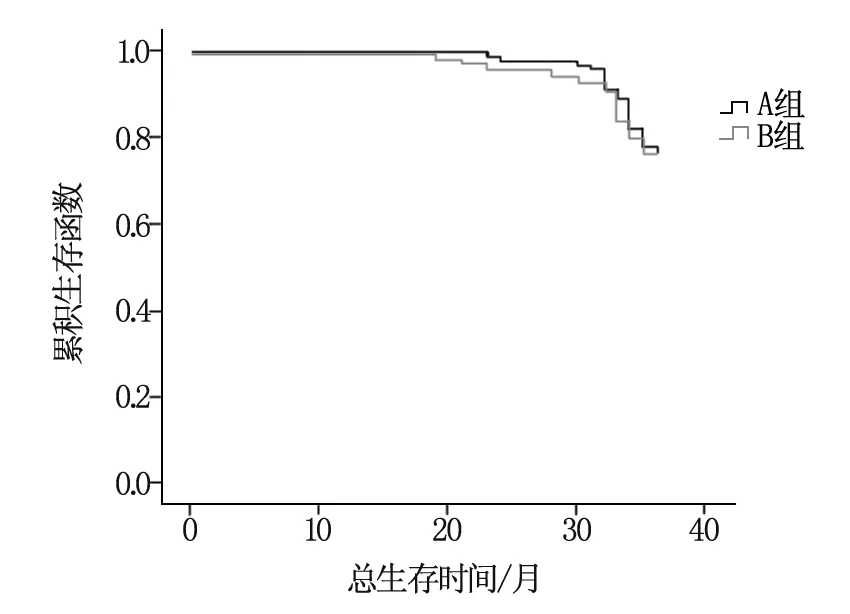
圖2 2組OS生存曲線
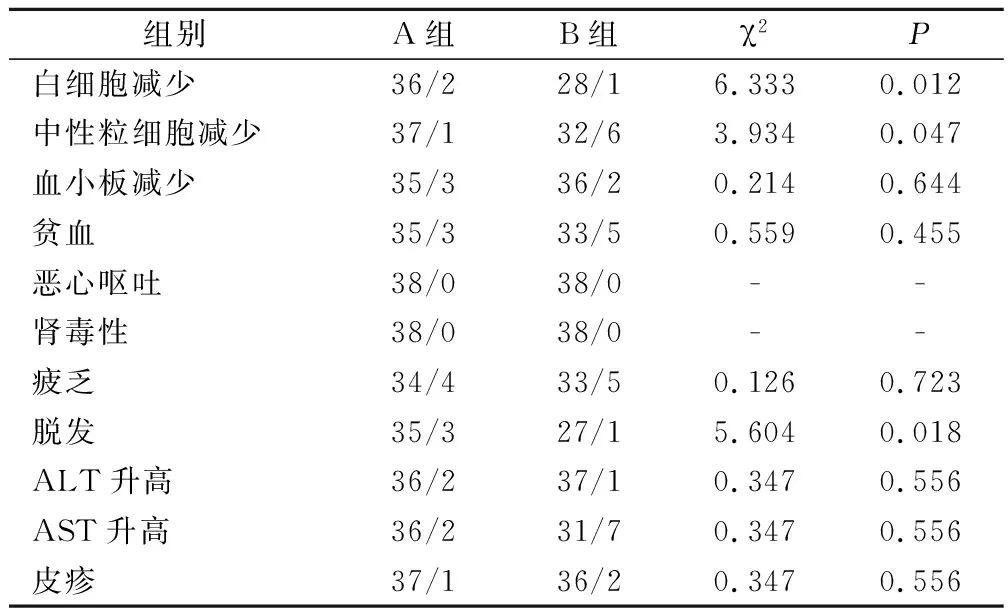
組別A組B組χ2P白細胞減少36/228/16.3330.012中性粒細胞減少37/132/63.9340.047血小板減少35/336/20.2140.644貧血35/333/50.5590.455惡心嘔吐38/038/0--腎毒性38/038/0--疲乏34/433/50.1260.723脫發35/327/15.6040.018ALT升高36/237/10.3470.556AST升高36/231/70.3470.556皮疹37/136/20.3470.556
3 討論
早期NSCLC最有效治療方式為手術切除,但60%以上ⅠB期~ⅢA期患者術后可能因復發致死[7]。肺癌根治術的操作,盡管完整切除了能夠宏觀看到的腫瘤病灶,但是若手術切除病灶前即出現了微轉移現象,將引起腫瘤復發。對于明確顯示因為病灶微轉移而產生的腫瘤復發,必須在術后采取輔助化療對策,可在一定程度上減少復發和死亡幾率。
培美曲塞屬于抗葉酸制劑,具有多靶點特性,可對二氫葉酸還原酶以及胸苷酸合成酶等的活性產生明顯抑制作用,導致嘌呤產物與胸腺嘧啶核苷生成物水平降低,從而干擾腫瘤組織細胞DNA合成過程,影響細胞增殖,其對多種腫瘤均能發揮抗癌功效。2008年,食品藥品監督管理局(food and drug administration,FDA)批準培美曲塞用于NSCLC一線治療[8-9]。多西紫杉醇一般以增強細胞微管聚合效果的方式抑制微管解聚,導致癌細胞處在M期、G2期不再進展,從而產生抗癌療效;順鉑屬于當前NSCLC臨床治療最有效藥品,對患者單純使用,有效率可達16%~20%,將其和多西紫杉醇聯用,可產生協同效果,屬于NSCLC患者標準化療方案[10-12]。然而,多西紫杉醇骨髓抑制以及過敏反應等均比較嚴重,患者液體潴留相對突出。臨床工作中,開始在肺腺癌根治術后輔助化療過程中使用培美曲塞聯合鉑類方案。相較于標準方案,該類輔助化療療效相關大型試驗報道較少。培美曲塞引起的不良反應主要和其酶抑制作用存在密切聯系,骨髓抑制是其較為常見血液學毒性,通常表現為中性粒細胞減少,有時伴隨血紅蛋白數或者血小板數減少反應[13-16]。非血液學毒性常見表現包括疲乏、惡心嘔吐、皮疹、腸胃不適、肝腎功能障礙、排便異常等。少數患者可產生感覺異常、胸痛以及黏膜炎等反應。
本組研究結果顯示,2組近期治療總有效率、3年內無病生存率、中位DFS、總生存率及中位OS比較無顯著差異,與梁亞海[17]研究結論一致。說明培美曲塞聯合順鉑和標準TP方案均能對肺腺癌患者術后產生一定化療效果,且在延長患者生存率與生存期方面的效果相當。結果還顯示,A組Ⅲ~Ⅳ級白細胞減少率、中性粒細胞減少率及脫發率均明顯低于B組,其他不良反應發生情況比較無顯著差異,提示相較于TP方案,在肺腺癌患者術后化療中采取培美曲塞聯合順鉑方案,可有效減輕患者白細胞減少、中性粒細胞減少與脫發等化療不良反應,而其他不良反應情況相似。有研究表明,培美曲塞+鉑類方案耐受性好,肺腺癌患者由于不能耐受而必須降低藥物劑量的只有2%~4%,可以很好完成該化方案的患者高達95%[18]。故在肺癌治療中,培美曲塞具有良好應用前景,將其聯合鉑類使用,可顯示出比較好的耐受性,化療不良反應更低。
綜上,培美曲塞聯合順鉑和標準TP方案均能在肺腺癌術后化療中獲得一定輔助化療效果,療效相近,但培美曲塞聯合順鉑可減輕患者化療不良反應,在患者耐受性方面具有更大優勢。

