利用577nm閾值下微脈沖激光治療糖尿病性黃斑水腫
陶 玥,姜海濤,劉加勇
0引言
糖尿病視網膜病變(diabetic retinopathy,DR)屬于糖尿病常見慢性微血管性并發癥之一,其中糖尿病性黃斑水腫(diabetic macular edema,DME)與增殖性糖尿病視網膜病變(proliferative diabetic retinopathy,PDR)分別為糖尿病患者發生視功能損害與致盲的直接誘因[1]。DME可發生于DR任何階段,多與血管滲漏促進因子表達、炎癥細胞因子作用及血流動力學改變所引起的血-視網膜屏障(blood retinal barrier,BRB)完整性、功能性遭到破壞有關[2]。目前臨床治療DME主要通過玻璃體腔注射藥物、激光光凝及玻璃體切割手術實現,其中反復玻璃體腔注射藥物不良反應較多,玻璃體切割手術對視功能改善效果仍有待優化,而激光光凝治療則操作要求較低,且兼具療效與安全性,仍是DME的公認最佳治療途徑[3]。傳統格柵樣激光具有短時高溫效應,對水腫吸收的促進效果已獲得廣泛認同[4],但由于其熱量傳導造成過多損傷,近年來有多項研究對其安全性提出質疑[5-7],臨床逐漸以其他激光模式取而代之。微脈沖激光作為短促高頻的重復脈沖激光類型,可借助閾值下能量控制特點,將靶點熱能傳播限制在較小范圍[8],但應用于光凝治療是否能達到預期效果仍有待進一步證實。對此,本研究旨在對比577nm閾值下微脈沖激光術與傳統格柵樣激光術應用于DME的療效與安全性,取得一定成果,現作如下報告。
1對象和方法
1.1對象回顧性分析。選取2016-04/2018-03于我院接受治療的48例64眼DME患者臨床資料,行577nm閾值下微脈沖激光術者納入觀察組(26例35眼),行傳統格柵樣激光術者納入對照組(22例29眼)。納入標準:(1)病史、癥狀及裂隙燈顯微鏡檢查、眼底熒光血管造影(FFA)、光學相干斷層掃描(OCT)結果均符合DME相關診斷標準者[9];(2)年齡為30~80歲者;(3)內分泌專科證實血糖控制良好者;(4)患者對術式預期療效及風險知情同意。排除標準:(1)診斷為視網膜靜脈阻塞、葡萄膜炎復發、玻璃體黃斑部牽拉、頓挫外傷、高度近視等其他因素引起黃斑水腫者;(2)合并眼壓異常、固視功能異常、屈光介質不清或感染性眼科疾病患者;(3)伴有高血壓或肝腎功能、凝血功能障礙等手術禁忌證者;(4)已接受藥物注射或有任何眼科手術史者;(5)妊娠期或哺乳期婦女;(6)依從性欠佳、改變治療方案或隨訪時間<6mo者。兩組一般臨床資料比較,差異均無統計學意義(P>0.05),后續指標觀測具有可比性,見表1。
1.2方法兩組患者術前完善各項眼科檢查,托吡卡胺散瞳,奧布卡因滴眼液充分表面麻醉,FFA影像資料對滲漏點進行準確定位,并擬定覆蓋性光凝策略。對照組行傳統格柵樣激光術,激光器設置為連續波模式,波長532nm,光斑直徑為90~120μm,曝光時間為0.1s,50~200mW范圍內逐步上調功率直至靶點產生淺白色光凝斑時,在中心凹外圍750μm位置,避開乳頭黃斑束作3~4排C型光凝斑。觀察組行577nm閾值下微脈沖激光術,預先在后極部視乳頭鼻側1DD位置進行能量閾值測試,連續波模式下逐步增大能量,以隱約可見視網膜變白(Ⅰ級淡灰色光斑)為宜,設定為能量閾值;將激光器轉變為微脈沖多點模式實施密集型治療,曝光時間為0.2s,波長577nm,光斑直徑140~160μm,光斑間距為0倍,工作負載率(脈沖通電占空比)5%,脈沖激光能量強度為上述所得閾值的1/2;根據FFA情況確定黃斑中心位置,光凝點在中心凹外圍500μm位置,在多點模式下作環形密集型光凝,兩組術后均持續隨訪6mo,囑患者按時回院復查。于術前及術后1、3、6mo時,采用LogMAR視力表對患眼進行最佳矯正視力(BCVA)評估;應用OCT檢測患眼黃斑中心凹視網膜厚度(CFT);借助視野計,0~20dB亮度范圍內固視十字形目標,對患眼黃斑10°范圍內平均光敏感度(MS)進行分析,并與基準視野范圍對比獲得平均視野缺損(MD)。回顧患眼眼底硬性滲出隨訪情況,統計其隨訪時間,并搜集術后6mo內并發癥發生情況進行分析。
2結果
2.1兩組患者手術前后BCVA比較重復測量設計方差分析顯示,LogMAR視力表測試結果在組間、時間、時間×組間交互作用因素中均受到顯著影響(F組間=18.233,F時間=48.217,F時間×組間=7.156;均P<0.05)。術后1、3、6mo時,兩組LogMAR視力表測試結果均較術前有顯著下降,且觀察組明顯低于同一時間對照組,差異均有統計學意義(P<0.05,表2)。
2.2兩組患者手術前后CFT比較重復測量設計方差分析顯示,CFT水平在組間、時間、時間×組間交互作用因素中均受到顯著影響(F組間=36.602,F時間=66.570,F時間×組間=9.642;均P<0.05)。術后1、3、6mo時,兩組CFT水平均較術前有顯著下降,且觀察組明顯低于同一時間對照組,差異均有統計學意義(P<0.05,表3)。
2.3兩組患者手術前后MS比較重復測量設計方差分析顯示,MS水平在組間、時間、時間×組間交互作用因素中均受到顯著影響(F組間=48.132,F時間=89.022,F時間×組間=12.847;均P<0.05)。術后1、3、6mo時,觀察組MS水平均較術前有顯著提升,且明顯高于同一時間對照組,差異均有統計學意義(P<0.05,表4)。
2.4兩組患者手術前后MD比較重復測量設計方差分析顯示,MD水平在組間、時間、時間×組間交互作用因素中均受到顯著影響(F組間=26.343,F時間=57.934,F時間×組間=7.336;均P<0.05)。術后1、3、6mo時,觀察組MD水平均較術前有顯著提升,明顯高于同一時間對照組,差異均有統計學意義(P<0.05,表5)。
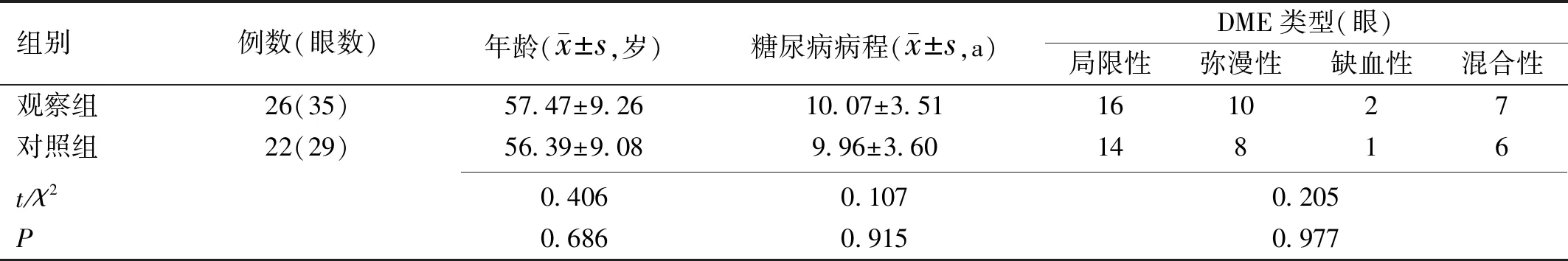
表1 兩組患者一般臨床資料比較
注:觀察組:行577nm閾值下微脈沖激光術者;對照組:行傳統格柵樣激光術者。
表2 兩組患者手術前后LogMAR視力表測試結果比較
注:觀察組:行577nm閾值下微脈沖激光術者;對照組:行傳統格柵樣激光術者。aP<0.05vs本組術前。
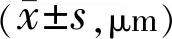
表3 兩組患者手術前后CFT水平比較
注:觀察組:行577nm閾值下微脈沖激光術者;對照組:行傳統格柵樣激光術者。aP<0.05vs本組術前。
表4 兩組患者手術前后MS水平比較
注:觀察組:行577nm閾值下微脈沖激光術者;對照組:行傳統格柵樣激光術者。aP<0.05vs本組術前。
表5 兩組患者手術前后MD水平比較
注:觀察組:行577nm閾值下微脈沖激光術者;對照組:行傳統格柵樣激光術者。aP<0.05vs本組術前。
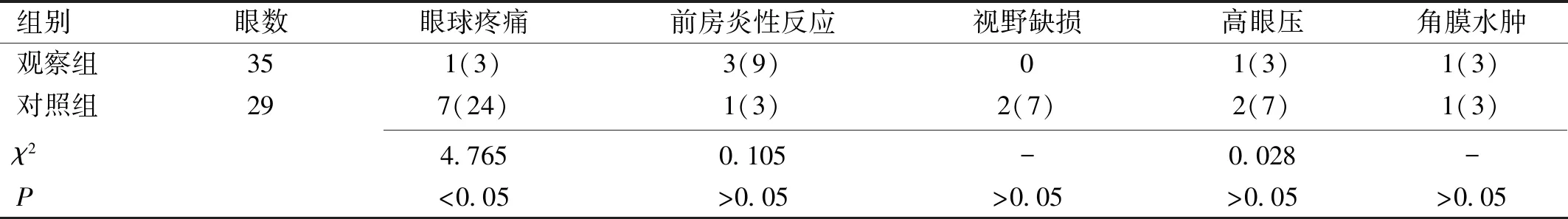
表6 兩組患者術后并發癥發生率比較眼(%)
注:觀察組:行577nm閾值下微脈沖激光術者;對照組:行傳統格柵樣激光術者。-:統計出部分理論頻數<1,轉而采用Fisher確切概率檢驗。
2.5兩組患者眼底硬性滲出持續時間比較觀察組眼底硬性滲出持續時間為3.39±0.80mo,明顯少于對照組(4.25±1.14mo),組間差異有統計學意義(t=3.536,P=0.001)。
2.6兩組并發癥發生情況比較術后6mo內,觀察組眼球疼痛發生率明顯低于對照組,差異有統計學意義(P<0.05),而前房炎性反應、視野缺損、高眼壓及角膜水腫發生率比較差異均無統計學意義(P>0.05,表6)。
3討論
局部激光光凝治療DME主要通過刺激視網膜色素上皮層(retinal pigment epithelium,RPE)細胞并封閉微動脈瘤滲漏,從而促進RPE衍生因子合成,更新RPE細胞[10],此外還將通過熱效應破壞視網膜外層光感受器,保障其內層氧供與代謝,抑制血管內皮生長因子(vascular endothelial growth factor,VEGF)表達,使微血管管腔收縮,血管壁通透性降低,進而維護視網膜外屏障功能,方能減輕水腫癥狀。傳統格柵樣激光術是應用較為廣泛的光凝治療方案,通過改善黃斑區微循環,減少血管滲漏與水腫癥狀,能極大程度保留黃斑病變患者殘存視力,降低中重度視力喪失風險[11]。本研究中,兩組患者術后CFT水平均獲得顯著減少,其中觀察組減少幅度較大,這表明兩種激光光凝策略均能有效緩解DME患者黃斑區水腫,其中577nm閾值下微脈沖激光術可能因治療范圍在中心凹外圍500μm處,相比于傳統格柵樣激光術的750μm,更接近于中心凹,故而治療效率更高,對加快水腫消退有利。
DME不僅是糖尿病微血管病變的眼部典型表現,還是糖尿病性末梢神經結構病變導致視神經元損害的綜合體現。據相關文獻報道,糖尿病神經變性相較于微血管病變早10mo左右,且病理變化多以軸突變性、神經節脫髓鞘、髓纖維缺失等形式呈現[12],最終可導致末端軸突不可逆性壞死,進而引起視錐細胞及其神經節細胞介導的神經通道功能障礙,可表現出視網膜MS偏低。本研究結果顯示,觀察組術后MS獲得顯著持續性改善,但對照組則直接惡化且持續改善幅度較小,提示577nm閾值下微脈沖激光術通過控制熱能擴散損傷,而對患眼光感受器損害較小,術后在保留MS基礎上恢復更快,相比之下傳統格柵樣激光術不僅對光感受器細胞造成損害,還可能由于引起水腫復發而阻礙MS復舊,后者并不利于患者預后視功能恢復。有學者認為,除治療方式外,術后血糖控制對MS恢復影響也較大,尤其糖尿病病程較長患者,視神經末梢對高血糖及缺血、缺氧環境更為敏感[13],臨床需引起足夠重視。
傳統光凝治療致力于從多個方面促進水腫消退,但其實質仍屬于對視網膜的破壞過程,除誘發疼痛外,還可造成周邊視野缺損,誘發玻璃體出血及視力下降等不良后果[14]。部分研究指出,DME經由激光光凝治療后30、90d隨訪時,患眼部分區域視野獲得轉歸,但仍不可控制出現新的視野缺損點,可知激光對周圍組織損害造成MS與空間分辨率同時受到影響[15],但也發現部分患者視力仍未受到負面影響,這可能與激光熱損害作用不同于黃斑病變的病理機制有關。本研究發現,觀察組經過治療,MD水平得到顯著提升,而對照組則有所下降,且前者中遠期改善幅度更顯著,這說明577nm閾值下微脈沖激光術能有效保留患眼整體空間分辨率,并在此基礎上推進術后視野恢復進程。相關專家表示,DME術后黃斑水腫逐漸消退,但光感細胞受損不能隨即恢復,患眼視野水平轉歸仍受到限制,且還可能導致固視穩定性及中心固視能力丟失[16],對患者生活質量恢復不利。
不同于傳統格柵樣激光術中激光作用時間等同于整個曝光時間,微脈沖激光由一系列完整且可重復的高頻脈沖組成,曝光過程由激光作用時間與間歇時間構成,調控激光作用時間越短,光熱效應傳播距離越近,從而減少激光對視網膜周圍組織的熱損傷[17],是保護患眼視功能的可靠手段。葉黃素對綠色光與黃色光不甚敏感,因此既往黃斑病變光凝治療的激光波長通常在495~590nm區間內進行選擇,然而近年研究發現,葉黃素對黃色光敏感性相較于綠色光更低,且光熱散射效應更小,選取570~590nm黃色激光可在保障安全性的前提下令光凝斑更接近于中心凹,且由于氪黃激光(568.2nm)造價高昂,故多選擇閾值下固態二極管黃色激光(577nm)應用于眼科臨床[18]。本研究中,采用577nm閾值下微脈沖激光術的觀察組術后同一時間BCVA改善效果明顯優于對照組,且硬性滲出持續時間顯著較短,提示該治療方案憑借精準且控制良好的光凝治療操作,可確保眼底血管通透性盡快復舊,進而術后水腫消退、視網膜下液吸收與黃斑功能轉歸效率更高,對視功能迅速恢復有積極意義。有關研究還發現,微脈沖激光術治療DME能有效改善患眼視野缺失,同樣相對傳統光凝治療方案具備較大優勢[19]。
相關指南要求,激光光凝治療后,能在眼底鏡下可見灰白色光凝斑方能確定治療充分[20],工作時間≥100ms的激光發射裝置基本能達到上述要求,甚至極易出現諸如視網膜下纖維化、光凝斑進行性增大及RPE細胞萎縮等過度治療征象。而閾值下條件是微脈沖控制激光強度的重要前提,如根據指南要求進行持續脈沖激光輻照,可能對視網膜內層造成不可逆損傷,因此應當先在視乳頭鼻側特定部位進行閾值能量測定,避開對術區的影響且能科學有效確定激光能量參數設定,可保障眼底鏡下不可見或僅見淡灰色光斑,從而避免過度治療。本研究中,雖然兩組患者術后前房炎性反應、視野缺損、高眼壓及角膜水腫發生率無顯著性差異,但觀察組眼球疼痛發生率明顯較低,這表明577nm閾值下微脈沖激光術的觀察組術中激光列陣范圍縮小,空間定位準確而操作周期有所縮短,對改善治療體驗有利。連海燕等[21]認為,閾值下微脈沖激光因安全性能更高,可將持續性或復發性視網膜病變納入適應證范圍,證實3a內約28%患眼需接受1次治療,約48%患眼需接受2次治療,約24%患眼需接受≥3次治療,有利于保障取得良好預后。
本研究僅就兩種激光光凝治療方案進行對比,觀察患眼術后短期內相關指標改變情況,缺乏長期隨訪資料回顧,且未對視野、對比敏感度等視功能重要指標進行比較,仍有待在往后研究中設計多中心研究思路加以探索。
綜上所述,577nm閾值下微脈沖激光術應用于DME治療可顯著改善患眼BCVA、CFT、MS、MD水平,術后眼球疼痛發生風險低,有利于加快患者預后視功能恢復。

