伊曲康唑霧化吸入預防侵襲性肺曲霉病藥效學研究
盧鑫 朱穎 王麗 施毅 高海燕 楊健 張秀偉南京醫科大學附屬江寧醫院呼吸內科00;解放軍南京總醫院呼吸與危重癥醫學科000
伊曲康唑是臨床應用廣泛的三唑類抗真菌藥物,傳統用藥方式為靜脈及口服給藥,主要針對真菌感染的預防性治療、經驗性治療、針對性治療和挽救性治療方面。氣道是人體抵御曲霉感染的第一道防線,霧化吸入應用抗真菌藥物可在肺局部形成較高藥物濃度,發揮抗真菌活性,抑制曲霉菌絲的侵襲性生長。本研究擬通過動物實驗觀察伊曲康唑霧化吸入、系統給藥及聯合給藥對侵襲性肺曲霉病(invasive pulmonary aspergillosis,IPA)小鼠生存率及肺部真菌負荷的影響,對霧化吸入伊曲康唑防治IPA 的用藥策略做初步探討。
1 材料與方法
1.1 實驗動物及菌株 本研究符合 《赫爾辛基宣言》的原則。選用6周齡雌性清潔級ICR 小鼠60只,分籠飼養,自由進食進水。選用MF13煙曲霉菌株。
1.2 實驗方法
1.2.1 實驗動物分組及處理 隨機分配為4 組,每組15只,設置對照組:感染未用藥;腹腔注射治療組:感染后第2天開始腹腔注射伊曲康唑至第7天;霧化預防組:感染前第2天開始霧化伊曲康唑至第7天;聯合防治組:感染前第2天開始霧化伊曲康唑聯合感染后第2天開始腹腔注射伊曲康唑至第7天。如圖1所示,每組中隨機選取9只小鼠觀察生存情況,時間截止到感染后第12天;其余6只小鼠在感染后第7天脫頸處死取肺組織勻漿化檢測肺真菌負荷,死亡的小鼠立即取肺組織勻漿化檢測肺真菌負荷。
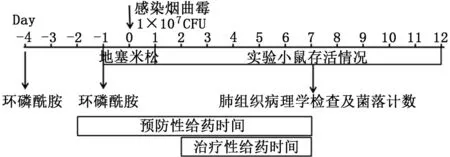
圖1 實驗流程示意圖
1.2.2 IPA 動物模型制備 實驗小鼠采用以下方法造成免疫抑制狀態:環磷酰胺250 mg/kg腹腔注射(感染前第4天及感染前第1天各1次),地塞米松50 mg/kg腹腔注射 (感染前第1天、感染當天及感染后第1天各1次)。免疫抑制后采用氣管插管氣管內滴入法接種50μl濃度為2×108菌落形成單位/毫升 (Colony-form Units/ml,CFU/ml)的煙曲霉孢子懸液[1]。
1.2.3 霧化吸入給藥 小鼠腹腔注射120μl 2%戊巴比妥麻醉后頭部固定,連接霧化器啟動霧化。用藥劑量為30 mg/kg,每天用藥一次,霧化時間為60 min。
1.2.4 腹腔注射給藥 固定小鼠并翻轉暴露腹部皮膚,選擇中下腹部為進針點,緩慢注入藥液后快速退針,保持此體位30 s,伊曲康唑用量為30 mg/kg。
1.2.5 肺組織真菌菌落負荷檢測方法 無菌條件下取小鼠新鮮右肺并勻漿化,電子天平稱重后按1 g濕肺組織∶10 ml磷酸鹽緩沖液 (含0.1%吐溫80)比例稀釋,取10μl稀釋液接種于沙保弱培養基平板上,置于真菌培養箱內培養,24 h 后讀取平板菌落數,假設菌落數為n,按以下公式計算:肺組織的真菌負荷=n×103CFU/g鼠肺組織,換算為Lg[1]。
1.2.6 小鼠存活情況 每日觀察各組實驗小鼠生存狀態直至感染后第12 天,記錄小鼠存活情況。繪制生存-時間曲線。
1.3 統計學分析 采用SPSS 16.0軟件進行數據處理,計量資料以±s表示,計數資料以百分數及百分比表示。組間計量資料的比較以單因素方差分析,組間資料采用χ2檢驗。
2 結果
2.1 腹腔注射伊曲康唑治療對IPA 小鼠生存率及肺真菌負荷的影響
2.1.1 生存率比較 將腹腔注射治療組與對照組進行比較,見圖2,腹腔注射伊曲康唑可使IPA 小鼠生存獲益,中位生存時間由6 d上升至8 d(P=0.039)。
2.1.2 肺真菌負荷比較 見圖3,對照組肺真菌負荷為5.383±0.196,腹腔注射治療組為4.817±0.154,2組比較差異有統計學意義 (P<0.05)。腹腔注射伊曲康唑可顯著降低實驗小鼠肺組織真菌負荷。
2.2 伊曲康唑霧化預防用藥對IPA 小鼠生存率及肺真菌負荷的影響
2.2.1 生存率 見圖2,霧化伊曲康唑預防性用藥與對照組(感染未治療)比較小鼠生存獲益,中位生存時間由6 d上升至>12 d (P=0.002),但與腹腔注射治療組比較小鼠生存率無明顯提高(P=0.080)。
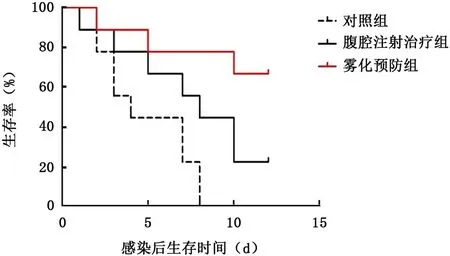
圖2 霧化預防組與腹腔注射治療組及對照組相比對IPA小鼠生存時間的影響
2.2.2 肺真菌負荷 見圖3,腹腔注射治療組肺真菌負荷為4.817±0.154,霧化預防組肺真菌負荷為4.233±0.199,2組比較差異有統計學意義(P<0.05),與腹腔注射治療組比較,霧化伊曲康唑預防性用藥可顯著降低實驗小鼠肺組織真菌負荷。
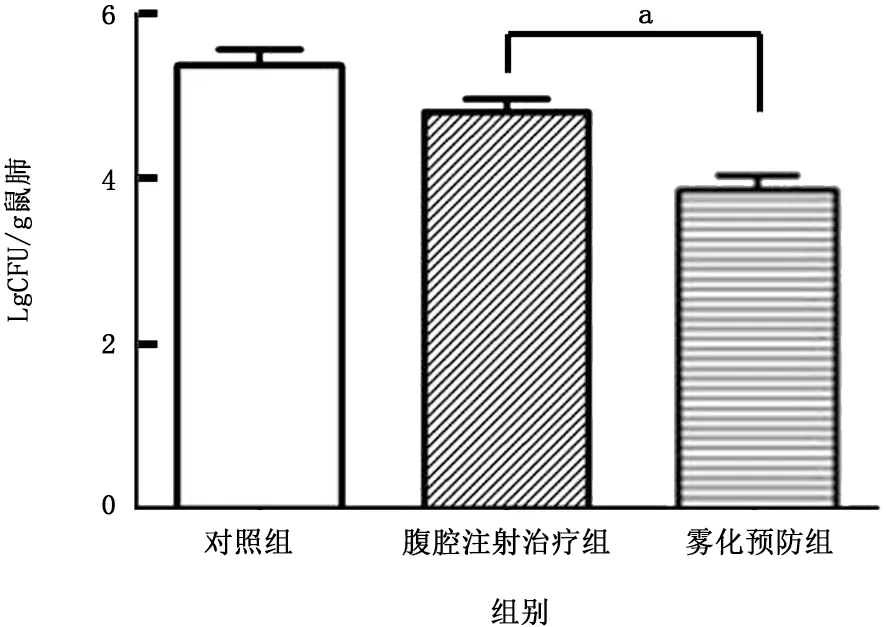
圖3 霧化預防組與腹腔注射治療組相比對IPA 小鼠肺真菌負荷的影響
2.3 伊曲康唑霧化預防及腹腔注射治療聯合應用對IPA 小鼠生存率及肺真菌負荷的影響
2.3.1 生存率 見圖4,聯合防治組與腹腔注射治療組相比較,小鼠生存率提高(P=0.028)。

圖4 聯合防治組與腹腔注射治療組及對照組相比對IPA小鼠生存時間的影響
2.3.2 肺真菌負荷 見圖5,與腹腔注射治療組(4.817±0.154)相比較,聯合防治組 (3.942±0.188)能有效降低小鼠肺真菌負荷 (P=0.005)。
3 討論
真菌感染是腫瘤化療、實體器官及干細胞移植受者等免疫抑制人群較常見的機會性感染之一[2]。盡管不斷有新的抗真菌藥物投入臨床,但IPA 一經診斷往往較難治愈,病死率高達50%~80%,占住院死亡患者總數的4%[3]。針對高危人群IPA的防治逐步為醫師所重視。治療策略也不斷完善,主要包括:預防性治療、經驗性治療、針對性治療和挽救性治療。
抗真菌藥物的霧化吸入給藥最早于1988年提出,為使藥物抵達肺泡內,要求霧化器可將藥液轉化為直徑介于0.5~5μm 的藥物微滴[4]。已有多項體外實驗研究證明利用現有霧化設備所產生的AmB藥物微粒中位直徑 (mean mass aerodynamic diameter,MMAD)在1.31~3.7μm[5-7],伊曲康唑MMAD 在2~3 μm[8-9],米卡芬凈在1.67~2.2μm[10]。國內學者在AmB、氟康唑等抗真菌藥物霧化吸入給藥的臨床研究中雖未涉及MMAD 等霧化效率指標,但良好的臨床效果同樣顯示了應用國產霧化裝置的可行性[11-13]。
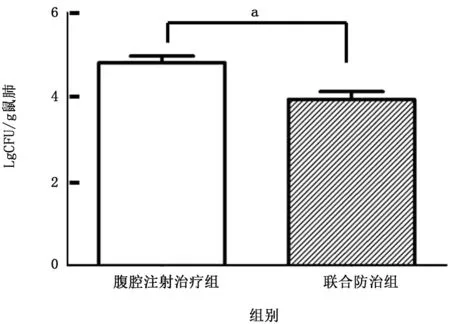
圖5 聯合防治組與腹腔注射治療組相比對IPA 小鼠肺真菌負荷的影響
對多種抗真菌藥物霧化吸入研究均采用注射制劑。藥代動力學研究顯示,動物接受AmB 霧化吸入6周后肺組織藥物濃度依然高達7.7~14.3μg/g濕肺組織[5];有學者報道霧化吸入AmB 后半衰期為1.3~4.5 d,同時血藥濃度維持在0.2 mg/L 以下[14]。霧化吸入伊曲康唑0.5~1 h后肺組織藥物濃度達到峰值,超過11.0μg/g濕肺組織[15-18],藥物半衰期為7 h。另有研究者報道伏立康唑霧化吸入后血藥濃度峰值達到7.1 mg/L[19]。
關于抗真菌藥物霧化吸入防治IPA 療效研究分為動物實驗和臨床研究兩個方面,Am B 霧化吸入已有6項臨床研究數據得到報道,有關Meta分析結果顯示,針對高危人群霧化吸入AmB 能有效預防IPA 的發生[20]。其他抗真菌藥物霧化吸入研究尚局限于動物實驗階段。在探討霧化吸入給藥有效性時往往將“腹腔注射AmB 治療”做為治療真菌感染的金標準,相關研究發現預防性霧化吸入伊曲康唑小鼠生存率明顯高于Am B 腹腔注射治療組[17,21]。但目前Am B 已不作為治療IPA 首選用藥,以此標準僅能初步判斷抗真菌藥物霧化吸入有可行性,難以對伊曲康唑霧化吸入藥效學進行準確評價。本研究將伊曲康唑腹腔注射用藥作為標準,對霧化吸入用藥在預防、治療的藥效學進行綜合評估,并對兩種給藥方式聯合應用進行評價。動物實驗中往往在感染前第2天開始給藥定義為預防性用藥,感染后第2天開始給藥定義為治療性用藥[22]。從生存率及肺部真菌負荷兩個方面加以評價。肺部真菌負荷有兩種檢測方法:平板菌落計數和熒光定量PCR,其中平板菌落計數是經典方法,應用也最為廣泛。
本研究首先觀察了腹腔注射伊曲康唑治療對IPA 小鼠病死率及肺真菌負荷的影響,結果顯示可提高小鼠生存率并降低肺真菌負荷,證明腹腔注射伊曲康唑治療IPA 是有效的。
觀察伊曲康唑不同給藥方式及治療策略的治療效果,研究發現與伊曲康唑腹腔注射治療相比,霧化預防組及聯合防治組可明顯減少實驗小鼠死亡并降低肺真菌負荷,推測在粒細胞缺乏小鼠肺內保持高藥物濃度,可有效抑制進入氣道的曲霉孢子萌發,聯合腹腔注射伊曲康唑達到較高血藥濃度,對侵襲生長的曲霉產生持續作用。
IPA 治療效果差,新藥研制周期長,探索已有藥物新的用藥方式及各種用藥方式聯合應用可能對治療疾病帶來益處。本研究僅對伊曲康唑霧化吸入給藥療效做初步探討,可見伊曲康唑霧化作為高危人群預防性用藥及與系統給藥聯合應用可能具有潛在的應用價值。
利益沖突所有作者均聲明不存在利益沖突

