肺癌立體定向體部放療以靶區為準進行錐形束CT在線配準的可行性研究
孫曉歡,譚麗娜,王中飛,肖鋒
空軍軍醫大學第一附屬醫院放療科,陜西西安710032
前言
立體定向體部放療(StereotacticBody Radiotherapy,SBRT)用于肺癌放療中,腫瘤局控率可以達到80%~90%[1-3],可以達到與手術相當的治療效果,但是肺部腫瘤受呼吸運動、體位固定、皮膚牽拉改變等因素的影響,易造成擺位重復性差等問題,在錐形束CT(Cone Beam CT,CBCT)配準時易導致以骨性標志或外輪廓配準時靶區與計劃圖像中的靶區嚴重偏離;反之,以靶區配準,則骨性標志或外輪廓容易出現嚴重偏離。而SBRT治療方式的特點是治療次數少、單次劑量大、劑量或正常器官超劑量。所以首先要保證的是擺位準確,才能做到劑量精確,否則將造成非常大的誤差。
四維計算機斷層成像(Four-Dimensional Computed Tomography,4DCT)技術的引入為靶區勾畫提供了指導,從一定程度上防止腫瘤脫靶并可以減少正常組織受照劑量。圖像引導放射治療(Image Guide Radiation Therapy,IGRT)技術可以糾正擺位誤差,進而可以縮小計劃靶區(Planning Target Volume,PTV),使得正常組織受量減小[4-7]。針對擺位誤差和腫瘤位移,Wu等[8]利用皮膚標記點、骨性標記和軟組織3種方法分別對圖像進行配準并利用得出的擺位誤差來模擬并對比腫瘤的劑量分布,Miura等[9]也模擬了腫瘤運動給靶區帶來的劑量誤差,此過程僅有腫瘤靶區(Gross Tumor Volume,GTV)移動而照射野并未跟隨腫瘤運動。還有一些研究從固定裝置或呼吸控制方法方面做研究,以期減小靶區運動范圍,另有一些研究從治療過程中動態追蹤靶區方面希望使得靶區始終處于照射范圍內。以上這些研究或是從劑量分布,或是從治療方式上進行研究,都是為了驗證靶區運動對劑量分布的影響,但是這些研究對腫瘤在CBCT配準出現偏差時,并未對不同大小的位置偏差提出如何應對,而本文以腫瘤移位1 cm為界進行研究,驗證腫瘤與骨性標志偏離0.5、1 cm時,以腫瘤作為配準依據,移動治療等中心能否使靶區得到準確的劑量分布。
1 材料與方法
1.1 病例選取
選取2016年6~12月間于空軍軍醫大學第一附屬醫院治療的9例肺癌患者,年齡30~60歲,中位數45歲。
1.2 CT定位及靶區勾畫
使用飛利浦公司Big Bore大孔徑CT模擬定位機對患者行4DCT掃描。患者采用仰臥位,熱塑體模固定,掃描層厚、層距均為5 mm。在Mip圖像上勾畫GTV,并分別與各時相配準核實,最后合并生成內靶區(Internal Target Volume,ITV),再將此ITV外放5 mm生成PTV。
1.3 計劃設計
采用美國瓦里安公司Eclipse 13.5計劃系統,分別為9例患者設計VMAT計劃,處方劑量為60 Gy/10次。采用6 MV X射線,依據腫瘤位置選擇合適的機架起始角度和弧數(3~4弧),劑量率由系統自動控制(瓦里安加速器劑量率為0~600 MU/min可變),計劃采用各向異性分析算法(Anisotropic Analytical Algorithm,AAA)進行計算。靶區劑量分布要求60 Gy需覆蓋95%以上靶區體積(靶區及正常器官受量應滿足RTOG-0915號報告要求)。計劃使用美國瓦里安公司帶有120片多葉準直器(Multi-leaf Collimator,MLC)的iX加速器實施照射。
1.4 模擬腫瘤位移對劑量分布的影響
將每例患者的PTV在原CT圖中向患者右側、背部、腳方向分別移動0.5和1 cm,治療等中心依據腫瘤的位移方向移動0.5 cm、1 cm,重新計算劑量分布,生成6個模擬計劃,再對比原計劃及模擬計劃的劑量分布,圖1所示為將患者的PTV在原CT圖中向患者右側、背部、腳方向分別移動1 cm,圖2為患者按照原計劃劑量分布及將PTV向患者右側移動1 cm后劑量分布。
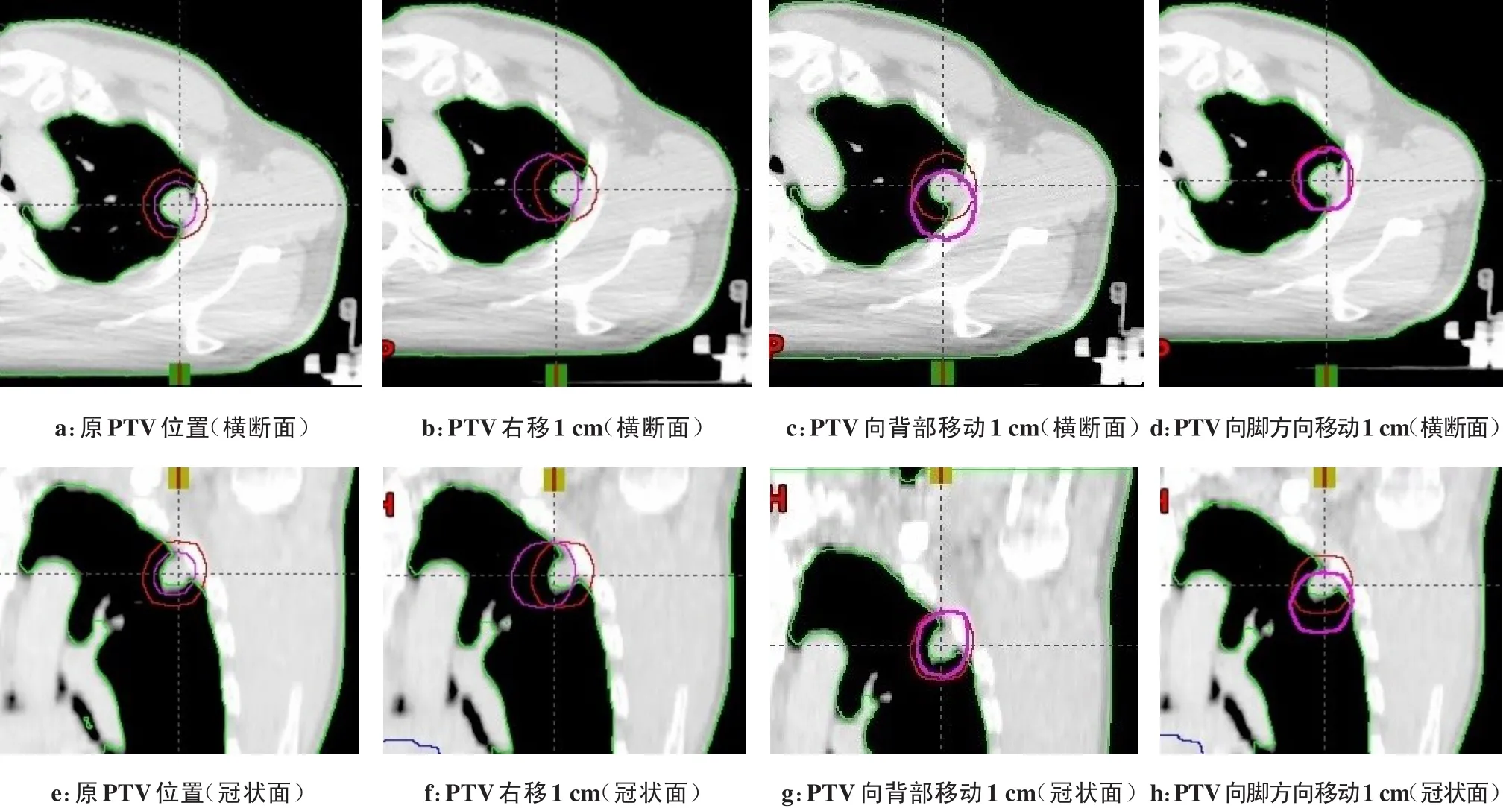
圖1 計劃靶區向患者右側、背部、腳方向移動1 cmFig.1 Planning target volume(PTV)shifted to the right,back and feet by 1 cm
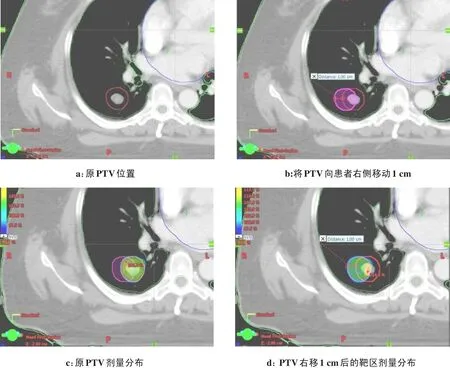
圖2 計劃靶區向患者右側偏移1 cm后劑量分布Fig.2 Dose distribution after PTV shifted to the right by 1 cm
1.5 統計學分析
采用SPSS 18.0統計軟件,對原計劃及模擬計劃的靶區和危及器官受照劑量進行符號秩檢驗,P<0.05為差異有統計學意義。
2 結果
表1為患者的腫瘤分布特點,表2為原計劃及模擬計劃靶區的Dmax,Dmin,Dmean(以相對處方劑量的百分數表示)及V60比較,表3為原計劃及模擬計劃的脊髓與全肺的受量比較。
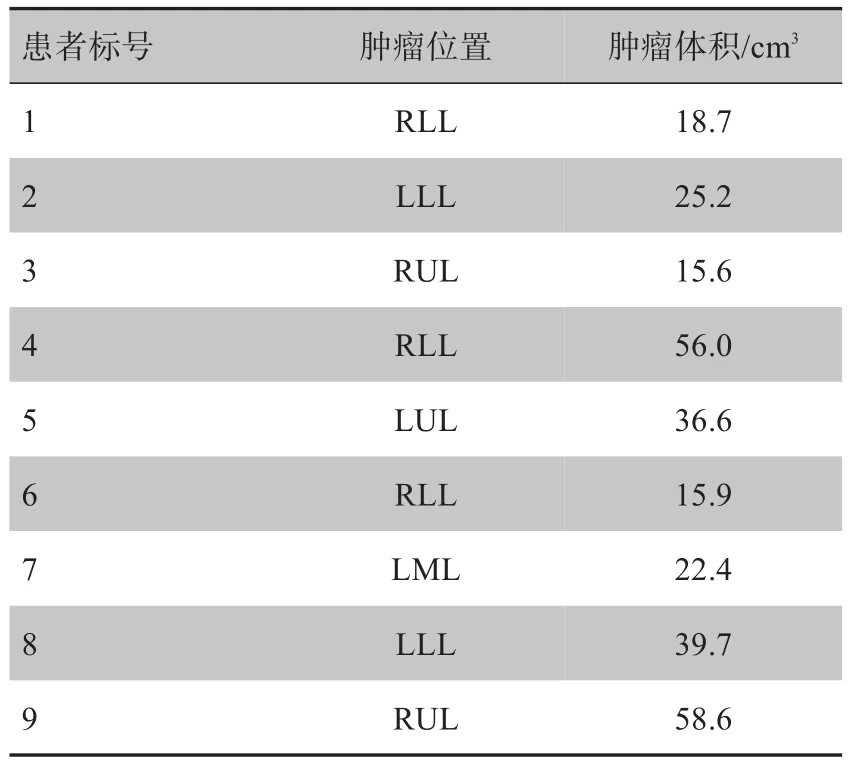
表1 患者的腫瘤分布特點Tab.1 Characteristics of tumor distributions in patients
從表2可以看出,靶區向患者右側移動1 cm、背部移動0.5和1 cm、腳方向移動0.5和1 cm后,Dmax較原計劃差異均具有統計學差異(P<0.05),向腳方向移動0.5 cm后Dmin與V60(60 Gy劑量包繞的靶區體積)較原計劃也具有統計學差異(P<0.05),但是結果仍然滿足RTOG0915號報告的要求。
從表3可知,當靶區向患者背部移動0.5和1.0 cm時,脊髓受量與原計劃差異具有統計學意義(P<0.05),靶區向患者腳方向移動0.5和1.0 cm時,全肺V20和Dmean與原計劃差異具有統計學意義(P<0.05),但這些結果均滿足RTOG0915號報告的要求。
3 討論
在目前的治療過程中,對于治療前CBCT與原CT圖的配準方法主要有3種:皮膚標記點、骨性標記和軟組織配準。許多人也做了不同的研究來驗證各個方法的準確性[10],結果均類似,均認為骨性標志配準與軟組織配準得出的結果差異較大,且利用骨性標記配準更容易導致靶區脫靶,但這些研究并未從劑量學分布上的影響來驗證各個方法的優劣。Wu等[8]用劑量分布的差異來驗證3種配準方法的優劣,實驗得出的結論為軟組織配準方法對劑量分布的影響要小于骨性標記配準方法及皮膚標記點配準方法。而在Miura等[9]也針對GTV偏移做了研究,但其只是模擬了GTV位移,并未將治療中心隨著GTV移動,故其得出的結論為腫瘤移位對GTV及PTV劑量分布影響較大。而本文在以前面的研究結論作為基礎,即以靶區作為CBCT配準依據,并直接給出了1 cm的運動范圍限制,計算靶區偏離在0.5及1.0 cm時,移動治療床進行劑量對比,選擇1.0 cm作為界限是因為若靶區配準后誤差范圍大于1 cm,筆者認為應該重新擺位。

表2 原計劃及模擬計劃的靶區參數比較(%)Tab.2 Comparison of dosimetric parameters of PTV between original plan and PTV-shift plan(%)
上述文獻中的研究均使用固定野調強技術來進行計劃設計,因為射野數目有限,劑量分布會相應的受到影響,而本文采用了VMAT技術,固定野調強技術與VMAT技術相比有一定的劣勢,如文獻[11]中研究結果證明,對計劃實施過程中出現的偏差,如MLC位置,機架角度等的偏差,VMAT受到的影響要小于固定野調強技術,另有文獻[12]中報道,對于前列腺病人的治療,VMAT受治療過程中病人外輪廓的變化的影響要小于固定野調強技術。所以,本文雖然將PTV移動了位置,其相對外輪廓、肺、脊髓等的位置與原計劃有差異,但最終的模擬結果是,PTV和正常組織的劑量分布均能滿足劑量分布要求,所以從本文的結果可以得出,對于肺部較小的病灶,在線CBCT配準時,本文建議可以直接利用可見腫瘤進行配準,若誤差小于1 cm,直接移動治療床并進行治療,腫瘤最終接受到的劑量與原計劃無明顯差異,利用這種配準方式才能保證病人接受到的劑量是準確的。
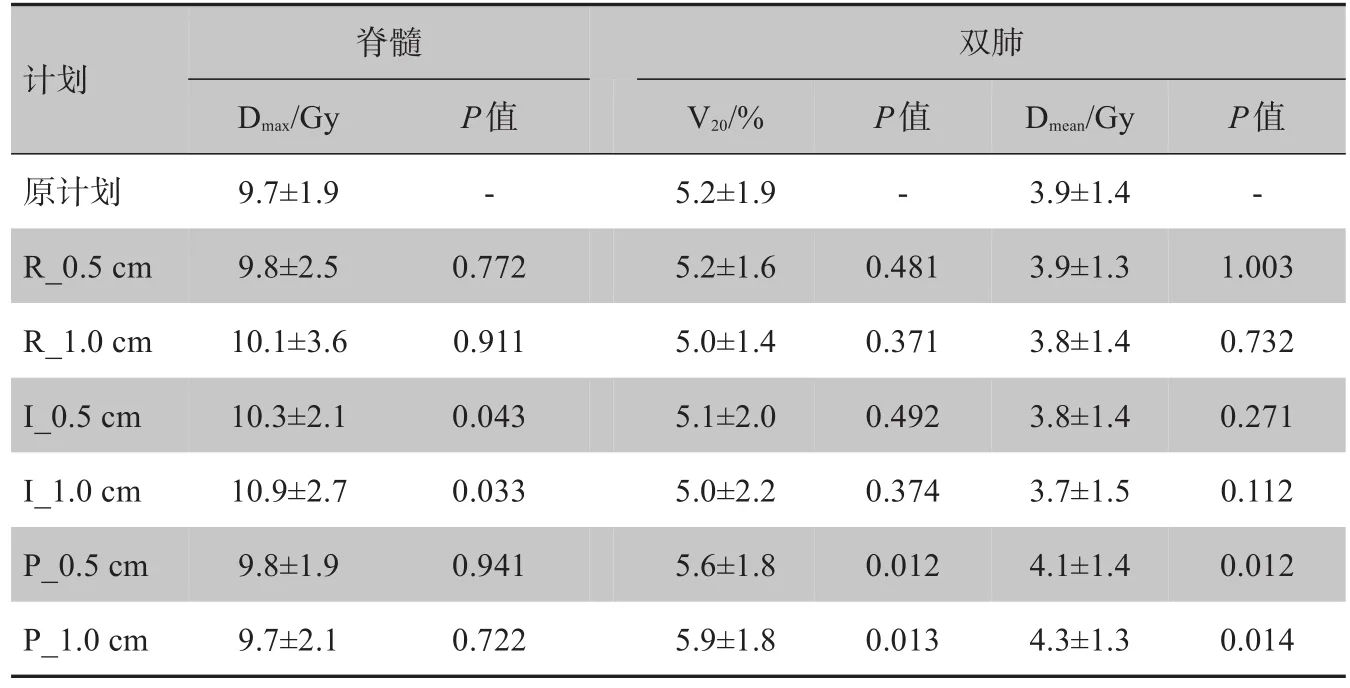
表3 原計劃及模擬計劃的危及器官受量比較Tab.3 Dosimetric comparison of organs-at-risk between original plan and PTV-shift plan

