食管癌調強計劃中鎢門鎖定和鎢門跟隨技術劑量學比較
陳艷,黃宇亮,吳昊,賈冬,賈霖,韓建軍,李晨光,張藝寶
1.綿陽市第三人民醫院/四川省精神衛生中心,四川綿陽621000;2.北京大學腫瘤醫院暨北京市腫瘤防治研究所放療科/惡性腫瘤發病機制及轉化研究教育部重點實驗室,北京100142
前言
多葉準直器(Multi-Leaf Collimators,MLC)是實現調強放療的關鍵設備[1]。作為瓦里安加速器的第三級準直系統,MLC的透漏率隨射線能量的不同可達0.9%~7.0%[2-3],但如果配合鎢門使用則可將透漏率降低至0.1%以下[4]。Wu等[5]和Feng等[6]分別報道了利用鎢門跟隨技術(Jaw Tracking)在容積調強(Volumetric Arc Therapy,VMAT)和固定野調強(Intensity-Modulated Radiation Therapy,IMRT)中有效降低MLC透漏劑量的應用。Chen等[7]的研究卻發現,鎢門鎖定(Fixed Jaw)有時能夠更好地保護腹盆部的危及器官。相對于腹盆部的放射性器官損傷風險,低劑量導致的放射性肺炎在臨床上更為常見。作為通過放療計劃預測和防范放射性肺炎的主要劑量學指標,肺平均劑量(Dmean)[8-9]、劑量高于 5 Gy 和20 Gy的肺體積(V5Gy和V20Gy)等[10],均對MLC透漏線十分敏感。鎢門鎖定技術在相關部位的研究報道尚顯不足。
本工作基于食管癌IMRT技術,研究比較鎢門鎖定和鎢門跟隨技術在靶區劑量覆蓋和危及器官保護方面的劑量學優劣,以期為臨床決策提供數據和方法參考。
1 材料與方法
1.1 病例選擇
回顧性選取2017年1月~2018年3月在綿陽市第三人民醫院放射治療中心接受固定野調強放療的48例患者放療計劃數據,男43人,女5人,TNM分期Ⅳ期(均有鎖骨上轉移),患者其他基本情況統計如表1所示。

表1 入組的48例食管癌患者基本情況統計Tab.1 Clinical data of 48 patients with esophageal cancer
其中,臨床靶區(Clinical Target Volume,CTV)涵蓋瘤床及相應淋巴引流區,包括下頸、鎖骨上、氣管食管旁、中上縱膈(2、4、5、7區),下界至隆突下3 cm,若病灶或吻合口位于胸中下段,則下界位于瘤床下緣3.0 cm,胸下段食管癌包括上腹部胃左動脈區域淋巴結。計劃靶區(Planning Target Volume,PTV)為CTV外放0.5~0.8 cm[11-12]。
1.2 計劃設計和優化目標
考慮到靶區和危及器官相對位置特點,所有計劃均采用7個固定野設計:第1、3、4、5、7 5個野的機架分別取160°、40°、0°、320°、200°,除第4野(0°)為保護心臟覆蓋部分靶區外,其余射野大小均與靶區適形;而第2、6野為降低肺受量,則只關注下頸和鎖骨上部分區域,機架角度分別為70°和290°,如圖1所示。準直器旋轉角度以MLC運動幅度范圍最小為標準進行個體化調整。在鎢門鎖定計劃(Fixed)組,7個射野的鎢門均鎖定;鎢門跟隨計劃(Tracking)組中,只有第2和第6野鎖定(否則射野會過大),其余5野均選擇跟隨。除了鎢門設置外,兩組計劃的其他布野條件、優化參數等均一致。計劃設計均在瓦里安Eclipse 10.0系統上,基于Clinac-ix加速器6 MV光子、Millennium 120 MLC完成。IMRT優化算法和劑量體積算法分別采用DVO-100282和AAA-100282。
所有的病例處方劑量均為:95%的PTV體積在28次治療中接受不低于50.4 Gy劑量。各計劃在計算完畢后先以此標準進行歸一,以便在足夠的靶區覆蓋前提下進行危及器官受量比較。優化目標分別為:雙肺 V20Gy<30%(最好<25%),V5Gy<65%(最好<60%);心臟V30Gy<40%、V40Gy<30%,并盡量降低平均劑量;脊髓最大劑量點Dmax<40 Gy;全局熱點盡量保持在110%以內(即55.44 Gy),若確有困難則盡量將熱點控制在靶區范圍并避開重要危及器官[13]。處理熱點的方法包括:將等劑量線轉化為輔助結構并賦予高權重壓制熱點,手工修改主要貢獻野的通量圖等[14]。為確保鎖定組計劃最終可以滿足臨床要求,在其他優化條件不變的情況下,對其進行熱點處理,成為修改(Modified)組。
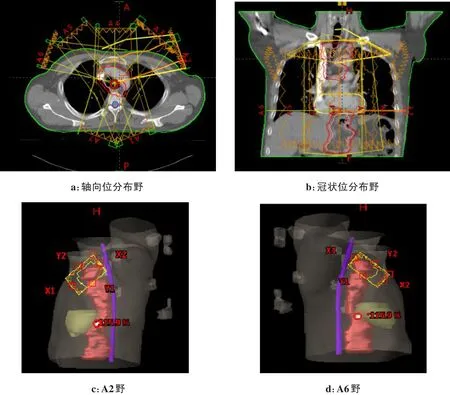
圖1 典型食管癌患者的布野示意圖Fig.1 Beam geometry in a patient with esophageal cancer
1.3 劑量學分析和比較
為避免手工獲取劑量-體積參數可能發生的錯誤并提高分析效率,本工作采用自動提取方法[15]。所有計劃的表格式DVH數據(DVH in tabular format)以0.10 Gy的間隔導出,用自編程序從中批量讀取靶區體積(用于填寫表2中的部分數據),脊髓Dmax,全局Dmax,心臟 V30Gy、V40Gy、Dmean,雙肺 V5Gy、V20Gy和 Dmean,適形度指數和均勻性指數[16-17]等。基于同樣數據,編寫程序為Fixed組和Tracking組分別計算30例患者的平均DVH值并用SigmaPlot 10.0軟件(Systat Software,Inc.,San Jose,CA)繪制成圖進行比較。
1.4 統計學方法
基于SPSS 21.0軟件,對于符合正態分布的數據采用配對t檢驗,不符合的則采用Wilcoxon秩和檢驗。正態分布檢驗方法為Shapiro-Wilk法。設P<0.05為結果有統計學差異。
2 結果
2.1 劑量學參數統計
表2展示了48例患者在優化條件和布野角度相同、僅僅改變鎢門準直器設置的情況下,Tracking組、Fixed組和Modified組計劃的劑量學參數統計結果。
表2 不同鎢門設置組48例食管癌患者固定野調強計劃的劑量學參數比較(±s)Tab.2 Dosimetric comparison of intensity-modulated radiotherapy(IMRT)with different jaw settings for esophageal cancers in 48 patients(Mean±SD)

表2 不同鎢門設置組48例食管癌患者固定野調強計劃的劑量學參數比較(±s)Tab.2 Dosimetric comparison of intensity-modulated radiotherapy(IMRT)with different jaw settings for esophageal cancers in 48 patients(Mean±SD)
*Tracking組vs Modified組,?表示數據符合正態分布,檢驗方法為配對t檢驗;其余的檢驗方法為Wilcoxon秩和檢驗。
參數脊髓Dmax/Gy心臟Tracking組36.42±0.68Fixed組36.63±0.91Modified組35.72±1.25 P值*<0.001?<0.001 V30 Gy/%V40 Gy/%Dmean/Gy 23.68±18.09 9.51±7.67 16.93±10.19 23.52±18.10 9.33±7.52 16.63±10.10 21.86±16.61 9.32±7.44 16.52±9.96<0.001 0.046<0.001適形度指數1.27±0.091.32±0.111.30±0.09<0.001?<0.001<0.001<0.001<0.001?
2.2 平均DVH圖比較
為更加直觀展示3種鎢門設置方法對于食管癌IMRT計劃的劑量學影響,圖2繪制了48例患者的平均DVH圖,其中,斷線、實線和點線分別代表了Tracking組、Fixed組和Modified組。
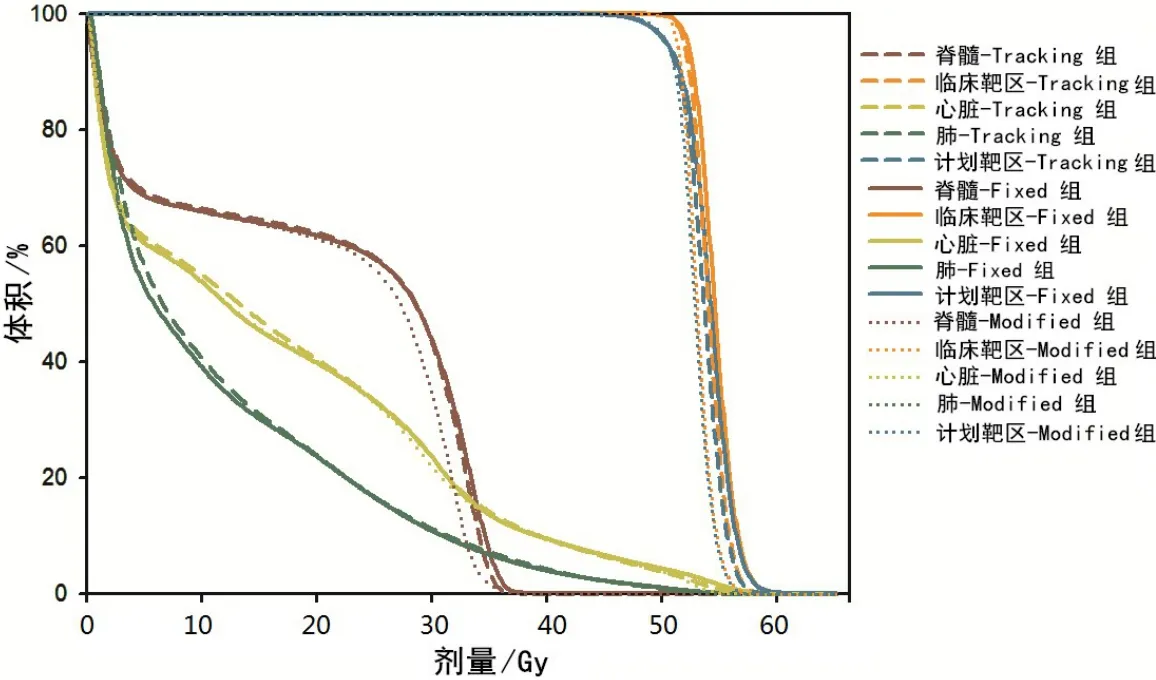
圖2 不同鎢門設置條件下48例食管癌患者IMRT計劃的平均DVH圖Fig.2 Mean dose-volume histogram of IMRT plans optimized with different jaw settings for 48 esophageal cancer patients
3 討論
如表2所示,相較于Tracking組,Fixed組能夠更好地保護心臟和肺組織。其中,心臟的V30Gy、V40Gy、Dmean分別平均降低了0.16%(0.68%)、0.18%(1.89%)、0.30 Gy(1.77%);而肺的 V5Gy、V20Gy、Dmean則分別平均降低了 3.88%(6.84%)、0.36%(1.50%)、0.49 Gy(4.06%)。適形度指數和均勻性指數均值的變化幅度均不大,分別為0.05和0.01。然而作為代價,Fixed組脊髓的Dmax和全局熱點分別增加了0.21 Gy(0.58%)和1.27 Gy(2.14%),但是可以在后續的熱點處理過程中得到解決(Modified組),由于IMRT的射野角度有限性導致其產生熱點難以避免,依賴人工后處理進行降低或消除的做法是臨床的常規手段。在保持Fixed組計劃其他條件不變的情況下,消除熱點后得到的Modified組脊髓Dmax和全局熱點均顯著低于 Tracking組(P<0.001),降幅分別為 0.70 Gy(1.92%)和1.41 Gy(2.38%)。其原因可能是全局熱點經常分布在脊柱旁,在人工對其進行后處理的同時,脊髓的Dmax也會得到一定程度的降低,如圖3示例。與此同時,Modified組在心臟和肺保護方面得到了很好的保持,心臟 V30Gy、V40Gy、Dmean;肺 V5Gy、V20Gy、Dmean等降幅分別為1.82%(7.69%)、0.19%(2.00%)、0.41 Gy(2.42%);3.72%(6.56%)、0.32%(1.33%)、0.45 Gy(3.73%),差異均具有統計學意義(P<0.05)。其中,心臟V30Gy、V40Gy、Dmean等參數的降幅進一步增大,降幅進一步降低的程度分別為7.01%、0.11%和0.65%。此外,Modified組因靶區外熱區部分被消除等原因,適形指數與Tracking組的差異進一步縮小。同樣因為熱點控制的原因,靶區的均勻性指數甚至好于Tracking組,且差異均具有統計學意義。

圖3 Modified組患者在處理熱點的同時壓低了脊髓DmaxFig.3 Spinal cord Dmaxin a patient from Modified group was reduced when processing the hotspot.
由于歸一的原因,圖2所示3組計劃的平均CTV和PTV曲線均能夠滿足處方要求。其中,Modified組在靶區劑量跌落和脊髓劑量等方面優勢明顯,而心臟和肺與Fixed組相當,且均明顯好于Tracking組。上述觀察均與表2提示的數據相符。
表2和圖2均證明了鎢門鎖定技術在特殊情況下比鎢門跟隨技術更能夠有效保護心臟、肺等重要器官。其原因可能是,雖然鎢門跟隨技術可以降低閉合MLC的透漏線,但受到優化算法的限制,MLC形成的射野形狀可能過大。利用鎢門鎖定技術適當限制某些射野的大小,利用主準直器遮擋重要危及器官能夠降低重要敏感器官的低劑量區,使其得到更好地保護。
4 結論
在設計食管癌固定野調強放療計劃時,合理使用鎢門鎖定技術遮擋重要危及器官,結合對熱點必要的人工后處理,可以取得比鎢門跟隨技術更好的劑量學效果,在保證靶區劑量覆蓋的情況下,可以顯著降低肺、脊髓和心臟等劑量,應在臨床實踐中予以充分考慮。

