基于整合藥理學的黃芪-三七藥對干預ARDS的分子機制研究*
梁 旭 李 雁 李 昕
(北京中醫藥大學東直門醫院,北京 100700)
急性呼吸窘迫綜合征(ARDS)是臨床常見的急危重癥,是由多種病因如感染、創傷等導致的以進行性呼吸困難、頑固性低氧血癥和肺組織水腫為主要特征的臨床綜合征[1]。ARDS的治療目前以保護性機械通氣、限制性液體管理等支持治療和控制原發病為主,臨床上多采用糖皮質激素、一氧化氮吸入、肺表面活性物質及對癥治療,但均無可靠的循證醫學證據。藥物等如β2受體激動劑、他汀類藥物和角質形成細胞生長因子雖在動物實驗中取得了一定療效,但并未獲得滿意的臨床效果,且可能出現較嚴重的臨床副作用[2-4]。Meta分析研究表明,中西醫結合治療ARDS在降低病死率等方面優勢明顯,中藥復方具有多靶點治療疾病的特點,相比單一的阻滯劑可能具有更好的臨床優勢,對ARDS的防治具有廣闊的應用前景[5]。
根據臨床表現,ARDS可歸屬于中醫 “暴喘”“肺衰”等范疇。中醫學認為肺氣虛損,毒瘀互阻,進而導致肺氣衰敗是ARDS的關鍵病機[6]。目前,關于中醫藥治療ARDS的報道甚少,課題組在前期工作中采用國家級名老中醫杜懷棠教授經驗方——益氣化瘀解毒方,以扶正祛邪為原則,從益氣、化瘀、解毒等方面對ARDS模型大鼠進行預防治療,結果發現益氣化瘀解毒方可顯著減輕肺組織損傷程度,并可減低炎癥因子及關鍵炎癥蛋白的表達水平,但具體的作用機制尚未完全闡明[7-9]。
整合藥理學平臺(TCMIP,http://www.tcmip.cn/)是整合了中藥成分、中藥材、中藥方劑、疾病/癥狀靶標等數據的中醫藥資源信息開源數據庫平臺,通過建立“中藥方劑-化學成分-作用靶標-疾病靶標”的多維網絡關聯,構建“中藥-成分-靶標-通路”復雜網絡,為中藥復方的作用機制研究提供了新思路[10]。本研究基于整合藥理學原理,對課題組前期有效方益氣化瘀解毒方中的益氣化瘀藥對——“黃芪-三七”進行研究,構建其干預ARDS作用機制的分子網絡,為深入研究該復方治療ARDS的機理和進一步闡述ARDS的發病機制提供科學依據。
1 數據來源與方法
1.1 “黃芪-三七”化學成分收集 TCMIP中藥材數據庫依據《中國藥典》(2015年版),收錄了400余味常用中藥材信息[10]。在其中藥信息設定界面對“黃芪”“三七”進行檢索并收集其所有化學成分,建立“黃芪-三七”藥對化學成分信息數據庫。
1.2 ARDS疾病候選靶標收集 在整合藥理學平臺疾病靶標信息數據檢索界面,以急性呼吸窘迫綜合征的英文縮寫“ARDS”作為關鍵詞進行檢索,可收集到疾病靶標數據庫中目前已知的ARDS治療靶點,作為“黃芪-三七”藥對的候選治療靶標。
1.3 靶標預測 TCMIP平臺利用Open Babel軟件對中藥成分進行二維結構相似性檢索,通過在中藥靶標預測界面選取相似性分數≥0.8的所有藥物靶標作為“黃芪-三七”藥對的潛在作用靶標,建立藥物候選靶標信息數據庫[11]。
1.4 蛋白質-蛋白質相互作用信息(PPI) TCMIP整合了 HAPPI、InAct、HPRD、Reactome、OPHID、MINT,PDZ Base,DIP等數據庫中蛋白質-蛋白質相互作用信息。通過該平臺的PPI數據庫,可獲得“黃芪-三七”藥對作用的潛在靶標與ARDS疾病靶標之間的PPI。
1.5 網絡構建與分析 通過網絡分析,計算“黃芪-三七”藥對潛在靶標與治療ARDS的疾病靶標之間的PPI信息網絡特征值,以節點連接度(degree)的2倍中位數為卡值,選取中藥靶標-疾病靶標互作網絡的核心節點;在此基礎上,以節點連接度、節點緊密度和節點介度的中位數為卡值,選取同時滿足3個卡值的節點為“黃芪-三七”藥對潛在靶標-ARDS疾病靶標相互作用網絡的關鍵節點[12]。通過基因功能和通路的富集分析,挖掘分析“黃芪-三七”藥對治療ARDS關鍵網絡靶標及其對應的活性成分,并構建 “中藥-核心成分-關鍵靶標-主要通路”的可視化網絡圖,進一步明確中藥干預疾病的作用機制。
1.6 關鍵靶標分析及通路富集 TCMIP整合基因本體數據庫 GO(http://www.gene ontology.org/)和 KEGG通路數據庫(http://www.kegg.jp)資源,可直接提取靶標基因或蛋白質的分子功能、細胞內定位及其所參與的生物學反應和通路,對“黃芪-三七”藥對干預ARDS的關鍵作用靶標進行基因功能分析和通路富集分析,并將GO和KEGG計算分析的結果以P值降序的方式排列顯示。
2 結 果
2.1 “黃芪-三七”藥對化學成分靶標預測及分析 通過TCMIP數據庫共收集得到黃芪化合物成分29個,主要為黃芪皂苷類和黃芪多糖類;三七化合物成分95個,主要為三七皂苷、人參皂苷、西洋參皂苷和氨基酸類。研究表明,黃芪甲苷Ⅳ抑制脂多糖(LPS)處理的小鼠中的NF-κB激活和炎性基因表達[13];黃芪多糖通過阻斷NF-κB活化抑制TNF-α處理的人血管內皮細胞中ICAM-1和VCAM-1的表達[14];三七中的人參皂苷Rb1可通過減少ICAM-1和ICAM-1基因的表達,改善肺微血管內皮細胞間連接,減輕肺損傷[15]。針對上述成分,共預測出黃芪的潛在作用靶標1 273個,三七的潛在作用靶標626個,經相似性分數≥0.8篩選后,得到黃芪預測靶標185個,三七預測靶標86個,二者共有的靶標71個,提示黃芪和三七在共性靶標之間存在潛在的疊加作用。
對“黃芪-三七”藥對候選靶標進行基因分析,取P值排名前20得到候選靶標具有的基因功能信息見表1,可見其功能涉及鈉離子通道復合體、突觸后膜電位的調節、細胞線粒體功能、電壓門控鈉通道活性、離子跨膜轉運調控、動作電位下的膜去極化、神經元動作電位、心肌細胞膜去極化的調節、肉堿代謝過程、痛覺感覺等條目。對“黃芪-三七”候選靶標進行通路富集分析,取P值排名前20得到候選靶標參與的通路信息見表2,可見涉及通路主要有循環系統、神經系統、PPAR信號通路、內分泌系統、過氧化物酶體、脂質代謝、心肌細胞腎上腺素能信號轉導、輔助因子和維生素的代謝、脂肪酸代謝、甘油磷脂代謝、半乳糖代謝、α-亞麻酸代謝等。
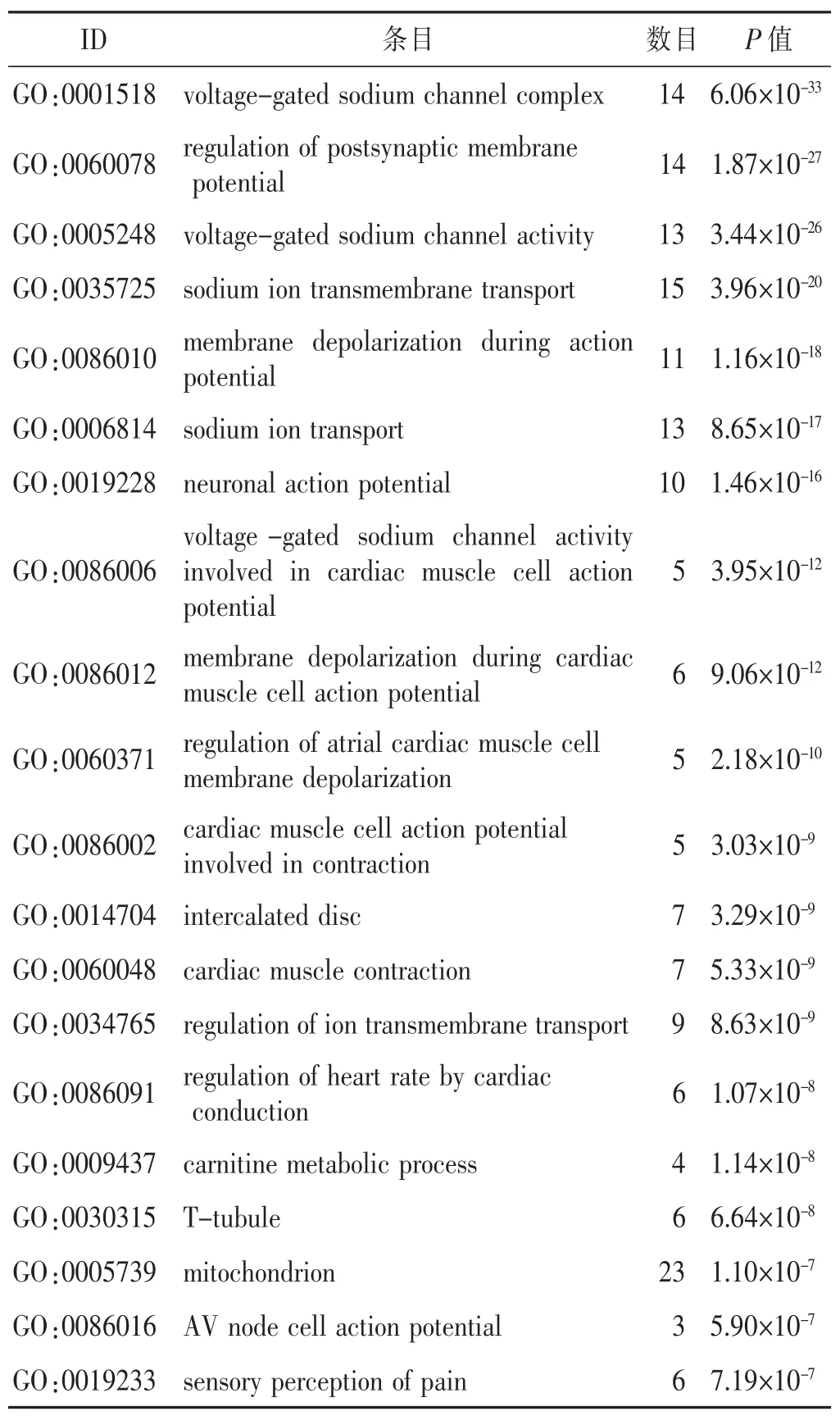
表1 “黃芪-三七”藥對候選靶標具有的功能信息
2.2 “黃芪-三七”藥對治療ARDS的核心靶標網絡通過TCMIP的PPI相互作用數據庫,構建 “黃芪-三七”藥對的潛在靶標與疾病靶標相互作用網絡。根據條件篩選出關鍵靶標655個,根據degree排序僅顯示排名前100的靶點,得到“黃芪-三七”治療ARDS的候選靶標網絡,見圖1。圖中節點的大小與degree成正比關系,其中已知治療ARDS的直接靶標78個,潛在藥物靶標3個,共同靶標2個。根據比較網絡中每條邊的介度值,發現TSC1、NSDHL、PIK3R1等靶標的節點介度值更大,在網絡中發揮的作用也更大。
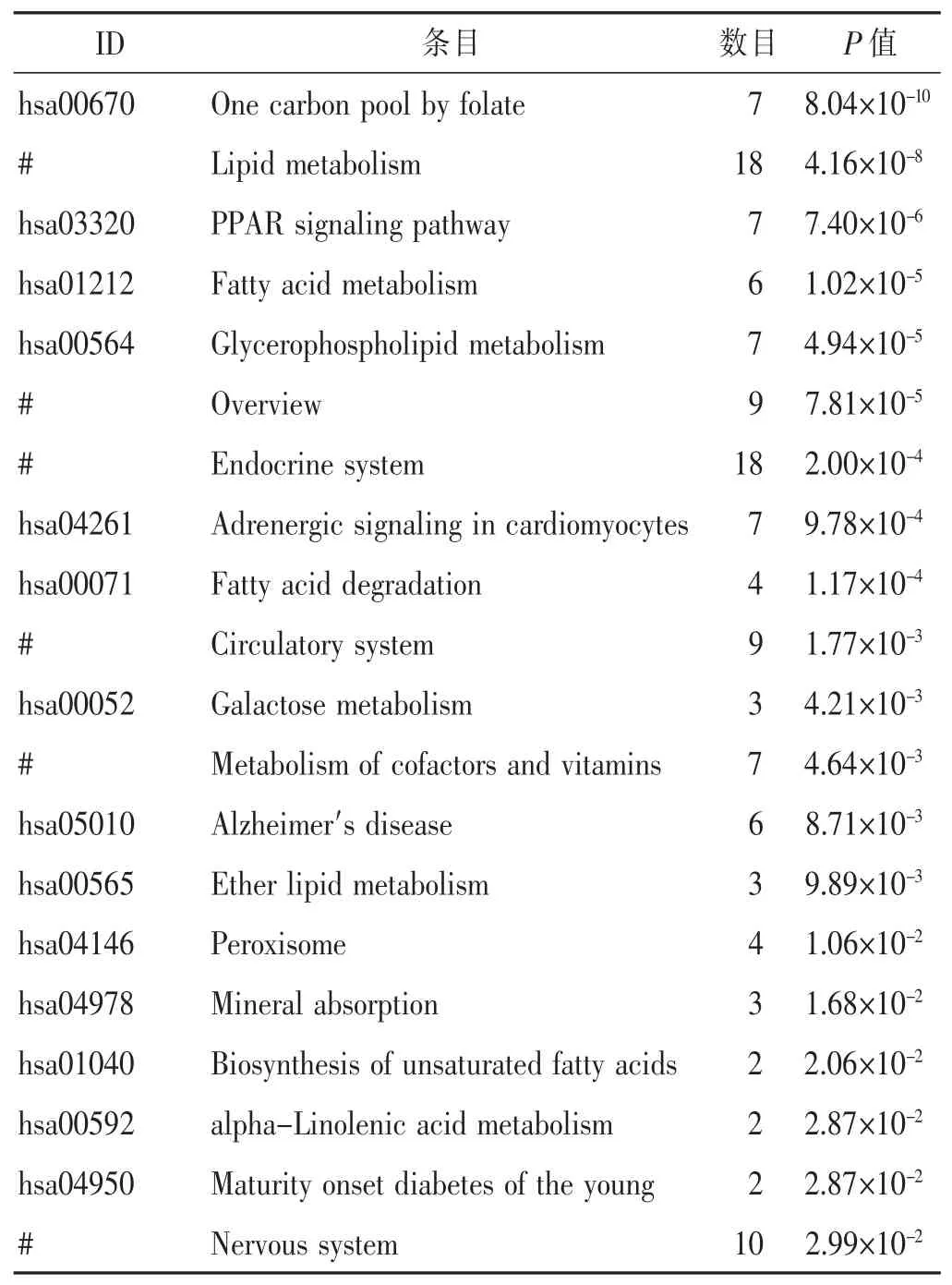
表2 “黃芪-三七”藥對候選靶標參與的通路信息

圖1 “黃芪-三七”藥對干預ARDS的候選靶標網絡
以上關鍵靶標中,部分已知疾病靶標如:前列腺素G/H合成酶2(PTGS2)主要與炎癥反應的調節、一氧化氮生物合成過程的正調節、NF-κB進入細胞核的正向調節、對腫瘤壞死因子的反應、炎癥細胞遷移的正調節、血管內皮生長因子生成的正調控、血小板衍生生長因子產生的正調節、細胞對流體剪切應力的反應、細胞對缺氧的反應、細胞周期的負向調控;絲氨酸/蘇氨酸-蛋白激酶A-Raf(ARAF)功能涉及ATP結合、蛋白激酶活性、受體信號傳導蛋白質活性、金屬離子結合等;絲氨酸/蘇氨酸蛋白磷酸酶PP1-γ催化亞基(PPP1CC)與有絲分裂細胞周期、轉化生長因子β受體信號通路、小GTP酶介導的信號轉導、蛋白質去磷酸化、細胞分裂、三酰甘油分解代謝過程相關。潛在藥物靶標:鈉/鉀轉運ATP酶亞基α-1(ATP1A1)功能主要與ATP結合、磷酸酶活性、鈉鉀離子結合相關;過氧化物酶體肉毒堿O-辛酰基轉移酶 (CROT)功能主要涉及脂肪酸β-氧化、細胞脂質代謝過程、輔酶A代謝過程產生前體代謝物和能量等;肉堿O-棕櫚酰轉移酶1(CPT1A),主要與細胞脂質代謝、蛋白質同源寡聚化、脂肪酸β-氧化、上皮細胞分化等功能相關。共同靶標2個:葡萄糖激酶(GCK),功能主要涉及ATP結合及葡萄糖的結合;絲氨酸/蘇氨酸蛋白激酶D1(YWHAE),功能主要與離子通道結合、蛋白質活性、MHCⅡ類蛋白質復合物結合、酶結合、RNA結合、ATP結合、蛋白激酶C活性等相關。
ARDS的發病機制較為復雜,其肺損傷過程涉及多個病理環節的不同分子作用過程。上述靶標涉及諸多生理病理分子機制,主要與炎癥反應的調節、血管內皮生長因子調節、蛋白質相互作用及代謝、細胞生長和死亡、信號因子的正負調節等相關,這不僅說明了ARDS的發病機制復雜,同時說明“黃芪-三七”藥對干預ARDS的作用主要是通過對炎癥反應-血管內皮功能-細胞生長及死亡的多靶點、網絡狀的綜合調控而實現。
2.3 “黃芪-三七”藥對治療ARDS關鍵靶標的GO基因功能分析 “黃芪-三七”藥物靶標與疾病靶標基因功能主要涉及細胞質代謝、蛋白質結合、細胞核核質、血小板活化、ATP結合、蛋白質磷酸化、轉錄模板DNA的正向調控、蛋白絲氨酸/蘇氨酸激酶活性、RNA聚合酶Ⅱ啟動子轉錄的正向調控、蛋白激酶結合及活性、有絲分裂細胞周期的G2/M轉換、凋亡過程的負調控、肽基絲氨酸磷酸化等,見表3。
2.4 “黃芪-三七”藥對治療ARDS的KEGG通路富集分析 根據P值排序僅顯示排名前20的KEGG通路,見表4。通路富集分析結果顯示,“黃芪-三七”藥對治療ARDS的主要作用通路有細胞生長與死亡、ErbB信號通路、FoxO信號轉導通路、神經營養因子信號轉導通路、細胞間通訊、癌癥信號通路、細胞周期、內分泌系統、胰腺癌、傳染性疾病、甲狀腺激素信號通路、前列腺癌、HTLV-Ⅰ感染等。

表3 “黃芪-三七”藥對治療ARDS關鍵靶標基因信息功能分析
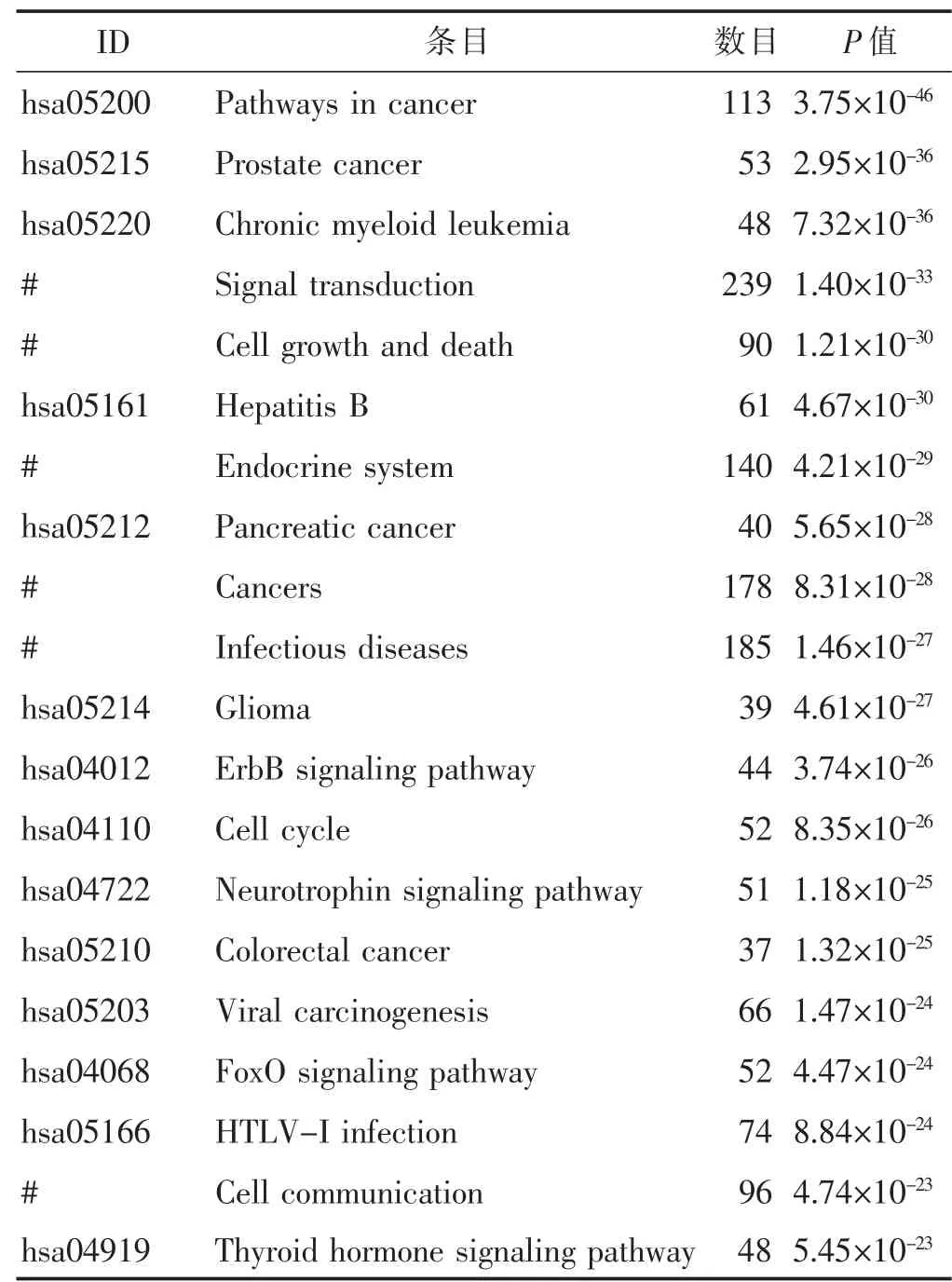
表4 “黃芪-三七”藥對治療ARDS關鍵靶標通路信息
2.5 “黃芪-三七”藥對治療ARDS的“中藥-成分-靶標-通路”多維網絡分析 如圖2。通過TCMIP數據庫分析可以看出,“黃芪-三七”藥對治療ARDS作用主要與52個化學成分相關聯,其中黃芪成分17個,三七成分34個,共有成分1個。黃芪成分以黃芪皂苷和黃芪苷為主,如黃芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ、Ⅶ等;三七主要成分以三七皂苷為主, 如三七皂苷 A、B、C、D、E、F、G、H、R1、R4,人參皂苷 Rc、Rg1,西洋參皂苷Ⅰ、Ⅲ、Ⅳ等。共有成分為十六烷酸(棕櫚酸)。
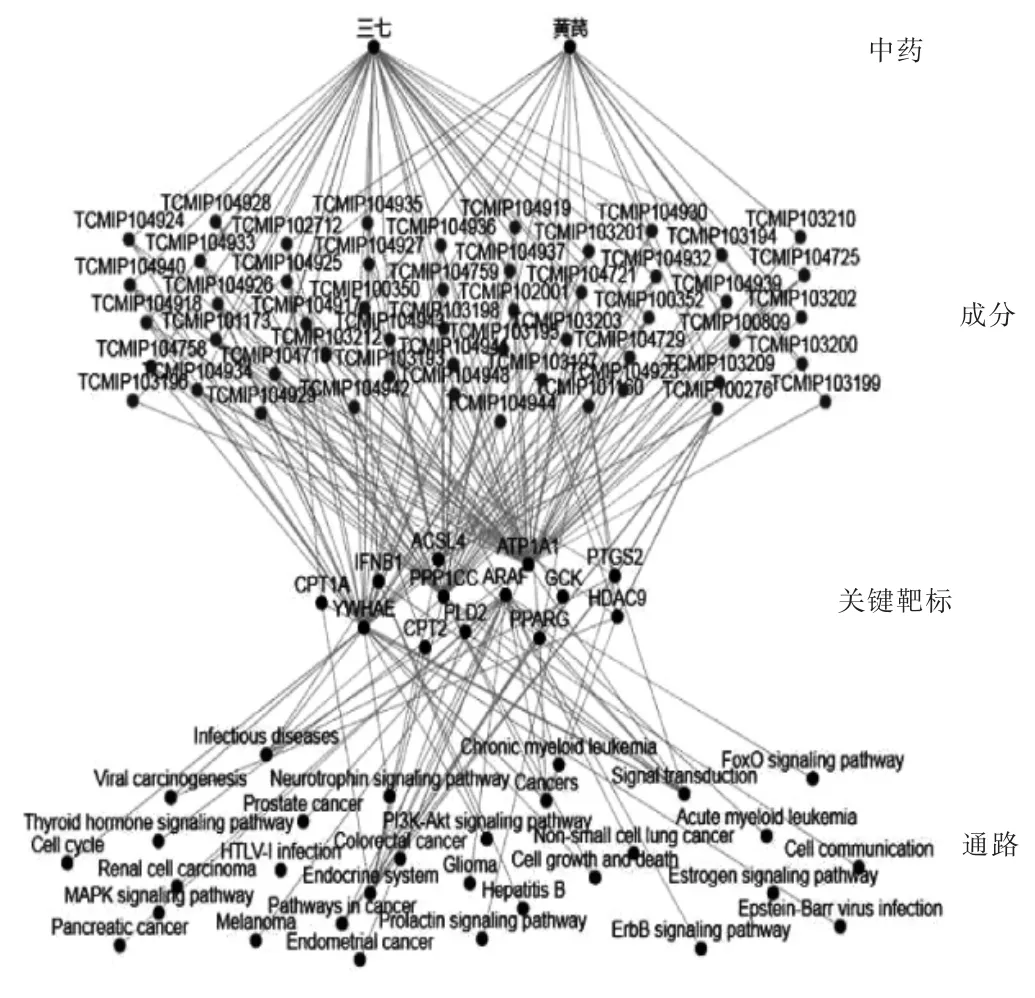
圖2 “黃芪-三七”藥對干預ARDS“中藥-成分-靶標-通路”多維網絡分析
其中,黃芪皂苷、三七皂苷、人參皂苷均已通過實驗證實具備減輕急性肺損傷(ALI)的藥理作用。張吉等發現黃芪甲苷可能通過抑制GRP78和CHOP蛋白表達調控內質網應激狀態,改善急性肺損傷狀態[16];趙建軍等觀察到黃芪甲苷能上調LPS致ALI大鼠肺水通道蛋白5的表達從而減輕LPS致ALI大鼠肺炎癥損傷反應[17];徐旭等發現黃芪皂苷可顯著延長電刺激大鼠頸總動脈形成血栓的時間,并能抑制血小板聚集,提高前列環素和一氧化氮(NO)水平,降低血栓素A2/前列環素比例,從而抗血栓形成[18];劉永琦、李金田等發現黃芪皂苷調節Th1/Th2型細胞因子的平衡及TNF-α含量可能是其抗肺纖維化的機理之一[19];陳宇清等發現,三七總皂苷可以明顯降低ALI大鼠的血清和BALF中的TNF-α、IL-6及-IL-10水平,有助于減緩或阻止ALI向ARDS發展[20]。人參皂苷具有擴張血管、改善微循環、抑制血小板的聚集,促進血管內皮細胞功能的恢復,調節血管活性物質,抗氧化、改善微循環、清除氧自由基、誘導細胞凋亡、抗組織損傷、抗腫瘤等藥理作用[21]。鞏秀麗研究發現,人參皂苷液可減緩ALI大鼠的呼吸窘迫程度,改善肺通氣和減輕肺水腫,通過抑制大鼠肺組織中 SP-A蛋白和SP-B蛋白含量的降低來治療 ALI[22]。
“黃芪-三七”藥對作用于ARDS的相關通路主要有MAPK信號通路、PI3K-Akt信號通路、ErbB信號通路、FoxO信號轉導通路、細胞生長及死亡、非小細胞型肺癌、細胞循環、細胞通訊、內分泌系統、神經營養因子信號通路、感染性疾病、HTLV-1感染、結直腸癌、胰腺癌、甲狀腺激素信號通路、雌激素信號通路等。
其中絲裂原活化蛋白激酶(MAPK)信號通路與各種細胞功能相關,包括細胞增殖,分化和遷移[23]。正常表達的MAPK相關蛋白分子包括細胞外信號相關激酶 (ERK)、Jun 氨基末端激酶 (JK1/2/3)、p38 蛋白和ERK5,IL-8可通過MAPK和PI3K信號通路誘發細胞趨化作用所需的黏附分子如整合蛋白MAC-1的表達。MAPK通路及PI3K通路亦可通過G蛋白等分子相聯通[24]。
磷脂酰肌醇3′-激酶(PI3K)-Akt信號傳導通路可被多種類型的細胞刺激或毒性損傷激活,主要與細胞轉錄、翻譯、增殖、生長和存活等相關,參與細胞凋亡、蛋白質合成與代謝等細胞周期過程[25]。
ErbB受體酪氨酸激酶(RTK)家族將細胞外生長因子配體與細胞內信號通路結合,調節多種生物反應,包括增殖、分化、細胞運動和存活[26]。RTK家族成員之一表皮生長因子受體(EGFR,也稱為ErbB-1或HER1),可誘導受體同源二聚體和異二聚體的形成以及內在激酶結構域的激活,進而誘導各種信號傳導途徑[27]。MAPK途徑是所有ErbB受體下游的共同靶標,同時PI3K途徑可被大多數ErbB直接或間接激活。
FoxO信號轉導通路參與調節細胞生理過程中特定基因的表達,包括細胞凋亡,細胞周期控制,葡萄糖代謝,抗氧化應激等[28]。FoxO蛋白的中心調節機制與胰島素、生長因子及PI3K下游的絲氨酸-蘇氨酸激酶Akt/蛋白激酶 B(Akt/PKB)的磷酸化相關[29]。
以上信號通路之間通過ERK、Akt等關鍵蛋白相互聯系溝通,形成了ARDS發病過程中的復雜分子通路,通過對 “中藥-成分-靶標-通路”多維網絡分析,發現“黃芪-三七”藥對成分在干預ARDS病程進展中發揮了重要作用,其調控炎癥反應、抗細胞凋亡及保護肺血管內皮細胞的分子機制與課題組前期實驗結果具有很高的吻合度[7-9]。
3 結 論
網絡藥理學注重整體性和動態性的特點,與中藥復方注重多組分配伍、多靶點干預及系統調控的思想不謀而合[30]。TCMIP結合大數據和模型計算,應用人工智能、數據挖掘、網絡科學構建了智能化和網絡化平臺,為中藥復方及經方藥對的研究提供了新思路和新方法。
益氣化瘀解毒方在防治ARDS的前期動物實驗中作用明顯,“黃芪-三七”作為益氣化瘀核心藥對作用突出,本研究通過網絡藥理學研究技術,發現“黃芪-三七”藥對主要活性成分可針對多個靶點、多條通路發揮干預ARDS的作用,其作用可能與 TSC1、NSDHL、PIK3R1等關鍵靶標及MAPK信號通路、PI3K-Akt信號通路、ErbB信號通路、FoxO信號轉導通路等有關,這些靶點及通路與文獻報道的急性肺損傷的發病機制及課題組的前期研究成果多有吻合。本研究是基于網絡藥理學原理的綜合數據分析,具體機制及物質基礎還將通過實驗加以驗證,望本研究能夠為復方核心藥對的進一步研究及ARDS的臨床治療提供參考。本研究表明,“黃芪-三七”藥對可通過多靶點、多途徑干預ARDS,為其進一步的藥效物質基礎分析和防治作用機制研究提供了依據。

