啤酒中微生物的衛生檢查與結果分析
◎ 陳光申
(武漢輕工大學生物與制藥工程學院,湖北 武漢 430023)
啤酒是世界上消費量最大的酒類飲料,全球啤酒產量連續多年保持增長;啤酒作為一種含二氧化碳的、起泡的、低酒精度發酵酒,在全球倍受歡迎。目前,我國是世界上最大的飲料酒生產和消費國,酒類品種繁多,釀造歷史悠久,是世界上產業規模最大的國家之一[1]。中國是全球啤酒市場中人均消費量增長最快的國家。2002年,中國啤酒總產量達2 386.83萬t,位居世界第一,并連續16年蟬聯。2013年,中國啤酒企業年總產量為5 061.54萬t,同比增長4.59%[2]。隨著啤酒行業的發展,消費者對啤酒質量的要求提高,在制作與銷售過程中的啤酒質量控制極為關鍵,作為食品監測中的一項,對啤酒微生物進行檢查與分析具有重要意義。
1 材料與方法[3-5]
1.1 材料
成品熟啤(市場在售啤酒隨機取樣)、無菌培養皿(Φ90 mm)、無菌吸管(1 mL、10 mL)、無菌生理鹽水、無菌試管、酒精燈、開瓶器、無菌紗布、無菌三角瓶、平板計數瓊脂培養基以及煌綠乳糖膽鹽(BGLB),雙料月桂基硫酸鹽胰蛋白胨肉湯(LST),1 mol·L-1NaOH,1 mol·L-1HCl,單料月桂基硫酸鹽胰蛋白胨肉湯(LST),pH試紙,接種環,超凈工作臺及電爐(微波爐)等。
1.2 樣品的采取與預處理
瓶裝啤酒采用原包裝樣品,取原包裝兩瓶;用滅菌容器采取500 mL散裝樣品,放入滅菌磨口瓶中。
在對啤酒取樣時,將瓶蓋部分浸入75%的乙醇1 min后用火灼燒,用石炭酸紗布蓋好,再用滅菌開瓶器啟開,由于啤酒含二氧化碳,可倒500 mL滅菌磨口瓶中,口勿蓋緊;覆蓋滅菌布,輕輕搖蕩5 min,待氣體全部逸出后,進行檢驗。散裝酒類,可直接吸取檢驗。
使用無菌1 mol·L-1NaOH調節樣品酒pH至6.5~7.5。
1.3 菌落總數的測定
啤酒中菌落總數測定常用有2種測定方法:平板菌落計數法和菌落總數PetrifilmTM。
①測試片法。平板菌落計數是將啤酒經過一系列處理后進行計數。②菌落總數PetrifilmTM法則是將啤酒樣液滴入含有培養基和指示劑的紙片上進行培養,紙片大多是滅菌濾紙、纖維膜、膠膜等,不同的培養基配置原料、方法、消毒滅菌過程等會影響PetrifilmTM的效果。
1.3.1 樣品的稀釋
①采用無菌操作吸取25 mL預處理后的啤酒樣品,放置于裝有225 mL無菌生理鹽水的滅菌錐形瓶內,振蕩,混合成1∶10的均勻樣品稀釋液。②無菌操作吸取1 mL 1∶10稀釋液,注入含有9 mL無菌生理鹽水的無菌試管內,振蕩,混合成1∶100的均勻樣品稀釋液。③同上,制備10倍系列稀釋樣品勻液。每遞增稀釋1次,換用1支1 mL無菌吸管。
1.3.2 樣品的處理
取稀釋后的樣品均液和空白稀釋液(不含啤酒樣品的無菌生理鹽水)各1 mL,注入無菌平皿中,每個稀釋度做兩個平皿。配制好的平板計數瓊脂培養基(PCA)冷卻到46 ℃后,注入平皿中約15 mL,并轉動平皿,混合均勻。空白稀釋液的無菌平皿做空白對照。
為使菌落均勻的分布在平板上,均勻樣品稀釋液加入平皿后,應盡快傾注培養基并且旋轉混合均勻,可以正反兩個方向旋轉,從開始稀釋到傾注最后一個平皿所用時間不宜超過20 min,以防止細菌死亡或繁殖。
1.3.3 培養
待瓊脂凝固后,翻轉平板,將其放置在(36±1)℃條件下培養(48±2)h。
1.3.4 菌落計數
培養規定時間后,立即計數。可以用肉眼觀察,必要時用放大鏡或菌落計數器檢查,以防止遺漏。記錄各平板的菌落總數,求出菌落總數。
1.3.5 菌落總數的計算方法
(1)若只有一個稀釋度平板上的菌落數在適宜計數范圍內(30~300 CFU),計算兩個平板菌落數的平均值,再將平均值乘以相應稀釋倍數,作為每克(毫升)樣品中菌落總數結果。
(2)若有兩個連續稀釋度平板上的菌落數在適宜計數范圍內時,按公式(1)計算:
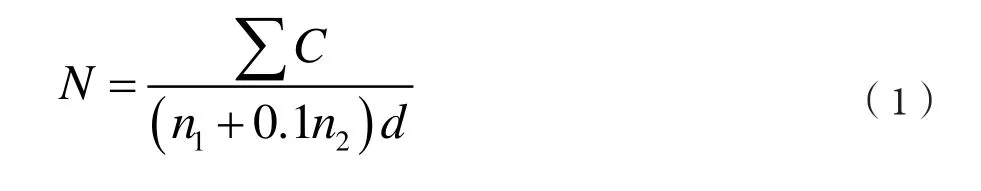
式(1)中:N—樣品中菌落數;∑C—平板(含適宜范圍菌落數的平板)菌落數之和;n1—第一個適宜稀釋度的平板數;n2—第二個適宜稀釋度的平板數;d—稀釋因子(第一稀釋度)。
1.3.6 結果報告
若空白平皿中沒有菌落,并且兩個平行平皿中菌落數相近,則菌落總數為兩平皿中的菌落平均數;若空白平皿中有菌落或兩平行平皿中的菌落總數相差太大,則該實驗需要重做。
1.4 大腸菌群的測定
1.4.1 樣品的稀釋
同1.3.1,但從制備樣品均液至樣品接種完畢全程應15 min內。
1.4.2 初發酵與復發酵試驗
第一步是初發酵,培養基是月桂基硫酸鹽胰蛋白胨肉湯(LST)。每個樣品需接種9個裝有小倒管的培養基試管。其中3個試管是雙料管,其余6個是單料管。取10 mL預處理樣品接種在3個雙料管和單料管中。經過(36±1)℃培養(24±2)h后,觀察發酵管中的小倒管中是否有氣泡產生,如未產氣則繼續培養至(48±2)h,記錄24 h和48 h內產氣的LST肉湯管數。都未產氣者,可直接判定該樣品的大腸菌群為陰性。產氣者需進行復發酵。其操作是:用接種環從所有(48±2)h內發酵產氣的LST肉湯管中取培養物1環,移種于煌綠乳糖膽鹽肉湯培養基(BGLB)復發酵管中,再經(36±1)℃培養(48±2)h后,觀察產氣情況。產氣者,計為大腸菌群陽性管。
1.4.3 大腸桿菌計數
初發酵未產氣者,可直接判定為大腸桿菌陰性,復發酵產氣者,計為大腸桿菌陽性,根據大腸菌群陽性管數和接種量,查大腸菌群檢索MPN表,報告每克(或毫升)該樣品中大腸菌群的MPN值。
2 結果與分析
啤酒的微生物部分衛生要求[6]如表1。

表1 啤酒的微生物要求表
其中,菌落總數指的是啤酒經過處理,1 mL啤酒在平板計數瓊脂培養基上在(36±1)℃條件下培養(48±2)h后,生長出來的微生物菌落總數。
菌落總數作為判定食品被污染程度的標志,也可以用這一方法觀察細菌在啤酒中繁殖的動態,以便對啤酒樣品進行衛生學評價時提供依據。
本檢測中的大腸桿菌指在(36±1)℃培養(48±2)h能發酵乳糖、產酸、產氣、需氧和兼性厭氧的革蘭氏陰性無芽孢桿菌。大腸菌群的數量以每100 mL啤酒中最可能數來表示。
由于大腸菌群直接或間接來源于人以及溫血動物的糞便。大腸菌群在啤酒的衛生檢查中有2方面的意義。①受糞便污染的指標菌。用來衡量啤酒生產過程中的操作衛生狀況。②可作為腸道致病菌污染啤酒的指示菌。大腸菌群數量越大,啤酒中腸道致病菌存在的可能性越大。
對啤酒樣品菌落總數重復測定10次,并對每個樣品做兩個平行測定,菌落總數、大腸桿菌測定結果如表2、表3。
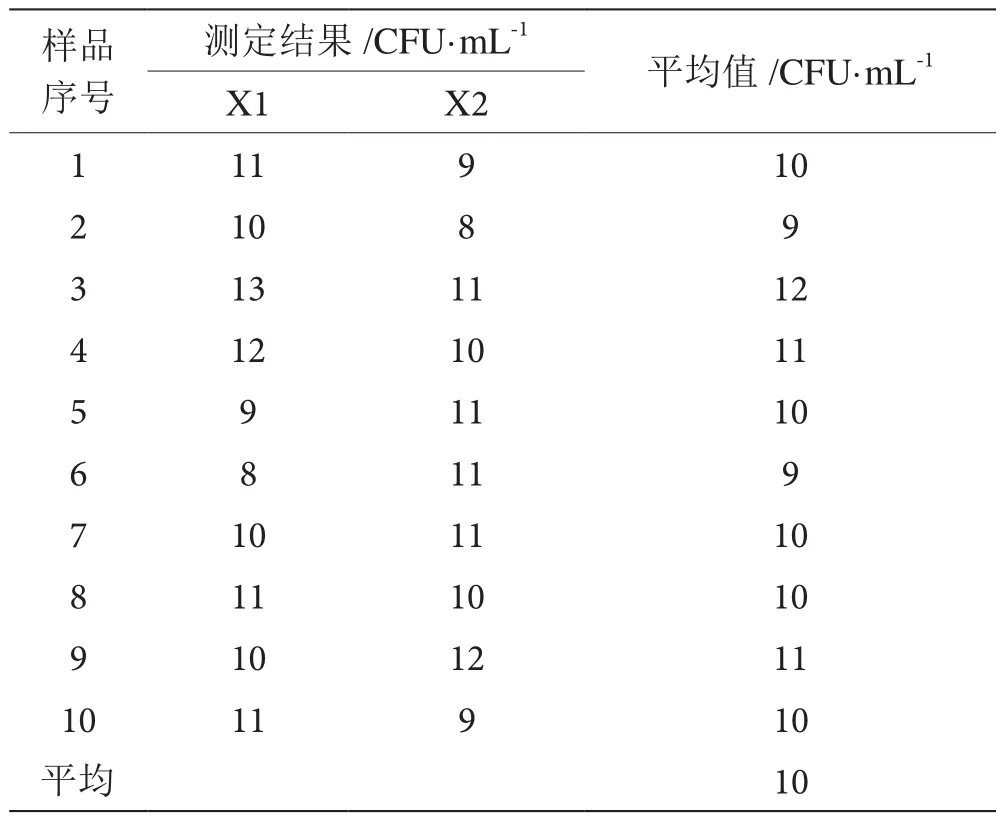
表2 樣品中菌落測定結果表
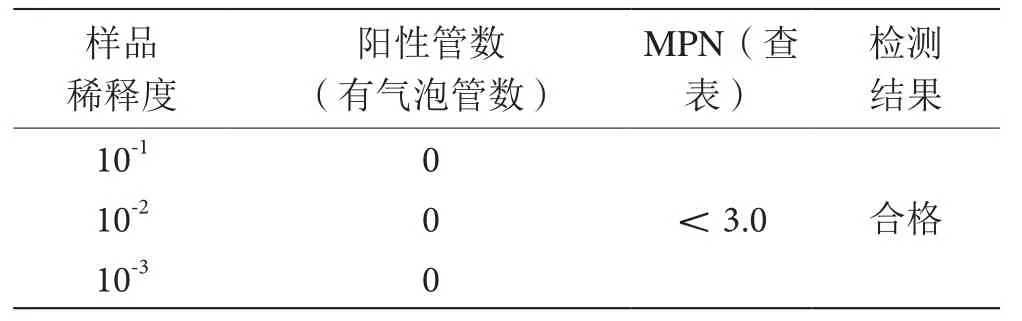
表3 大腸桿菌測定結果表
對比國家標準可以看出,該批次啤酒樣品微生物衛生檢查結果為合格。
3 討論
啤酒作為人們社會生活中主要的酒類消費品之一,其質量與安全不僅影響著生產企業的利益,更關乎消費者的身體健康。就要求啤酒生產企業嚴格按照國家標準對啤酒進行微生物衛生檢查;在生產過程中,要有明確的衛生控制與詳細的微生物檢驗標準。總之,只有徹底消除啤酒中有害微生物或將有害微生物數量控制在一定范圍內,才能生產出高質量的、符合消費者需求的、產品穩定性強的啤酒。因此,對啤酒中微生物的檢測與分析,具有十分重要的意義。

