胸腺肽α1聯合化療對晚期結直腸癌患者免疫功能的影響
劉 杰 徐建林
(南京中醫藥大學附屬鹽城市中醫院腫瘤科,江蘇 鹽城 224000)
結直腸癌是世界范圍內高發生率腫瘤疾病,在晚期結直腸癌的治療中,以化療為主的綜合治療方案已成為臨床共識[1]。奧沙利鉑聯合卡培他濱(XELOX方案)是晚期結直腸癌化療的主要方案,具有療效確切及不良反應少等優點。但晚期結直腸癌患者的自身免疫能力較差,加之化療本身對正常組織細胞具有一定殺傷性,部分患者往往難以耐受而中止化療或生活質量降低。胸腺肽α1是一種非特異性免疫增強劑,在化療過程中配合使用有輔助治療作用。本研究進一步探討了胸腺肽α1聯合XELOX方案對晚期結直腸癌患者免疫功能的影響。
1 資料與方法
1.1 臨床資料。研究對象:我院2015年5月至2017年5月收治的62例晚期結直腸癌患者;分組:用隨機數字表法分為觀察組(31例)與對照組(31例)。
1.2 納入標準:①符合結直腸癌診斷標準Ⅳ期的患者;②35歲≤年齡≤75歲;③治療前>1個月未接受相關治療;④預計生存期≥3個月;⑤Karnofsky評分≥60分和(或)體力狀況評分(ECOG)分級為0~2分;(6)簽知情同意書。
1.3 排除標準:①對本研究用藥過敏者;②合并嚴重肝、腎臟器功能障礙者;③合并有嚴重心臟病和(或)腦血管疾病者;④精神異常和(或)有嚴重精神疾病既往史者;⑤伴嚴重感染者;⑥妊娠期婦女、哺乳期婦女。
1.4 方法:對照組患者予以XELOX方案治療,即奧沙利鉑注射液靜脈滴注3 h,劑量為130 mg/m2,d1;卡培他濱,1000 mg/(m2·d),分2次口服,服用2周。化療前3天常規予以格拉司瓊、維生素B1、維生素B6、還原型谷胱甘肽等予以止嘔、保肝及防治外周神經炎。3周為化療1個周期。觀察組在對照組治療的基礎上,加用胸腺肽α1,1.6毫克/次,每周2次,皮下注射。
1.5 觀察指標:兩組治療前及治療4個周期后進行臨床觀察及評價。①免疫功能:采集空腹靜脈血5 mL經肝素鈉抗凝處理,常規于3000 r/min轉速下離心10 min,留取血漿進行預處理。應用Beckman流式細胞儀測定CD4+Th17、CD4+CD25+Treg以及Th17/Treg細胞比例。②功能狀態:根據KPS評分標準評價功能狀態。③臨床獲益評價:以滿足以下三項中的至少1項且維持≥4周判定為臨床獲益:a.止痛藥物用量或癌痛程度降低≥50%;b.提高KPS評分超過20分;c.體質量提高≥7%。④不良反應評價:按WHO抗癌藥物亞急性不良反應分級標準[3]分級評價(0~Ⅳ級)。
1.6 統計學分析:采用SPSS19.0版統計學軟件分析數據,以均數±標準誤差描述計量資料,比較經t檢驗,以P<0.05為差異有統計學意義。
2 結 果
2.1 兩組治療前后T細胞水平比較:治療后兩組Th17細胞比例、Treg細胞比例、Th17/Treg比值都降低,而且治療組較對照組更低(P<0.05)。見表1。
表1 兩組治療前后T細胞水平比較
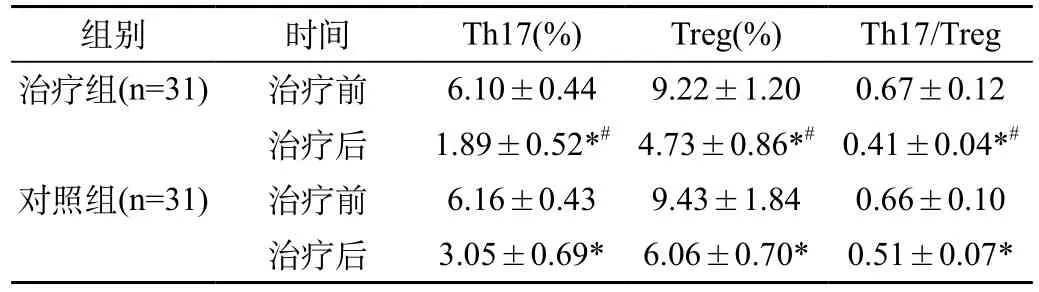
表1 兩組治療前后T細胞水平比較
注:與對照組治療后比較,#P<0.05;與本組治療前比較,*P<0.05
組別 時間 Th17(%) Treg(%) Th17/Treg治療組(n=31) 治療前 6.10±0.44 9.22±1.20 0.67±0.12治療后 1.89±0.52*#4.73±0.86*#0.41±0.04*#對照組(n=31) 治療前 6.16±0.43 9.43±1.84 0.66±0.10治療后 3.05±0.69* 6.06±0.70* 0.51±0.07*
2.2 兩組功能狀態評分比較:兩組治療后KPS評分均提高,且治療組KPS評分提高幅度更大(P<0.05)。見表2。
2.3 兩組綜合受益比較:治療組綜合受益24例(77.42%),對照組21例(67.74%),治療組高于對照組(P<0.05)。
2.4 兩組不良反應比較:兩組的胃腸道反應、骨髓抑制及周圍神經毒性比較沒有差異(P>0.05)。
表2 兩組治療前后KPS評分比較(分)
注:與本組治療前比較,*P<0.05;與對照組治療后比較,#P<0.05
組別 時間 KPS評分治療組(n=31) 治療前 66.33±4.32治療后 82.15±12.02*#對照組(n=31) 治療前 65.44±4.13治療后 76.53±8.90*
3 討 論
在結直腸癌的發生、發展及臨床轉歸中,免疫機制占有重要地位,大部分結直腸癌患者體內存在免疫細胞失衡。CD4+T細胞可以調控機體免疫反應,是腫瘤微環境關鍵細胞,利用不同細胞因子誘導,可以將CD4+T細胞分化為Th1、Th2、Th17和Treg細胞等不同亞型,Th17和Treg細胞在正常機體內數量保持動態平衡[2],而在結直腸癌患者體內發現Th17細胞過度分化,Treg細胞升高,Th17/Treg比值升高,Sfanos KS等還發現結直腸癌淋巴結轉移與Th17細胞比例及Th17/Treg比值升高有一定程度相關性,認為Th17/Treg比例失衡不僅提示結直腸癌患者免疫功能紊亂,并且可能是疾病進展的預測因子之一[2]。張亞軍等認為Th17、Treg細胞在結直腸癌中的表達與腫瘤微環境中的相關細胞因子水平有關[4]。
非特異性免疫增強劑在惡性腫瘤的臨床輔助免疫治療中扮演著重要的角色,臨床效果明確。胸腺肽α1是常用免疫增強劑,能誘導Th細胞表達,調節淋巴組織增值反應,促進抗體產生,促進T細胞反應及NK細胞活動等,抑制某些腫瘤的生長[5]。在我們的觀察中,治療組和對照組治療后Th17%、Treg%、Th17/Treg比值都降低,且治療組較對照組降低幅度更大(P<0.05)。提示胸腺肽α1聯合化療治療晚期結直腸癌時可以進一步保護或改善患者的免疫功能,改善臨床預后。
Imamoto等[6]認為,有效的腫瘤治療并不是要求完全殺滅癌細胞,其關鍵應是機體的反應性,惡性腫瘤患者的臨床轉歸更大程度反映再生存質量等臨床受益指標上。本研究中治療組患者的臨床癥狀評分較對照組明顯改善,綜合受益明顯高于對照組,證明胸腺肽α1輔助XELOX方案治療晚期結直腸癌能夠使患者獲益更大。所以,胸腺肽α1輔助化療可以增強機體免疫及提高臨床受益。

