基于先驗信息的人體肺癌電阻抗層析成像*
李 佳, 岳士弘, 王亞茹
(天津大學 電氣自動化與信息工程學院 自動化系,天津 300072)
0 引 言
醫學電阻抗層析成像(electrical impedance tomography,EIT)是當前生物醫學工程的研究熱點[1]。目前,針對醫學EIT技術的研究包括肺部呼吸成像、乳腺癌診斷、癲癇病灶診斷等[2,3]。在肺癌早期,癌變組織尚未形成結節,傳統的影像技術無法完成準確診斷,且頻繁使用會對人體造成傷害,但電導率(介電常數)已隨組織的病變發生變化,可以利用EIT技術通過對電導率(介電常數)的檢測,完成對早期肺癌的診斷和預警。
EIT技術具有“軟場”效應和不適定性,導致重建圖像分辨率較低,為提高圖像質量,本文根據人體胸腔的計算機斷層掃描(computed tomography,CT)掃描圖片,利用計算機輔助設計(computer-aided design,CAD)軟件構建胸腔器官的結構模型,并結合器官、組織的電導率等先驗信息構建正則化矩陣,引入到擴展Kalman濾波(extended Kalman filtering,EKF)的狀態空間表達式中,完成肺癌組織的圖像重建。
1 算 法
1.1 電阻抗層析成像原理
電阻抗層析運算過程主要分為正問題和逆問題。圖像重建即屬于逆問題的求解。EIT的線性模型為[4]
ΔU=U′(σ0)Δσ=JΔσ
(1)
式中 ΔU為邊界測量電壓變化量,Δσ為電導率變化量,J為Jacobian矩陣。
1.2 建立含有先驗信息的正則化矩陣
對肺部進行圖像重建時,真實的胸腔器官結構信息有利于提高重建圖像精度。因此,根據人體的CT胸腔掃描圖片,利用CAD軟件,對人體胸腔器官組織進行建模,如圖1所示。主要包括心臟、肺、脊髓、脂肪4部分,及其電導率σ(Ω/m)變化范圍[5]。
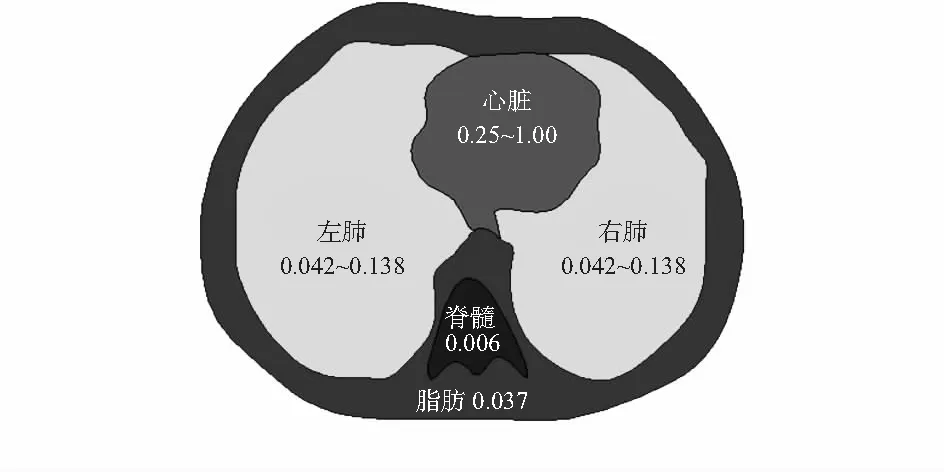
圖1 人體胸腔模型及器官電導率變化范圍
在模型數值變化范圍內隨機取值,構建500個可能的電導率分布向量σn(n=1,2,3,…,500)作為學習集。利用主成分分析(principal component analysis,PCA)法對學習集進行降維處理。將特征值按從大到小順序排列,前5個最大特征值中λ1=3.7570,與其他特征值相差很大,λ1所對應的特征向量w1中已包含了絕大部分胸腔電導率分布的先驗信息。
構建正則化矩陣L,使L的零空間與向量w1張成的子空間Sw相等[6,7],即
L=I-WWT
(2)
式中I為單位向量,W的列向量由特征向量w1構成。
1.3 含先驗信息的EKF算法
EKF方法是一種狀態估計次優方法[8],利用EKF對肺部癌變組織進行圖像重建時,需建立狀態空間模型
σk=Fk/k-1σk+ωk,Uk=Vk(σk)+υk
(3)
式中σk為tk時刻的電導率;Fk/k-1為tk-1~tk時刻的狀態轉移矩陣,一般取單位矩陣;Uk為tk時刻的電壓測量值;Vk為電壓值與電導率的函數關系;ωk與υk分別為tk時刻的系統噪聲和測量噪聲,為0均值、互不相關的白噪聲序列,相應的協方差矩陣分別為Qk,Rk。
對Uk關于初始電導率σ0進行泰勒展開,得線性形式
(4)

EKF基于狀態誤差協方差最小的原則對狀態值進行估計,加入含先驗信息的正則化項后,構建新的代價函數[9]

(5)
式中Pk/k-1為誤差協方差矩陣;σ*為先驗電導率分布;α為正則化參數,通常由經驗獲得;L為正則化矩陣,由式(2)計算得到。
式(5)變形并最小化,得到含先驗信息EKF濾波方程
(6)
2 仿真實驗及結果分析
仿真條件:酷睿i7 3.4 GHz CPU,12 GB內存臺式機。將人體胸腔模型導入Comsol 3.5a軟件中,進行物理條件仿真和有限元剖分,并利用MATLAB R2009a軟件實現正問題的求解和圖像重建。EIT系統共有16個電極,采用相鄰電流激勵、相鄰電壓測量的激勵—測量模式,共獲得208個測量值,胸腔被剖分為1 283個單元。
利用Comsol 3.5a建立3種肺癌模型,如圖2(a),圖中圓表示癌變組織。仿真時,模型中電導率設置心臟0.7,肺0.12,脊髓0.006,脂肪0.037,肺癌組織0.2,同時向電壓測量值中添加均值為0,協方差矩陣R為10-2I208×208的白噪聲,分別采用共軛梯度法(conjugate gradient,CG)、EKF方法和含先驗信息的EKF方法進行圖像重建。EKF和含先驗信息的EKF方法的初值按經驗選取[10],分別為電導率初值取0 Ω/m,誤差協方差矩陣Po初值取5I208×208,另外系統噪聲協方差矩陣Q取10-2I1 283×1 283。CG算法取迭代500次時重建結果,EKF算法和含先驗信息的EKF算法均取迭代兩次時的重建結果,各方法重建圖像如圖2。

圖2 各方法仿真實驗重建圖像
可以看出,對模型1,當癌變組織較少時,三種方法均可較為準確地重建出癌變組織的位置和形狀,其中EKF和含先驗信息的EKF算法的形狀與癌變形狀更為接近。對模型2,CG算法的重建圖像位置開始發生偏移,且形狀也與真實形狀相差較大,而EKF算法和含先驗信息的EKF算法仍可較為準確地重建出癌變組織位置,其中含先驗信息的EKF算法重建圖像偽影更小。對模型3,CG算法已發生嚴重形變,無法分開左肺中的2個癌變組織,但EKF算法和含先驗信息的EKF算法仍可較為準確地重建出癌變組織位置,可以分隔開左肺的2個癌變組織,但右肺的成像也與真實形狀相差較大,比較2種方法,含先驗信息的EKF算法的偽影更小。
為定量比較重建圖像的質量,采用圖像相對誤差e作為評價參數
(7)

經計算3種模型中含先驗信息的EKF方法圖像的相對誤差最小,說明其重建圖像質量最好。其中CG算法與其他2種方法的相對誤差值相差較大,說明CG算法重建圖像質量最差。對模型3,癌變組織較多時,含先驗信息的EKF方法較EKF方法的誤差更小,重建圖像質量更好。
3 結 論
利用人體胸腔器官分布結構和器官組織電導率等先驗信息建立正則化矩陣,并將正則化項引入EKF中,進行肺癌組織的圖像重建。仿真實驗表明:與共軛梯度算法和傳統的EKF算法相比,含先驗信息的EKF算法得到的重建圖像相對誤差更小,圖像質量更好。

