羥考酮與嗎啡在大鼠內臟痛鎮痛效應的差異
郭偉兵,李文君,段 姣,陳春龍,胡玉萍,劉清珍,張利東,李偉彥
0 引 言
疼痛是現代人類健康和社會發展的主要問題之一,困擾全球數以億計的人群。阿片類藥物在治療諸多形式的疼痛過程中應用廣泛。但在肌肉和內臟引起的深部痛的治療過程中發現嗎啡并不能提供充分的鎮痛效應,而且μ受體的中樞神經系統作用會產生很多副作用,如欣快感、呼吸抑制以及惡心等[1]。而羥考酮是一種μ、κ阿片受體激動劑,與單純μ受體激動劑嗎啡的藥理效應不同。臨床上也觀察到羥考酮在治療疼痛中比嗎啡可能具有更強的鎮痛效應,有文獻[2]報道,羥考酮與嗎啡的鎮痛效應在不同組織也不一致,在皮膚和肌肉部位的疼痛,鎮痛效應是等效的,而對在食道部位的熱和機械刺激引起的疼痛,羥考酮則比嗎啡具有更強的鎮痛效果,可能與κ阿片受體有關。而羥考酮在對內臟痛的鎮痛效應中,κ、μ阿片受體各自的占比仍不清楚。因此本文擬探討羥考酮與嗎啡在內臟痛及炎性痛疼痛模型中的鎮痛效應差異,研究羥考酮在不同疼痛模型的鎮痛效應差異中與κ受體的結合能力的關系,并初步探討羥考酮對內臟痛發揮鎮痛效應中的κ、μ阿片受體各自占比。
1 材料與方法
1.1藥品和試劑鹽酸羥考酮注射液(oxycodone,Oxy)由Hamol Limited有限公司生產;鹽酸嗎啡注射液(morphine,Mor)由東北制藥集團沈陽第一制藥有限公司生產;冰醋酸溶液由成都市新都區化工試劑廠生產;甲醛注射液由西隴科學股份有限公司生產;選擇性μ受體拮抗劑naloxonazine購于Sigma公司;選擇性κ受體拮抗劑nor-binhorphimine(Nor-BIN)購于Abcam公司。這6種藥物均用等滲鹽水溶解或稀釋,等滲鹽水由石家莊四藥有限公司生產。
1.2動物雄性Sprague-Dawley(SD)大鼠360只,體重200~250 g,清潔級,由南京軍區總醫院比較醫學科提供,實驗動物生產許可證號:scxk(軍)2012-0014;使用許可證號:syxk(軍)2012-0047。實驗室光照時間6:00-18:00,溫度控制在18~22 ℃,在安靜環境中進行行為學觀察。為減少生物節律對動物行為的影響,實驗時間為每日9:00-12:00,實驗前動物不禁飲食。
1.3實驗方法SD大鼠360只,在實驗開始前均先放入觀察箱中適應30 min。觀察者、指標統計者均不知相應分組情況。
1.3.12%醋酸扭體模型其中156只SD大鼠以腹腔注射化學物質引起的大鼠扭體反應作為內臟痛的實驗模型。隨機均分為13組,分別為內臟痛對照組,羥考酮(0.4、0.64、1.0、1.6、2.6、4.2 mg/kg)組;嗎啡(0.4、0.64、1.0、1.6、2.6、4.2 mg/kg)組。上述藥物均用生理鹽水進行配置,分別將上述藥液經右側腹壁注入腹腔,其中對照組注射等量等滲鹽水。注藥后15 min,將等滲鹽水稀釋的2%冰醋酸以4 mL/kg經另一側腹壁注入腹腔,然后立即放入觀察箱中觀察(開始計時),以腹部內凹伴后肢伸展計為扭體1次,計數每5 min內出現的扭體次數,作為內臟痛程度的定量指標,計算60 min內扭體總數,并根據各組扭體平均次數計算扭體反應的抑制率。根據扭體抑制率分別計算羥考酮及嗎啡在2%醋酸扭體模型中的半數有效量(50% effective dose, ED50)。扭體反應的抑制率計算公式如下:
扭體反應的抑制率=(對照組平均扭體次數-試驗組平均扭體次數)/對照組平均扭體次數×100%
1.3.25%甲醛炎性痛模型將180只SD大鼠以左足底注射5%甲醛作為炎性痛模型,隨機分為15組,分別為炎性痛對照組,羥考酮(0.6、0.96、1.54、2.46、3.9、6.3、10.0 mg/kg)組;嗎啡(0.6、0.96、1.54、2.46、3.9、6.3、10.0 mg/kg)組。甲醛實驗在30 cm×30 cm×30 cm有機玻璃籠中進行,分別將上述藥液經右側腹壁注入腹腔,其中對照組注射等量等滲鹽水。注藥后15 min,參照Zhang等[3]方法,使用30G注射器于大鼠左后爪掌側皮下注射5%甲醛50 uL后立即放入觀察箱中,箱下放置與地面成45°角的鏡子以便觀察。注射后1、5、10、15、20、25、30、35、40、45、50、55 min進行甲醛疼痛評分[4]:0分為注射爪可正常承重并自由活動,1分為注射爪可接觸地面但不能承重,2分為注射爪不能接觸地面,3分為大鼠舔咬注射爪。本研究根據權重評分法[4]計算每個觀察時間點的甲醛疼痛評分(PIR)作為炎性痛程度的定量指標。PIR=(1*T1+2*T2+3*T3)/60,T1、T2、T3分別為出現評分為1、2、3分行為學表現的持續時間。其中以0~5 min為Ⅰ相,15~60 min為Ⅱ相[4]。根據Ⅰ相、Ⅱ相中甲醛疼痛評分,分別計算Ⅰ相、Ⅱ相的甲醛疼痛抑制率。根據甲醛疼痛抑制率分別計算羥考酮及嗎啡在5%甲醛炎性痛模型中的ED50。甲醛疼痛抑制率計算公式如下:
甲醛疼痛抑制率=(對照組平均甲醛疼痛評分-試驗組平均甲醛疼痛評分)/對照組平均甲醛疼痛評分×100%
1.3.3羥考酮在內臟痛模型的鎮痛效應中κ、μ受體的比例測定根據羥考酮在2%醋酸扭體模型中所測出的ED50值,將24只SD大鼠隨機均分為4組,繼續使用2%醋酸扭體模型,分對照組(D組)、羥考酮ED50組(E組)、κ受體拮抗劑Nor-BNI 20 mg/kg+羥考酮ED50組(K組)、μ受體拮抗劑naloxonazlne 20 mg/kg+羥考酮ED50組(U組),計算扭體次數及扭體抑制率。將上述各組藥液經右側腹壁注入腹腔,其中D組注射等量等滲鹽水。注藥后15 min,將等滲鹽水稀釋的2%冰醋酸以4 mL/kg經另一側腹壁注入腹腔,然后立即放入觀察箱中觀察(開始計時),觀察扭體次數。其中κ受體拮抗劑Nor-BNI、μ受體拮抗劑naloxonazlne的劑量均通過預實驗得出繼續增加劑量后扭體次數不再增加,從而確定為最佳給藥劑量,分別得出給藥劑量為Nor-BNI 20 mg/kg,naloxonazine 20 mg/kg,于試驗前24 h經皮下給藥[5]。得出羥考酮在2%醋酸扭體模型發揮鎮痛效應的κ、μ受體所占的比例。
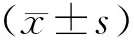
2 結 果
2.1腹腔注射羥考酮與嗎啡在2%醋酸扭體模型中的鎮痛效應與對照組相比,腹腔注射各濃度嗎啡及羥考酮組60 min內扭體次數減少,差異有統計學意義(P<0.05)。羥考酮ED50為0.6602 mg/kg(95%CI=0.02712~16.07 mg/kg)、嗎啡為1.942 mg/kg(95%CI=0.2773~13.60 mg/kg),羥考酮ED50/嗎啡ED50約為1∶2.94。見圖1。
2.2羥考酮與嗎啡在5%甲醛炎性痛模型中的ED50與對照組比較,Ⅰ相及Ⅱ相中腹腔注射各濃度嗎啡組及羥考酮組在60 min內舔足抬腿評分減少,差異有統計學意義(P<0.05)。其中Ⅰ相中羥考酮ED50為1.921 mg/kg(95%CI:1.199~3.077 mg/kg)、嗎啡ED50為4.484 mg/kg(95%CI:1.797~11.19 mg/kg),羥考酮ED50/嗎啡ED50比值約為1∶2.334;Ⅱ相羥考酮ED50為2.262 mg/kg(95%CI=1.378~3.715 mg/kg)、嗎啡ED50為3.812 mg/kg(95%CI:1.769~8.213 mg/kg),羥考酮ED50/嗎啡ED50比值約為1∶1.69。見圖2、圖3。
2.3羥考酮在2%醋酸扭體模型中κ、μ受體的鎮痛效應D組在2%醋酸扭體模型中的扭體次數為(45.8±2.5)次,E組為(22.5±2.4)次,K組為(37.8±1.7)次, U組為(26.8±2.1)次。與D組比較,各組扭體次數減少(P<0.05)。在2%醋酸扭體內臟痛模型中,羥考酮發揮鎮痛作用的κ受體與μ受體的比例約為2.375∶1。

a:嗎啡的劑量-效應曲線;b:羥考酮的劑量-效應曲線;c:嗎啡的log(劑量)-效應曲線;d:羥考酮的log(劑量)-效應曲線與對照組相比,*P<0.05,n=12圖1 羥考酮及嗎啡在2%醋酸扭體模型中的鎮痛效應曲線

a:嗎啡的劑量效應曲線;b:羥考酮的劑量效應曲線;c:嗎啡的log(劑量)-效應曲線;d:羥考酮的log(劑量)-效應曲線與對照組相比,*P<0.05,n=12圖2 羥考酮與嗎啡在5%甲醛炎性痛模型I相中的鎮痛效應曲線

a:嗎啡的劑量效應曲線;b:羥考酮的劑量效應曲線;c:嗎啡的log(劑量)-效應曲線;d:羥考酮的log(劑量)-效應曲線與對照組相比,*P<0.05,n=12圖3 羥考酮與嗎啡在5%甲醛炎性痛模型Ⅱ相中的鎮痛效應曲線
3 討 論
內臟痛的臨床表現復雜多樣,同一部位的疼痛可能包含有多個內臟器官的痛覺信號,且內臟損傷程度與疼痛強度無確切聯系,目前,內臟痛的傷害性刺激可分為機械性刺激、化學性刺激、缺血性刺激、電刺激、心理應激及溫度刺激等,通過這些傷害性刺激引起內臟的傷害性反應從而建立起內臟痛模型。扭體反應模型作為經典的內臟痛實驗模型,是通過腹腔注射乙酸、硫酸鎂、乙酰膽堿、緩激肽等刺激壁層腹膜和腹腔臟器產生以體腔壁痛為主的內臟痛,引起弓背、腹部肌肉收縮、后肢伸展的行為改變。本研究通過預實驗及參考姚明等[6]方法選擇以2%醋酸腹腔注射作為內臟痛模型,劑量選擇4 mL/kg均可出現扭體反應,且較為穩定,60 min內扭體次數大約為45次,之后基本不出現扭體。大鼠甲醛模型是急性組織損傷介導疼痛的經典試驗模型[4],通過足底注射甲醛后可出現雙相疼痛行為改變,第一相疼痛的產生是炎性物質直接刺激傷害性感受器,產生傷害性刺激傳導至中樞形成痛覺;而第二相反應的產生是因為肥大細胞釋放組胺等炎性介質的外周機制使得中樞發生敏化而產生[7],所以本文將5%甲醛50 μL足底掌側注射作為炎性痛模型。本研究使用此上述兩種實驗模型探討阿片類藥物在內臟痛、炎性痛鎮痛效應,并探討羥考酮在內臟痛模型中發揮鎮痛效應時κ受體與μ受體的占比。
本研究發現,腹腔給以嗎啡及羥考酮均可呈劑量依賴性發揮鎮痛效應,其中羥考酮ED50/嗎啡ED50的比值在甲醛模型的Ⅰ相、Ⅱ相分別為1∶2.334、1∶1.69,而在醋酸扭體模型中為1∶2.94,即相較于炎性痛模型,羥考酮與嗎啡的比值在內臟痛模型中較小,提示相較于炎性痛,羥考酮在內臟痛中可能具有更加優越的鎮痛效果。有研究[8]認為,外周效應的不同可能在兩種藥物的鎮痛效應中起到了重要作用。有研究[9]證實相同劑量的嗎啡腹腔給藥后可降低內臟痛模型的扭體次數,而靜脈給藥則沒有任何鎮痛作用,表明嗎啡經腹腔給藥時可能是通過外周效應發揮鎮痛效應。而羥考酮作為半合成的阿片類藥物,通過激動κ受體、μ受體發揮鎮痛作用,且可通過主動運輸跨越血腦屏障,發揮中樞性鎮痛效應,有研究[10]發現,在甩尾試驗和熱板試驗大鼠模型中,經鞘內給藥后嗎啡的鎮痛效應為羥考酮的14倍,但經皮下和腹腔給藥時羥考酮的鎮痛效應為嗎啡的2~4倍,可能與羥考酮的外周效應有關。在中樞神經系統及肺、消化道等外周器官中均有阿片受體分布,是阿片藥物發揮鎮痛作用的一個重要靶點,而且在炎癥環境中,外周傳入神經纖維末梢以κ受體為主的阿片受體表達增加[11],因此羥考酮發揮鎮痛的作用增強。Simonin等[12]發現,在醋酸扭體模型中,敲除κ受體基因的小鼠疼痛反應更劇烈,即對內臟痛更加敏感,使用κ受體激動劑可減輕疼痛反應,而μ受體基因敲除的小鼠對于熱痛刺激更加敏感,提示κ受體對于內臟痛的形成至關重要。有研究使用低頻振蕩振幅算法靜息態功能磁共振發現,與內臟痛形成的相關腦區活動異常[13],而另有研究發現κ受體也廣泛存在相關腦區中,提示κ受體在中樞效應中對內臟痛的形成也必不可少,具體機制仍有待探討[14-15]。本研究發現,在以醋酸等化學物質引起的內臟痛及甲醛引的炎性痛中,羥考酮的鎮痛作用均強于嗎啡,且對于內臟痛的鎮痛效應更強,可能與此有關,但具體機制仍需進一步研究。
羥考酮發揮鎮痛效應時κ受體、μ受體各自的占比仍不清楚,本研究初步探討在2%醋酸扭體模型中兩者的比例,通過前期預實驗得出κ受體、μ受體特異性拮抗劑的最佳給藥劑量,通過得出的羥考酮ED50給藥,計算扭體次數,初步估計κ受體、μ受體兩者的比例為2.375∶1,提示在醋酸扭體模型中,羥考酮主要通過κ受體發揮鎮痛作用,可能與內臟痛中κ受體起主要鎮痛作用有關[9]。
綜上所述,羥考酮及嗎啡在內臟痛鎮痛效應的差異可能與阿片受體的外周效應有關,本文也初步探討了羥考酮在內臟痛模型發揮鎮痛作用時的κ、μ受體各自的占比,但在內臟初級傳入神經纖維末梢的μ、κ受體具體激活以及調控的分子機制方面,尚需進一步研究。

