TiO2/聚砜超濾膜成膜熱力學(xué)及成孔劑溶出動(dòng)力學(xué)研究
王坤
(新沂市星辰新材料科技有限公司, 江蘇 新沂 221400)
工業(yè)上最廉價(jià)的超濾膜材料是聚砜,它具有以下優(yōu)點(diǎn):價(jià)格低廉且易獲得,相對(duì)于其他材料它的機(jī)械強(qiáng)度、抗壓密性以及耐熱性、化學(xué)穩(wěn)定性都非常好,它使用的pH范圍也很寬(pH值為2~12);但也存在缺點(diǎn),憎水性使疏水溶質(zhì)易在膜表面產(chǎn)生吸附和沉積,阻塞膜孔造成膜污染,使膜的性能降低,壽命縮短,利用率下降,因此聚砜膜的改性非常重要,受到廣大科研人員的重視。目前,二氧化鈦(TiO2)是研究最為廣泛的一種無(wú)機(jī)材料,因?yàn)門iO2具有很多優(yōu)點(diǎn),包括無(wú)毒、無(wú)光腐蝕;抗菌、光催化性;防紫外線、超親水性[1];能夠降解大多數(shù)有機(jī)污染物;在苛刻件下的穩(wěn)定性;商業(yè)實(shí)用性,易于制備等優(yōu)勢(shì)。在水處理和膜技術(shù)中TiO2被越來(lái)越多的人應(yīng)用,其中有人研究并報(bào)道了納米TiO2作為催化劑光催化降解水中頑固的污染物[2~3]。通過(guò)研究表明,膜的親水性因?yàn)門iO2與高分子超濾膜的復(fù)合得到了顯著的改善[4],同時(shí)在鑄膜液中添加適當(dāng)?shù)母叻肿犹砑觿┯兄诟牧糚SF超濾膜的截留率與滲透性,聚乙烯吡咯烷酮(PVP)和聚乙二醇(PEG)[5~8]是常用的高分子添加劑[9]。引入高分子添加劑后鑄膜液的性質(zhì)發(fā)生了改變,對(duì)成膜動(dòng)力學(xué)過(guò)程也有一定的影響,從而決定了超濾膜的微觀結(jié)構(gòu)與性能。除此之外,超濾膜的制備條件特別是溫度,顯著影響著鑄膜液的性質(zhì)與超濾膜的微觀結(jié)構(gòu)。因此為了明確改性劑TiO2的作用機(jī)制在研究成膜機(jī)制方面的意義,需要深入研究TiO2的濃度和凝膠浴溫度對(duì)鑄膜液動(dòng)力學(xué)和熱力學(xué)性質(zhì)的影響。
本文主要以PVP高分子聚合物為成孔劑,采用濁點(diǎn)滴定法繪制三元相圖,通過(guò)控制改性劑TiO2的濃度以及溫度研究L-S相轉(zhuǎn)化法成膜過(guò)程熱力學(xué)機(jī)理;以PEG高分子聚合物為成孔劑,通過(guò)控制改性劑TiO2的濃度、凝膠浴溫度和揮發(fā)時(shí)間來(lái)研究L-S相轉(zhuǎn)化法成膜過(guò)程中PEG的溶出動(dòng)力學(xué),以實(shí)現(xiàn)通過(guò)添加改性劑調(diào)整鑄膜液的組成及控制成膜外部條件改變超濾膜的結(jié)構(gòu),增強(qiáng)超濾膜性能,延長(zhǎng)超濾膜壽命,提高超濾膜利用率,以及通過(guò)研究高分子聚合物的溶出動(dòng)力學(xué)來(lái)確定聚合物固化成膜的相分離過(guò)程,為將來(lái)探究高分子聚合物溶出速率對(duì)膜結(jié)構(gòu)和性能的影響做好充分的準(zhǔn)備。
1 實(shí)驗(yàn)材料與方法
1.1 實(shí)驗(yàn)儀器與試劑
1.1.1 實(shí)驗(yàn)儀器
實(shí)驗(yàn)主要儀器見表1。
1.1.2 實(shí)驗(yàn)材料
實(shí)驗(yàn)主要試劑見表2。

表1 主要儀器

表2 主要試劑
1.2 實(shí)驗(yàn)方法
1.2.1 鑄膜液的制備過(guò)程
根據(jù)一定的配比配置不同TiO2濃度的鑄膜液,總質(zhì)量為40 g,配比分別為PSF16%,即6.4 g,PVP(PEG)為10%,即4 g,DMAc分別為73.9%、73.8%、73.7%、73.6%,即質(zhì)量分別為 29.56 g、29.52 g、29.48 g、29.44 g,TiO2質(zhì)量比分別為0.1%、0.2%、0.3%、0.4%,即質(zhì)量為0.04 g、0.08 g、0.12 g、0.16 g。實(shí)驗(yàn)步驟如下:先將PSF放在電熱鼓風(fēng)干燥箱內(nèi)烘干,溫度設(shè)置為80℃,時(shí)間為6 h;待PSF烘干后放入干燥器內(nèi)冷卻,稱取 DMAc質(zhì)量分別為 29.56 g、29.52 g、29.48 g、29.44 g放在80 mL小燒杯中,放入轉(zhuǎn)子,用塑料薄膜將其封住,放在磁力攪拌器上,稱取PVP(PEG)4 g,邊攪拌邊加入PSF,為使其充分溶解需加熱攪拌,待PVP(PEG)溶解后,稱取TiO2質(zhì)量分別為0.04 g、0.08 g、0.12 g、0.16 g分別加入到對(duì)應(yīng)的DMAc溶液中,待TiO2溶解,溶液由透明變?yōu)榛鞚岬娜榘咨珪r(shí)稱取PSF6.4 g加入小饒杯中將其封住,攪拌,直至完全溶解,制成均一的鑄膜液,此過(guò)程大約需要12 h,停止攪拌后需靜置脫泡24 h,以便除去氣泡,為后續(xù)刮膜做好準(zhǔn)備。
1.2.2 PSF超濾膜的制備過(guò)程
PSF超濾膜的制備大致可分為三個(gè)步驟,第一步,確定好超濾膜的厚度后制備刮膜器,刮膜器可以用玻璃棒制備,在玻璃棒兩端纏繞一定圈數(shù)的透明膠帶,此實(shí)驗(yàn)纏繞的圈數(shù)為6圈,制備好刮膜器后,需要制備玻璃板,玻璃板可以用10 cm×10 cm玻璃板進(jìn)行打磨,打磨成4 cm×5 cm長(zhǎng)方形的玻璃板以便放入1 000 mL的燒杯中;第二步,清洗玻璃板和玻璃棒并將其擦干,將靜置脫泡后的鑄膜液均勻倒在玻璃板前端,用玻璃棒將鑄膜液刮下,開始時(shí)把玻璃棒在鑄膜液上均勻的旋轉(zhuǎn)半圈以除去氣泡,刮膜過(guò)程要注意用力均勻,防止刮好的膜厚度不均,影響實(shí)驗(yàn)結(jié)果;第三步,室溫下預(yù)蒸發(fā)一定時(shí)間,大約10 s左右,將涂有鑄膜液的玻璃板放入凝膠浴中,凝膠成膜,直至超濾膜自動(dòng)從玻璃板上脫落,將制得的超濾膜放入蒸餾水中浸泡。
1.3 濁點(diǎn)滴定
在制備超濾膜的過(guò)程中,為了改良PSF超濾膜的截留率與滲透性,需要在鑄膜液中添加適當(dāng)?shù)母叻肿痈男詣緦?shí)驗(yàn)添加TiO2。為真實(shí)地反映制備超濾膜過(guò)程中的熱力學(xué)過(guò)程,實(shí)驗(yàn)將研究PSF-PVP-TiO2-S-NS的五元體系的三元相圖。為得到PSF-PVPTiO2-S-NS的五元體系的三元相圖,便于闡述體系的熱力學(xué)過(guò)程,本實(shí)驗(yàn)把TiO2看作溶劑,將它的質(zhì)量算到所用溶劑的質(zhì)量中去。
(1)控制鑄膜液的溫度分別為15、20、25及30℃,得到不同溫度時(shí)PSF-PVP-TiO2-S-NS體系濁點(diǎn)相圖。
(2)在20℃下,保持PSF含量不變,改變PVP質(zhì)量分?jǐn)?shù),使PVP含量分別為6%、8%、10%及12%(質(zhì)量分?jǐn)?shù))配制鑄膜液,得到不同PVP含量時(shí)PSF-PVP-TiO2-S-NS的濁點(diǎn)相圖。
(3)在20℃下,保持PVP濃度不變,改變PSF質(zhì)量分?jǐn)?shù),使PSF含量分別為15%、16%、17%及18%(質(zhì)量分?jǐn)?shù))配制鑄膜液,得到不同PSF含量時(shí)PSF-PVP-TiO2-S-NS的體系濁點(diǎn)相圖。
目前關(guān)于成膜熱力學(xué)過(guò)程的研究主要是借助濁點(diǎn)曲線三元相圖來(lái)描述,聚合物的復(fù)雜體系在非溶劑和溶劑中的相轉(zhuǎn)變、聚合物分子鏈重排以及固化的成膜過(guò)程可以用三相圖來(lái)具體的描述。
實(shí)驗(yàn)步驟大體如下:將裝有鑄膜液的燒杯用鐵架臺(tái)固定在大功率電動(dòng)攪拌器上,將燒杯用塑料薄膜封住口以防DMAc蒸發(fā),依據(jù)需要調(diào)整攪拌器的速度,邊攪拌邊用注射器向鑄膜液中添加去離子水,鑄膜液遇到去離子水后迅速凝固,一段時(shí)間后溶解,如果最后一滴去離子水一段時(shí)間后沒(méi)有溶解,則滴定達(dá)到終點(diǎn),記錄下所用去離子水的質(zhì)量。
本實(shí)驗(yàn)按照總質(zhì)量為40 g,配比為PSF16%,即6.4 g,PVP為 10%, 即 4 g,DMAc分 別 為 73.9%、73.8%、73.7%、73.6%,即質(zhì)量分別為29.56 g、29.52 g、29.48 g、29.44 g,TiO2質(zhì)量比分別為0.1%、0.2%、0.3%、0.4%,即質(zhì)量分別為0.04 g、0.08 g、0.12 g、0.16 g,配置四個(gè)梯度的TiO2的鑄膜液。控制溫度分別為15℃、20℃、25℃、30℃,在不同溫度下進(jìn)行滴定,記錄下數(shù)據(jù)。重復(fù)以上步驟進(jìn)行測(cè)試。
1.4 平板超濾膜中PEG溶出量的監(jiān)測(cè)
1.4.1 顯色劑的配置
據(jù)材料顯示,聚乙烯二醇(PEG)可以碘化鉍鉀試劑(Dragendoff試劑)發(fā)生反應(yīng)生成桔紅色的絡(luò)合物[21],因此利用此理論來(lái)測(cè)量PSF超濾膜中PEG的溶出量。然而,在此過(guò)程中存在諸多問(wèn)題,影響實(shí)驗(yàn)的準(zhǔn)確度,如以下情況。
(1)此絡(luò)合物見光易分解;
(2)在室溫下配置碘化鉍鉀試劑時(shí),次硝酸鉍在冰乙酸中的溶解度不高且溶解的速度較慢;
(3)當(dāng)酸性條件達(dá)不到要求時(shí)碘化鉍鉀與聚乙二醇(PEG)發(fā)生反應(yīng)的過(guò)程中易產(chǎn)生沉淀等。
本次實(shí)驗(yàn)改良了傳統(tǒng)的聚乙二醇配制方法,具體的操作步驟如下所示:
(1)A液的配置:準(zhǔn)確稱取3.2 g次硝酸鉍放于小燒杯中,準(zhǔn)確量取20 mL濃硝酸將其溶解。準(zhǔn)確稱取NaOH顆粒8 g置于另一燒杯中,加適量蒸餾水使其溶解,最后將兩者混勻置于200 mL棕色容量瓶中,準(zhǔn)確量取40 mL冰乙酸加入容量瓶中,再加蒸餾水,稀釋至刻度線。
(2)B液的配置:因?yàn)榈饣浺姽庖追纸猓渲脮r(shí)在遮光的條件下準(zhǔn)確稱取80.0 g置于燒杯中加適量蒸餾水溶解,然后置于200 mL棕色容量瓶中,再加蒸餾水,稀釋至刻度線。
(3)Dragendoff試劑的配置:準(zhǔn)確量取A液B液各50 mL置于1 000 mL棕色容量瓶中,再加蒸餾水稀釋至刻度線,其有效期為半年。
1.4.2 標(biāo)準(zhǔn)曲線的制作
(1)取適量聚乙二醇(PEG)放入電熱鼓風(fēng)干燥箱內(nèi),烘干以便去除水分,時(shí)間為4 h,溫度為60oC,后放在干燥器內(nèi)冷卻。
(2)待聚乙二醇(PEG)冷卻后,準(zhǔn)確稱取0.5 g溶解于500 mL的容量瓶中,配置成1 000 mg/L的聚乙二醇溶液,然后分別吸取聚乙二醇溶液 0、1、2、3、4、5 mL稀釋于100 mL 容量瓶中,配制成濃度為0、10、20、30、40、50 mg/L的聚乙二醇標(biāo)準(zhǔn)溶液。
(3)標(biāo)準(zhǔn)曲線的制作
將配置好的濃度為0、10、20、30、40、50 mg/L的聚乙二醇標(biāo)準(zhǔn)溶液。用25 mL移液管依次準(zhǔn)確量取25 mL加入到50 mL的棕色容量瓶中。其次量取6 mL冰乙酸加入到容量瓶中,搖動(dòng)容量瓶使溶液與冰乙酸混勻,然后量取6 mL Dragendoff試劑加入到容量瓶中搖勻,最后加蒸餾水稀釋至刻度線,搖勻,靜置15 min,最后用紫外分光光度計(jì)和玻璃比色皿測(cè)吸光度,波長(zhǎng)為510 nm,在這之前要用蒸餾水作空白。記錄下數(shù)據(jù),繪制圖表。PEG-4000的標(biāo)準(zhǔn)曲線如圖1所示。

圖1 PEG-10000溶液標(biāo)準(zhǔn)曲線
1.4.3 樣品的測(cè)試
本實(shí)驗(yàn)中用到的取樣裝置如圖2所示:
(1)取1 000 mL的大燒杯,洗凈,用蒸餾水沖洗,用于盛放蒸餾水,使用水銀溫度計(jì)調(diào)節(jié)溫度,將水放在冰箱和水浴鍋內(nèi)調(diào)節(jié)溫度,用作凝膠浴。
(2)將配置好的鑄膜液均勻倒在玻璃板上進(jìn)行刮膜,開時(shí)前稱取玻璃板的質(zhì)量,刮好膜后,再稱取鑄膜液和玻璃板的質(zhì)量記下數(shù)據(jù),此過(guò)程需在預(yù)蒸發(fā)時(shí)間內(nèi)完成,作差即可得到鑄膜液的質(zhì)量。
(3)將刮好的膜,經(jīng)預(yù)蒸發(fā)時(shí)間后放入一定溫度的凝膠浴中,開啟磁力攪拌器,取不同時(shí)間的溶液各25 mL,時(shí)間分別為1、2、3、4、5 min,分別加入到50 mL容量瓶中。
(4)準(zhǔn)確量取冰乙酸與Dragendoff試劑各6 mL,加入到容量瓶中,在這個(gè)過(guò)程中要注意先加冰乙酸調(diào)節(jié)酸度搖勻,再加Dragendoff試劑搖勻顯色,最后用蒸餾水稀釋至刻度線搖勻,靜置15 min,使用3 cm厚的玻璃比色皿在510 nm波長(zhǎng)下使用紫外分光光度計(jì)測(cè)定吸光度,蒸餾水為參比液。
(5)根據(jù)吸光度,利用標(biāo)線求出濃度,求出對(duì)應(yīng)質(zhì)量下PEG的溶出量,最后統(tǒng)一換算成0.5 g下的PEG的溶出量以便比較。

圖2 取樣裝置圖
2 結(jié)果與分析
2.1 TiO2在不同溫度下對(duì)PSF-PVP-S-NS四元體系濁點(diǎn)的影響
濁點(diǎn)滴定時(shí),控制鑄膜液中TiO2濃度分別為0.1%、0.2%、0.3%、0.4%,用去離子水作為滴定液。圖3為15、20、25、30 ℃下不同TiO2濃度的濁點(diǎn)圖。從圖中可以看出以下規(guī)律:
(1)對(duì)任意的一條濁點(diǎn)曲線而言,隨鑄膜液中TiO2濃度的升高,濁點(diǎn)曲線逐漸靠近溶劑軸(DMAc+PVP+TiO2軸),這說(shuō)明隨著鑄膜液中TiO2濃度的升高,鑄膜液對(duì)非溶劑的容納能力減小,這主要是因?yàn)門iO2的比表面比較大,且儲(chǔ)存了大量的表面能,其表面富含的羥基與 PSF分子鏈產(chǎn)生了吸附作用,因此TiO2的濃度越大,與大分子之間的這種相互作用越強(qiáng),體系的黏度也就越大故PSF分子相互接觸的幾率變大,鑄膜液中溶劑的分子濃度減小,當(dāng)溶液中含有少量的非溶劑時(shí),PSF分子即可發(fā)生聚集,產(chǎn)生液-液相分離,從而減小了鑄膜液對(duì)非溶劑的容納能力[9~12]。
(2)從圖中可以看出不同溫度下的四條曲線都保持一致即隨著滴定溫度的升高,濁點(diǎn)曲線漸漸遠(yuǎn)離溶劑軸,這說(shuō)明隨著滴定溫度的升高鑄膜液對(duì)非溶劑的容納能力漸漸增大,這主要是因?yàn)殍T膜液中溶劑化作用的強(qiáng)度隨著滴定溫度的升高而加強(qiáng),從而使得PSF分子鏈在溶液中更加容易伸展,與此同時(shí)PSF分子的熱運(yùn)動(dòng)也更加的劇烈,這使得PSF分子間聚集的可能性減小,因此也就增加了鑄膜液對(duì)非溶劑的容納能力[13~16]。
2.2 時(shí)間對(duì)PEG溶出動(dòng)力學(xué)的影響
2.2.1 時(shí)間對(duì)PEG溶出量的影響
配置TiO2濃度分別為0.1%、0.2%、0.3%、0.4%的鑄膜液,制備PSF超濾膜,控制溫度分別為15、20、25、30℃,進(jìn)行溶出量的測(cè)定。圖4分別為15、20、25、30℃下PEG的溶出量。由圖可以看出,溶出量隨時(shí)間的增加逐漸增加,并且在第一分鐘第二份時(shí)溶出迅速,幾乎全部溶出,第3、4、5 min后溶出量趨于穩(wěn)定。同時(shí)可以看出當(dāng)溶出量趨于穩(wěn)定時(shí)15℃時(shí)溶出量最高,30℃最低,即隨著溫度的升高,超濾膜中PEG的溶出量逐漸降低。這主要是因?yàn)殡S著凝膠浴溫度的升高,PEG與溶劑的擴(kuò)散速度增大,于是鑄膜液的表層便能迅速的生成,而且比較致密,從而成為內(nèi)部PEG溶出的阻礙,所以溫度高時(shí)PEG溶出量低于溫度低時(shí)PEG的溶出量[17~19]。
2.2.2 時(shí)間對(duì)PEG溶出速率的影響
如上所述制備TiO2濃度為0.1%的PSF超濾膜,分別在不同溫度下測(cè)量,將溶出量進(jìn)行擬合可得到溶出量擬合方程,對(duì)溶出量擬合方程求導(dǎo)即可得到PEG溶出速率方程,如表3所示,根據(jù)溶出速率方程即可求得到溶出速度,圖5為對(duì)應(yīng)TiO2濃度下的PEG溶出量擬合曲線圖和溶出速率圖,由圖可以看出隨著時(shí)間的增加溶出總量逐漸增加后趨于穩(wěn)定,溶出速率逐漸減小,主要是因?yàn)殡S著時(shí)間的增加,鑄膜液中PEG的量逐漸減小,溶出速率逐漸減小[20]。同時(shí)也可以看出30℃時(shí)溶出速率最大。
表4為TiO20.2%時(shí)的溶出量擬合方程和溶出速率方程,圖6為溶出量擬合圖和溶出速率圖,由圖可以看出隨著時(shí)間的增加溶出總量逐漸增加后趨于穩(wěn)定,溶出速率逐漸減小最終趨于零。
如表5為TiO20.3%時(shí)的溶出量擬合方程和溶出速率方程,圖7為溶出量擬合圖和溶出速率圖,由圖可以看出隨著時(shí)間的增加溶出總量逐漸增加后趨于穩(wěn)定,溶出速率逐漸減小最終趨于零。
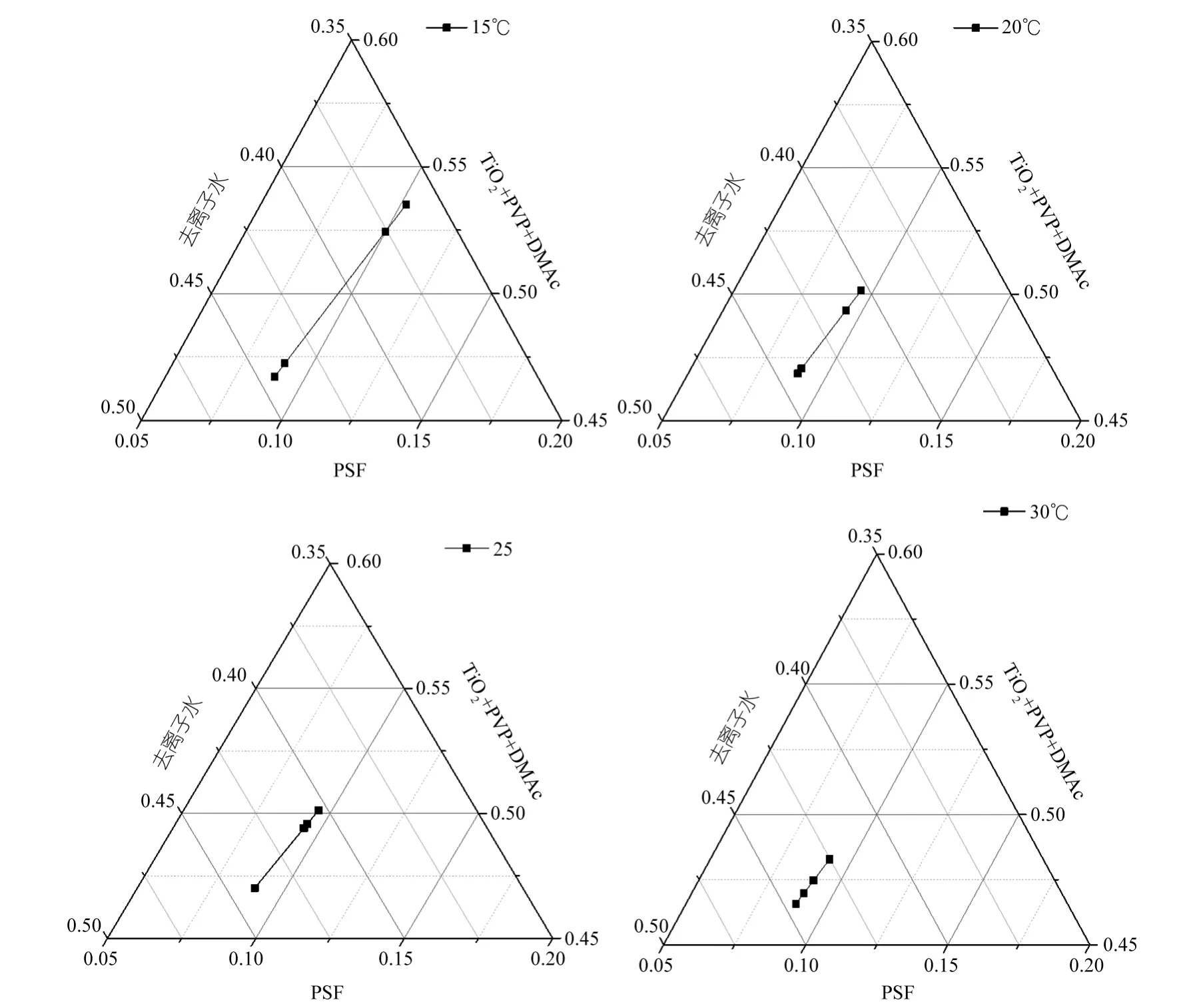
圖3 不同溫度下不同TiO2濃度鑄膜液的沉淀值

表3 TiO2為0.1%時(shí)PEG隨時(shí)間溶出量、溶出速率方程

表4 TiO2為0.2%時(shí)PEG隨時(shí)間溶出量、溶出速率方程
表6為TiO20.4%時(shí)的溶出量擬合方程和溶出速率方程,圖8為溶出量擬合圖和溶出速率圖,由圖可以看出隨著時(shí)間的增加溶出總量逐漸增加后趨于穩(wěn)定,溶出速率逐漸減小最終趨于零。
2.3 溫度對(duì)PEG溶出動(dòng)力學(xué)的影響
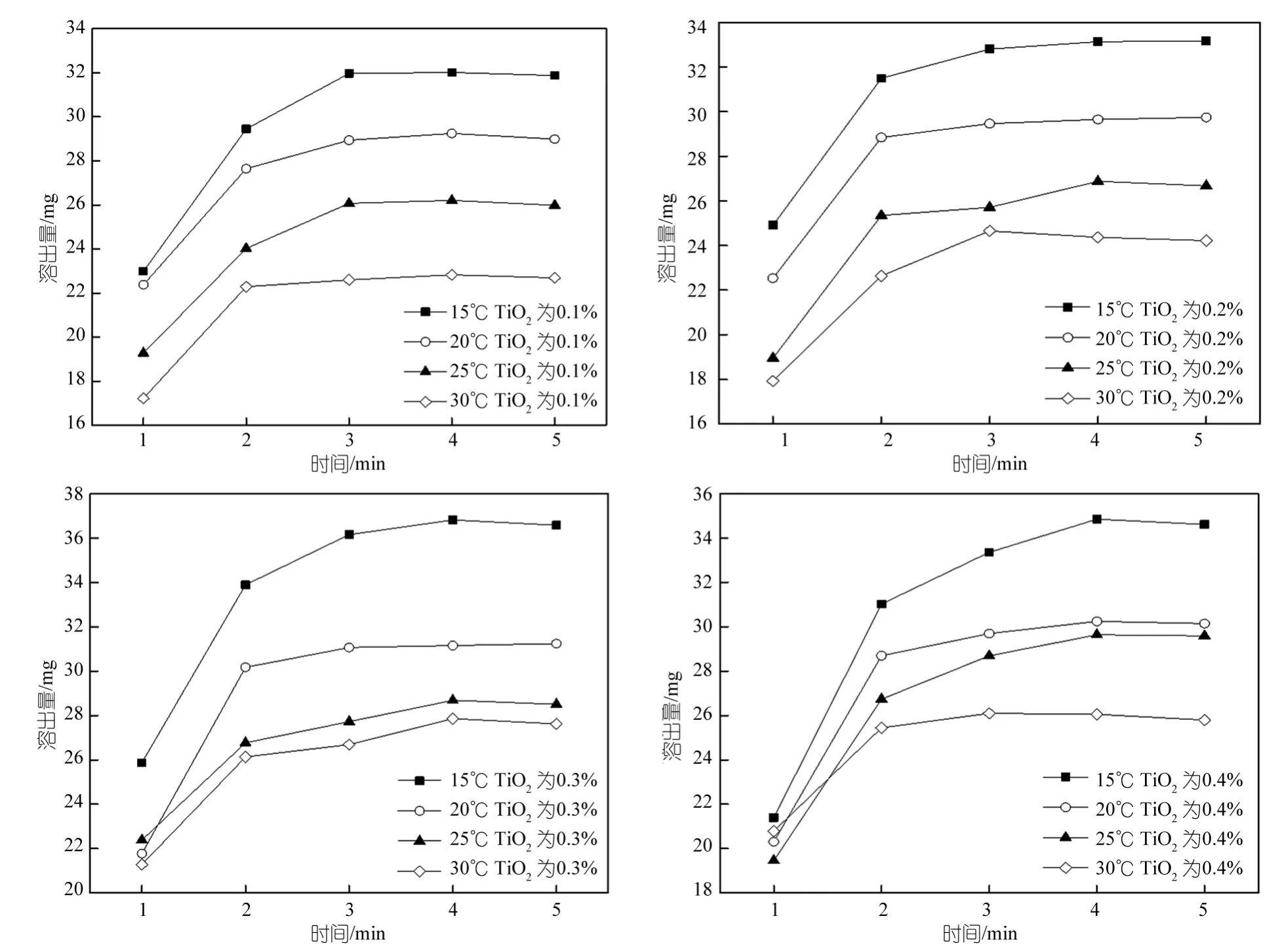
圖4 不同TiO2濃度下時(shí)間對(duì)PEG溶出量的影響

圖5 TiO2為0.1%時(shí)PEG隨時(shí)間溶出量擬合圖和溶出速率圖
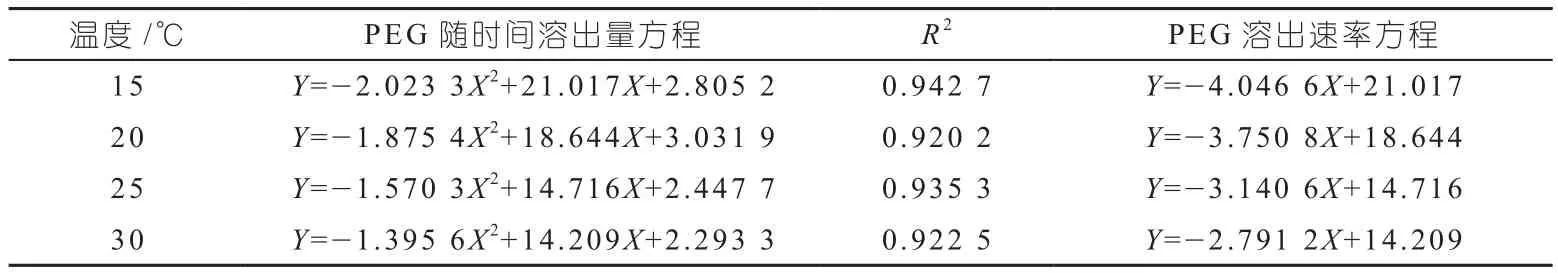
表5 TiO2為0.3%時(shí)PEG隨時(shí)間溶出量、溶出速率方程
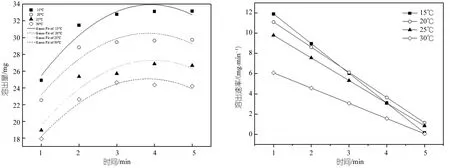
圖6 TiO2為0.2%時(shí)PEG隨時(shí)間溶出量擬合圖和溶出速率圖

圖7 TiO2為0.3%時(shí)PEG隨時(shí)間溶出量擬合圖和溶出速率圖

表6 TiO2為0.4%時(shí)PEG隨時(shí)間溶出量、溶出速率方程

圖8 TiO2為0.4%時(shí)PEG隨時(shí)間溶出量擬合圖和溶出速率圖
成膜過(guò)程中PEG的溶出與凝膠浴的溫度有密切的關(guān)系,同時(shí)凝膠浴的溫度對(duì)鑄膜液體系的黏度也有一定的影響,因?yàn)檫@些原因溶劑和非溶劑的擴(kuò)散速度也受到影響,然而溶劑與非溶劑的擴(kuò)散速度對(duì)鑄膜液的凝膠速度有極其重要的影響。由圖9可以看出隨著凝膠浴溫度的升高鑄膜液中PEG的溶出量逐漸降低,這主要是因?yàn)殡S著凝膠浴溫度的升高,PEG與溶劑的擴(kuò)散速度增大,于是鑄膜液的表層便能迅速的生成,而且比較致密,從而成為內(nèi)部PEG溶出的阻礙,然而溫度低時(shí),PEG與溶劑的擴(kuò)散速度降低,膜表層形成速度慢,PEG溶出量多且形成比較大的膜孔,從而使內(nèi)部的PEG溶出量增多,所以溫度低時(shí)PEG的溶出量大[21]。

圖9 溫度對(duì)PEG溶出量的影響
2.4 TiO2濃度對(duì)PEG溶出動(dòng)力學(xué)的影響
由圖10可以看出隨著TiO2濃度的升高鑄膜液中PEG的溶出量逐漸的增加,這主要是因?yàn)椋?/p>
(1)鑄膜液中添加了改性劑TiO2后,TiO2的表面含有大量的羥基,正因?yàn)檫@些羧基的存在改善了PSF超濾膜的親水性,因此隨著TiO2濃度的增加,PSF超濾膜表面吸附和鑲嵌的TiO2粒子也隨之增加,從而使膜的水接觸角逐漸的減小,親水性也隨之增強(qiáng)。
(2)TiO2顆粒改變了表層下面的結(jié)構(gòu),加強(qiáng)了表面孔和亞表層的連通性[21]。故隨著TiO2濃度的升高鑄膜液中成孔劑PEG的溶出量也隨之逐漸的增加。
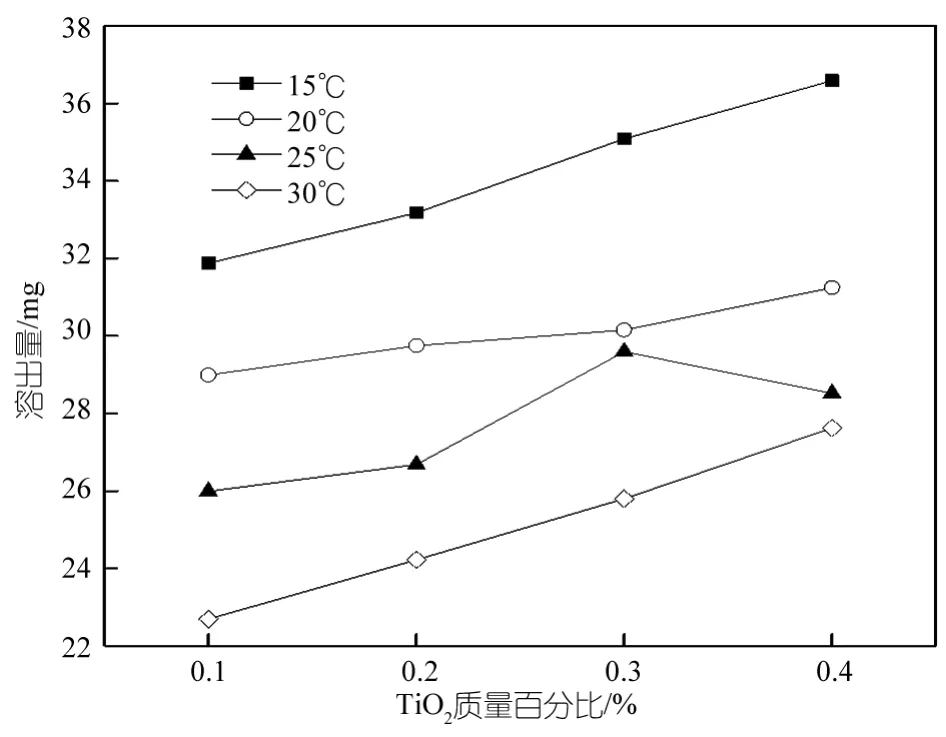
圖10 TiO2濃度對(duì)PEG溶出量的影響
3 結(jié)論
本文采用濁點(diǎn)滴定法利用相圖理論研究TiO2濃度及溫度在成膜過(guò)程中對(duì)熱力學(xué)相圖的影響。利用紫外分光光度計(jì)法研究了溫度、時(shí)間以及TiO2濃度對(duì)成膜過(guò)程中PEG溶出量和速度的影響。得出以下四條結(jié)論:
(1)隨鑄膜液中TiO2濃度的升高,濁點(diǎn)曲線逐漸靠近溶劑軸,鑄膜液對(duì)非溶劑的容納能力降低,隨著滴定時(shí)溫度的升高濁點(diǎn)曲線逐漸遠(yuǎn)離溶劑軸,鑄膜液對(duì)非溶劑的容納能力提高。
(2)隨時(shí)間的增加成膜過(guò)程中PEG的溶出量逐漸增加且慢慢趨于穩(wěn)定,PEG溶出速率隨時(shí)間的增加而減小。
(3)隨著凝膠浴溫度的升高,PEG的溶出量逐漸降低。
(4)隨著TiO2濃度的升高,PEG的溶出量逐漸升高。

