離子液體對CO2捕集及電轉化的研究
成麗蘋,郝永超,李 敏,王秀玲,趙 哲,馬曉剛,王 月
(邢臺學院 化學工程與生物技術學院,河北 邢臺 054001)
CO2是溫室效應的主要因素,溫室效應愈演愈烈,已造成氣候變暖等極其嚴重的問題,引起了全世界的重視。如何緩解溫室效應造成的環境問題,一方面減少CO2的排放量,另一方面收集利用CO2也是解決問題的途徑之一。CO2可作為碳資源,將其轉化成燃料,那么對于解決能源危機是非常有幫助的[1]。所以從能源和環境兩個方面來看,CO2的捕集和利用都是非常有意義的。目前吸收固定CO2的方法有物理法、化學法、生物法等固定方法,物理固定是通過將CO2封存于海底,但是這種方法易導致海水酸化;生物法固定是通過植物的光合作用固定二氧化碳,但是近年來植被的破壞,光合作用也嚴重受限,無法與人類生產活動釋放的二氧化碳總量持平;化學法固定是實現二氧化碳循環利用最有效的途徑[2],工業上普遍使用的是以醇胺法固定二氧化碳的化學吸附,但是因其具有揮發性和腐蝕性,對儀器設備破壞性大[3],因此,開發綠色無污染的方法是目前亟待解決的。
離子液體(Ionic Liquids)在室溫下呈液態,是由特定陰、陽離子構成,被稱為新型“綠色溶劑”、“軟”功能材料[4-6],也被稱作室溫離子液體、低溫熔融鹽、有機離子液體等。目前尚無統一的名稱,但傾向于簡稱離子液體。它不揮發、不可燃,具有良好的化學穩定性,液體穩定范圍和電化學窗口都較寬,循環使用性能較好[7]。
離子液體的制備方法有微波合成法和其他輔助波法,微波法是在磁場中將交變電磁能轉化為介質內能的一種加熱方法,該方法具有加熱速度快、均勻、節能高效等優點。本文采用微波法合成咪唑氨基酸([Amim]Gly)、咪唑四氟硼酸鹽([Bmim]BF4)和咪唑六氟磷酸鹽([Bmim]PF6)離子液體,并對不同類型離子液體吸附CO2特性進行考察,并以咪唑氨基酸類離子液體作為電解質,對二氧化碳進行電化學還原,探究其對CO2電轉化甲醇的催化效能。
1 實驗部分
1.1 儀器與試劑
儀器:XH-100B電腦微波催化合成/萃取儀,RE-52AA 旋轉蒸發儀,HDY-I 恒電位儀,Agilent 789A氣相色譜儀。
試劑:1-甲基咪唑,氯丙烯,四氟硼酸鈉,六氟磷酸鉀,溴代正丁烷,二氯甲烷,甘氨酸,丙酮,環己烷,乙酸乙酯,無水乙醇,無水硫酸鈉,氯化鈉,鹽酸,氫氧化鈉,無水碳酸鈉,濃硫酸,無水乙醚,甲醇(除甲醇為色譜純外均為分析純),去離子水。
1.2 功能化離子液體的制備
[Amim]Gly離子液體的制備。采用微波-動態離子交換法合成。先合成氯化1-甲基-3-烯丙基咪唑,取0.1 mol 1-甲基咪唑加入10 mL氯丙烯,磁力攪拌10min。設置微波參數功率:500 W,溫度:55 ℃,在微波條件下反應120min。用20 mL的環己烷萃取三次,等體積的乙酸乙酯萃取兩次[8]。除去溶劑,得到中間體氯化1-甲基-3-烯丙基咪唑。將中間體用乙醇稀釋加入活化后的離子交換樹脂層析柱中,控制液滴速率(10s/滴),直至液滴pH為中性,產物蒸發一半溶劑。再加入等物質的量的甘氨酸,室溫攪拌12 h,加入無水硫酸鈉干燥,減壓抽濾,抽濾所得液體經減壓蒸餾后,恒溫干燥24 h。
[Bmim]BF4離子液體的制備。稱取0.3 mol 1-甲基咪唑,0.33 mol(稍過量)溴代正丁烷于微波專用反應瓶中,設置參數進行反應,產物用乙酸乙酯進行洗滌,再蒸去乙酸乙酯,得到中間體溴代1-丁基-3-甲基咪唑。稱取0.1 mol溴化1-丁基-3-甲基咪唑和11 g四氟硼酸鈉于錐形瓶中,加入150 mL丙酮,磁力攪拌5 h,除去不溶物,蒸出丙酮,加入200 mL二氯甲烷,每次用15 mL水洗滌,直到水層用AgNO3溶液檢測不到溴離子為止,下層加入過量無水MgSO4,除去不溶物,蒸去二氯甲烷溶劑得到離子液體,烘干,備用。
[Bmim]PF6離子液體的制備。先用少量水溶解0.1 mol上述中間體,稱取18.4 g六氟磷酸鉀于燒杯中,溶解并逐滴滴入中間體溶液中,室溫磁力攪拌2 h,靜置分層,有機層溶液加入去離子水洗滌,直到水層用AgNO3溶液檢驗無沉淀為止。烘干,備用。
1.3 離子液捕集CO2
碳酸鈉和鹽酸溶液反應制備CO2,經過飽和碳酸鈉溶液吸收氯化氫氣體,濃硫酸吸收水蒸氣后通入裝有離子液的小試管中。通過稱重計算CO2吸附量。
準確稱量H型電解槽的質量,將樣品的水溶液(樣品與水的體積體比為7∶3)50 mL加入H型電解槽中,鉑電極為陽極,銀電極為陰極,甘汞電極為參比電極,還原之前,向電解槽內通入CO210 min,進行CO2飽和捕獲,再次稱取電解槽,計算捕獲CO2的質量。在外加-0.5 V過電位下,電化學還原25min,用無水乙醚萃取得到還原產物[1],還原產物用氣相檢測CO2轉化甲醇的含量。
1.4 檢測條件
氣相色譜條件:HP-INNOWAX毛細管柱(30 m×320 μm×0.25 μm);載氣:N2,流量:1.3 mL/min;進樣口溫度180 ℃;程序升溫:27 ℃保持10min,然后以25 ℃/min升到220 ℃,保持10min;檢測器溫度:230 ℃;分流比:50∶1;進樣量1 μm[9]。
標準曲線:精密量取0.1、0.2、0.3、0.4、0.5 mL甲醇分別置于10 mL容量瓶中,用無水乙醇稀釋至刻度,制成體積分數分別為0.1%、0.2%、0.3%、0.4%、0.5%的甲醇溶液。進行氣相檢測,得到標準曲線方程為y = 0.948x + 0.0019,R2=0.9989。
2 結果與討論
2.1 離子液體的FT-IR分析
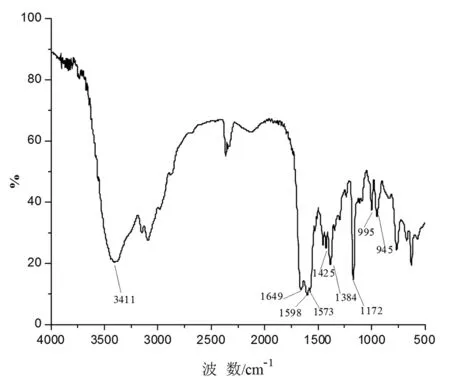
圖1 [Amim]Gly的紅外譜圖
圖1是[Amim]Gly的紅外譜圖。波數為1573 cm-1是咪唑環特征振動峰,1172 cm-1是咪唑環C-H面內彎曲振動峰。1649 cm-1和1425 cm-1分別是烯丙基上C=C伸縮振動峰和雙建上的C-H彎曲振動峰。3411 cm-1是N-H伸縮振動峰,1598 cm-1和1384 cm-1是甘氨酸中C=O伸縮振動峰。995 cm-1是-CH=CH2的C-H面外彎曲振動峰,945 cm-1是-CH=CH2的C-H面內搖擺振動峰。
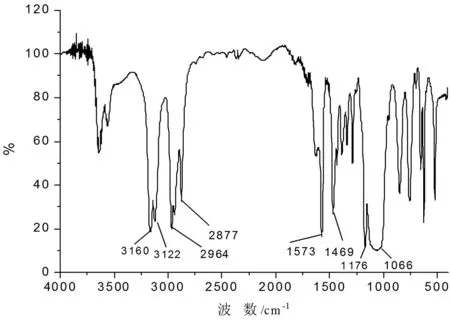
圖2 [Bmim]BF4的紅外譜圖
圖2是[Bmim]BF4的紅外譜圖。波數為3160cm-1和3122cm-1是咪唑環上的C-H伸縮振動峰,波數為2964 cm-1和2877 cm-1是CH3-和CH2-的伸縮振動峰,波數為1573 cm-1和1469 cm-1咪唑環振動峰,波數為1176 cm-1是咪唑環C-H面內彎曲振動峰,波數為1066 cm-1是B-F伸縮振動峰,波譜特征與文獻一致[10]。
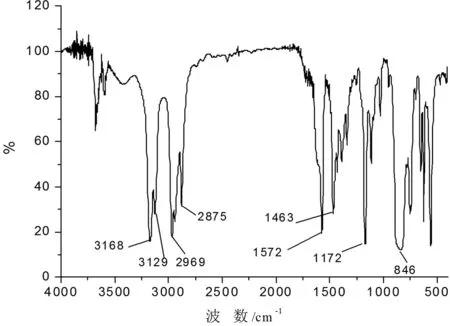
圖3 [Bmim]PF6的紅外譜圖
圖3是[Bmim]PF6的紅外譜圖。波數為3168 cm-1和3129 cm-1是咪唑環上的C-H伸縮振動峰,波數為2969 cm-1和2875 cm-1是CH3-和CH2-的伸縮振動峰,波數為1572 cm-1和1463 cm-1是咪唑環振動峰,波數為1172 cm-1是咪唑環C-H面內彎曲振動峰,波數為846 cm-1是P-F伸縮振動峰,波譜特征與文獻一致[10]。
2.2 離子液體對CO2吸附量的研究
在常溫下,考察CO2吸附量隨時間的變化,分別稱取相同質量[Amim]Gly、[Bmim]BF4和[Bmim]PF6離子液體置于小試管中,將純凈的CO2以鼓泡形式通入離子液體中,控制鼓入速度,每隔5 min稱重,計算二氧化碳的質量變化,如表1。由表1可知,開始時CO2吸附量增加較快,當吸附10 min后產物CO2的吸附量變化不大,20 min達到飽和,最大吸附量為每摩爾離子液吸收0.24 mol CO2。[Bmim]BF4開始時吸附CO2的量增加較快,當通入20 min之后,吸附CO2的量變化較緩慢,當通入30 min之后則不再發生變化,最大吸附量經過計算為每摩爾離子液吸收0.024 mol的CO2。[Bmim]PF6開始吸附CO2的量上升較快,當通入15min之后,吸附CO2的量變化不明顯,當通入20 min之后則不再發生變化,最大吸附量經過計算為每摩爾離子液吸收0.015 mol CO2。
經過比較,[Amim]Gly離子液體對CO2的吸附量效果較好,選擇[Amim]Gly離子液體進行電催化還原的研究。
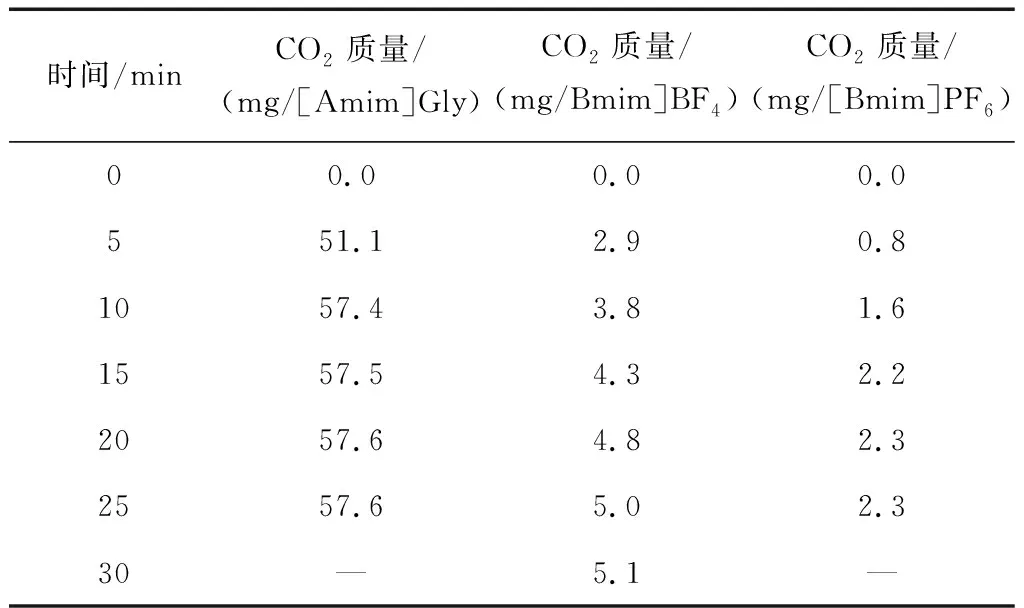
表1 離子液體吸附CO2量隨時間的變化
2.3 CO2電轉化甲醇含量的測定
使用新鮮的吸附了CO2的離子液體進行電化學還原,萃取后取樣于小試管,并編號為1;用萃取后的離子液體重新吸附CO2進行電催化還原,萃取后取樣于小試管,并編號為2;以此類推重復五次。上述五種電化學還原產物進行氣相檢測,在檢測標準溶液的條件下分別檢測待測試樣,記錄檢測數據,然后將數據帶入上述方程求得甲醇的濃度,計算轉化率,結果如表2所示。
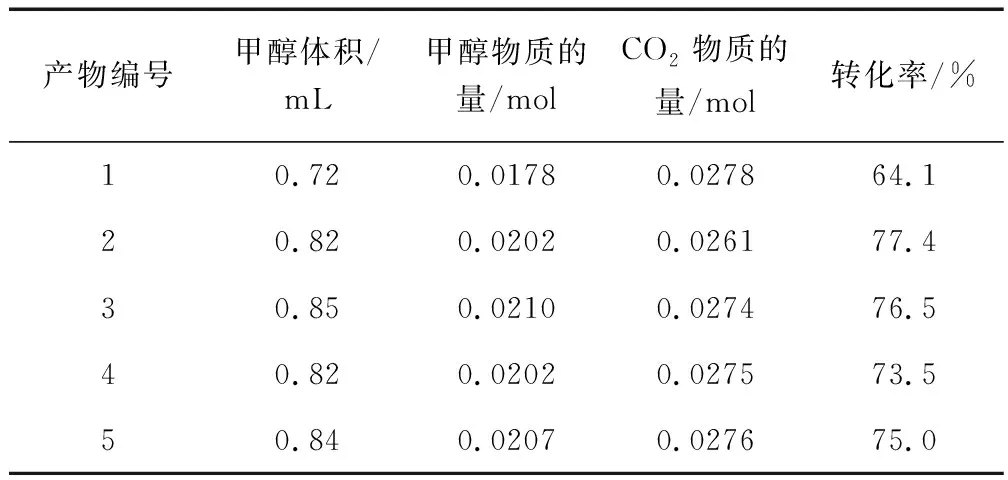
表2 CO2的轉化率
由表2可知,[Amim]Gly離子液重復使用,CO2轉化率在64.1%~77.4%之間變化。在重復使用的離子液體中CO2轉化率比在新鮮的離子液體的轉化率高,可能是由于在電還原條件下,離子液體形成了聚合離子液體,這種聚合離子液體提高了CO2轉化率。
3 結論
本文采用微波法合成了[Amim]Gly、[Bmim]BF4和[Bmim]PF6功能型離子液體,考察吸附CO2性能,最大吸附量分別為每摩爾離子液吸收0.24 mol、0.023 mol、0.015 mol的CO2,[Amim]Gly離子液體對于CO2具有良好的捕獲性。室溫條件下,并以[Amim]Gly離子液體為電解質,當吸附20 min時CO2達到飽和,外加-0.5 V過電位下,通電25 min,轉化率即可達到64.1%~77.4%。[Amim]Gly離子液體在使用后只需簡單處理即可重復使用。與以往的甲醇工業生產相比,此方法成本低、無污染、反應時間短,為工業生產甲醇提供了一種新方法。
[1]朱家藝,賀軍輝.二氧化碳的捕集、存儲及轉化[J].影像科學與光化學,2011,29(3):170-172.
[2]劉芙蓉.基于離子液體的二氧化碳電催化還原研究[D].長沙:湖南大學,2014:1-28.
[3]范 薇,孫曉霞,蘇 巖.基于離子液體固定二氧化碳的研究進展[J].化學研究,2009,20(3):101-102.
[4]文啟忠,喬玉樓.愛護地球從自己做起—紀念第38個世界地球日[J].今日科苑,2007(9):41-43.
[5]張 慧,陸建剛,嵇 艷,等.離子液分離/固定二氧化碳的研究進展[J].現代化工,2009,29(11):32-36.
[6]鄧友全.離子液體:性質、制備和應用[M].北京:中國石化出版社,2006.
[7]張星辰.離子液體--從理論基礎到研究進展[M].北京:化學工業出版社,2009.
[8]趙衛星,姜洪波,張來新.咪唑類離子液體的制備與合成[J].貴州化工,2010,35(4):9-11.
[9]王化同,王洪瑩.毛細管氣相色譜法測定白酒中甲醇含量的研究[J].中國社區醫師,2014,30(22):136.
[10]黃一波.咪唑類離子液體的合成與表征[J].天津化工,2007,21(6):28-29.

